Фосфиновая модификация трипептида GPE и моделирование его свойств
Автор: Головаш С.Р., Винюков А.В., Рагулин В.В.
Журнал: Международный журнал гуманитарных и естественных наук @intjournal
Рубрика: Химические науки
Статья в выпуске: 12-1 (51), 2020 года.
Бесплатный доступ
Поиск и получение новых физиологически-активных веществ для терапии нейродегенеративных нарушений является одной из самых важных задач для органической химии. Подход, основанный на замене пептидной связи в молекуле пептида структурно изостерным негидролизуемым метиленфосфорильным фрагментом, позволяет увеличить метаболическую стабильность пептидных молекул к разрушительному действию пептидаз. В настоящей работе нами была осуществлена модификация трипептида глицин-пролин-глутамат (GPE), обладающего нейропротекторными свойствами, путем замены пептидной связи C(O)NH в молекуле пептида структурно изостерным негидролизуемым метиленфосфорильным фрагментом P(O)CH2. Кроме того, посредством программ PASS и GUSAR были осуществлены прогноз и относительное сравнение биологической активности и токсичности исходного трипептида и его фосфинового аналога.
Аналоги переходного состояния, фосфиновые псевдо-пептиды, амидоалкилирование гидрофосфорильных соединений, изостеры аминокислот и пептидов
Короткий адрес: https://sciup.org/170190711
IDR: 170190711 | DOI: 10.24411/2500-1000-2020-11643
Phosphinic modification of GPE tripeptide and simulation of its properties
The search and production of new physiologically active substances to treat neurodegenerative disorders is essential for organic chemistry. The approach based on replacing a peptide bond in a peptide molecule with a structural isostere, non-hydrolyzable methylene phosphoryl fragment makes it possible to increase the metabolic stability peptide molecules to the destructive action of peptidases. In this work, we modified the glycine-proline-glutamate (GPE) tripeptide, which has neuroprotective properties, by replacing the peptide bond C(O)NH in the peptide molecule with a structural isostere non-hydrolyzable methylene phosphoryl fragment P(O)CH2. Using the PASS and GUSAR programs, a prediction and relative comparison of the biological activity and toxicity of the parent tripeptide and its phosphine analog were carried out.
Текст научной статьи Фосфиновая модификация трипептида GPE и моделирование его свойств
Введение. Исследования, проведенные в 1989 году, выявили что Gly-Pro-Glu (GPE) находится в организме как часть инсулиноподобного фактора роста 1 и является новым нейроактивным пептидом с мощным действием на высвобождение ацетилхолина, а также играет роль в регуляции функций мозга [1]. В этих исследованиях было обнаружено, что GPE участвует в различных процессах в центральной нервной системе. GPE был синтезирован и показал, что ингибирует связывание глутамата с рецептором N-метил-D-аспартата (NMDA). Кроме того, GPE имел мощное стимулирующее действие на калий-индуцированное высвобождение ацетилхолина из срезов коры головного мозга крыс [2]. В дальнейшем было множество исследований посвященным нейропротек-торному и ноотропному действию Gly-Pro-Glu [3-9] и на данный момент GPE является одним из перспективных нейропротек- торных агентов. В настоящей работе осуществлялась модификация трипептида GPE путем замены одной пептидной связи C(O)NH в молекуле трипептида негидролизуемым метиленфосфорильным фрагментом P(O)(OH)CH2. Такой подход в последние несколько лет используется в качестве основного ключа для построения фосфиновых кислых изостеров пептидов и является достаточно успешным в плане поиска лекарственных средств противовирусного, противоопухолевого характера, средств против иммунодефицита [10] и ряда других болезней [11-13]. Фосфиновые кислотные псевдо-пептиды, у которых пептидная связь заменена на негидролизуемый метиленфосфорильный фрагмент, являются ингибиторами процессов, происходящих с гидролитическим или ферментативным расщеплением пептидной связи, что позволяет использовать псевдопептиды как соединения-имитаторы, для изучения и, главным образом, возможной регуляции ряда метаболически важных процессов. Эти предпосылки позволяют предполагать достаточно высокую степень сохранения свойств исходной молекулы в молекуле структурного фосфоизостера, что справедливо для какого-либо короткого пептида, свойства которого главным образом определяются конкретной аминокислотной последовательностью. Предлагаемая фосфиновая замена пептидной связи сохраняет исходную аминокислотную последовательность и увеличивает устойчивость псевдо-пептидной связи образовавшегося фосфоизостера к гидролитическому воздействию пептидаз на пути к биомишени, что и позволяет рассчитывать на повышение его эффективности в сравнении с исходной гидролитически лабильной молекулой.
Результаты. На первом этапе работы нами был осуществлен синтез фосфинового аналога дипептида псевдо-пролилглутамата Pro-[P(O)(OH)CH2]-Glu 1.1 [14] (рис. 1), с соответствующими защитными группами на атоме фосфора и карбоксильных концах, для дальнейшего использование в качестве N-компоненты в пептидном синтезе. Дальнейшая обработка фосфиновой кислоты 1.2 смесью адаман-тилбромида и оксида серебра в хлороформе позволили получить адамантиловый эфир фосфиновой кислоты 1.3 в соответствии с известной методологией защиты гидроксифосфорильной функции. После чего осуществлялось селективное снятие защитной группы с атома азота путем каталитического гидрирования (рис. 1).
Рис. 1. Синтез фосфинового P,С-защищенного пролилглутаматного блока
Далее нами был осуществлен успешный синтез модифицированного «псевдопептида» Gly-Pro-[P(O)(OH)CH2]-Glu (GPE(phos)) 2.1, фосфинового аналога GPE, путем присоединения N-Boc-защищенной аминокислоты глицина к фосфиновому P,С-защищенному пролилг- лутаматному блоку Pro-[P(O)(OH)CH2]-Glu 1.1, в соответствии с известными методиками пептидного синтеза (рис. 2). Препаративная очистка и анализ осуществлялись при помощи методов высокоэффективной жидкостной хроматографии и масс-спектрометрии.
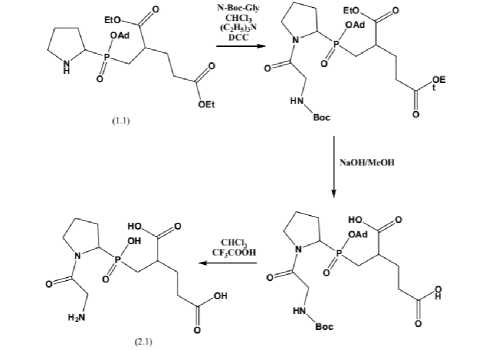
Рис. 2. Схема синтеза фосфинового «псевдо-пептида» Gly-Pro-[P(O)(OH)CH 2 ]-Glu
Прогноз биологических активностей исходного трипептида GPE (табл. 1) и его фосфинового аналога GPE(phos) (табл. 2) осуществлялся программой PASS (“Prediction of Activity Spectra for Substances”), разработанная в Институте биомедицинской химии им. В.Н. Ореховича РАМН. Она содержит более 250000 веществ с известной биологи- ческой активностью, включает более 3500 фармакологических эффектов и механизмов действия. Результаты прогноза биологической активности представлены в виде спектра биологической активности, включающих список активностей и вероятностей: Ра - «быть активным», Рi - «быть неактивным».
Таблица 1. Пр сходного трипептида GPE програм мой “Prediction of
NH
O
O
O
HN
OH
OH
|
0,905 |
0,004 |
e inhibitor |
|
0,898 |
0,004 |
or |
|
, |
, |
X-Pro dipeptidase inhibitor |
|
0,837 |
0,014 |
Methylenetetrahydrofolate reductase (NADPH) inhibitor |
|
0,835 |
0,002 |
Saccharolysin inhibitor |
|
0,819 |
0,005 |
Analeptic |
|
0,815 |
0,004 |
Antihypoxic |
|
0,804 |
0,032 |
Phobic disorders treatment |
|
0,800 |
0,009 |
Protein-disulfide reductase (glutathione) inhibitor |
|
0,774 |
0,004 |
Pyroglutamyl-peptidase II inhibitor |
|
0,763 |
0,020 |
Glutamate-5-semialdehyde dehydrogenase inhibitor |
|
0,756 |
0,007 |
Limulus clotting factor C inhibitor |
|
0,752 |
0,007 |
Methylamine-glutamate N-methyltransferase inhibitor |
|
0,728 |
0,003 |
Meprin A inhibitor |
|
0,727 |
0,022 |
Acylcarnitine hydrolase inhibitor |
|
0,721 |
0,004 |
Acrosin inhibitor |
|
0,712 |
0,003 |
Catalase inhibitor |
|
0,699 |
0,015 |
Dimethylargininase inhibitor |
|
0,698 |
0,023 |
Fibrinolytic |
|
0,682 |
0,010 |
Pyroglutamyl-peptidase I inhibitor |
|
0,659 |
0,003 |
Bontoxilysin inhibitor |
|
0,649 |
0,011 |
Renal tissue kallikrein inhibitor |
|
0,649 |
0,005 |
Tripeptidyl-peptidase I inhibitor |
|
0,646 |
0,057 |
Nootropic |
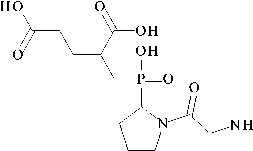
Таблица 2. Про стей фосфинового аналога GPE(phos) программой “Predictio ances”
|
0,851 |
0,010 |
ehyde dehydrogenase inhibitor |
|
0,734 |
0,005 |
Stroke treatment |
|
0,711 |
0,014 |
Immunostimulant |
|
0,690 |
0,056 |
CDP-glycerol glycerophosphotransferase inhibitor |
|
0,661 |
0,023 |
Phosphatase inhibitor |
|
0,614 |
0,001 |
N-Acetylated alpha-linked acidic dipeptidase inhibitor |
|
0,591 |
0,127 |
Phobic disorders treatment |
|
0,536 |
0,087 |
Antiischemic, cerebral |
|
0,514 |
0,033 |
Anticonvulsant |
Результаты прогноза биологической активности исходного трипептида GPE и его фосфинового аналога GPE(phos), осуществленного при помощи программного пакета PASS, показал заметное изменение биологической активности при замене пептидной связи в молекуле трипептида на метиленфосфорильный фрагмент.
Также была использована программа GUSAR (“General Unrestricted StructureActivity Relationships”), позволившая дать прогноз по острой токсичности для крыс (LD50 мг/кг) для полученного соединения GPE(phos) соединений по сравнению с исходным трипептидом GPE (табл. 3).
Таблица 3. Прогноз по острой токсичности для крыс (LD50 мг/кг) для полученного соединения GPE(phos) соединений по сравнению с исходным трипептидом GPE
|
ВБ LD50 (мг/кг) |
ВВ LD50 (мг/кг) |
ПО LD50 (мг/кг) |
ПК LD50 (мг/кг) |
|
|
GPE |
1340 |
1968 |
3894 |
1498 |
|
GPE(phos) |
456 |
732 |
2233 |
256,6 |
QSAR модели были разработаны для порядка 10000 соединений, протестированных на крысах по четырем видам токсичности – пероральной (ПО), внутривенной (ВВ), внутрибрюшинной (ВБ) и подкожной (ПК). Для оценки острой токсичности для описания структур химических соединений в программе используются дескрипторы многоуровневых атомных окрестностей (MNA – Multilevel Neighborhoods of Atoms) и количественных атомных окрестностей (QNA – Quantitative Neighborhoods of Atoms). В GUSAR для построения моделей используется алгоритм самосогласованной регрессии (SCR).
Согласно классификации острой токсичности Организации экономического сотрудничества и развития (OECD) оба соединения являются нетоксичными или малотоксичными по всем способам введения (4 и 5 классы токсичности). Однако важно отметить, что наблюдается некоторое увеличение токсичности GPE(phos) по всем способам введения.
Заключение. Таким образом основным результатом настоящей работы стала апробация нового синтетического подхода к получению физиологически активных веществ в ряду соединений пептидного характера, обладающих активностью, путем замены пептидной связи [C(O)NH] изо-стерным метиленфосфорильным фрагментом [P(O)CH 2 ] с обязательным сохранением исходной аминокислотной последовательности. В ходе настоящей работы был получен псевдо-пептид Gly-Pro-[P(O)(OH)CH 2 ]-Glu, фосфиновый аналог известного физиологически-активного трипептида Gly-Pro-Glu, а также были осуществлены прогноз и относительное сравнение биологической активности и токсичности исходного трипептида и его фосфинового аналога.
Список литературы Фосфиновая модификация трипептида GPE и моделирование его свойств
- Sara V.R., Carlsson-Skwirut C., Bergman T., Jörnvall H., Roberts P.J., Crawford M., Hakansson L.N., Civalero I., Nordberg A. Identification of Gly-Pro-Glu (GPE), the aminoterminal tripeptide of insulin-like growth factor 1 which is truncated in brain, as a novel neuroactive peptide. Biochem Biophys Res Commun. 1989 Dec 15;165(2):766-71.
- Nilsson-Håkansson L., Civalero I., Zhang X., Carlsson-Skwirut C., Sara V.R., Nordberg A. Effects of IGF-1, truncated IGF-1 and the tripeptide Gly-Pro-Glu on acetylcholine release from parietal cortex of rat brain. Neuroreport. 1993 Sep; 4(9): 1111-4.
- Saura J., Curatolo L., Williams C.E., Gatti S., Benatti L., Peeters C., Guan J., Dragunow M., Post C., Faull R.L., Gluckman P.D., Skinner S.J. Neuroprotective effects of Gly-Pro-Glu, the N-terminal tripeptide of IGF-1, in the hippocampus in vitro. Neuroreport. 1999 Jan 18; 10(1): 161-4.
- Aguado-Llera D., Martín-Martínez M., García-López M.T., Arilla-Ferreiro E., Barrios V. Gly-Pro-Glu protects beta-amyloid-induced somatostatin depletion in the rat cortex. Neuroreport. 2004 Aug 26; 15(12): 1979-82.
- Alonso De Diego S.A., Muñoz P., González-Muñiz R., Herranz R., Martín-Martínez M., Cenarruzabeitia E., Frechilla D., Del Río J., Jimeno M.L., García-López M.T. Analogues of the neuroprotective tripeptide Gly-Pro-Glu (GPE): synthesis and structure-activity relationships. Bioorg Med Chem Lett. 2005 May 2; 15(9): 2279-83.


