Фотодинамически активные вещества индуцируют устойчивость растения огурца (Cucumis sativus L.) к оливковой пятнистости
Автор: Пасечник Т.Д., Лапикова В.П., Романова Т.С., Аверьянов А.А.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Иммунитет и защита растений
Статья в выпуске: 3 т.60, 2025 года.
Бесплатный доступ
Индуцированная болезнеустойчивость растений перспективна для практического использования, поскольку задействует их внутренние ресурсы и позволяет снизить нагрузку на окружающую среду. Показано, что вещества, влияющие на про-/антиокислительный баланс, участвуют в механизме системной приобретенной устойчивости. Подобной способностью обладают и фотодинамически активные вещества. В настоящей работе впервые установлено, что относящиеся к этой группе соединений метиленовый синий, бенгальский розовый и 2-меркапто-пиридин-N-оксид защищают растения огурца от оливковой пятнистости (возбудитель Cladosporiumcucumerinum Ell. et Arth.), как и известные индукторы системной устойчивости (K2HPO4 и β-аминомасляная кислота). Цель - изучить защитное действие фотодинамически активных веществ в отношении оливковой пятнистости, сравнить его с таковым у известных индукторов болезнеустойчивости и исследовать участие активных форм кислорода в осуществлении механизма индукции. Были испытаны известные и предполагаемые индукторы болезнеустойчивости - K2HPO4, БАМК (b-аминомасляная кислота), фотодинамические красители бенгальский розовый (БР) и метиленовый синий (МС), светозависимый источник гидроксильного радикала 2-МПНО (2-меркапто-пиридин-N-оксид). Растения огурца ( Cucumis sativus L.) восприимчивого к оливковой пятнистости сорта Феникс выращивали в натуральной почве в климатической камере Conviron EF7 («Conviron», Канада). На стадии 1-го настоящего листа растения обрабатывали растворами исследуемых веществ (10 капель на лист, контроль - вода). Примерно через 2 нед подсчитывали долю капель, давших ожоги. Через 6-8 сут после обработки у половины растений во всех вариантах следующий, 2-й лист заражали суспензией спор Cladosporium cucumerinum штамма C5 в концентрации 105 спор/мл. У другой половины растений на 2-й лист наносили капли воды (10 капель по 20 мкл). Растения помещали в темный термостат (Смоленское СКТБ СПУ, Россия) при 18 °С на 22-24 ч. Через 6-8 сут учитывали симптомы. Для получения диффузатов 1-го листа на него наносили капли воды или исследуемых растворов (10 капель по 20 мкл каждая). Через 24 ч их удаляли. В те же самые места помещали такие же капли дистиллированной воды. Еще через 1 сут их собирали, центрифугировали 10 мин при 8000 g, использовали супернатант. Для получения диффузатов незараженных листьев на них наносили воду, для получения диффузатов зараженных листьев - суспензию спор. Споровые диффузаты получали из суспензии спор. Образование супероксидного радикала в диффузатах определяли по окислению экзогенного адреналина. Для учета прорастания спор воду, диффузаты или тестируемые растворы (по 40 мкл) смешивали с 5 мкл суспензии (3,5×104 спор/мл) и 5 мкл воды. Материал инкубировали в темноте 24 ч в климатической камере, затем фиксировали этанолом (1-2 капли на лунку) и подсчитывали проросшие споры. Чтобы судить об участии АФК в механизме действия диффузатов на споры, вместо 5 мкл воды в диффузаты добавляли либо антиоксиданты (50 мкг/мл супероксиддисмутазы или 50 мкг/мл каталазы), либо перехватчики гидроксильного радикала (10 мМ маннит или 1 мМ формиат натрия). Затем так же подсчитывали проросшие споры. При исследовании влияния света на прорастание спор смесь диффузатов со спорами освещали в течение 1 ч при 90 мкмоль·м-2·с-1, затем инкубировали 23 ч в темноте. Для предварительной оценки природы веществ, выделяемых листьями, проверяли, как кипячение диффузата (1 ч на водяной бане) влияет на прорастание спор. Также исследовали влияние предполагаемых индукторов на прорастание спор. Растворы препаратов (45 мкл) смешивали с 5 мкл суспензии (3,5×104 спор/мл) и проращивали в тех же условиях на свету и в темноте. Установлено, что испытанные вещества локально повреждали 1-й лист. Степень развития болезни на 2-м листе в вариантах с обработкой была меньше, что говорит об индукции системной устойчивости. Степень подавления болезни при обработке фотосенсибилизаторами была примерно такой же, как при обработке известными индукторами. На 1-м листе образование супероксида при обработке фотосенсибилизаторами и известными индукторами было выше, чем при обработке водой. Эти же обработки стимулировали образование супероксида как в незараженных, так и в зараженных 2-х листьях. Диффузаты незараженных листьев необработанных растений стимулировали прорастание спор относительно прорастания в воде. БР, МС, K2HPO4 и БАМК снижали стимуляцию, 2-МПНО придавал фунгитоксичность. Диффузаты зараженных листьев необработанных растений прорастание не стимулировали. При обработках исследованными веществами прорастание в диффузатах снижалось (за исключением K2HPO4), что указывало на выделение зараженными растениями фунгитоксичных веществ. Поскольку экзогенные антиоксиданты не влияли на прорастание спор в диффузатах листьев, действие экзометаболитов реализуется не через АФК. Свет усиливал фунгитоксичность, следовательно, некоторые их этих экзометаболитов - фотосенсибилизаторы.
Индукция болезнеустойчивости растений, активные формы кислорода, фотосенсибилизаторы
Короткий адрес: https://sciup.org/142246211
IDR: 142246211 | УДК: 635.63:632 | DOI: 10.15389/agrobiology.2025.3.503rus
Involvement of reactive oxygen species in resistance of cucumber (Cucumis sativus L.) plants to cucumber scab induced by photodynamically active substances
Induced disease resistance of plants is promising for practical use, since it involves internal plant resources and allows reducing the load on the environment. substances affecting the pro/antioxidant balance are shown to participate in the mechanism of systemic acquired resistance. Photodynamically active substances also have a similar ability. This work demonstrates for the first time the ability of photodynamically active substances (methylene blue, Bengal rose and 2-mercapto-pyridine-N-oxide) to protect cucumber plants like the known inducers of systemic resistance (K2HPO4 and β-aminobutyric acid). The objective is to study the protective action of photodynamically active substances on cucumber scab, compare it with that of the known disease resistance inducers and investigate the participation of active oxygen species in the implementation of the induction mechanism. Known and suspected disease resistance inducers were tested: K2HPO4, BABA (β-aminobutyric acid), photodynamic dyes Bengal rose (BR) and methylene blue (MB), light-dependent source of hydroxyl radical 2-MPHO (2-mercapto-pyridine-N-oxide). Cucumber plants ( Cucumis sativus L.) of the Phoenix variety susceptible to cucumber scab were grown in natural soil in a Conviron EF7 climate chamber (Conviron, Canada). At the stage of the 1st true leaf, the plants were treated with solutions of the studied substances (10 drops per leaf, water as control). After approximately 2 weeks, the proportion of drops that caused burns was calculated. 6-8 days after treatment, in half of the plants in all variants, the next, 2nd leaf was infected with a suspension of Cladosporium cucumerinum Ell. et Arth. strain C5 spores at a concentration of 105 spores/ml. In the other half of the plants, drops of water (10 drops of 20 µl) were applied to the 2nd leaf. The plants were placed in a dark thermostat (Smolensk SKTB SPU, Russia) at 18 °С for 22-24 h. Symptoms were counted 6-8 days later. To obtain diffusates of the 1st leaf, drops of water or the studied solutions (10 drops of 20 μl each) were applied to it. They were removed after 24 h. The same drops of distilled water were put in the same points. After another 24 h, they were collected, centrifuged for 10 min at 8000 g, and the supernatant was used. To obtain diffusates of uninfected leaves, water was applied to them. The spore suspension was applied on leaves to obtain diffusates of infected ones. Spore diffusates were obtained from the spore suspension. The formation of superoxide radical was analyzed in diffusates by the oxidation of exogenous adrenaline.To assess spore germination, water, diffusates, or test solutions (40 μl each) were mixed with 5 μl of suspension (3.5×104 spores/ml) and 5 μl of water. The material was incubated in the dark for 24 h in a climatic chamber, then fixed with ethanol (1-2 drops per well), and germinated spores were counted. To assess the involvement of ROS in the action of diffusates on spores, antioxidants were added instead of 5 μl of water, the 50 μg/ml of SOD or 50 μg/ml of catalase, or hydroxyl radical scavengers, the 10 mM mannitol or 1 mM sodium formate. Then, germination was counted in the same way. To study effect of light on germination, a mixture of diffusates with spores was illuminated for 1 h at 90 μmolłm-2·s-1 and then incubated for 23 h in the dark. For a preliminary assessment of the nature of substances secreted by the leaves, we checked how boiling the diffusate (1 h in a water bath) affects spore germination. The effect of putative inducers on spore germination also was studied. The preparation solutions (45 μl) were mixed with 5 μl of suspension (3.5×104 spores/ml) and germinated under the same conditions, in the light and in the dark. It was found that the tested substances locally damaged the 1st leaf. The degree of disease development on the 2nd leaf in the variants with treatment was less, which indicates the induction of systemic resistance. The degree of disease suppression during treatment with photosensitizers was approximately the same as during treatment with known inducers. On the 1st leaf, superoxide formation during treatment with photosensitizers and known inducers was higher than during treatment with water. The same treatments stimulated superoxide formation in both uninfected and infected second leaves. Diffusates of uninfected leaves of untreated plants stimulated spore germination relative to germination in water. BR, MS, K2HPO4 and BAMK reduced stimulation, 2-MPNO imparted fungitoxicity. Diffusates of infected leaves of untreated plants did not stimulate germination. When treated with the studied substances, germination in diffusates decreased (except for K2HPO4), which indicated the release of fungitoxic substances by the infected plants. Since exogenous antioxidants did not affect spore germination in leaf diffusates, the action of exometabolites is not realized through ROS.
Текст научной статьи Фотодинамически активные вещества индуцируют устойчивость растения огурца (Cucumis sativus L.) к оливковой пятнистости
Активный кислород играет важную роль в реакциях фитоиммунитета, в том числе в индуцированной болезнеустойчивости (1). Выделяют два типа защитных реакций. Один из них — PAMP-инициируемый иммунитет (pathogen-associated molecular patterns-triggered, или pattern-triggered immunity, PTI), который включается в ответ на микробные паттерны (MAMP или PAMP). К его механизмам относятся укрепление клеточных стенок, фосфорилирование, в результате которого остаток фосфорной кислоты передается на рецептор, активируя ассоциированный с ним фермент, образование фитоалексинов и белков, связанных с патогенезом (PR-белков), образование активных форм кислорода (АФК). При другом типе ответа микробные эффекторы узнаются внутриклеточными рецепторами и запускают активируемый эффектором иммунитет (effector-triggered immunity, ETI). Это сопровождается реакцией сверхчувствительности (hypersensitive response, HR) в месте заражения. Первый путь индуцируется салициловой кислотой и действует против биотрофных и гемибиотрофных патогенов, второй опосредован жасмоновой кислотой и этиленом и действует против некротро-фов (2-4).
Индукторы устойчивости — это вещества естественного и синтетического происхождения, активирующие защитные механизмы. В настоящее время известны индукторы устойчивости различной природы (5). В частности, это могут быть метаболиты патогенов (олигосахариды, пептиды). Салициловая кислота (СК) обеспечивает устойчивость пшеницы к Fusarium (6), метилжасмонат — к нематодам и некротрофным патогенам. Примерами химических индукторов могут служить адипиновая и гексановая кислоты. Ксенобиотик в -аминомасляная кислота (БАМК) известна как индуктор против биотрофных и некротрофных патогенов (7, 8). Фосфат способен индуцировать устойчивость как при обработке листьев (9), так и при внесении в почву (10). Устойчивость также может быть индуцирована некоторыми белками (11).
Важную роль в системной устойчивости играет активный кислород (12). Перекись водорода, супероксидный и гидроксильный радикалы — это короткоживущие и цитотоксичные соединения, которые постоянно образуются в клетках и содержатся в клеточных компартментах (в хлоропластах, митохондриях, пероксисомах, клеточных стенках и т.д.). Образование АФК — универсальная неспецифическая реакция на фитопатогены и стрессовые факторы. АФК могут оказывать прямое действие на патоген, участвовать в лигнификации клеточной стенки, реакции сверхчувствительности, перекисном окислении липидов. Также они служат сигнальными и регуляторными молекулами, способствующими формированию адаптивных механизмов и повышению устойчивости растений (1, 13).
Взаимодействие патогена и хозяина начинается в инфекционной капле. Апопластные активные формы кислорода могут образовываться при 504
узнавании микроорганизмов растением и быть сигналом к системной активации реакций фитоиммунитета, в том числе вторичного окислительного взрыва, синтеза фитоалексинов и других веществ, подавляющих развитие патогена. Окислительный взрыв можно также вызвать искусственно посредством обработки растения веществами, активирующими кислород.
Свет — важный фактор для жизни растений (14), который влияет на развитие патогена и устойчивость растения-хозяина (15, 16), а также на антимикробное действие некоторых пестицидов и растительных метаболитов (17). Ранее мы показали, что фотодинамические красители (18) индуцируют устойчивость риса к пирикуляриозу. Их защитное действие связано с выделением в инфекционную каплю фунгитоксических веществ и образованием АФК. Отметим, что потенциал фотосенсибилизаторов как индукторов болезнеустойчивости малоизучен.
В настоящей работе впервые установлено, что фотодинамически активные вещества (метиленовый синий, бенгальский розовый и 2-меркапто-пиридин-К-оксид) защищают растения огурца от оливковой пятнистости, как и известные индукторы системной устойчивости (K 2 HPO 4 и р -амино-масляная кислота).
Цель — изучить защитное действие фотодинамически активных веществ в отношении оливковой пятнистости огурца, сравнить его с таковым у известных индукторов болезнеустойчивости и исследовать участие активных форм кислорода в механизме индукции защитных реакций растения.
Методика. В лабораторных тестах (Московская обл., 2015-2022 годы) использовали штамм Cladosporium cucumerinum Ell. et Arth. C5, полученный из Всероссийского НИИ селекции и семеноводства овощных культур. Штамм сохраняется в Центре коллективного пользования Государственная коллекция фитопатогенных микроорганизмов и сортов-идентификаторов (дифференциаторов) патогенных штаммов микроорганизмов. Споры штамма С5 смывали с культуры, выращенной на картофельно-глюкозном агаре (КГА), и разбавляли до нужной концентрации (105 спор/мл).
Растения огурца ( Cucumis sativus L.) восприимчивого к оливковой пятнистости сорта Феникс (19) выращивали в натуральной почве в климатической камере Conviron EF7 («Conviron», Канада) при 12-часовом освещении Na-люминесцентными лампами мощностью 60 В (110-160 мкмоль • м - 2 •с - 1), температуре 26 ° C днем и 18 ° С ночью, влажности 60 %.
На стадии 1-го настоящего листа (14-17-е сут) растения в климатической камере обрабатывали растворами исследуемых веществ (10 капель на лист, каждая по 10 мкл, контроль — вода). Примерно через 2 нед подсчитывали долю (%) капель, давших ожоги. Были испытаны известные и предполагаемые индукторы болезнеустойчивости — K 2 HPO 4 («ДиаМ», Россия), БАМК ( в -аминомасляная кислота, beta-amino butyric acid, BABA, «Sigma», США), фотодинамические красители бенгальский розовый (БР, «Serva», Канада) и метиленовый синий (МС, «Sigma», США), а также светозависимый источник гидроксильного радикала 2-МПНО (2-меркапто-пиридин-N-оксид, 2-mercaptopyridine-N-oxide, sodium salt, «Aldrich», США) (20).
Через 6-8 сут после обработки у одной половины растений во всех вариантах следующий, 2-й лист заражали суспензией спор C. cucumerinum штамма C5 в концентрации 105 спор/мл (10 капель по 20 мкл). У другой половины растений на 2-й лист наносили капли воды (10 капель по 20 мкл).
Растения помещали в темный термостат (Смоленское СКТБ СПУ, Россия) при 18 °С на 22-24 ч для создания условий, благоприятствующих заражению.
Для наблюдения за развитием симптомов зараженные растения возвращали в климатическую камеру. Через 6-8 сут после заражения (14-16 сут после обработки) учитывали симптомы. На зараженном 2-м листе подсчитывали долю капель, давших некротические инфекционные пятна (сильная восприимчивость, S, балл 3), хлоротические пятна (слабая восприимчивость, MS, балл 2) и не оставивших пятен (устойчивость, R, балл 1).
Степень развития болезни подсчитывали по общепринятой формуле (21): R = ( ^ а х b)/(N х K), где ^ а х b — сумма произведений числа больных растений (а) на балл поражения (b), N — общее число растений; К = 3 — высший балл учетной шкалы.
Для получения диффузатов 1-го листа на него наносили капли воды или исследуемых растворов (10 капель по 20 мкл каждая). Через 24 ч их удаляли фильтровальной бумагой. В те же самые места помещали такие же капли дистиллированной воды. Еще через 1 сут их собирали, объединяли в пробирках по вариантам, центрифугировали (Jouan BR4i, «Jouan», Франция) 10 мин при 8000 g, использовали супернатант.
Для получения диффузатов незараженных листьев на них наносили воду, для получения диффузатов зараженных листьев — суспензию спор. Споровые диффузаты получали из суспензии спор. Ее капли (каждая по 20 мкл, 10 5 спор/мл) инкубировали 24 ч в пластиковых чашках Петри в том же термостате. Капли собирали через 24 ч после нанесения, центрифугировали в том же режиме.
Концентрацию образовавшегося супероксидного радикала в диффу-затах оценивали по окислению экзогенного адреналина, продукт которого имеет максимум оптической плотности при X = 480 нм (22). В лунке 384-луночного планшета (Microplate 384 well, F-bottom, «Greiner Bio-One», Германия) смешивали 35 мкл воды или диффузата, 5 мкл 20 мМ калий-фосфатного буфера (рН 8,2) и 5 мкл воды или супероксиддисмутазы (СОД, бычий эритрокупреин, 4,47 Ед/мг, «Sigma-Aldrich», Германия, EC 1.15.1.1). Реакцию запускали добавлением 5 мкл 1 мМ адреналина («Sigma-Aldrich», Германия) в кислой (рН 2,0) воде, что доводило pH смеси до 7,8. После 60-минутной инкубации при 25 ° С измеряли оптическую плотность при X = 480 нм (А 480 ) на спектрофотометре Benchmark Plus («Bio-Rad», США). Из А 480 диффузатов вычитали А 480 воды (для учета автоокисления). Биологическим контролем служил показатель А 480 диффузатов листьев, обработанных водой.
Для учета прорастания спор воду, диффузаты или тестируемые растворы (по 40 мкл) смешивали с 5 мкл суспензии (3,5х104 спор/мл) и 5 мкл воды в лунке 96-луночного планшета Cellstar («Greiner Bio-One», Германия). Материал инкубировали в темноте 24 ч в климатической камере, затем фиксировали этанолом (1-2 капли на лунку) и подсчитывали проросшие споры (в 4-кратной повторности по 100 спор) под инвертированным микроскопом Diavert Inverted Research Microscope («Leitz», Германия).
Чтобы судить об участии АФК в механизме фунгитоксического действия диффузатов на споры, в диффузаты вместо 5 мкл воды добавляли антиоксиданты (50 мкг/мл СОД либо 50 мкг/мл каталазы, 13200 ед/мг, «Sigma», США) или перехватчики гидроксильного радикала (10 мМ маннит, «Sigma», США, или 1 мМ формиат натрия, «Merck», Германия). Затем так же подсчитывали долю проросших спор.
При исследовании влияния света на прорастание спор смесь диффузатов со спорами освещали в климатической камере Conviron EF7 («Con-viron», Канада) в течение 1 ч при 90 мкмоль •м-2 • с-1 (такая доза сама по себе не влияла на прорастание спор), затем инкубировали там же 23 ч в темноте.
Для предварительной оценки природы веществ, выделяемых листьями, проверяли, как кипячение диффузата (1 ч на водяной бане) влияет на прорастание спор.
Также исследовали влияние предполагаемых индукторов на прорастание спор. Растворы препаратов (45 мкл) смешивали с 5 мкл споровой суспензии (3,5*104 спор/мл) и проращивали в тех же условиях на свету и в темноте.
Статистическую обработку проводили с использованием программ Microsoft Excel 2003, Statistica 6.0 («StatSoft, Inc.», США). В таблицах и на графиках приведены средние значения показателей ( M) и стандартные ошибки средних (±SEM). При оценке достоверности различий применяли t -критерий Стьюдента.
Результаты. Взаимодействия растения с использованными индукторами и патогенами начинается в слое жидкости. Обработку обычно проводят растворенными препаратами, заражение происходит во влажный период, часто после дождя или росы. Поэтому мы использовали капли жидкости, собранные с растений. В такие капли выделяются различные биологически активные вещества и их свойства характеризуют ранние стадии взаимодействия хозяин-патоген (3).
Использованные препараты вызывали ожоги 1-х листьев огурца (табл. 1). Больше всего их было при обработке K 2 HPO 4 (85 % от нанесенных капель), меньше — при обработке БАМК (23 %).
На 2-х листьях не обработанных препаратами растений развивались преимущественно инфекционные пятна совместимого типа, представляющие собой светло-коричневые некрозы. Степень развития болезни составляла 87 %. На обработанных растениях болезнь развивалась слабее. Более сильной оказалась защита в вариантах БАМК, 2-МПНО и K 2 HPO 4 .
1. Частота развития ожогов на 1-м листе и степень развития оливковой пятнистости на 2-м листе у растений огурца ( Cucumis sativus L.) сорта Феникс при обработке фотосенсибилизаторами и известными индукторами устойчивости ( M ±SEM, лабораторный опыт, 2015-2017 годы)
|
Вариант |
Ожоги, % |
Степень развития болезни, % |
|
Вода (контроль) |
87±5 |
|
|
50 мМ K 2 HPO 4 |
85±5 |
25±3* |
|
10 мМ БАМК |
23±8 |
23±2* |
|
0,02 мМ МС |
52±9 |
31±5* |
|
0,02 мМ БР |
50±7 |
35±2* |
|
1 мМ 2-МПНО |
59±8 |
17±3* |
Примечание. БАМК — в -аминомасляная кислота, МС — метиленовый синий, БР — бенгальский розовый, 2-МПНО — меркаптопиридин-К-оксид. Средние значения в каждом независимом эксперименте были получены из 6-8 аналитических повторов и использованы в качестве повторов в статистических тестах ( n = 4).
* Различия между контрольными и обработанными растениями статистически значимы при p < 0,01.
Следовательно, помимо того, что БАМК (23) и K 2 HPO 4 (9) защищают растения от многих болезней, они системно защитили огурцы от оливковой пятнистости. Такая способность показана и для фотосенсибилизаторов на примере риса (18). Механизм защитного действия этих веществ на огурце не исследован.
В диффузатах 1-го листа в контроле наблюдалось СОД-зависимое окисление адреналина. В случае испытанных веществ образование супероксида было более интенсивным. Наименьший эффект оказывала БАМК (рис. 1), где число ожогов было меньше. Таким образом, локальные повреждения листьев сопровождались окислительным взрывом, который мог быть сигналом для индукции устойчивости.
На 2-м листе и в диффузатах спор также наблюдалось образование супероксида (рис. 2). Без заражения C. cucumerinum оно было выше при обработках как фотосенсибилизаторами, так и известными индукторами. В зараженных листьях генерация супероксида становилась еще выше, в том числе после обработок. При обработке K2HPO4 в диффузатах незараженых листьев генерация О2- оказалась значительно выше, чем при обработке другими веществами. В диффузатах зараженных листьев она оставалась такой же высокой.
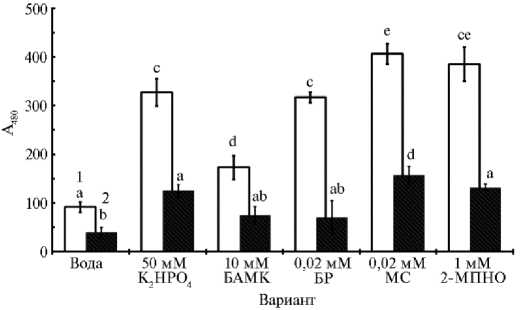
Рис. 1. Накопление супероксида у растений огурца ( Cucumis sativus L.) сорта Феникс в диффуза-тах 1-го листа после его обработки фотосенсибилизаторами и известными индукторами устойчивости: БАМК — в -аминомасляная кислота, МС — метиленовый синий, БР — бенгальский розовый, 2-МПНО — меркаптопиридин-N-оксид; 1 — без СОД (супероксиддисмутаза), 2 — СОД. Средние значения в каждом независимом эксперименте были получены из 6 аналитических повторов и использованы в качестве повторов в статистических тестах ( n = 3) ( M ±SEM, лабораторный опыт, 2019 год).
Разными буквами обозначены статистически значимые различия (р < 0,05).
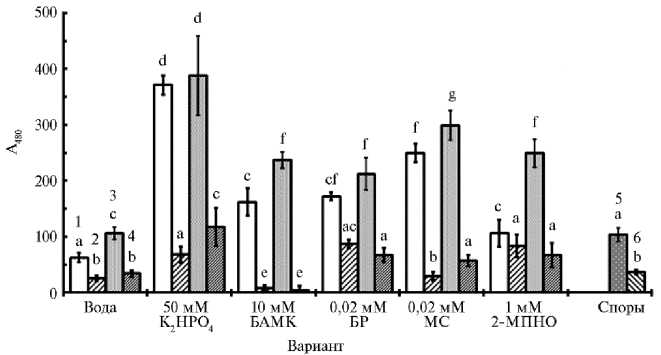
Рис. 2. Накопление супероксида у растений огурца ( Cucumis sativus L.) сорта Феникс в диффуза-тах 2-го листа при его заражения суспензией спор Cladosporium cucumerinum Ell. et Arth. штамма C5 после обработки 1-го листа фотосенсибилизаторами и известными индукторами устойчивости: БАМК — в -аминомасляная кислота, МС — метиленовый синий, БР — бенгальский розовый, 2-МПНО — меркаптопиридин-N-оксид; 1 — здоровые листья, без СОД (супероксиддисмутаза), 2 — незараженные листья, СОД, 3 — зараженные листья, без СОД, 4 — зараженные листья, СОД, 5 — споры, без СОД, 6 — споры, СОД. Средние значения в каждом независимом эксперименте были получены из 6 аналитических повторов и использованы в качестве повторов в статистических тестах ( n = 3) ( M ±SEM, лабораторный опыт, 2018 год).
Разными буквами обозначены статистически значимые различия (р < 0,05).
Таким образом, испытанные соединения вызывали окислительный взрыв и в здоровом, и в зараженном листе. В то же время обработки снижали степень развития болезни (см. табл. 1). Это может быть проявлением прайминга, который становится реакцией организма на стресс. Прайминг включает эпигенетические, клеточные, гормональные и другие фенотипические изменения, не затрагивающие генетической информации в ДНК (24, 25). Возможно, использованные вещества, повреждая растения за счет окислительного взрыва, вызывают стресс, который модифицирует последующие реакции. Так растения подготавливаются к будущему стрессу (например, к заражению).
Представляет интерес выяснить, связано ли ослабление развития болезни, вызванное фотосенсибилизаторами, с выделением фунгитокси-ческих веществ в инфекционную каплю и зависит ли эта фунгитоксич-ность от АФК.
Диффузат здоровых листьев огурца стимулировал прорастание спор (примерно на треть по сравнению с прорастанием в воде). Диффузат спор стимулировал незначительно. В случае зараженных листьев стимуляции не наблюдали. Известно, что некоторые грибы нуждаются в дополнительных источниках питания. Возможно, таким образом растения могут регулировать ранние стадии развития гриба (прорастение спор, развитие апрес-сориев и внедрение) (26).
Если 1-й лист обрабатывали K 2 HPO 4 , БАМК, БР или МС, стимуляция прорастания спор в диффузате незараженного листа была меньше по сравнения с прорастанием в воде, а при обработке 2-МПНО диффузаты незараженных листьев становились токсичными. При заражении обработки ВАВА, БР, МС или 2-МПНО делали диффузат более фунгитоксичным. При обработке K 2 HPO 4 сохранялась небольшая стимуляция прорастания (рис. 3). Возможно, в последнем случае устойчивость не связана с фунгитоксиче-скими веществами в инфекционной капле, а реализуется внутри тканей.
Освещение не влияло на прорастание спор в воде и диффузате спор (см. рис. 3). При обработке 1-го листа водой оно снизило стимуляцию прорастания в диффузате 2-го незараженного листа и придало слабую токсичность диффузату зараженного. После обработки K 2 HPO 4 стимуляция прорастания в диффузате незараженного листа на свету усиливалась, в диффузате зараженного мы стимуляцию не наблюдали. В случае БАМК свет снизил прорастание спор в диффузате здорового листа и усилил токсичность диффузата зараженного. При обработке БР стимуляция прорастания в диффузате незараженного листа отсутствовала, а фунгитоксичность при заражении увеличилась. При обработке МС токсичность диффузата здорового листа не изменилась, зараженного — усилилась; при обработке 2-МПНО она усилилась в обоих вариантах.
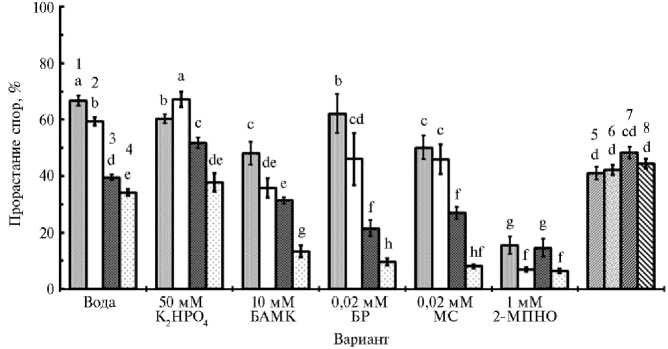
Рис. 3. Прорастание спор Cladosporium cucumerinum Ell. et Arth. штамма C5 в воде и диффузатах листьев огурца (Cucumis sativus L.) сорта Феникс и спор C. cucumerinum под влиянием света при обработке 1-го листа фотосенсибилизаторами и известными индукторами устойчивости и заражения 2-го листа суспензией спор С. cucumerinum: БАМК — в-аминомасляная кислота, МС — метиленовый синий, БР — бенгальский розовый, 2-МПНО — меркаптопиридин-Ы-оксид; 1 — здоровые листья, темнота, 2 — здоровые листья, свет, 3 — зараженные листья, темнота, 4 — зараженные листья, свет, 5 — прорастание в воде, темнота, 6 — прорастание в воде, свет, 7 — диффузат спор, темнота, 8 — диффузат спор, свет. Средние значения в каждом независимом эксперименте получены из 4 повторностей по 100 спор и использованы в качестве повторов в статистических тестах (n = 3) (M±SEM, лабораторный опыт, 2019 год).
Разными буквами обозначены статистически значимые различия (р < 0,05).
Таким образом, судя по действию света на диффузаты, в инфекционной капле присутствуют фотодинамически активные вещества. Эти вещества могут участвовать в ингибировании развития гриба на листьях.
Антиоксиданты не снижали фунгитоксичность в тех вариантах, где она проявлялась (данные не приведены), по-видимому, АФК в инфекционной капле на листьях огурца были скорее сигналом, чем токсикантом.
После кипячения диффузаты спор или здоровых листьев стимулировали прорастание спор сильнее, чем нативные. В вариантах со всеми обработками фунгитоксичность после кипячения исчезала или снижалась (табл. 2). Видимо, диффузаты содержали как термостабильные стимуляторы (например, сахара), так и термолабильные ингибиторы (белки), а результат зависел от их соотношения.
2. Прорастание спор Cladosporium cucumerinum Ell. et Arth. штамма C5 в нативных и подвергнутых кипячению диффузатах 2-го листа при его заражении суспензией спор C. cucumerinum C5 и обработке 1-го листа растений огурца ( Cucumis sativus L.) сорта Феникс фотосенсибилизаторами и известными индукторами устойчивости, а также в диффузатах спор C. cucumerinum C5 ( M ±SEM, лабораторный опыт, 2016 год)
|
Вариант обработки 1-го листа |
Инокуляция 2-го листа |
Прорастание спор в диффузате, % |
|
|
нативном |
после кипячения |
||
|
В диффузатах |
листьев |
||
|
Вода |
Здоровые |
67±2 |
81±2** |
|
Зараженные |
40±1 |
72±2** |
|
|
50 мМ K 2 HPO 4 |
Здоровые |
60±4 |
78±1** |
|
Зараженные |
52±2 |
82±3 |
|
|
10 мМ БАМК |
Здоровые |
48±4 |
67±4* |
|
Зараженные |
31±1 |
37±2* |
|
|
0,02 мМ МС |
Здоровые |
50±4 |
49±3 |
|
Зараженные |
36±1 |
67±1** |
|
|
0,02 мМ БР |
Здоровые |
27±2 |
48±2** |
|
Зараженные |
22±3 |
38±2** |
|
|
1 мМ 2-МПНО |
Здоровые |
16±3 |
33±9* |
|
Зараженные |
15±3 |
30±9* |
|
В диффузатах спор
63±1 81±1**
В воде (контроль) 41±1 42±1 Примечание. БАМК — р -аминомасляная кислота, МС — метиленовый синий, БР — бенгальский розовый, 2-МПНО — меркаптопиридин-К-оксид. Средние значения в каждом независимом эксперименте получены из 4 повторностей по 100 спор и использованы в качестве повторов в статистических тестах ( n = 3). * и ** Различия между вариантами без кипячения и с кипячением статистически значимы соответственно при р < 0,05 и р < 0,01.
Некоторые из испытанных веществ сами оказались фунгитоксич-ными (табл. 3). Они могли бы защищать от болезни и как индукторы устойчивости, и как контактные фунгициды.
Следовательно, вещества с фотодинамической активностью, а также известные индукторы вызывают образование супероксида в диффузатах, собранных с обработанных листьев. На системно защищенном листе в диффузатах обработанных растений генерация супероксида тоже была выше. Это может служить сигналом для других защитных реакций. Ранее на рисе были получены данные о влиянии экзометаболитов листьев на развитие спор гриба (18). По-видимому, потенциальные индукторы вызывали локальные повреждения листьев, сопровождавшиеся окислительным взрывом. На листьях следующего яруса наблюдался окислительный взрыв, который сопровождался выделением фунгитоксичных веществ в инфекционную каплю. По нашим данным, механизмы устойчивости огурца к оливковой пятнистости и риса к пирикуляриозу различаются. В случае пирикуля-риоза не наблюдалось стимуляции прорастания спор в диффузатах здоровых листьев необработанных растений, а токсичность диффузатов обработанных листьев снижалась антиоксидантами (18). В диффузатах листьев огурца при отсутствии обработки и заражения наблюдалась стимуляция прорастания спор гриба. Антиоксиданты не влияли на прорастание спор в зараженных вариантах. То есть действие диффузатов не было связано непосредственно с АФК.
3. Фунгитоксичность фотосенсибилизаторов и известных индукторов устойчивости для спор Cladosporium cucumerinum Ell. et Arth. штамма C5 под влиянием света ( M ±SEM, лабораторный опыт, 2021 год)
|
Среда инкубации спор |
Прорастание спор, % |
|
|
в темноте |
на свету |
|
|
Вода |
46±2 |
46±2 |
|
50 мМ K 2 HPO 4 |
6±3 |
5±2 |
|
10 мМ БАМК |
41±2 |
30±2* |
|
0,02 мМ МС |
35±3 |
3±1* |
|
0,02 мМ БР |
10±2 |
0±0* |
|
1 мМ 2-МПНО |
0±0 |
0±0 |
Примечание. БАМК — в -аминомасляная кислота, МС — метиленовый синий, БР — бенгальский розовый, 2-МПНО — меркаптопиридин-К-оксид. Средние значения в каждом независимом эксперименте получены из 4 повторностей по 100 спор и использованы в качестве повторов в статистических тестах ( n = 3). * Различия с контролем (инкубация в темноте) статистически значимы при p < 0,01.
Токсичность усиливалась при слабом освещении, что свидетельствует о выделении в инфекционную каплю фотосенсибилизаторов. Утрата фунгитоксичности после кипячения указывает на наличие ингибиторов в диффузатах, возможно, белковой природы. Увеличение процента проросших спор по сравнению с контролем (вода) после кипячения свидетельствует о том, что в инфекционную каплю могут выделяться стимуляторы прорастания (например, сахара).
В настоящее время известно много индукторов устойчивости различной природы (5). Многие организмы обладают способностью к прай-мингу, когда слабый стресс вызывает устойчивость к более сильному, причем не обязательно к тому же самому (26, 27). Процесс начинается с восприятия стимула, которым могут быть метаболиты гриба, растения или химические вещества. И системная приобретенная устойчивость (systemic acquired resistance, SAR), и индуцированная системная устойчивость (induced systemic resistance, ISR) приводят к аналогичным результатам (4).
Роль АФК во взаимоотношениях хозяин-патоген разнообразна (28). Они могут участвовать в физиологических процессах растений и патогенов (29). Генерация АФК — одна из стратегий реагирования на биотические и абиотические стрессовые факторы (25, 30, 31). При этом АФК могут быть сигнальными молекулами либо непосредственно подавлять развитие патогенов (32, 33).
Известно также, что пестициды, кроме действия через мишени, могут усиливать образование АФК, что способно вызывать окисление липидов, белков и ДНК, а также апоптоз. Некоторые пестициды активируют кислород непосредственно, передавая электрон (34). Ранее мы показали, что обработка риса известными фунгицидами — трициклазолом, фталидом и пробеназолом — стимулирует образование АФК и выделение фунгиток-сических веществ (35). Действие последних также зависит от АФК. Изучение ранних стадий развития патогена на растениях важно, поскольку оно определяет степень развития болезни. В дальнейшем, чтобы выяснить, участвуют ли АФК в механизме устойчивости на этой стадии, следует проверить влияние антиоксидантов, добавленных непосредственно в инокулюм.
Итак, обработка фотодинамически активными веществами (метиленовый синий, бенгальский розовый и 2-меркапто-пиридин-N-оксид) и известными индукторами устойчивости (K 2 HPO 4 и в -аминомасляная кислота) системно защищала растения огурца восприимчивого сорта от оливковой пятнистости. Это проявлялось в снижении степени развития болезни на листе следующего яруса. Степень подавления болезни при обработке фотосенсибилизаторами была примерно такой же, как при обработке известными индукторами. Все исследованные соединения способствовали образованию активных форм кислорода (в частности супероксида) как в обработанном, так и в системно защищенном листе. Обработка фотосенсибилизаторами или известным индуктором в -аминомасляной кислотой стимулировала выделение из листьев в инфекционную каплю фунгитоксических веществ. Некоторые из них термолабильны и проявляют светозависимую токсичность. Это приводит к подавлению развития патогена на ранних стадиях инфекционного процесса. Полученные результаты свидетельствуют о перспективности использования веществ, способствующих активации кислорода, в качестве индукторов устойчивости. Они могут быть не только индукторами, но и полифункциональными фунгицидами, оказывая как системное, так и контактное действие.
Авторы благодарят Н.В. Стацюк (ВНИИФ) за помощь в статистической обработке и обсуждении статьи, С. Елизарову за поддержание культуры патогена, а также доктора C.J. Baker (ARS, USDA) за плодотворное сотрудничество.


