Фотодинамическое воздействие лазерного излучения с длиной волны 450 нм в комбинации с рибофлавин-мононуклеотидом на ионный гомеостаз и клеточную гибель клеток меланомы B16F10 in vitro
Автор: Гильмутдинова А.К., Юрова Е.В., Хохлова А.В., Сугак Д.Е., Саенко Ю.В.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Биологические науки
Статья в выпуске: 1, 2026 года.
Бесплатный доступ
Меланома кожи относится к числу наиболее агрессивных злокачественных новообразований, характеризующихся высоким метастатическим потенциалом и устойчивостью к химиои радиотерапии. Фотодинамическая терапия (ФДТ) считается эффективным локальным методом лечения поверхностных форм меланомы благодаря ее способности индуцировать селективную клеточную гибель с минимальным повреждением окружающих тканей. В качестве потенциального фотосенсибилизатора для ФДТ в последнее время все чаще рассматривается рибофлавин, отличающийся природным происхождением и низкой токсичностью. Цель – оценить влияние лазерного излучения с длиной волны 450 нм и рибофлавина, а также их сочетанного применения на внутриклеточную концентрацию ионов натрия, калия и кальция, а также на клеточную гибель в культуре клеток меланомы B16F10. Материалы и методы. Клетки меланомы B16F10 инкубировали с рибофлавином и подвергали воздействию лазерного излучения (450 нм, 4,2 Дж/см2). Оценку внутриклеточной концентрации ионов натрия, калия и кальция, а также уровней апоптоза и некроза проводили с использованием флуоресцентной микроскопии с применением ион-селективных красителей, красителей Yo-PRO и пропидия йодида. Количественный анализ выполняли на основе скорректированной интегральной флуоресценции клеток. Результаты. Лазерное излучение и рибофлавин по отдельности вызывали умеренные изменения ионного гомеостаза и показателей клеточной гибели. Комбинированное фотодинамическое воздействие приводило к выраженному нарушению ионного баланса, характеризующемуся повышением внутриклеточной концентрации Na⁺ и Ca²⁺ и снижением уровня K⁺, а также к достоверному увеличению числа флуоресцентных маркеров апоптоза и некроза, особенно через 3 ч после воздействия.
Фотодинамическая терапия, меланома, лазерное излучение, апоптоз, некроз, активные формы кислорода, ионный гомеостаз, калий, натрий, кальций
Короткий адрес: https://sciup.org/14134859
IDR: 14134859 | УДК: 616-006.81:615.849.19 | DOI: 10.34014/2227-1848-2026-1-122-133
PHOTODYNAMIC EFFECT OF 450 NM LASER RADIATION COMBINED WITH RIBOFLAVIN MONONUCLEOTIDE ON ION HOMEOSTASIS AND CELL DEATH OF B16F10 MELANOMA CELLS IN VITRO
Cutaneous melanoma is one of the most aggressive malignant neoplasms, characterized by high metastatic potential and resistance to chemotherapy and radiotherapy. Photodynamic therapy (PDT) is considered an effective local treatment for superficial melanoma due to its ability to induce selective cell death with minimal damage to surrounding tissue. Recently, riboflavin has been increasingly considered as a potential photosensitizer for PDT, due to its natural origin and low toxicity. The aim of the study is to evaluate the effect of 450 nm laser radiation, riboflavin, and their concomitant use on the intracellular concentration of sodium, potassium, and calcium ions, as well as on cell death in the B16F10 melanoma cell culture. Materials and Methods. B16F10 melanoma cells were incubated with riboflavin and exposed to laser radiation (450 nm, 4.2 J/cm2). Intracellular concentrations of sodium, potassium, and calcium ions, as well as apoptosis and necrosis levels, were assessed using fluorescence microscopy with ion-selective dyes, Yo- PRO, and propidium iodide. Quantitative analysis was performed based on corrected total cell fluorescence. Results. Laser radiation and riboflavin, when administered independenty, induced moderate changes in ion homeostasis and cell death markers. Combined photodynamic therapy resulted in a pronounced disruption of ionic balance, characterized by increased intracellular Na+ and Ca2+ concentrations and a decrease in K+ levels. Furthermore, a significant increase in fluorescent markers for apoptosis and necrosis was obsered, especially 3 hours after exposure.
Текст научной статьи Фотодинамическое воздействие лазерного излучения с длиной волны 450 нм в комбинации с рибофлавин-мононуклеотидом на ионный гомеостаз и клеточную гибель клеток меланомы B16F10 in vitro
Введение. Меланома кожи – это одна из наиболее агрессивных злокачественных опухолей, характеризующаяся значительной скоростью роста, высоким метастатическим потенциалом и выраженной лекарственной устойчивостью [1]. Несмотря на значительные успехи традиционной терапии лечение поверхностных форм меланомы остается актуальной клинической задачей, особенно на ранних стадиях, когда предпочтение отдают локализованным и малоинвазивным методам.
Одним из них является фотодинамическая терапия (ФДТ), основанная на активации фотосенсибилизатора светом определенной длины волны с последующим образованием активных форм кислорода (АФК), вызывающих окислительное повреждение и гибель опухолевых клеток [2, 3]. Преимуществами ФДТ являются высокая селективность, низкая системная токсичность и возможность локального контроля опухолевого процесса, что делает ее особенно перспективной для лечения поверхностных кожных новообразований, включая меланому [3]. Особое внимание привлекают природные фотосенсибилизаторы, обладающие хорошей биосовместимостью и высокой безопасностью.
К их числу относится рибофлавин (витамин B2) – водорастворимое соединение, активно участвующее в митохондриальном дыхании в составе коферментов – флавинмононуклеотида (FMN) и флавинадениндинуклеотида (FAD). Под воздействием синего света (~450 нм) рибофлавин эффективно генерирует АФК, включая супероксид и синглетный кислород, что приводит к развитию фототоксического эффекта [4, 5]. Более того, исследования in vitro и in vivo демонстрируют селективное накопление рибофлавина в клетках меланомы по сравнению с нормальными клетками кожи [6]. Также показано, что лазерное излучение синего диапазона (450–470 нм) самостоятельно влияет на метаболизм клеток меланомы B16F10, вызывая подавление пролиферации, митохондриальную дисфункцию и активацию апоптоза за счет генерации АФК даже без участия фотосенсибилизатора [7, 8].
В последние годы растет интерес к изучению ионного гомеостаза как одного из ключевых регуляторов клеточной гибели. Нарушение баланса ионов калия, натрия и кальция способствует запуску апоптотических и некротических сигнальных путей: потеря калия активирует каспазный каскад, а увеличение цитозольного кальция связано с открытием пор митохондриальной проницаемости [9–11].
Несмотря на наличие данных о фототокси-ческом действии синего лазерного излучения и рибофлавина остается недостаточно изученным вклад ионного дисбаланса в механизмы клеточной гибели при фотодинамическом воздействии, а также временная динамика изменений концентрации Na + , K + и Ca2+ в клетках меланомы.
Таким образом, исследование механизмов ионного дисбаланса, возникающего в ответ на лазерное и фотодинамическое воздействие, является актуальным и может способствовать поиску новых подходов к повышению эффективности ФДТ.
Цель исследования. Оценить влияние лазерного излучения с длиной волны 450 нм и рибофлавина, а также их сочетанного применения на внутриклеточную концентрацию ионов натрия, калия и кальция, а также на клеточную гибель в культуре клеток меланомы B16F10.
Материалы и методы. Эксперимент проводили на культуре клеток мышиной меланомы B16F10. Клетки содержались в инкубаторе Sanyo MCO-18AIC (Япония) при влажности 100 %, температуре 37 °C и концентрации
CO 2 5 % в культуральной среде RPMI-1640 («ПанЭко», Россия) с добавлением 10 % эмбриональной бычьей сыворотки (Biosera, Франция) и гентамицина в концентрации 80 мг/л («ПанЭко», Россия).
В исследовании использовали следующие экспериментальные группы:
-
1) контроль (без обработки);
-
2) лазерное излучение с длиной волны 450 нм;
-
3) рибофлавин-мононуклеотид (50 мкМ) без облучения;
-
4) фотодинамическое воздействие (рибофлавин + лазерное излучение).
За 24 ч до эксперимента клетки сеяли в 8-луночные слайд-флаконы (SPL Lifesciences, Южная Корея) в концентрации 50 000 клеток на ячейку. Через 24 ч среду меняли на свежую, содержащую 50 мкМ фотосенсибилизатора, в качестве которого применяли рибофлавин в форме флавинмононуклеотида («Фармстан-дарт-УфаВИТА», Россия), и инкубировали в полной темноте в течение 90 мин. Затем среду удаляли, клетки дважды промывали фосфатно-солевым буфером (PBS, pH 7,4).
Клетки подвергали воздействию синего лазерного излучения. Использовали лазерный диод 450 нм (MDL-111-450-1000 mw, Changchun New Industries Optoelectronics Tech, Китай) со следующими параметрами: мощность излучения – 4 мВт, время облучения – 15 мин, площадь пятна – 0,857 см2, плотность энергии – 4,2 Дж/см2. Плотность энергии (E, Дж/см2) лазерного излучения рассчитывается по формуле E=Pt/S, где P – средняя выходная мощность, Вт; t – время облучения, с; S – площадь облучения, см2. Облучение проводили в камере настольного инкубатора UNO H501-T (Okolab, Италия) в идентичных условиях культивирования. При воздействии на опытную ячейку контрольная закрывалась металлической фольгой для защиты. Эксперименты проводились не менее чем в 3 повторах.
В ходе эксперимента с помощью флуоресцентной микроскопии определяли концентрацию ионов кальция, натрия и калия, а также оценивали клеточную гибель сразу, через 3 ч и 24 ч после облучения. Для этого использовали красители Rhod 2 AM (кальций), ION NatriumGreen 2
AM (натрий), ION PotassiumGreen 2 AM (калий), Yo PRO 1 и йодид пропидия (PI). Конечная концентрация всех красителей составляла 1 мкМ.
Yo PRO 1 проникает в клетки с умеренно повышенной проницаемостью мембраны, характерной для ранних стадий программируемой клеточной гибели. PI проникает только в клетки с выраженным нарушением целостности мембраны, что характерно для поздних стадий клеточной гибели, включая некроз или поздний апоптоз [12]. Окрашенные Yo PRO клетки рассматривались как клетки с ранними признаками апоптотической гибели, а окрашенные PI клетки – как клетки с признаками некроза (или позднего апоптоза).
Результат окрашивания оценивали с использованием инвертированного микроскопа NikonTi-S, обработку изображений проводили в компьютерной программе ImageJ. Скорректированную интегральную флуоресценцию клетки (СИФК) рассчитывали по формуле СИФК = интегральная плотность – (площадь выделенной клетки × фоновое значение флуоресценции).
Статистическую обработку полученных данных проводили с помощью программы Microsoft Excel. Достоверность различий между количественными показателями вычисляли, используя параметрический t-критерий Стьюдента (р<0,05).
Результаты. Клеточная гибель. Воздействие лазерного излучения с длиной волны 450 нм и плотностью энергии 4,2 Дж/см2 на клетки, сенсибилизированные рибофлавином, сразу приводит к активации процессов клеточной гибели. Лазерное излучение и рибофлавин по отдельности вызывают снижение клеточной гибели, что отражает относительно высокую жизнеспособность клеток (рис. 1).
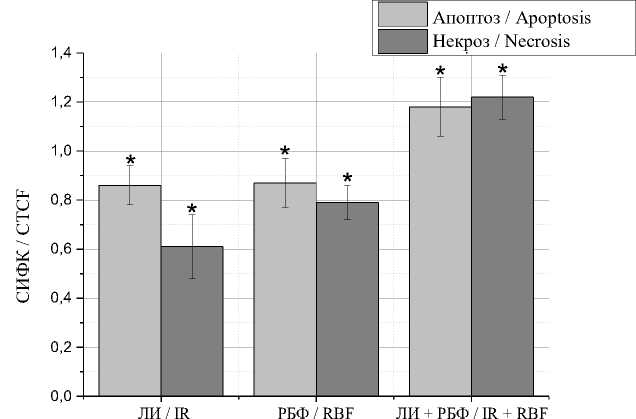
Рис. 1. Уровень апоптоза и некроза в клетках меланомы B16F10 сразу после воздействия (Ранние признаки апоптотической гибели обозначены как «апоптоз», поздние стадии клеточной гибели, включая некроз, – как «некроз»; данные представлены как отношение СИФК к контролю;
* – статистически достоверное отличие между экспериментом и контролем, p<0,05; ЛИ – лазерное излучение, РБФ – рибофлавин, ЛИ+РБФ – лазерное излучение+ рибофлавин. Далее обозначения те же)
Fig. 1. Levels of apoptosis and necrosis in B16F10 melanoma cells immediately after exposure to laser irradiation (Early signs of apoptotic death are designated as “apoptosis”, late stages of cell death, including necrosis, are designated as “necrosis”; data are presented as the ratio of corrected total cell fluorescence (CTCF) to the control; * – the differences between the experimental and control groups are statistically significant (p<0.05); LI – laser radiation, RBF – riboflavin, LI+RBF – laser radiation + riboflavin.
Hereinafter designations are the same)
Максимальная клеточная гибель наблюдается через 3 ч после воздействия (рис. 2). Лазерное излучение вызывает достоверное усиление процессов ранней апоптотической гибели в 1,49 раза, при этом изменений на поздних стадиях, включающих некроз, не выявлено. Обра- ботка рибофлавином усиливает как ранние, так и поздние проявления клеточной гибели. Наиболее выраженный апоптотический эффект наблюдается при облучении клеток, сенсибилизированных рибофлавином: уровень раннего апоптоза увеличивается более чем в 2,24 раза.
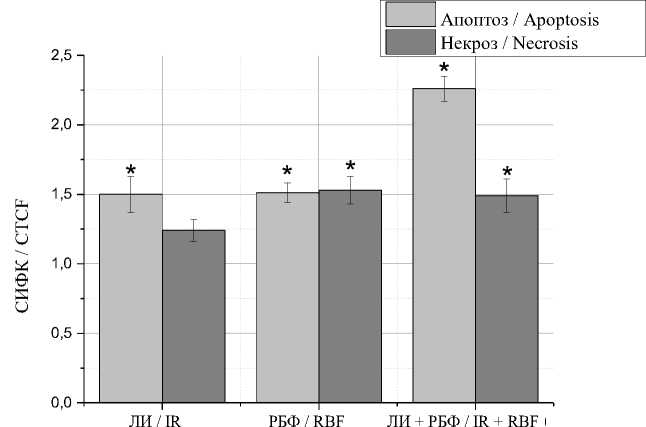
Рис. 2. Уровень апоптоза и некроза в клетках меланомы B16F10 через 3 ч после воздействия
Fig. 2. Levels of apoptosis and necrosis in B16F10 melanoma cells 3 hours after exposure to laser irradiation
Через 24 ч при воздействии только лазерного излучения не наблюдалось достоверных изменений уровня раннего апоптоза или позднего апоптоза/некроза. В то же время в группах, обработанных рибофлавином или под- вергнутых комбинированному воздействию лазера и рибофлавина, уровень раннего апоптоза оставался повышенным – в 1,39 и 1,59 раза соответственно по сравнению с контролем (рис. 3).
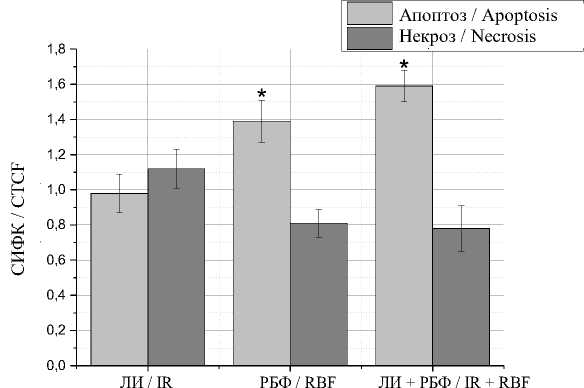
Рис. 3. Уровень апоптоза и некроза в клетках меланомы B16F10 через 24 ч после воздействия
Fig. 3. Levels of apoptosis and necrosis in B16F10 melanoma cells 24 hours after exposure to laser irradiation
Определение концентрации ионов . Фотодинамическое воздействие существенно влияет на ионный баланс в клетках меланомы B16F10.
Воздействие лазерным излучением с длиной волны 450 нм сразу вызывало повышение уровня ионов натрия в 1,75 раза по сравнению с контролем (рис. 4). Через 3 ч концентрация снижалась до 1,3-кратного значения, но оставалась выше контрольных показателей даже спустя 24 ч (в 1,2 раза). Обработка клеток рибо- флавином в концентрации 50 мкМ также приводила к увеличению содержания ионов натрия в 1,3 раза сразу после воздействия. Максимум концентрации фиксировался через 3 ч (в 2,9 раза выше контроля) с последующим восстановлением до исходного уровня к 24 ч. Комбинированное воздействие рибофлавина и лазерного излучения вызывало повышение концентрации ионов натрия в 2 раза спустя 3 ч после обработки.
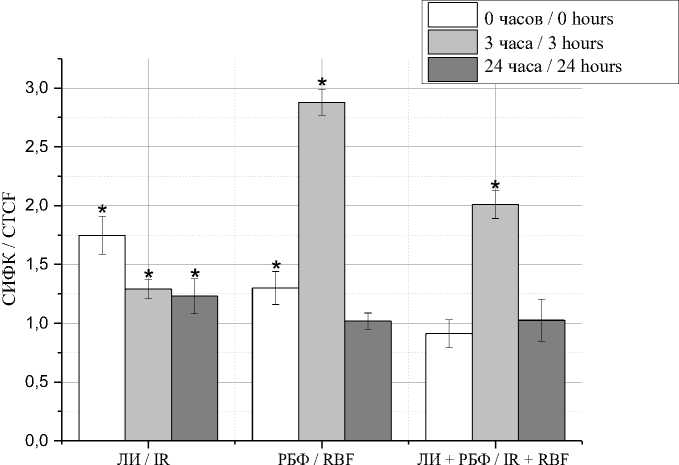
Рис. 4. Внутриклеточная концентрация ионов натрия в клетках мышиной меланомы B16F10 сразу, через 3 ч и 24 ч после воздействия
Fig. 4. Intracellular sodium ion concentration in B16F10 murine melanoma cells immediately, 3 hours and 24 hours after exposure to laser irradiation
На рис. 5 показано, что облучение синим лазером с длиной волны 450 нм сначала увеличивает концентрацию калия в 1,3 раза, затем вызывает ее значительное снижение – в 2 раза через 24 ч. При воздействии рибофлавина в качестве сенсибилизатора отмечено незначительное повышение уровня калия (в 1,2 раза сразу после добавления). Фотодинамическое воздействие лазера и рибофлавина вызывает резкие колебания калиевого баланса: быстрое повышение в 1,4 раза, значительное снижение через 3 ч и последующее повышение через 24 ч.
Концентрация кальция в клетках мышиной меланомы при воздействии лазерного излучения снижается (рис. 6). При добавлении к клеткам рибофлавина уровень кальция значительно возрастает (в 1,4 раза) с достижением максимальных показателей (в 2,2 раза) через 3 ч и снижением к 24 ч, но остается высоким относительно контрольных значений на протяжении всего времени. В фотодинамической модели комплексного воздействия лазера и рибофлавина статистически достоверное повышение концентрации кальция в 2 раза зафиксировано через 3 ч.
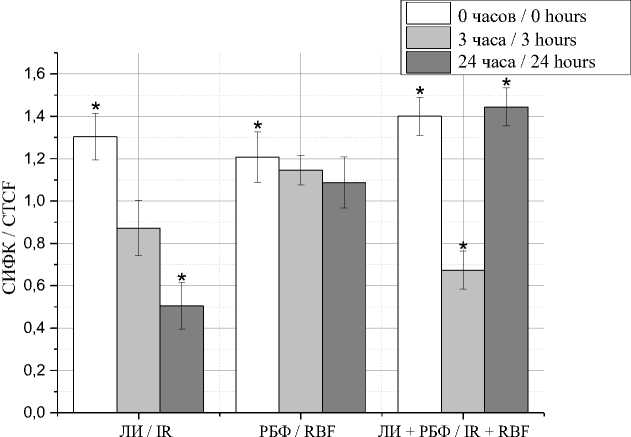
Рис. 5. Внутриклеточная концентрация ионов калия в клетках мышиной меланомы B16F10 сразу, через 3 ч и 24 ч после воздействия
Fig. 5. Intracellular potassium ion concentration in B16F10 murine melanoma cells immediately, 3 hours, and 24 hours after exposure to laser irradiation
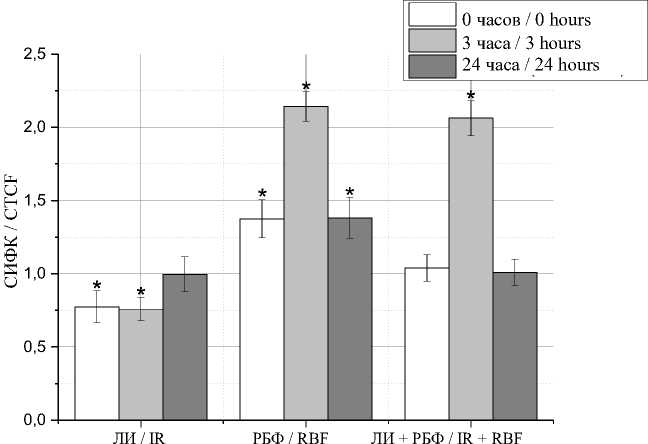
Рис. 6. Внутриклеточная концентрация ионов кальция в клетках мышиной меланомы B16F10 сразу, через 3 ч и 24 ч после воздействия
Fig. 6. Intracellular calcium ion concentration in B16F10 murine melanoma cells immediately, 3 hours, and 24 hours after exposure to laser irradiation
Обсуждение. Полученные результаты свидетельствуют о том, что низкоинтенсивное лазерное излучение синего спектра (450 нм) и рибофлавин-мононуклеотид как по отдельности, так и в комбинации оказывают влияние на ионный гомеостаз и жизнеспособность клеток меланомы B16F10 in vitro. Ранее было показано, что излучение синего спектра обладает выраженным фототоксическим эффектом в отношении клеток меланомы B16F10 даже без применения фотосенсибилизатора [13]. Наши данные подтверждают эти наблюдения и демонстрируют дополнительное усиление эффекта при использовании рибофлавина.
Известно, что облучение клеток светом синего диапазона индуцирует образование АФК за счет возбуждения эндогенных флавинов (FMN и FAD), входящих в состав митохондриальных дыхательных комплексов. Флавинсодержащие оксидазы являются одними из основных внутриклеточных хромофоров, способных поглощать излучение в синей области спектра, что приводит к восстановлению молекулярного кислорода с образованием супероксида и пероксида водорода [14–17].
Генерация АФК приводит к окислительному повреждению мембранных структур, нарушению митохондриального мембранного потенциала и активации сигнальных путей клеточной гибели [18, 19].
В настоящем исследовании воздействие лазерного излучения с длиной волны 450 нм сопровождалось умеренным ростом апопто-тической гибели, что согласуется с ранее описанными данными о проапоптотическом действии синего света при низких энергетических дозах [21, 22].
Одним из ключевых наблюдений настоящей работы является изменение внутриклеточных концентраций ионов Na + , K + и Ca2+ в ответ на лазерное и фотодинамическое воздействие.
Изменение кальциевого гомеостаза играет важную роль в реализации фотодинамического эффекта. В данном исследовании повышение концентрации ионов кальция, особенно при комбинированном воздействии лазерного излучения и рибофлавина, наблюдалось через 3 ч после обработки, что совпадало с пиком апоптотической гибели. Известно, что увеличение цитозольного кальция может быть связано с выходом Ca2+ из митохондрий и эндоплазматического ретикулума, а также с открытием пор митохондриальной проницаемости, приводящим к активации кальций-за-висимых сигнальных путей клеточной гибели [10, 23, 24]. Таким образом, выявленные кальциевые сдвиги могут рассматриваться как один из ключевых медиаторов фотодинамически индуцированного повреждения клеток меланомы.
Повышение уровня натрия, зафиксированное после облучения лазером, может указывать на деполяризацию плазматической мембраны и нарушение активности Na + /K + -АТФазы. Такие изменения характерны для ранних стадий окислительного стресса и предшествуют развитию программируемой клеточной гибели. Снижение концентрации калия, особенно выраженное через 3 ч после фотодинамического воздействия, совпадает по времени с максимальным увеличением уровня апоптотических маркеров, что позволяет предположить участие потери внутриклеточного K + в активации каспазного каскада [25].
При этом повышение внутриклеточной концентрации Ca2+ при фотодинамическом воздействии может выступать не только в роли сигнального события, но и в качестве триггера активации Ca2+-зависимых калиевых каналов. Известно, что ROS-чувствительные кальциевые каналы, включая TRPM2, при окислительном стрессе обеспечивают вход Ca2+, что в свою очередь приводит к выходу K + из клетки и снятию ингибирующего влияния калия на каспазный каскад [9, 26].
Применение рибофлавина в качестве фотосенсибилизатора представляется перспективным направлением для повышения эффективности ФДТ, особенно с учетом его избирательного накопления в меланомных клетках [6]. Полученные нами результаты также свидетельствуют о том, что рибофлавин способен снижать жизнеспособность клеток даже без фотоактивации, что может указывать на его цитотоксическое действие [26, 27]. Инкубация клеток с рибофлавином сопровождалась значительным повышением концентрации всех исследуемых ионов, особенно ионов натрия и кальция. С учетом роли рибофлавинового мо-нонуклетида как кофактора в дыхательном комплексе митохондрий можно предположить, что его избыточное накопление способно модифицировать митохондриальный потенциал, нарушать работу Na+/K+-АТФазы и Ca2+-зави- симых транспортных систем, опосредуя активацию апоптотических сигналов [19].
Комбинированное фотодинамическое воздействие лазерного излучения и рибофлавина вызывало наиболее выраженные ионные сдвиги, особенно в отношении ионов калия и кальция, а также статистически значимое увеличение уровня маркеров апоптоза и некроза. Это позволяет предположить, что накопление АФК при фотоактивации рибофлавина усиливает повреждение мембран и митохондриальных структур, что приводит к выраженному ионному дисбалансу и активации различных форм клеточной гибели. Частичное восстановление ионных градиентов в более поздние сроки наблюдения, вероятно, связано с компенсаторной активностью выживших клеток и репаративными процессами.
Заключение. В настоящем исследовании показано, что фотодинамическое воздействие лазерного излучения синего спектра (450 нм) в комбинации с рибофлавин-мононуклеоти- дом приводит к выраженным изменениям внутриклеточного ионного гомеостаза и сопровождается активацией апоптотических и некротических механизмов клеточной гибели в культуре клеток меланомы B16F10 in vitro.
Комбинированное воздействие вызывало наиболее выраженные ионные сдвиги, характеризующиеся повышением концентрации ионов натрия и кальция и снижением уровня калия, что согласуется с представлениями о роли ионного дисбаланса в реализации путей клеточной гибели. Полученные результаты указывают на участие ионных каналов в механизмах фотодинамического повреждения клеток.
Эти данные открывают возможности для целенаправленной модуляции ионных потоков, включая применение специфических блокаторов ионных каналов, с целью усиления чувствительности опухолевых клеток к фотодинамической терапии, что может быть использовано для оптимизации протоколов ФДТ в меланоме.
Работа выполнена при финансовой поддержке Министерства науки и высшего образования Российской Федерации (проект № FEUF-2025-0001 (125041105147-5)).


