Фотофизические свойства производных циклоалкил- и циклоалкенилтиофенов и 2, 2'-битиофенов
Автор: Мешковая В.В., Юдашкин А.В., Климочкин Ю.Н.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Физика и электроника
Статья в выпуске: 6-1 т.13, 2011 года.
Бесплатный доступ
В статье рассмотрены спектры поглощения и люминесценции тиофенов и 2,2'-битиофенов, содержащих циклоалкильные фрагменты, проведен анализ зависимости «структура - люминесцентные свойства
Спектры поглощения, спектры люминесценции, циклоалкил-2, 2'-битиофены
Короткий адрес: https://sciup.org/148200517
IDR: 148200517 | УДК: 539.22
Photophysical properties of the cycloalkyl- and cycloalkenylthiophenes and 2, 2'-bithiophenes derivatives
In the article we described absorption and fluorescent spectra of thiophenes and 2,2 bithiophenes with cycloalkyl and cycloalkenyl moieties, we analyzed the correlation between the structure and fluorescent spectra of this compounds.
Текст научной статьи Фотофизические свойства производных циклоалкил- и циклоалкенилтиофенов и 2, 2'-битиофенов
Люминесцентные вещества и материалы находят широкое применение в качестве добавок в ткани, пластики, чернила, лазерных красителей широкого диапазона действия, биологических маркеров [1]. Особый интерес представляют ди-замещенные 2,2’-битиофены, обладающие интенсивной люминесценцией. Разнообразные производные олиготиофенов, проявляющие полупроводниковые и электролюминесцентные свойства, применяются в электронных устройствах как хранители энергии и переносчики электронных импульсов [2]. Наличие в структуре 2,2’-битиофена в положениях 5 и 5’, характеризующие наиболее длинную цепь р-сопряжения молекулы и максимальный батохромный сдвиг, различных по электронной природе электронодонорных и электроноацепторных заместителей увеличивает фотостабильность системы и интенсивность люминесценции и повышению квантового выхода [3].
Конструирование новых органических люминофоров с использованием молекулы 2,2’-би-тиофена показал наибольшую активность атомов С5 и С5’, которые являются концевыми в нераз-ветвленной линейной цепочке, включающей четыре двойные связи [4]. Введение электронодонорного или гетероциклического и электроноа-цепторного заместителей в эти положения должно привести к появлению значительного дипольного момента в S0 и S1 π - π * состояниях и внутримолекулярного переноса заряда, увеличению силы осциллятора и батохромному сдвигу S0 и S1 π - π * перехода.
Известно, что молекула 2,2’-битиофена находится в двух конформациях – s-цис- и s-транс-, при этом показано, что s-транс-конформер обладает большим дипольным моментом. Для молекул с возможным внутренним вращением необходимо, чтобы при S0 и S1 π - π * переходе порядки межциклических связей возрастали, т.е. в S1 π - π * состоянии молекула должна быть более плоской по сравению с S0 состоянием. Это увеличивает «жесткость» молекулы и уменьшает вероятность энергетических потерь за счет внутреннего вращения. Интерес представляют производные 2,2’-битиофена, содержащие циклоалкильный либо каркасный заместитель. Реакцией Гриньяра взаимодействием 2-тиенилмагнийбромида или 5-(2,2’-битиенил)магнийбромида с циклическими кетонами получены соответствующие третичные спирты и циклоалкены, которые проформилиро-ваны в условиях реакции Вильсмейера-Хаака.
При возбуждении молекулы происходит частичная фиксация конформации циклического фрагмента, либо в виде кресла, либо в виде ванны. С уменьшением количества метиленовых групп в циклоалкильном фрагменте становится затруднительным изменение конформации, что отмечено увеличением длины волны максимума люминесценции у соединения БТ-1, по сравнению с БТ-2 и БТ-4. Наличие в соединении БТ-3 двойной С=С-связи увеличивает цепь сопряжения и смещает максимум длины волны люминесценции на 2 нм, по сравнению с третичным спиртом БТ-2.
Отмечено, что 2,2’-битиофен, содержащий адамантановый фрагмент обладает наименьшим максимумом длины волны поглощения (313,5 нм) и люминесценции (461 нм) и значительным стоксовым сдвигом. Наличие 2,2’-битиофенового фрагмента во втором положении адамантанола приводит к образованию в возбужденном состоянии внутримолекулярной водородной связи атома серы с водородом гидроксигруппы. В спектре
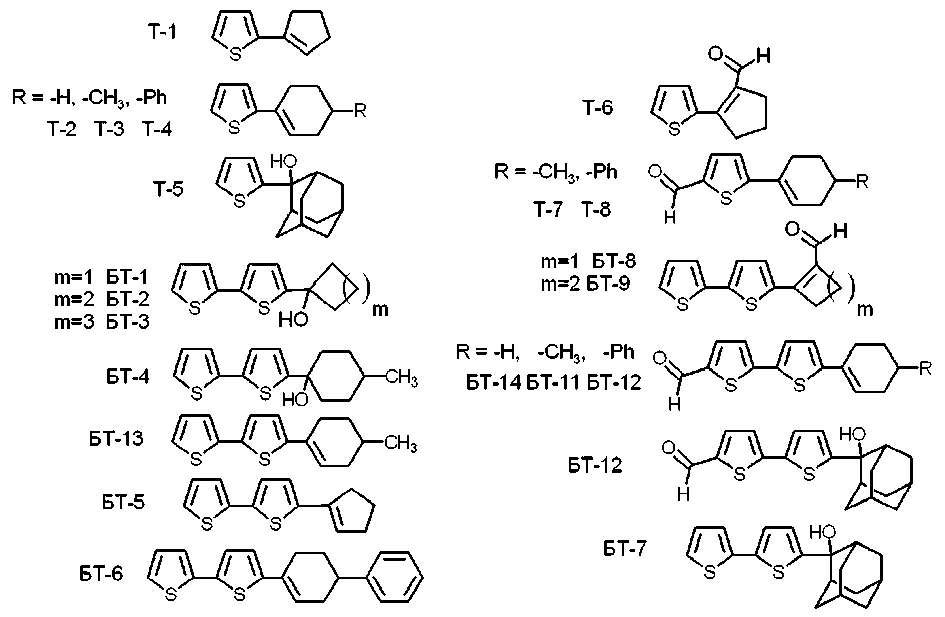
Схема 1. Циклоалкилтиофены и 2,2’-битиофены
поглощения соединения БТ-7 наблюдается смещение полосы на 10,5 нм по сравнению с 2,2’-би-тиофеном, что объясняется наличием адамантанового заместителя. Возникновение интенсивной люминесценции в области 487 нм. Длина волны люминесценции 2-(2,2’-битиенил-5)адамантола-2 смещена на 80 нм в батохромную область, по сравнению с циклоалкил-2,2’-битиофенами (БТ-2 – БТ-6), что объясняется конформационной стабильностью адамантанового каркаса.
Исследования показали, что в соединениях, содержащих альдегидную группу (Т6-T9) про- исходит перенос заряда существующих состояний, вовлекающий электронный переход ароматических π-электронов в π*-антисвязывающую орбиталь в формильной группе. Введение альдегидной группы смещает длину волны поглощения исходного 5-(2-гидроксиадамантил-2)-2,2’-битиофена (БТ-7) на 51 нм, а длина волны максимума люминесценции смещается на 46 нм.
Введение адамантанового фрагмента приводит к увеличению стабильности молекулы [5]. Ароматические системы, содержащие 1-адаман-тильный фрагмент, имеют незначительный кван-
Таблица 1. Характеристики поглощения и люминесценции соединений.
|
Соединение |
λ погл. [нм ] |
λ люм. [нм] |
Стоксов сдвиг [нм] |
Соединение |
λ погл. [нм] |
λ люм. [нм] |
Стоксов сдвиг [нм] |
φ |
|
Т-1 |
281 |
346 |
65 |
БТ-1 |
323 |
426 |
103 |
|
|
T-2 |
279 |
346 |
67 |
БТ-2 |
341 |
408 |
69 |
|
|
T-3 |
283 |
344 |
61 |
БТ-3 |
316 |
424 |
108 |
|
|
Т-4 |
279 |
344 |
65 |
БТ-4 |
338 |
432 |
94 |
|
|
Т-5 |
236 |
346 |
110 |
БТ-5 |
340 |
410 |
70 |
|
|
Т-6 |
260, 286 |
434 |
148 |
БТ-6 |
341 |
408 |
67 |
|
|
Т-7 |
334 |
406 |
72 |
БТ-7 |
313.5 |
461, 487 |
147.5 |
|
|
Т-8 |
334 |
410 |
76 |
БТ-8 |
396 |
518 |
122 |
0.37 |
|
БТ-9 |
385 |
515 |
130 |
0.35 |
||||
|
БТ-10 |
392 |
500 |
107 |
0.43 |
||||
|
БТ-11 |
390 |
497 |
107 |
0.42 |
||||
|
БТ-12 |
364.5 |
507, 532 |
142.5 |
|||||
|
БТ-13 |
341 |
406 |
65 |
|||||
|
БТ-14 |
389 |
502 |
113 |
0.34 |
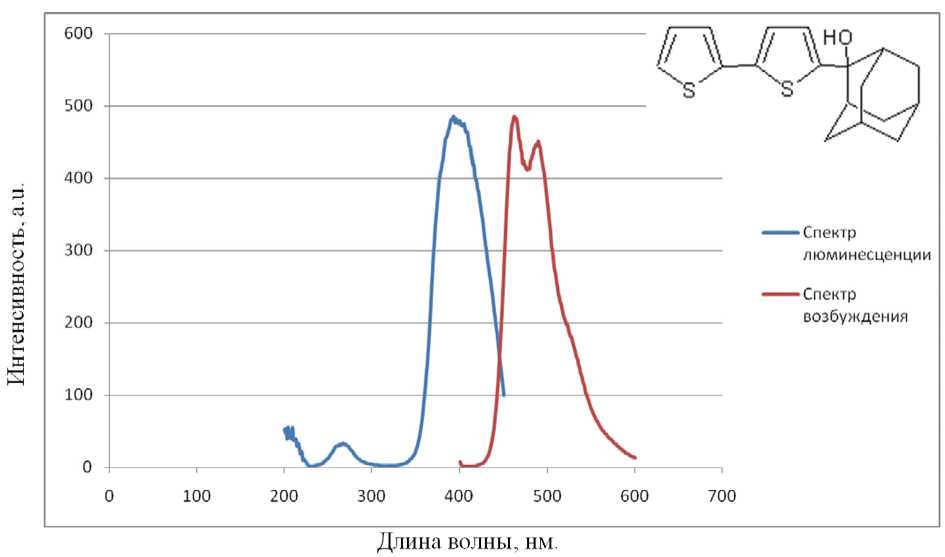
Рис. 1. Спектр возбуждения и люминесценции соединения БТ-7
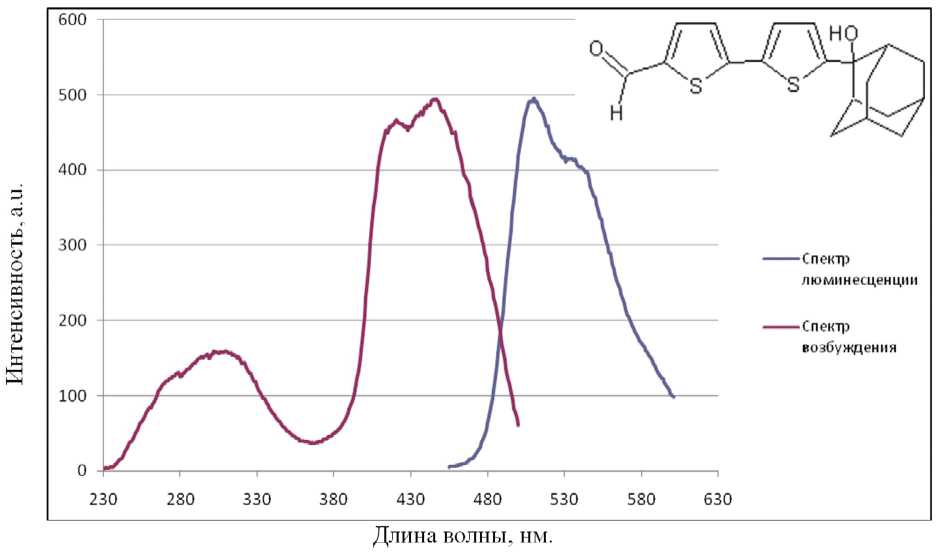
Рис. 2. Спектр возбуждения и люминесценции соединения БТ-12
товый выход люминесценции. Отмечено, что 2,2’-битиофен, содержащий адамантановый фрагмент обладает наименьшим максимумом длины волны поглощения (313,5 нм) и люминесценции (461 нм), и аномально большим стоксовым сдвигом, что говорит о стабильности молекулы. Возможно, в данном случае наличие ароматического заместителя во втором положении адамантанового каркаса способствует стабилизации системы и возникновению интенсивной люминесценции. Введение альдегидной группы смещает длину волны поглощения исходного адамантил-2,2’-битиофена на 51 нм, а длина волны максимума люминесценции смещается на 46 нм. Наблюдается большой Стоксов сдвиг у соединения БТ-13, который объясняется большой потерей энергии из-за происходящего выброса энергии во время возбуждения и объясняется взаимодействием между флуорофором и молекулами растворителя, соответственно, изменением диполя молекулы и образованием заряженных комплексов.
Спектры поглощения измерены на приборе Shimadzu UV-mini, спектры люминесценции измерены на приборе Cary Eclipse в 95% этаноле в кварцевых кюветах (l 1 см). В качестве стандарта для измерения квантового выхода использовался 9,10-дифенилантрацен, ширина щели 2,5 нм [6].
Работа выполнена при финансовой поддержке ФЦП «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2007-2013 г.» (ГК № 11.519.11.2012) с использованием научного оборудования ЦКП СамГТУ «Исследование физикохимических свойств веществ и материалов».
Список литературы Фотофизические свойства производных циклоалкил- и циклоалкенилтиофенов и 2, 2'-битиофенов
- Batista R.M.F., Costa S.P.G., Raposo M.M.M. Synthesis of new fluorescent 2-(2',2"-bithienyl)-1,3-benzothiazoles//Tetrahedron letters. 2004. V. 45. P. 2825-2828.
- Raposo M.M.M., Fonseca A.M.C., Kirsch G. Synthesis of donor acceptor substituted oligothiophenes by Stille coupling//Tetrahedron. 2004. V. 60. P. 4071-4078.
- Юдашкин А.В. Синтез и строение ацил и нитропроизводных 5-N-ацетиламино и 5-метил 2,2'-битиофенов: Автореферат дисс. … канд. хим. наук. Москва, 1983. 16 с.
- Игнатов В.Ф. Электронное строение, спектрально-люминесцентные и генерационные свойства произ водных 2,2'-битиофена -нового класса органических люминофоров и лазерных красителей: Автореферат дисс. … канд. физ. мат. наук. Москва, 1982. 22 с.
- Shen X. M., Jiang X. L., Huang C. C., Zhang H. H., Huang J. D. Highly photostable silicon(IV) phthalocyanines containing adamantane moieties: synthesis, structure, and properties//Tetrahedron. 2010. V. 66. P. 9041-9048.
- Fery Forgues S., Lavabre D. Are fluorescence quantum yields so tricky to measure? A demonstration using familiar stationery products//Journal of Chemical Education. 1999. V. 76. N. 9. P. 1260-1264.


