Фотоника и применение новых люминофоров на основе комплексов дипирролилметенов
Автор: Аксенова Юлия Викторовна, Кузнецова Римма Тимофеевна, Березин Михаил Борисович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Физика и электроника
Статья в выпуске: 2-1 т.17, 2015 года.
Бесплатный доступ
Представлены результаты изучения спектрально-люминесцентных свойств ряда новых эффективно излучающих флуорофоров (дифторборатов дипирролилметенов - BODIPY) различного строения. Исследованы генерационные и фотохимические свойства комплексов под действием лазерного облучения. На основе анализа полученных результатов обсуждаются возможности практического применения данных соединений для создания различных оптических устройств.
Дипиррометены, фотоника лазерных красителей, фотостабильность
Короткий адрес: https://sciup.org/148203638
IDR: 148203638 | УДК: 535.37:539.19:541.14
Photonics and applications of new luminophores based on dipyrrolilmethene complexes
The results of the study of spectral-luminescent properties of new effective fluorophores (dipyrrolilmethene boron fluorinated complex - BODIPY) with different structures were presented. Lasing and photochemical properties of the complexes were measured under laser radiation. Based on the analysis of the results discussed possibilities of practical application of these compounds to creating various optical devices.
Текст научной статьи Фотоника и применение новых люминофоров на основе комплексов дипирролилметенов
Обладая интенсивной флуоресценцией в видимой области и хорошей фотостойкостью [1-3] борфторидные комплексы дипирролилметенов (BODIPY) успешно зарекомендовали себя в качестве активных сред жидкостных и твердотельных перестраиваемых лазеров. Активно исследуются возможности применения в зависимости от строения в качестве сенсибилизаторов генерации водорода под действием солнечного света, в биологических исследованиях для генерации синглетного кислорода (1О2), люминесцентных сенсоров и меток [1, 4].
Известно, что в зависимости от структуры лиганда и растворителя BF2-дипирролилметены обладают различными спектральными свойствами и фотостабильностью [1, 2]. Для целенаправленного синтеза соединений с заданными свойствами необходимо фундаментальное изучение спектральных и фотофизических свойств химических модификаций борфторидных комплексов дипирролилметенов, что позволит решить проблему оптимального практического использования соединений данного класса.
ОБЪЕКТЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Объектами исследования в данной работе являются новые борфторидные комплексы дипир-ролилметенов (BODIPY), синтезированные в Институте химии растворов РАН по методикам, подробно описанным в [5] с соблюдением контроля чистоты соединений методами тонкослойной хроматогра-
фии, ПМР и ИК спектроскопии. На рис. 1 приведены структурные формулы, названия и обозначения изученных соединений.
В качестве растворителей использовались этанол (96%), циклогексан и этилацетат марки ХЧ.
Спектрально-люминесцентные характеристики измерены на спектрометре СМ2203 (SOLAR, Беларусь). Эффективность генерации и характеристики фотостабильности: ресурс и квантовый выход фотопревращений – изучены при возбуждении растворов красителей излучением второй ( λ ген=532 нм) и третьей ( λ ген=355 нм) гармониками Nd:YAG-лазера. Энергия возбуждения и генерации измерялись в каждом импульсе оптическими измерителями OPHIR NOVA II (Израиль) и GENTEC E DUO (Канада). Ресурс Р90, являющийся характеристикой генерационной фотостабильности среды, измерялся удельной суммарной энергией накачки (Дж/см3), поглощенной в процессе генерации, в результате чего первоначальный КПД0=Еген/Енак уменьшился на 10 %. Квантовый выход фотопревращений ϕ ф определялся с погрешностью 5 % по изменениям стационарных спектров поглощения, измеренных до и после облучения согласно методике, подробно описанной в [6].
Для оценки стабильности комплексов BODIPY и эффективности образования протонированного лиганда выбрана величина рКа, характеризующая вероятность отрыва комплексообразователя и присоединения протона основанием-лигандом при взаимодействии с протонодонорным растворителем. Для определения данной величины изучались растворы комплексов BODIPY в этаноле с различным содержанием соляной кислоты методом спектрофотометрического титрования. При этом происходили изменения электронных спектров поглощения и флуоресценции (рис. 2), по которым строились кривые титрования для определения значений рКа в S0, S1фл, S1Ф-К состояниях [7].
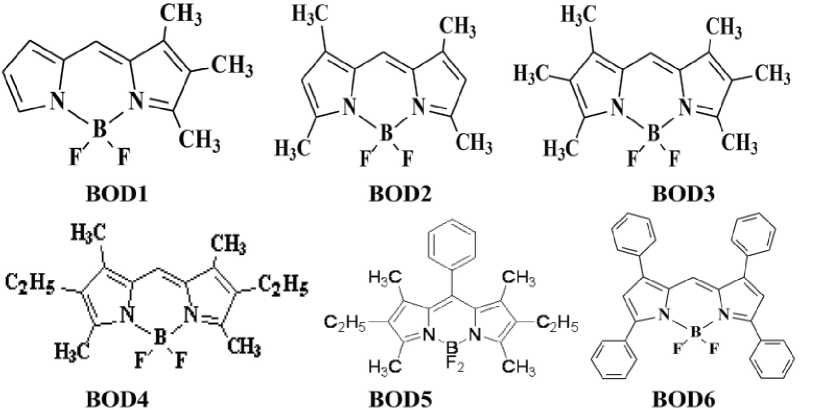
Рис. 1 . Структурные формулы и обозначения BODIPY
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЯ
Анализ спектрально-люминесцентных свойств комплексов BOD1–BOD6 показал, что введение различных заместителей в ядро BODIPY оказывает существенное влияние на проявляемые свойства комплекса. Согласно экспериментальным данным, алкилзамещенные борфторидные комплексы дипирролилметенов характеризуются высокоинтенсивными макиму-мами поглощения в области 505-530 нм, отвечающими электронному переходу S0-S1, и излучения S1-S0 в области 515-545 нм. Введение фенильных циклов в структуру комплекса приводит к общему батохромному сдвигу максимумов поглощения и флуоресценции комплексов и увеличению стоксова сдвига ( BOD6 : λ погл=565 нм, λ фл=600 нм). При возбуждении в область 440-520 нм изученные соединения демонстрируют хорошие излучательные способности ( γ =0,7-1).
фл ,
Следует отметить низкий порог генерации изученных BODIPY: Wпор<1,5-2 МВт/см2. Для всех соединений существует область оптимальных интенсивностей возбуждения, для которых приведены генерационные характеристики (табл. 1). Алкилзамещенные красители генерируют в области 550-560 нм и превосходят по эффективности коммерческие красители для этой области [4]. Так, BOD4 достигает эффективности 74% при мощности накачки 25 МВт/см2. Тетрафе-нилпроизводный BOD6 генерирует в наиболее длинноволновой области спектра практически в максимуме полосы флуоресценции, при этом благодаря большому стоксовому сдвигу реабсорбции практически не наблюдается, малый КПД связан с поглощением Т-состояний на λ ген.
Соединения BOD1 и BOD2 возбуждалось излучением 355 нм, поскольку не поглощают на 532 нм. Данные соединения генерируют в наиболее коротковолновой области спектра. Эф-
Таблица 1 . Флуоресцентные, генерационные, кислотно-основные и фотохимические свойства комплексов BODIPY в этаноле
|
Комплекс |
Х фл , нм |
Х Ген , НМ ( Х возб ,нм) |
КПД,% ( Х возб ,нм) |
ф фот Х 10 5 ( ^ возб , нм), [Р 90 , Дж/см3] |
pKa(S o ) |
pKa (S i° -K) |
|
BOD1 |
518 |
547 (355) |
26 (355) |
6 (355) [112] |
–0.1 |
–3.8 |
|
BOD2 |
514 |
537 (355) |
20 (355) |
0.3 |
–2.9 |
|
|
BOD3 |
538 |
0.6 |
–3.1 |
|||
|
BOD4 |
545 |
560 (532) |
74 (532) |
7 (532) [500] |
0.4 |
–3 |
|
BOD5 |
538 |
551 (355) 551 (532) |
16 (355) 56 (532) |
190 (355) [5] 4 (532) [1800] |
–0.77 |
|
|
BOD5+ DABCO |
546 |
553(355) |
20(355) |
20 (355) [50] |
||
|
BOD6 |
599 |
601 (532) |
8,5 (532) |
–0.9 |
0.02 |
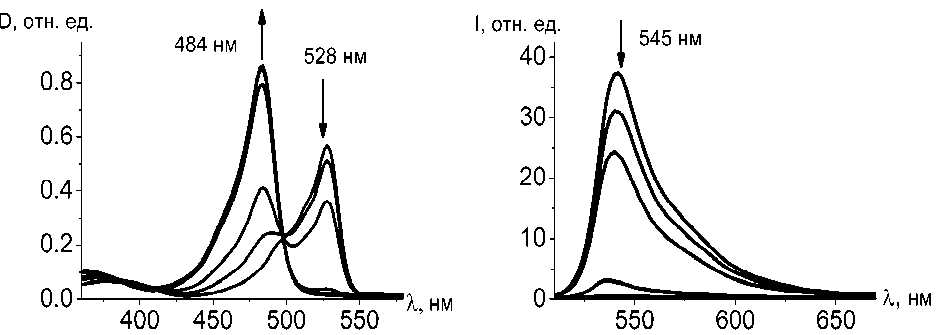
(а) (б)
Рис. 2 . Изменение спектров поглощения (а) и флуоресценции (б)
BOD4 в этаноле, 10-5 М при добавлении НСl (до 15 %)
фективность генерации в оптимальных условиях достигает 20-26%. Наименьшим выходом фотопревращений при возбуждении в S0-S1 полосу обладает BOD5 , однако, при возбуждении в более высоколежащие состояния ( λ возб =355нм) фотостабильность уменьшается на 2 порядка (табл. 1) за счет увеличения интерконверсии и образования 1О2, с которым взаимодействует комплекс [3]. Добавление в растворы DABCO–известного тушителя триплетов и 1О2 улучшает фотохимические характеристики и эффективность генерации при возбуждении на 355 нм (табл. 1).
Вопрос о механизме фотопревращений BODIPY достаточно сложный. В работе [9] показано, что при облучении дифторбората дибензилме-таната фотопревращения осуществляются через отрыв комплексообразователя BF2 с последующим образованием 1О2 и взаимодействием с ним.
В связи с этим наряду с нейтральными были изучены спектрально-люминесцентные свойства подкисленных этанольных растворов BODIPY. Согласно [8], первой стадией протолитической диссоциации борфторидных комплексов ди-пирролилметенов является протонирование атомов F с последующим отщеплением BF2 и образование протонированной по азоту формы лиганда. На рис. 2 видно, что при увеличении концентрации НСl уменьшается интенсивность полосы поглощения комплекса и увеличивается смещенное в коротковолновую сторону поглощение протонированного по азоту лиганда с одной изобестической точкой, что свидетельствует о переходе одной формы в другую. Интенсивность флуоресценции комплексов при подкислении падает до 0. На основе этих изменений определяется величина рКа, характеризующая стабильность комплекса в S0, а по сдвигу полосы поглощения – в S1Ф-К состояниях [7], при этом стабильность в возбужденном состоянии характеризует фотостабильность в протонодонорном растворителе-этаноле (табл. 1). Чем выше рКа, тем меньше стабильность комплекса в соответ- ствующем состоянии. На скорость данных процессов существенно влияет природа введенного заместителя. Согласно нашим результатам, в ряду алкилзамещенных комплексов наиболее нестабильным в основном состоянии является гексаметилзамещенный BOD3 (табл. 1). Далее в ряду уменьшения симметричности замещения происходит увеличение стабильности комплекса: BOD3 Приведенные данные свидетельствуют об уменьшении эффективности протонирования комплексов во Франк-Кондоновском возбужденном состоянии, т.е. о повышении фотостабильности комплексов по механизму декомплексации в протонодонорных растворителях. Такая фотостабильность должна коррелировать с величиной рКа, приведенной в последнем столбце таблицы 1. Если фотостабильность не коррелирует с этим рядом, это означает, что фотопревращения осуществляются по другому механизму: не через фотоотрыв комплексообразователя в протонодонорных средах, а, например, через отрыв протонированного электроноакцепторного фенильного заместителя, как предполагается в [3]. ЗАКЛЮЧЕНИЕ Введение различных заместителей существенно влияет на фотонику BODIPY, что позволяет получать генерацию в широком спектральном диапазоне и использовать данные комплексы в качестве активных сред для перестраиваемых лазеров. Полученные данные позволяют рекомендовать соединение BOD3 в качестве основы для создания лазерной активной среды в непротонодонорном растворителе. Выявлены особенности протонирования представленного ряда комплексов дифторборатов дипирролилметенов в зависимости от введенных заместителей. Полученные данные по генерационной и молекулярной фотостабильности в различных условиях возбуждения также указывают на перспективность использования BOD5 и BOD6 красителей в качестве твердотельных (ТЭОС золь-гель-матрица) активных лазерных сред. Работа выполнена при финансовой поддержке РФФИ-БРФФИ (грант № 14-03-90011-Бел_а), РФФИ (грант № 14-03-31023) и НШ-1305.2014.2.
Список литературы Фотоника и применение новых люминофоров на основе комплексов дипирролилметенов
- Loudget A., Burgess K. BODYPY dyes and their derivatives: syntheses and spectroscopic properties.//Chem. Rev., 2007, v. 107, p. 4891-4932.
- Ulrich G., Ziessel R., Harriman A. The chemistry of fluorescent bodipy dyes: versatility unsurpassed.//Angew. Chem. Int. Ed., 2008, v. 47, p. 1184-1201.
- Mula S., Ray A.K., Banerjee M., Chaudhuri T., Dasgupta K., Chattopadhyay S. Design and development of a new pyrromethene dye with improved photostability and laser efficiency: theoretical rationalization of photophysical and photochemical properties.//J. Org. Chem., 2008, v. 73, p. 2146-2154.
- Kuznetsova R.T., Aksenova Y.V., Telminov E.N., Samsonova L.G. Spectral, luminescent, photochemical and laser properties of a series of boron fluoride complexes of dipyrrolylmethenes in solutions.//Opt. and Spec., 2012, v. 112, p. 746-754.
- Berezin M.B., Antina E.V., Guseva G.B., Vyugin A.I., Semeikin A.S., Yutanova S.L. Synthesis and properties of (1,2,3,7,9-pentamethyldipyrrolylmethen-8-yl)-(1,2,3,7,8-pentamethyldipyrrolylmethen-9-yl)methane and bis(1,2,3,7,9-p pentamethyldipyrrolylmethen-8-yl)trifluoromethylmethane dihydrobromides.//Rus. J. Gen. Chem., 2012, v. 82, p. 1287-1292.
- Kuznetsova R.T., Maier G.V., Kopylova T.N., Svetlichnyi V.A., Telminov E.N., Filinov D.N. Phototransformations of organic compounds upon powerful laser exetation under nonlinear absorbtion conditions.//High Energ. Chem., 2002, v. 36, p. 338-343.
- Теренин А.Н. Фотоника молекул красителей. Л.: Наука, 1967,120 с.
- Banuelos J., Lopez Arbeloa F., Arbeloa T., Salleres S., Vilas J.L. Photophysical characterization of new 3-amino and 3-acetamido BODIPY dyes with solvent sensitive properties.//J. Fluoresc., 2008, v. 18, p. 899-907.
- Zakharova G.V., Chibisov A.K., Sazhnikov V.A., Kononevich Yu.N., Muzafarov A.M., Alfimov M.V. Photodegradation of Boron Difluoride Dibenzoylmethanate in solutions.//High Energ. Chem., 2013, v. 47. p. 327-330.


