Функциональная идентификация Cl-/ H+- антипортера в мембранной фракции клеток корня галофита Suaeda altissima (L.) Pall
Автор: Шувалов Алексей Витальевич, Орлова Юлия Викторовна, Мясоедов Николай Александрович, Беляев Денис Вадимович, Халилова Людмила Абдулгадиевна, Андреев Игорь Михайлович, Балнокин Юрий Владимирович
Журнал: Труды Московского физико-технического института @trudy-mipt
Рубрика: Молекулярная и биологическая физика
Статья в выпуске: 3 (15) т.4, 2012 года.
Бесплатный доступ
На выделенном из корней галофита Suaeda altissima мембранном препарате, обогащенном плазмалеммой, показано функционирование Cl−/H+-антипортера. Идентификацию Cl−/H+-антипортера и исследование свойств осуществляемого им Cl−/H+-обмена проводили с помощью оптических зондов (акридиновый оранжевый, пиранин и сафранин О), позволяющих регистрировать изменения pH внутри везикул и изменения электрического трансмембранного потенциала, которые происходят при наложении на мембрану концентрационного градиента Cl−. Предполагается, что физиологическая роль Cl−/H+-антипортера состоит в поддержании концентраций Cl− в цитоплазме на нетоксическом уровне в условиях засоления.
Галофит suaeda altissima, мембранная фракция, плазмалемма, cl−/h+-антипортер, cl− гомеостаз
Короткий адрес: https://sciup.org/142185854
IDR: 142185854
Functional identification of the Cl- /H+-antiporter in the membrane fraction from root cells of the halophyte Suaeda altissima (L.) Pall
The Cl− gradient dependent Cl−/H+ exchange across the membranes is identified and characterized in the plasmalemma-enriched membrane fraction isolated from roots of a halophyte Suaeda altissima. The intravesicular pH and the transmembrane electric potential changes are detected with ΔpH indicator acridine orange, pH indicator pyranine and electric potential indicator safranine O. The physiological role of the proposed Cl−/H+ antiporter is thought to maintain chloride in the cytoplasm below toxic levels under salinity conditions.
Текст научной статьи Функциональная идентификация Cl-/ H+- антипортера в мембранной фракции клеток корня галофита Suaeda altissima (L.) Pall
Исследование механизмов, лежащих в основе устойчивости растений к высоким концентрациям солей в почве, является одной из актуальных проблем современной биологии растений. При высоких концентрациях NaCI в почве равновесный электрический потенциал С1- на плазмалемме (ПМ) клеток корня может быть более отрицательным, чем трансмембранный электрический потенциал, т.е. возможна ситуация, при которой ионы С1- поступают из экстраклеточной среды в цитоплазму по градиенту электрохимического потенциала [1]. Пассивный транспорт С1- внутрь предполагает наличие активного транспорта С1-, направленного обратно в экстраклеточную среду или в вакуоль.
Механизмы экспорта С1- из цитоплазмы растительных клеток, в отличие от механиз мов экспорта Ха+. слабо изучены. Известно, что в трапемембраппый перенос С1-вовлечепы мембранные белки семейства. CLC, которое включает анионные каналы и анион/протонные антипортеры. Гены семейства CLC и их продукты обнаружены у бактерий, животных и растений [2; 3]. К представителям этого семейства относятся С1-/Н+-антипортеры, которые осуществляют вторично активный транспорт С1- в обмен на Н+, используя энергию градиента, электрохимического потенциала, протонов. Такой переносчик мог бы транспортировать С1- из цитоплазмы растительных клеток обратно в апопласт или в вакуоль.
Функционирование С1-/Н+-антипортера продемонстрировано в плазмалемме прокариот [4, 5] и внутренних мембранах клеток животных [6; 7]. Несмотря на то, что гены семейства CLC обнаружены у нескольких растений [8], сведения о С1-/Н+-антипортерах растительного происхождения крайне скудны. Имеется лишь одна, работа, свидетельствующая о функционировании такого переносчика, названного AtCLCc, в клетках растений [9]. Показано, что продукт гена AtCLCc локализован в тонопласте замыкающих клеток устьиц Arabidopsis thaliana, где он вовлечен в накопление С1- вакуолями. Выключение гена AtCLCc посредством вставки Т-ДНК привело к нарушению транспорта С1- через тонопласт этих клеток и к нарушению работы устьичного аппарата.
Мы предположили, что С1-/Н+-антипортер выполняет функцию поддержания концентраций С1- в цитоплазме на нетоксическом уровне в клетках галофитов — растений, обитающих на засоленных почвах. Настоящая работа посвящена функциональной идентификации С1-/Н+-антипортера в выделенной из клеток корня S. altissima мембранной фракции, обогащенной везикулами плазмалеммы.
Материалы и методы
Семена Suaeda altissima (L.)Pall. проращивали во влажном песке при комнатной температуре, на пятнадцатые сутки проростки пересаживали на аэрируемый раствор Робинсона и Даунтона [10], в который был добавлен NaCI в конечной концентрации 100 мМ. Дальнейший рост S. altissima осуществляли в факторостатной камере при 24 °C в условиях водной культуры. Растения освещали натриевыми лампами высокого давления Reflux, ДНаЗ-400 (Россия) 12 часов в сутки при интенсивности света 150 вт/м2.
Мембранную фракцию из клеток корней, обогащенную везикулами плазмалеммы, получали путем центрифугирования суспензии микросом в ступенчатом градиенте плотности сахарозы по модифицированной методике [11]. Модификации состояли в применении сахарозных градиентов иных профилей (см. подписи к рис.) и во введении в среды, использовавшиеся при выделении мембран, дополнительно 5 мМ /3-меркаптоэтанола. Содержание плазмалеммы и тонопласта в выделенной мембранной фракции оценивали по чувствительности АТФ-зависимого закисления везикулярного люмена к ингибитору Н+-АТФазы плазмалеммы ортованадату и ингибитору Н+-АТФазы тонопласта нитрату.
О функционировании С1-/Н+-антипортера судили по ДрСГзависимому переносу Н+ через мембрану, а также по генерации трансмембранного электрического потенциала ( Дф) при наложении на везикулярную мембрану концентрационного градиента С1 -.
Перенос Н+через мембрану регистрировали двумя методами: по изменению дифференциальной абсорбции (ДА492-54о) ДрН-индикатора акридинового оранжевого (АО) [12] и по изменению параметров флуоресценции pH-индикатора пиранина ( Хех = 405 нм, Хех = 463 нм, Хет = 510 нм), находящегося внутри везикул [13]. Пиранин загружали в везикулы с помощью гипоосмотического шока, ресуспендируя выделенные мембранные везикулы в содержащих пиранин средах низкой осмолярности. Снижение осмолярности среды приводило к разрыву и последующему замыканию везикул, которое сопровождалось захватом «загрузочной» среды. Пиранин удаляли из среды, пропуская суспензию везикул через колонку с сефадексом G-50.
Генерацию Дф со знаком «минус» внутри везикул регистрировали как увеличение разности поглощения (А554—А524) потенциал-чувствительного индикатора сафранина О [14].
Разность поглощения АО и сафранина О регистрировали с помощью двухволнового спектрофотометра «Hitachi 557». Для измерения параметров флуоресценции пиранина использовали спектрофлуориметр «Hitachi 850».
Результаты
При внесении С1- в суспензию везикул протоны транспортировались наружу, и происходило защелачивание везикулярного люмена. Один из экспериментов, демонстрирующих трансмембранный С1-/Н+обмен, показан на рис. 1. Выделенные везикулы содержали ионы Ха+. которые попадали в везикулярный люмен на начальной стадии процедуры выделения везикул при гомогенизации корней. Встраивающийся в мембрану экзогенный Na+/Н+ — антипортер, моненсин, вызывал обмен содержащихся внутри ионов Na+ на наружные протоны и приводил к генерации ДрН с более кислым значением pH внутри везикул, чем в среде. Генерацию ДрН такой направленности регистрировали как снижение дифференциальной абсорбции АО. Последующее внесение в суспензию С1- (в форме холинхлорида)
вызывало диссипацию предварительно созданного АрН (возрастание дифференциальной абсорбции АО). Проникающий через мембрану липофильный катион тетрафенилфосфоний (ТФФ+) ускорял диссипацию АрН.
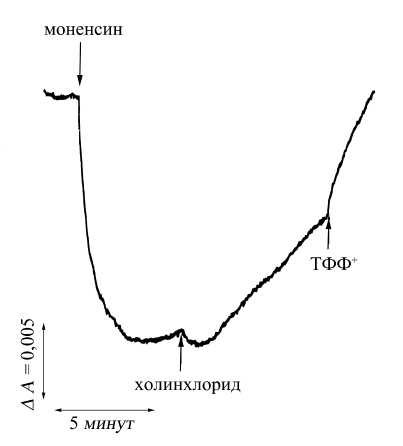
Рис. 1. АрС1-зависимая диссипация АрН с более кислым pH внутри везикул чем в наружной среде (эксперимент с АрН-индикатором акридиновым оранжевым). Мембраны выделяли в сахарозном градиенте плотности (25/34%), отбирая везикулы на границе двух слоев. Реакцию проводили в среде следующего состава (в мМ): 500 сахарозы; 20 BTP-MES, pH 7,5; 2 MgSO4, 2,5 EGTA. АрН на мембране был предварительно создан путем внесения Na + /Н+-антипортера моненсина в суспензию везикул, содержащих Na +. Исходные концентрации Na+ и С1- в везикулярном люмене составляли 20 и 50 мМ соответственно. Липофильный катион ТФФ + ускорял АрС1-зависимую диссипацию АрН. Вещества вносили в суспензию в следующих концентрациях: моненсин — 10 мкМ, холинхло-рид - 200 мМ, ТФФ + - 1 мМ
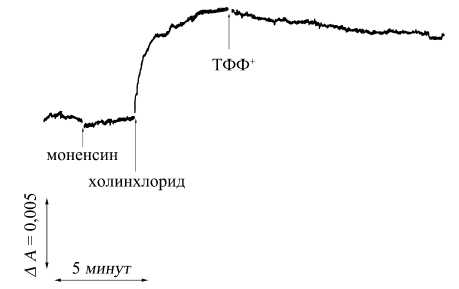
Рис. 2. АрС1-зависимая генерация Аф на везикулярной мембране (эксперимент с Аф-индикатором сафранином О). ТФФ + приводил к медлеиной диссипации Аф. Условия проведения эксперимента такие же, как указано в подписи к рис. 1
Использование Аф-индикатора сафранина О выявил о электрогенный характер Cl-/ Н+ обмена (рис. 2). Последовательность добавок к суспензии везикул была такой же, как в эксперименте, представленном на рис. 1. Внесение в суспензию моненсина не обнаружило заметного изменения Аф, поскольку этот ионофор осуществляет электронейтральный Na +/Н+-обмен. Однако последующее добавление холинхлорида приводило к генерации Аф со знаком «минус» внутри везикул (возрастание дифференциальной абсорбции сафранина О). Добавление тфф + вызывало медленную диссипацию сформированого в присутствии С1 - трансмембранного электрического потенциала (Аф), что регистрировалось как сниже- ние дифференциальной абсорбции сафранина О.
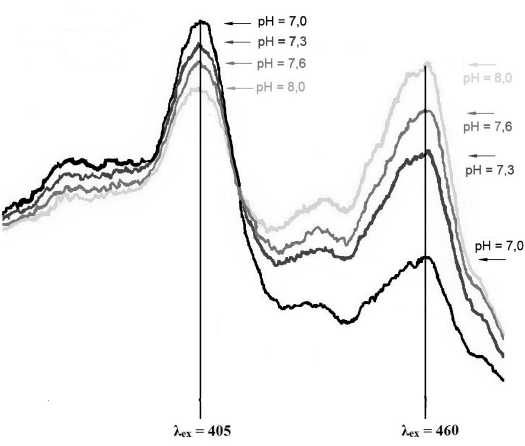
Рис. 3. Спектр возбуждения флуоресценции пиранина при разных значениях pH раствора, Хет = 510 нм
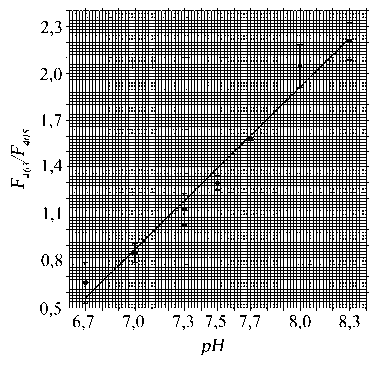
Рис. 4. Зависимость отношений интенсивностей флуоресценции пиранина, загруженного в везикулы, при Хех = 463 нм и Хех = 405 нм (Хет = 510 нм) от pH в везикулярном люмене. Мембраны выделяли в сахарозном градиенте плотности (34/64 %), отбирая везикулы на границе двух слоев. Везикулы загружали буферными растворами (20 мМ BTP-MES) с разными pH, содержащими 200 мкМ пиранина. Загрузку производили гипоосмотическим шоком (см. раздел «Материалы и методы»). Спектры возбуждения флуоресценции пиранина, загруженного в везикулы при разных pH, регистрировали в средах следующего состава (в мМ): 100 сахароза, 20 BTP-MES с pH, соответствующих их внутривезикулярным значениям
Использование флуоресцентного pH-индикатора, пиранина, который загружали в везикулы, также показало наличие ApCl-зависимого транспорта Н+ через мембрану. Применение этого индикатора, в отличие от АО, не требует предварительной генерации на мембране АрН. С помощью пиранина можно количественно определять изменения pH внутри везикул. Спектр возбуждения флуоресценции пиранина, записанный при постоянном значении длины волны эмиссии (Хет = 510 нм) имеет два характерных пика при Хех = 405 нм и Хех = 463 нм (рис. 3). При защелачивании раствора интенсивность флуоресценции пиранина при Хех = 405 нм снижается, а при Хех = 463 нм возрастает. На рис. 4 показана зависимость отношения интенсивностей флуоресценции пиранина при двух указанных длинах волн в спектре возбуждения флуоресценции от pH везикулярного люмена. В этом эксперименте везикулы загружали растворами пиранина с разными значениями pH. В последующих экспериментах полученную зависимость использовали как калибровочную кривую для определения pH внутри везикул.
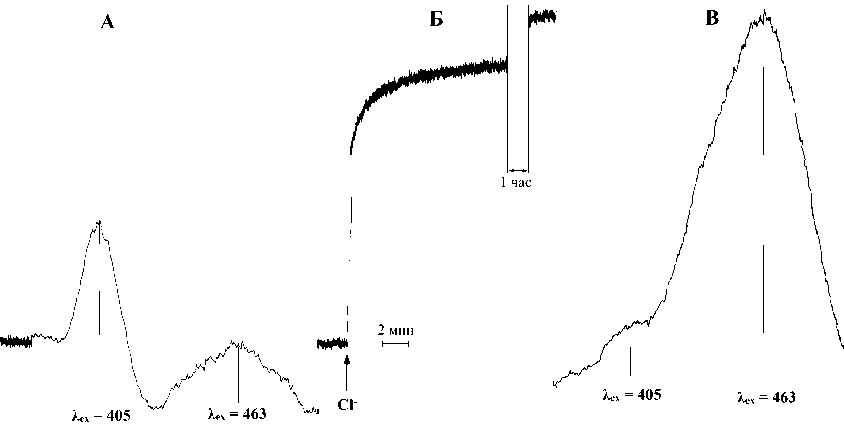
Рис. 5. Защелачивание везикулярного люмена в ответ на внесение в суспензию везикул С1- (эксперимент с рЯ-индикатором пиранином, загруженным в везикулы). Везикулы выделяли и загружали пиранином как указано в подписи к рис. 4. Исходная концентрация хлорида в везикулярном люмене 2 мМ, pH 6,8 (20 мМ BTP-MES). Реакцию проводили в среде следующего состава: 100 мМ сахароза, 20 мМ BTP-MES, pH 7,2. А — спектр возбуждения флуоресценции пиранина до внесения С1- в суспензию; Б — кинетика изменения флуоресценции пиранина после внесения С1-в суспензию в концентрации 200 мМ (Аеж = 463, Ает = 510 нм); В — спектр возбуждения флуоресценции пиранина после внесения в суспензию С1- и достижения состояния равновесия. Конечное значение pH в везикулярном уровне 8,2
Рис. 5 демонстрирует защелачивание везикулярного люмена в ответ на внесение С1 -в среду. На рис. 5а показан спектр возбуждения флуоресценции пиранина при исходном значении pH везикулярного люмена, равном 6,8 и концентрации С1 - в люмене 2 мМ. На рис. 56 — кинетика изменения флуоресценции пиранина при Аеж = 460 нм и Ает = 510 нм после внесения в суспензию С1 - в конечной концентрации 200 мМ, на рис. 5в — спектр возбуждения флуоресценции пиранина после достижения состояния равновесия. Конечное значение pH внутри везикул составило 8,2.
Следующий эксперимент показал, что С1 --опосредованньш транспорт Н+ зависит от трансмембранного электрического потенциала. Электрический потенциал той или иной величины задавали, поддерживая на мембране соответствующий диффузионный калиевый потенциал. Для этой цели помимо пиранина везикулы нагружали ионами К + в разных концентрациях. Концентрации К + варьировали также в наружной среде. При разных отношениях концентраций К + снаружи и внутри везикул в присутствии калиевого ионофора валиномицина на мембране генерировались разные диффузионные потенциалы К +. В трех вариантах эксперимента наружные и внутренние концентрации К +([К+о] / [К+^Д), выраженные в мМ, были следующими: 50/5, 50/50, 5/50. При этом диффузионный потенциал описывается уравнением Нернста
. , RT, [ ^ + ]
△ ^дифф.К + р ln
где R,T и F имеют обычные термодинамические значения. Согласно уравнению Нернста (1), для этих вариантов эксперимента диффузионный калиевый потенциал на мембране должен составить +58, 0, и -58мВ соответственно.
При трех заданных значениях электрического потенциала и разных отношениях концентраций С1- снаружи и внутри везикул по изменению отношения интенсивности флуоресценции пиранина при Аеж = 405 и 463 нм (Ает = 510 нм) определяли изменение внутри-везикулярного pH (рис. 6). Можно видеть, что (1) изменение внутривезикулярного pH, а именно защелачивание, тем больше, чем больше концентрационный градиент С1- на мембране, (2) защелачивание больше при положительном значении электрического потенциала и оно снижается по мере смещения потенциала в отрицательную область, (3) не было обнаружено реверсии транспорта Н+через мембрану. Вход Н+ внутрь везикул (закисление везикулярного люмена) не наблюдался ни при каких условиях данного эксперимента.
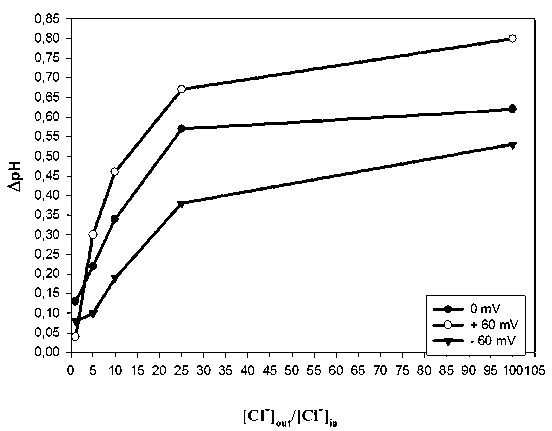
Рис. 6. Защелачивание везикулярного люмена в ответ на создание на везикулярной мембране концентрационного градиента С1- при разных значениях электрического потенциала. Везикулы выделяли и загружали пиранином, как указано в подписи к рис. 4. Исходная концентрация С1- в везикулах 2 мМ, pH 7,5. Различные концентрационные градиенты С1- на мембране создавали путем изменения концентрации этого иона в наружной среде Электрический потенциал задавали, поддерживая на мембране соответствующий диффузионный калиевый потенциал
Обсуждение результатов
Одним из наиболее продуктивных подходов в идентификации ионных транспортеров мембраны является исследование транспорта ионов на выделенных мембранных везикулах. Получаемые препараты ПМ обычно более чем наполовину состоят из инвертированных везикул, т.е. мембранных пузырьков, обращенных цитоплазматической стороной наружу. В некоторых случаях это создает определенные удобства, в частности, при исследовании функций локализованных в плазмалемме АТФаз. Поскольку активные центры АТФаз находятся на цитоплазматической стороне мембраны, то при работе на выделенных везикулах можно инициировать транспорт иона через ПМ, добавляя АТФ в суспензию везикул. Этот подход был использован нами для оценки содержания везикул плазмалеммы и тонопласта в полученной фракции. Н+-АТФаза плазмалеммы растительных клеток специфически подавляется ортованадатом — ингибитором АТФаз P-типа и не чувствительна к нитрату, тогда как Н+-АТФаза вакуолярной мембраны, наоборот, подавляется нитратом и не чувствительна к ортованадату. В наших экспериментах АТФ-зависимый транспорт Н + через мембрану ингибировался ортованадатом и практически не подавлялся нитратом, что говорит о преимущественном содержании в препарате везикул ПМ (данные не приведены).
Основной результат, полученный в настоящей работе, состоит в демонстрации ДрС1-зависимого защелачивания везикулярного люмена (рис. 1, 5, 6). Наблюдавшееся защелачивание не может быть объяснено транспортом Н + по градиенту электрохимического по- тенциала. Во всех проведенных экспериментах исходное значение pH внутри везикул было таким же, как в среде. Внесение С1- в суспензию везикул в форме холинхлорида могло приводить к генерации электрического потенциала на мембране со знаком «минус», но не «плюс» внутри везикул, поскольку мембраны в гораздо большей степени проницаемы для С1-. чем для холина. Перенос С1- внутрь везикул посредством С1- Н+-аитипортера. также осуществляет генерацию электрического потенциала со знаком «минус» внутри. Эксперименты с Аф-индикатором сафранином О (рис. 2) прямо указывают на генерацию электрического потенциала со знаком «минус» внутри после добавления к суспензии везикул С1-. Таким образом, пассивное движение Н+ в этих условиях возможно лишь внутрь везикул. Однако при создании на мембране концентрационного градиента С1-, направленного внутрь везикул, мы наблюдали защелачивание, но не закисление внутривезикуляр-ного люмена. Полученный результат прямо указывает на функционирование в ПМ клеток корня S. altissima Cl-/Н+-антипортера. Перенос С1-внутрь везикул и перенос Н+ в противоположном направлении обеспечивают перенос отрицательных зарядов внутрь везикул. Электрогенный обмен двух ионов должен зависеть от электрического потенциала на мембране, что нашло подтверждение в экспериментах с разным диффузионным калиевым потенциалом на мембране (рис. 6). При отрицательных значениях электрического потенциала («минус» внутри везикул) защелачивание было слабее, чем при нулевом значении потенциала. Смещение потенциала к положительным значениям усиливало защелачивание. Представленное ниже уравнение (2), описывающее работу С1-/Н+-антипортера [4], связывает равновесный трансмембранный потенциал (Еец), т.е. потенциал, при котором отсутствует движение С1- и Н+через мембрану, с концентрационными градиентами С1- и Н+'.
(n + 1)Афе,F = -nRTln -И- + RT ln Л0], (2) V^UnJ [rrjnJ где n — стехиометрия обмена, т.е. число обмениваемых ионов С1- на 1Н+.
Проведенные нами эксперименты не позволяют произвести расчеты по уравнению (2), однако его анализ показывает, что при отрицательных значениях Аф и градиентах С1- на мембране небольшой величины должно происходить обращение направления транспорта Н+и С1-, и защелачивание везикулярного люмена должно сменяться закислением. Однако закисления не наблюдалось ни при каких условиях данного эксперимента (рис. 6). Наиболее вероятной причиной этого является наличие на мембране других процессов (наряду с С1-/Н+-обменом), связанных с переносом протонов и приводящих к защелачиванию везикулярного люмена. Не исключено также, что полученные нами везикулы не являются идеальной системой, способной поддерживать трансмембранный электрический потенциал (диффузионный калиевый потенциал) в соответствии с заданными по уравнению (1) значениями. Например, из-за высокой протонной проводимости мембраны возможен пассивный транспорт протона из среды в везикулярный люмен и смещение благодаря этому Аф к более положительным значениям.
Физиологическая роль обнаруженного нами С1-/Н+-антипортера ПМ, по-видимому, состоит в выведении С1- из цитоплазмы в апопласт в условиях засоления среды. Функционирование С1-/Н+-антипортера в клетках сопровождается деполяризацией ПМ. Это в свою очередь должно приводить к стимуляции работы Н+-АТФазы и снижению движущей силы пассивного транспорта Na+ из наружной среды в клетку.
Дальнейшие исследования С1-/Н+-антипортера ПМ клеток корня S. altissima будут направлены на получение мембранных препаратов более высокого качества, дающих возможность произвести расчеты ион-транспортных параметров С1-/Н+-антипортера в соответствии с уравнением (2) и определить стехиометрию С1-/Н+-обмена.
Работа поддержана грантом РФФИ № 09-04-00-709-а.
Список литературы Функциональная идентификация Cl-/ H+- антипортера в мембранной фракции клеток корня галофита Suaeda altissima (L.) Pall
- Teakle N.L., Tyerman S.D. Mechanisms of Cl-transport contributing to salt tolerance//Plant, Cell and Environment. -2010. -V. 33, I. 4. -P. 566-589.
- Marmagne A., Vinauger-Douard M., Monachello D., Falcon de Longevialle A., Charon C., Allot M., Rappaport F., Wollman F.A., Barbier-Brygoo H., Ephritikhine G. Two members of the Arabidopsis CLC (Chloride Channels) family, AtCLCe and AtCLCf, are associated with thylakoid and Golgi membranes respectively//Journal of Experimental Botany. -2007. -V. 58. -P. 3385-3393.
- Jentsch T.J. CLC Chloride Channels and Transporters: From Genes to Protein Structure, Pathology and Physiology//Crit. Rev. Biochem. Mol. Biol. -2008. -V. 43, N. 1. -P. 3-36.
- Accardi A., Miller C. Secondary active transport mediated by a prokaryotic homologue of CLC Cl-channels//Nature. -2004. -V. 427. -P. 803-807.
- Jayaram H., Accardi A., Wu F., Williams C., Miller C. Ion permeation through a Cl-selective channel designed from a CLC Cl-/H+ exchanger//PNAS. -2008. -V. 105, N. 32. -P. 11194-11199.
- Graves A.R., Curran P.K., Smith C.L., Mindell, J.A. The Cl-/H+ antiporter CLC-7 is the primary chloride permeation pathway in lysosomes//Nature. -2008. -V. 453. -P. 788-792.
- Pusch M., Zifarelli G. It's the proton also in ClC-2//Journal of Physiology. -2009. -V. 587, I. 7. -P. 1379-1380.
- de Angeli A., Thomine S., Frachisse J.M., Ephritikhine G., Gambale F., Barbier-Brygoo H. Anion channels and transporters in plant cell membranes//FEBS Letters. -2007. -V. 581, I. 12. -P. 2367-2374.
- Jossier M., Kroniewitcz, L., Dalmas, F., Le Thiec, D., Ephritikhine, G., Thomine, S., Barbier-Brygoo, H., Vavasseur, A., Filleur, S., and Leonhardt, N. The Arabidopsis vacuolar anion transporter, AtCLCc, is involved in the regulation of stomatal movements and contributes to salt tolerance//Plant Journal. -2010. -V. 64, I. 4. -P. 563-576.
- Robinson S.P., Downton W.J.S. Potassium, Sodium and Chloride Ion Concentration in Leaves and Isolated Chloroplasts of the Halophyte Suaeda australis R. Br.//Aust. J. Plant Physiol. -1985. -V. 12. -P. 471-478.
- Луньков Р.В., Андреев И.М., Мясоедов Н.А., Хайлова Г.Ф., Куркова Е.Б., Балнокин Ю.В. Функциональная идентификация Н+-АТФазы и Na+/H+ антипортера в плазма-тической мембране, выделенной из клеток корня соленакапливающего галофита Suaeda altissima//Физиология растений. -2005. -Т. 52. -С. 717-725.
- Palmgren M.G. Acridine orange as a probe for measuring pH gradients across membranes mechanism and limitations//Anal. Biochem. -1991. -V. 192, I. 2. -P. 316-321.
- Overly C.C., Lee K.D., Berthiaume E., Hollenbeck P.J. Quantitative measurement of intraorganelle pH in the endosomal-lysosomal pathway in neurons by using ratiometric imaging with pyranine//PNAS. -1995. -V.92, I. 8. -P. 3156-3160.
- Akerman K.E., Wikstrцm M.K. Safranine as a probe of the mitochondrial membrane potential//FEBS Letters. -1976. -V. 68, I. 2. -P. 191-197.


