Галофильный штамм-деструктор бензойной кислоты Halomonas sp. D2
Автор: Д. И. Усанина, А. А. Пьянкова, Е. Г. Плотникова
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 3, 2021 года.
Бесплатный доступ
Бензойная кислота используется в промышленности, а также является промежуточным продуктом микробиологического разложения многих ароматических соединений – загрязнителей окружающей среды. Штамм Halomonas sp. D2, выделенный из глинистых отложений соляной шахты Верхнекамского месторождения (г. Соликамск, Пермский край), способен использовать бензойную кислоту (БК) в качестве единственного источника углерода и энергии. Halomonas sp. D2 растет на богатой среде Раймонда в присутствии 10–300 г/л NaCl и на минеральной среде с БК (1 г/л) при 30– 70 г/л соли. В геноме штамма выявлен ген benA, кодирующий α-субъединицу бензоат 1,2диоксигеназы – ключевого фермента разложения БК. Анализ нуклеотидной последовательности гена benA штамма D2 показал наиболее высокий уровень сходства (94.86%) с последовательностью benA-гена типового штамма Halomonas taeanensis BH539T, с которым штамм D2 наиболее филогенетически близок и по гену 16S рРНК (сходство 99.43%). Выявленные свойства штамма Halomonas sp. D2 делают его перспективным для использования в биотехнологиях восстановления засоленных почв и водоемов, загрязненных ароматическими углеводородами.
Галофильные бактерии, Halomonas, разложение бензойной кислоты, секвенирование, ген benA.
Короткий адрес: https://sciup.org/147235109
IDR: 147235109 | УДК: 579.26:57.083.18 | DOI: 10.17072/1994-9952-2021-3-171-177
Benzoic acid-degrading halophilic strain Halomonas sp. D2
Benzoic acid is widely used in various fields of industry, and it is a intermediate in the bacterial catabolism of many aromatic compounds, environmental pollutants. Halomonas sp. D2 strain, isolated from clay deposits of the salt mine of the Verkhnekamsky salt deposit (Solikamsk, Perm krai) is capable of using benzoic acid (BA) as a sole source of carbon and energy. Halomonas sp. D2 grows in the rich Raymond’s medium in the presence of 10-300 g/L NaCl and in the mineral medium with BA (1 g/L) in the presence of 30-70 g/L NaCl. The gene (benA) encoding the benzoate 1,2-dioxygenase alpha subunit was detected in the strain D2. Analysis of benA gene of the strain D2 showed the highest similarity (94.86%) with benA gene of Halomonas taeanensis BH539T with which the strain D2 is the most phylogenetically close in the 16S rRNA gene (99.43% similarity). The revealed properties of Halomonas sp. D2 strain makes it promising for use in biotechnologies for the restoration of saline soils and water contaminated with aromatic hydrocarbons
Текст научной статьи Галофильный штамм-деструктор бензойной кислоты Halomonas sp. D2
способные осуществлять разложение бензойной кислоты и использовать ее в качестве единственного источника углерода и энергии [Field, Sierra-Alvarez, 2008; Егорова, Пьянкова, 2019]. В то же время крайне ограничена информация о галофиль-ных бактериях-деструкторах, строении и функционировании их метаболических, генетических систем, контролирующих разложение бензойной кислоты в условиях засоления [Fathepure, 2014].
Ранее из соляной шахты района промышленных разработок Верхнекамского месторождения калийно-магниевых солей (ВМКС) были выделены галофильные бактерии, которые на основании морфологических, физиологических и генетических исследований были идентифицированы как представители семейства Halomonadaceae (класс Gammaproteobacteria ) [Пьянкова и др., 2020]. На настоящем этапе изучения проводится дальнейшая характеристика выделенных галофилов, в том числе для перспективы использования в биотехнологических целях. Цель настоящей работы – изучение способности галофильного штамма Halomonas sp. D2 разлагать бензойную кислоту в условиях повышенной солености среды, а также выявление и филогенетическая характеристика ключевого гена катаболизма бензойной кислоты ( benA ).
Материалы и методы исследования
Объектом исследования являлся штамм Halomonas sp. D2, выделенный из глинистых донных отложений рассолоотводящей выработки одного из рудников ВМКС [Пьянкова и др., 2020]. Также в работе был использован типовой штамм Halomonas taeanensis BH539T из рабочей коллекции лаборатории микробиологии техногенных экосистем «ИЭГМ УрО РАН».
Среды и условия культивирования. При культивировании бактерий использовали минеральную среду Раймонда (МСР) [Raymond, 1961], а также богатую среду Раймонда (БСР) с триптоном (5 г/л) и дрожжевым экстрактом (2.5 г/л), с разным содержанием NaCl (от 10 до 300 г/л). Для агаризованных сред добавляли 15 г/л агара. Культивирование проводили при 28 °С.
Устойчивость бактерий к различным концентрациям хлорида натрия оценивали по появлению и размеру колоний при росте на агаризо-ванной БСР без соли и с содержанием NaCl от 10 до 300 г/л. Оценку роста колоний проводили через 2 недели после культивирования.
Рост бактерий на ароматических соединениях оценивали при культивировании в жидкой минеральной среде Раймонда (30 г/л NaCl). Бензойную кислоту, нафталин, бифенил, орто-фталат, как единственный источник углерода и энергии, добавляли в среду в количестве 1 г/л, салициловую кислоту – 0.5 г/л. Культивирование проводили на термошейкере при 28°С при 140 об./мин. Рост штаммов оценивали при определении оптической плотности культуры (ОП600) на спектрофотометре UV-Visible BioSpec-mini («Shimadzu», Япония) при длине волны 600 нм в кювете с длиной оптического пути 1 см.
Ростовые характеристики штамма D2 определяли при выращивании в жидкой МСР с бензойной кислотой (1 г/л) и содержанием 30 г/л NaCl, оптимальным для роста культуры. Культивирование проводили на термошейкере при 28°С при 140 об./мин. в течение 2 недель. Рост штаммов оценивали при определении оптической плотности культуры (ОП 600 ). Параметры роста культуры рассчитывали согласно Г. Шлегеля [1987]. Эксперименты были выполнены в трехкратной повторности. Полученные данные обрабатывали с использованием стандартных пакетов компьютерных программ Microsoft Excel.
Выделение бактериальной ДНК. Единичную колонию чистой культуры бактерий при помощи платиновой петли помещали в пробирку «эппен-дорф», содержащую 100 мкл 0.05 NaOH. Смесь инкубировали при 95°C в течение 15 мин., затем охлаждали 15 мин. при температуре -20°C, далее центрифугировали при 12 000 об./мин. 30 сек. Процедуру повторяли 4 раза. Для проведения ам-плифкации отбирали 1 мкл супернатанта.
Амплификация и определение нуклеотидных последовательностей гена benA . Для амплификации гена benA , кодирующего α-субъединицу бензоат 1,2-диоксигеназы, использовали праймеры benA-F (5’-GCCCACGAGAGCCAGATTCCC-3’) и benA-R (5’-GGTGGCGGCGTAGTTCCAGTG-3’) при условиях, приведенных в публикации [Baggi et al., 2008]. Амплификацию осуществляли на приборе C1000 TouchTM Thermal Cycler («Bio-Rad Laboratories», США). В качестве положительного контроля был использован штамм Rhodococcus wratislaviensis КТ112-7, деструктор бензойной кислоты [Егорова и др., 2013]. Анализ продуктов амплификации и документирование полученных результатов осуществляли, как описано ранее [Пьянкова и др., 2020].
Определение нуклеотидных последовательностей гена benA проводили на автоматическом секвенаторе Genetic Analyzer 3500xl («Applied Biosystems», США), с применением реактивов Big Dye Terminator Ready Reaction Kit v 3.1 («Applied Biosystems», США), согласно рекомендациям производителя, на кафедре ботаники и генетики растений Пермского государственного национального исследовательского университета. Поиск гомоло- гичных последовательностей гена benA осуществляли с использованием базы данных GenBank . Множественное выравнивание транслированных аминокислотных последовательностей гена benA и построение филогенетического дерева проводили с использованием программы MEGA 7.0. При построении филогенетического дерева применяли кластерный метод «neighbor-joining». Оценку статистической достоверности ветвления («bootstrap»-анализ) устанавливали на основе 1000 альтернативных деревьев. Нуклеотидная последовательность гена benA депонирована в базу данных GenBank под номером MW862487.
Результаты и их обсуждение
Ранее из образца глинистых отложений соляной шахты ВКМС был выделен грамотрицательный штамм D2. В результате секвенирования и сравнения последовательностей гена 16S рРНК с типовыми штаммами из базы данных EzBioCloud было установлено, что данный штамм относится к се- мейству Halomonadaceae (класс Gammaproteobacteria) и имеет наибольшее сходство (99.43% по гену 16S рРНК) с типовым штаммом Halomonas taeanensis BH539T [Пьянкова и др., 2020].
Проведенные исследования по изучению дегра-дационных свойств штамма D2 показали, что он способен использовать в качестве единственного источника углерода и энергии бензойную кислоту, но не другие моно- и полиароматические соединения (в частности, салициловую, орто -фталевую кислоты, нафталин, бифенил).
Установлено, что штамм Halomonas sp. D2 является галофильным организмом и способен к эффективному росту в БСР при содержании хлорида натрия от 10 до 300 г/л. В сравнении, штамм Halomonas taeanensis BH539T выдерживал не более 250 г/л NaCl при культивировании в аналогичных условиях. Оба штамма не росли при отсутствии соли в среде. В МСР с использованием в качестве субстрата бензойной кислоты (1 г/л) штаммы Halomonas sp. D2 и H. taeanensis BH539T росли в присутствии 10‒70 г/л соли (табл. 1).
Таблица 1
Рост бактерий рода Halomonas в присутствии различных концентраций хлорида натрия
|
Штамм |
Агаризованная БСР, NaCl (г/л) |
Жидкая МСР, бензойная кислота (1 г/л), NaCl (г/л) |
|||||||||
|
Без NaCl |
10 |
100 |
150 |
200 |
250 |
300 |
Без NaCl |
30 |
50 |
70 |
|
|
H. taeanensis DSM 16463T |
– |
+ |
+ |
+ |
+ |
+ |
– |
– |
+++ |
++ |
+ |
|
Halomonas sp. D2 |
– |
+ |
+ |
+ |
+ |
+ |
+ |
– |
+++ |
+++ |
++ |
Примечание. «–» – рост не обнаружен; «+» – на агаризованной среде, колонии размеров больше 2 мм; «+» – в жидкой среде, ОП 600 от 0.1 до 0.3 ед.; «++» – ОП 600 от 0.4 до 0.7 ед.; «+++» – ОП 600 выше 0.7 ед.
Штамм D2 демонстрировал наибольший прирост биомассы при выращивании на бензоате в присутствии 30 г/л NaCl. На рисунке 1 представлена кривая роста штамма D2. На начальных этапах культивирования наблюдался замедленный рост культуры (ОП600 не превышала 0.2 ед.), толь- ко через 150 ч. был отмечен активный прирост биомассы. Максимальная ОП600, равная 1.05 ед., наблюдалась при 259 ч. (11-е сут.) культивирования. Скорость экспоненциального роста (µ) составляла 0.0211±0.003 ч–1.
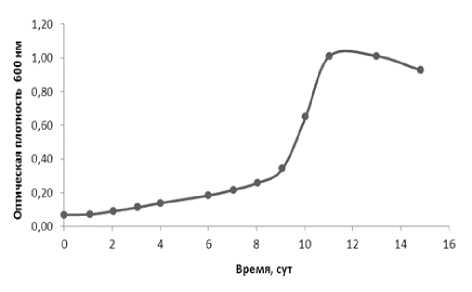
Рис. 1 . Рост штамма Halomonas sp. D2 в МСР (30 г/л NaCl) на бензойной кислоте (1 г/л) в качестве единственного источника углерода и энергии
На ДНК-матрице штамма D2 был амплифици-рован ген benA, кодирующий α-субъединицу бен- зоат 1,2-диоксигеназы – ключевого фермента, участвующего на начальном этапе окислении бен- зоата [Parales, Resnick, 2006]. Также фрагмент аналогичного размера (около 521 п.н.) был обнаружен в ДНК штамма H. taeanensis BH539T, что указывает на присутствие гена benA в ДНК типового штамма (рис. 2).
М 1 2 К+К-
Рис. 2 . Электрофореграмма результатов амплификации гена benA :
M – маркер 100+ bp DNA Ladder (Евроген, Россия), 1 – Halomonas sp. D2, 2 – H. taeanensis BH539 T , K+ – Rhodococcus wratislaviensis
КТ112-7, K- – отрицательный контроль
Полученный ампликон гена benA Halomonas sp. D2 был секвенирован. Проведен сравнительный анализ нуклеотидных последовательностей фрагмента гена benA штамма Halomonas sp. D2 с гомологичными последовательностями из базы данных GenBank (табл. 1). Установлено, что наиболее близким к изучаемому гену является ген α-субъединицы бензоат/толуат-1,2-диоксигеназы типового штамма H. taeanensis BH539T (FNCI01000003). Сходство гена benA штамма Halomonas sp. D2 c гомологичным геном H. taeanensis BH539T составляло 94.86%. С другими подобными генами представителей рода Halomonas уровень сходства не превышал 89.38%, а с генами штаммов других родов семейства Halomonadaceaе – 78.13% (ближайшая последовательность гена benA Chromohalobacter sp. HS2, EU155151) (табл. 2).
Таблица 2
Сравнительный анализ гена benA штамма Halomonas sp. D2 с ближайшими гомологичными последовательностями из базы данных GenBank
|
Гомологичные гены |
Номер в GenBank* |
Номер в GenBank** |
Сходство, % |
Место выделения |
Ссылка |
|
Бензоат/толуат 1,2-ДО, H. taeanensis BH539T |
FNCI01000003 |
SDF94072 |
94.86 |
Солнечная солеварня, Корея |
н.д. |
|
Бензоат 1,2-ДО, H. aestuarii Hb3 |
CP018139 |
APE30514 |
89.38 |
Солеварня, Корея |
н.д. |
|
Белок с кластером Риске [2Fe-2S], Halomonas sp. BM-2019 |
CP071922 |
QTF93273 |
87.90 |
Озерная вода, Танзания |
н.д. |
|
Бензоат 1,2-ДО, H. beime-nensis NTU-111 |
CP021435 |
ATJ82503 |
87.50 |
Солеварня, Тайвань |
Chen et al., 2017 |
|
Бензоат 1,2-ДО, H. organivorans CECT 5995T |
FN997646 |
CBR26855 |
86.74 |
Засоленная почва, Испания |
García et al., 2004 |
|
Белок с кластером Риске [2Fe-2S], Halomonas sp. PGE1 |
CP053032 |
QJQ97940 |
86.70 |
Гиперсоленая экосистема, Нидерланды |
н.д. |
|
Бензоат 1,2-ДО, Chromo-halobacter sp. HS2 |
EU155151 |
ABV82781 |
78.13 |
Солёные ферментированные моллюски |
Kim et al., 2008 |
Примечание: «н.д.» – нет данных; * – нуклеотидные последовательности; ** – аминокислотные последователь- ности.
На основании полученных данных построено филогенетическое дерево, показывающее положение транслированных аминокислотных последовательностей benA штамма Halomonas sp. D2 и гомологичных последовательностей представителей семейства Halomonadaceaе (рис. 3).
Гены benA, кодирующие большую субъединицу ключевого фермента деструкции БК – бензоат 1,2-диоксигеназы, выявлены в геномах бактерий различных таксономических групп [Егорова, Пьянкова, 2019]. На настоящем этапе исследований пока- зано, что ген benA штамма Halomonas sp. D2 является наиболее филогенетически близким benA-генам галофильных бактерий-деструкторов бензоата, рода Halomonas (сем. Halomonadaceae) и, кроме того, имеет высокий процент сходства (94.86%) с benA-геном типового штамма вида H. taeanensis, который является наиболее близкородственным по гену 16S рРНК штамму D2 [Пьянкова и др., 2020]. Таким образом, мы предполагаем, что benA-ген может быть использован в качестве филогенетического маркера для определения бакте- рий рода Halomonas среди деструкторов БК раз- личных таксонов прокариот.
- Бензоат 1,2-ДО, Halonwnas sp. D2 (MW862487)
Бензоат/толуат 1.2-ДО.Я kiwmensis BH539T(SDF94072)
------Бензоат 1.2-ДО.//, aestitarii НЬЗ(АРЕЗО514)
--------Бензоат 1.2-ДО, Н. beimenensisYTO-X 11 (ATJ82503)
-----------Белок с кластером Риске. HalomoiMs sp. ВМ-2019 (QTF93273)
----------Белок с кластером Риске. Halomonas sp. PGE1 (QJQ97940) Бензоат 1.2-ДО. //. organivomns СЕСТ 5995T(CBR26855)
------------Бензоат 1.2-ДО. Chromohalobacter sp HS2 (ABV82781)
।----------------------------------1
Ml
Рис. 3 . Филогенетическое дерево, построенное с использованием метода neighbor-joining, показывающее положение транслированных аминокислотных последовательностей гена benA Halomonas sp. D2 и ближайших последовательностей из базы данных GenBank
Заключение
В результате проведенных исследований было установлено, что штамм Halomonas sp. D2 является активным деструктором бензойной кислоты, способным осуществлять ее разложение (1 г/л) в присутствии высоких концентраций хлорида натрия (30‒70 г/л). Полученные данные указывают на возможность использования штамма при разработке технологий, направленных на очистку объектов окружающей среды от токсичных ароматических поллютантов.
Работа выполнена в рамках государственного задания, номер госрегистрации темы: АААА-А19-119112290008-4.
Список литературы Галофильный штамм-деструктор бензойной кислоты Halomonas sp. D2
- Егорова Д.О. и др. Деструкция ароматических углеводородов штаммом Rhodococcus wratislaviensis KT112-7, выделенным из отходов соледобывающего предприятия // Прикладная биохимия и микробиология. 2013. Т. 49, № 3. С. 267–278.
- Егорова Д.О., Пьянкова А.А. Скрининг гена альфа-субъединицы бензоат диоксигеназы в бактериальных ассоциациях, полученных в результате селекции на (хлор)ароматических соединениях // Вестник Пермского университета. Сер. Биология. 2019. Вып. 4. С. 464–470.
- Пьянкова А.А. и др. Характеристика бактерий, выделенных из рудника Верхнекамского месторождения солей (Пермский край) // Вестник Пермского университета. Сер. Биология. 2020. Вып. 4. С. 312–320.
- Шлегель Г. Общая микробиология: пер. с нем. М.: Мир, 1987. 567 с.
- Baggi G. et al. Co-metabolizm of di- and trichlorbenzoates in a 2-chlorobenzoate-degrading bacterial culture: Effect of the position and number of halosubstituents // International Biodeterioration and Biodegradation. 2008. Vol. 62, № 1. P. 57−64.
- Chen Y. et al. Revealing the saline adaptation strategies of the halophilic bacterium Halomonas beimenensis through high-throughput omics and transposon mutagenesis approaches // Science Reports. 2017. Vol. 7. P. 183−195.
- Fathepure B.Z. Recent studies in microbial degradation of petroleum hydrocarbons in hypersaline environments // Frontiers in Microbiology. 2014. Vol. 5. P. 173.
- Field J.A., Sierra-Alvarez R. Microbial transformation of chlorinated benzoates // Reviews in Environmental Science and BioTechnology. 2008. Vol. 7. P. 191–210.
- García M.T. et al. Halomonas organivorans sp. nov., a moderate halophile able to degrade aromatic compounds // International Journal of Systematic and Evolutionary of Microbiology. 2004. Vol. 54, № 5. P. 1723−1728.
- Kim D. et al. Molecular cloning and functional characterization of the genes encoding benzoate and phydroxybenzoate degradation by the halophilic Chromohalobacter sp. strain HS-2 // FEMS Microbiology Letters. 2008. Vol. 280, № 2. P. 235−241.
- Parales R.E., Resnick S.M. Aromatic ring hydroxylating dioxygenases // Pseudomonas / Eds. J.L. Ramos, R.C. Levesque. Boston: Springer, 2006. P. 287–340.
- Pieper D.H. Aerobic degradation of polychlorinated biphenyls. // Applied Microbiology Biotechnology. 2005. Vol. 67, № 2. P. 170–191.
- Raymond R.L. Microbial oxidation of n-paraffinic hydrocarbons // Developments in Industrial Microbiology. 1961. Vol. 2, № 1. P. 23–32.


