Гематологические особенности у больных ревматоидным артритом при эндопротезировании тазобедренного сустава
Автор: Ершов Антон Сергеевич, Антропова Ирина Петровна, Волокитина Елена Александровна, Евстигнеева Людмила Петровна
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 5 т.27, 2021 года.
Бесплатный доступ
Актуальность. У больных ревматоидным артритом (РА) и исходной анемией могут быть повышены риски развития осложнений после эндопротезирования тазобедренного сустава. Воспалительный процесс при РА является основным фактором, манифестирующим анемию, нейтропению, тромбоцитоз и эозинофилию. Данные изменения показателей крови имеют немаловажное значение для исходов больших ортопедических вмешательств. Цель. Определение гематологических особенностей у больных РА, нуждающихся в эндопротезировании тазобедренного сустава (ЭТС), и оценка их связи с кровопотерей при проведении данной операции. Материалы и методы. Изучены результаты эндопротезирования тазобедренного сустава у 44 пациентов в возрасте от 41 до 70 лет с III стадией обменно-дистрофического коксартроза (21) и коксартроза на фоне РА (23), пролеченных с 2018 по 2019 год в ГАУЗ СО СОКБ № 1 (г. Екатеринбург). Применены клинический, рентгенологический, компьютерно-томографический, лабораторный и статистические методы исследования. Показатели крови изучали с использованием автоматического гематологического анализатора Sysmex XT-4000i. Для анализа данных использовали программу Statistica. Изучаемые группы сравнивали с помощью непараметрического U-теста Манна-Уитни, для определения связи между показателями использовали расчет коэффициента корреляции Спирмена. Результаты принимались статистически значимыми при р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Эндопротезирование тазобедренного сустава, ревматоидный артрит, остеоартроз, тромбоциты, гематологические показатели
Короткий адрес: https://sciup.org/142231541
IDR: 142231541 | УДК: 616.155.25:616.728.2-002.77-001.5-089.227.844-77 | DOI: 10.18019/1028-4427-2021-27-5-514-520
Hematological parameters of rheumatoid arthritis patients undergoing total hip replacement
Background Patients with rheumatoid arthritis (RA) and baseline anemia may have an increased risk of complications after total hip replacement (THR). Inflammation in RA is the main factor manifesting anaemia, neutropenia, thrombocytosis and eosinophilia. The changes in blood components are important for the outcomes of major orthopaedic surgery. The purpose was to identify hematological parameters in RA patients undergoing THR and assess the effect on intraoperative blood loss. Material and methods Outcomes of 44 THR patients treated for grade III degenerative coxarthrosis (n = 21, OA group) and RA coxarthrosis (n = 23, RA group) in Ekaterinburg regional hospital № 1 between 2018 and 2019 were reviewed. The patients' age ranged from 41 to 70 years. Clinical, radiological, laboratory examinations, computed tomography and statistical analysis were used for the study. Cell counting was produced with the Sysmex XT-4000i automated hematology system. Statistical analysis was performed using the tools of Statistica software. Non-parametric Mann-Whitney test was used to compare cell counts between the groups. The Spearman Rank correlation was used to analyse the correlation between the the cell counts in the groups. For calculations, a significance level of р function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Гематологические особенности у больных ревматоидным артритом при эндопротезировании тазобедренного сустава
Ревматоидный артрит (РА) является системным ауто- менения в системе крови. Тяжелые поражения суставов иммунным заболеванием, характеризующимся синови- при РА приводят к необходимости проведения операции альным воспалением, прогрессирующим разрушением эндопротезирования, которая позволяет восстановить суставов и внесуставными проявлениями, включая из- опорно-двигательную функцию пораженного сочле-
нения и существенно снизить болевой синдром [1]. Имплантация искусственного тазобедренного или коленного сустава является достаточно травматичным хирургическим вмешательством, которое, само по себе, сопровождается интенсивным воспалительным процессом и нередко осложняется значительной кровопотерей и/или тромбозом [2, 3]. Проведено значительное число работ, в которых показано, что наличие РА у пациентов повышает риски осложнений эндопротезирования: исходная анемия, низкий уровень гемоглобина могут приводить к необходимости периоперационной гемотрансфузии [4–6]. Ряд исследователей отмечают, что клинические результаты тотальной артропластики крупного сустава при РА хуже, чем результаты аналогичной операции при ОА [5, 7, 8]. Вместе с тем, некоторыми авторами представлены доказательства того, что пациенты с РА, перенесшие эндопротезирование крупного сустава, имеют не больше риска осложнений по сравнению с пациентами с ОА [9,10]. Было показано, что в медицинском центре с большим объемом операций по эндопротезированию у пациентов с РА, наличие данной патологии не увеличивает послеоперационные нежелательные явления по сравнению с пациентами, страдающими ОА [11]. Воспалительный процесс при РА является основным фактором, манифестирующим анемию, нейтропению, тромбоцитоз и эозинофилию [12, 13]. Очевидно, что изменения, которые наблюдаются в крови больных РА, имеют немаловажное значение для исходов больших ортопедических вмешательств.
Целью работы являлось определение гематологических особенностей у больных РА, нуждающихся в эндопротезировании тазобедренного сустава (ЭТС), и оценка их связи с кровопотерей при проведении данной операции.
МАТЕРИАЛЫ И МЕТОДЫ
Данное исследование базируется на анализе результатов первичного эндопротезирования тазобедренного сустава у 44 пациентов в возрасте от 41 до 70 лет с III стадией обменно-дистрофического коксартроза (21) и коксартроза на фоне РА (23), пролеченных в травматологическом отделении ГАУЗ СО «Свердловская областная клиническая больница № 1» (ГАУЗ СО СОКБ № 1, г. Екатеринбург) с 2018 по 2019 год. Женщин было 23 (75 %), мужчин – 11 (25 %). Преобладающее большинство (67,4 %) составили пациенты трудоспособного возраста, однако из-за выраженного болевого синдрома многие из них на момент поступления в клинику были неработоспособными. Всем пациентам до операции был проведен комплекс клинических исследований с целью подтверждения диагноза и определения степени тяжести заболевания.
Критериями включения пациентов в исследование были достоверный диагноз обменно-дистрофического коксартроза, подтвержденный клинико-рентгенологическими данными, и коксартроза на фоне ревматоидного артрита (РА), в соответствии с критериями Европейской антиревматической лиги (EULAR) ACR 2010 г., возраст пациентов от 41 до 70 лет, согласие пациента на участие в исследовании. Критериями исключения явились возраст менее 41 и старше 70 лет, тяжелые сопутствующие заболевания в стадии обострения или декомпенсации, наличие которых могло повлиять на результаты исследования.
В основную группу были включены 23 пациента с РА (группа РА), в группу сравнения вошел 21 пациент с обменно-дистрофическим коксартрозом (группа ОА). В группе РА мужчин было 2, в группе ОА – 8 (р = 0,247). Средний возраст больных с РА составил 57,2 ± 8,4 года (среднее ± SD), больных с ОА – 57,3 ± 7,2 года (среднее ± SD) (р = 0,762). Сопутствующая соматическая патология встретилась в 39 случаях (88,6 %): в основном пациенты страдали гипертонической болезнью (52,7 %), сахарным диабетом II типа (6,5 %), гастритом (13,4 %). В 73,9 % случаев отмечен избыточный вес, ожирение I–II степени выявлено у 18 (39,1 %) больных. На момент включения в исследование базисную противовоспалительную терапию получали 68,75 % пациентов группы РА: преимущественно применялся метотрексат (43,75 %), сульфасалазин (25 %) и лефлуномид (6,25 %). Глюкокортикоиды принимали 81,25 % пациентов: в большинстве случаев (62,5 %) – предни- золон (от 5 до 15 мг в сутки), в 18,75 % случаев – метилпреднизолон (от 4 до 48 мг в сутки).
В клинике с 2018 года используется система углубленной подготовки пациента в предоперационном периоде с минимизацией операционной травмы («Fast-track» – хирургия – быстрый путь в хирургии) в сочетании с активной послеоперационной реабилитацией («ERAS» (early rehabilitation after surgery) – ранняя реабилитация после операции), которая позволяет наиболее эффективно хирургически пролечить больных травматолого-ортопедического профиля с минимальным риском каких-либо осложнений. Все больные РА перед ЭТС на 2 недели госпитализировались в профильное ревматологическое отделение ГАУЗ СО СОКБ № 1, где проводилось комплексное обследование и консервативное лечение для снижения активности РА и коррекции анемии перед ортопедической операцией. Все пациенты были прооперированы одной хирургической бригадой: выполнена первичная тотальная артропластика тазобедренного сустава стандартными эндопротезами фирм «DePuy» цементной (24) и бесцементной (20) фиксации из переднелатерального доступа в модификации Мюллера, в положении пациента на боку. За 12 часов до операции пациенты получали фрагмин в дозе 2500 ЕД, за 30 минут до начала операции 2 грамма цефазолина.
Продолжительность вмешательства (с момента начала выполнения анестезии и до наложения асептических повязок на область раны) составила 80,4 ± 21,1 мин. в группе РА и 83,1 ± 23,3 мин. в группе ОА. Введение кристаллоидов проводилось интраоперационно всем пациентам по стандартной схеме. Количество потерянной крови определяли измерением объема аспирата в операционном отсосе «Армед 7Е-А» (Россия). Салфетки для гемостаза и просушки раны при операциях у больных этих двух групп не использовали. Дренажи в послеоперационной ране не оставляли, зашивали рану без дренажей. Кровопотерю оценивали также по снижению количества эритроцитов и гемоглобина в течение первых суток после операции. Гемотрансфузий периоперационно не было проведено ни у одного из обследованных лиц. В обеих изучаемых группах осложнений хирургического лечения выявлено не было. Использование принципов «fast track» хирургии, а также ERAS, включающих подбор методов анестезии, минимально инвазивных способов оператив- ного лечения, оптимального контроля боли и активного послеоперационного восстановления, уменьшало стрессовые реакции и дисфункцию органов, значительно сокращая время, необходимое для полного восстановления. Продолжительность лечения в стационаре составила среднем 10 ± 2 дня.
Исследуемые группы были сопоставимы по полу, возрасту, стадийности заболевания, сопутствующей патологии, по периоперационному ведению, виду хирургического вмешательства, способу его выполнения, способу фиксации протеза и виду используемой имплантационной системы.
Показатели крови анализировались с использованием автоматического гематологического анализатора Sysmex XT-4000i. Образцы крови собирали в пробирки с К2ЭДТА (дикалий этилендиаминтетрауксусная кислота) в качестве антикоагулянта и анализировали в течение одного часа после венопункции для исключения набухания тромбоцитов [14].
Статистическую обработку данных производили с помощью пакета анализа данных Statistica. Статистическую значимость различий сравниваемых признаков в группах выявляли с помощью непараметрического U-теста Манна-Уитни, при проведении корреляционного анализа использовали расчет коэффициента корреляции Спирмена. Результаты принимались как статистически значимые при р < 0,05.
Соблюдение этических принципов: пациенты подписали добровольное информированное согласие на публикацию их данных без идентификации личности.
РЕЗУЛЬТАТЫ
Результаты определения гематологических параметров до и через 1 сутки после операции представлены в таблице 1. До операции существенных различий по общему количеству лейкоцитов, уровню нейтрофилов, лимфоцитов, моноцитов, эозинофилов между основной (РА) и контрольной (ОА) группами не обнаружено. В то же время в группе РА выявили выраженную тенденцию к снижению числа эритроцитов и существенное снижение уровня гемоглобина по сравнению с группой ОА. Тромбоцитарные показатели также имели существенные различия между группами: в группе РА количество тромбоцитов было значительно выше, но средний объем тромбоцитов (MPV) был значительно ниже, чем в группе ОА.
Спустя сутки после ЭТС в обеих группах значения большинства показателей изменились: повысилось общее количество лейкоцитов, в частности, нейтрофилов, снизилось количество лимфоцитов, эритроцитов, тромбоцитов, уровень гемоглобина, тромбокрит. При этом после операции значимых различий между группами по показателям как белой, так и красной крови выявлено не было. Различия между группами по среднему объему тромбоцитов нивелировались, однако количество тромбоцитов в группе РА сохранялось на более высоком уровне, чем в группе ОА.
Прямое определение количества потерянной крови при эндопротезировании у пациентов, включенных в исследование, не выявило статистически значимых различий, хотя в группе РА кровопотеря была несколько меньше, чем в группе ОА: 210 [200; 270] и 230 [210; 290] мл (рис. 1, а). Падение уровня эритроцитов было значительно ниже в группе РА по сравнению с группой ОА: 0,73 [0,52; 1,02] и 1,01 [0,83; 1,41] × 106/мкл соответственно (р = 0,038) (рис. 1, б). Падение уровня гемоглобина также было менее выраженным в группе РА по сравнению с группой ОА: 23,0 [12,0; 31,0] и 29,0 [23,0; 36,0] г/л соответственно (p = 0,068) (рис. 1, в).
Таблица 1
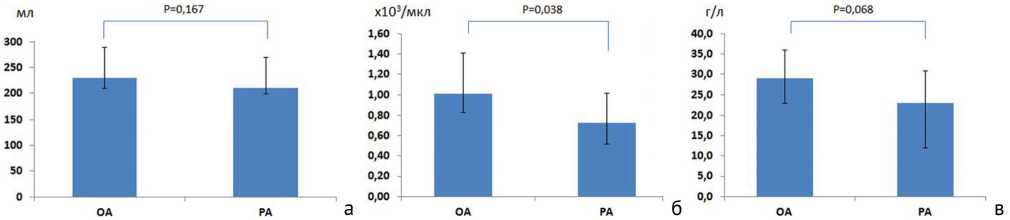
Рис. 1. Кровопотеря (а), снижение уровня эритроцитов (б) и гемоглобина (в) у пациентов с остеоартритом (ОА) и ревматоидным артритом (РА) при эндопротезировании тазобедренного сустава. Результаты представлены как медиана [интерквартильный интервал]
Гематологические показатели у пациентов с РА и ОА перед эндопротезированием тазобедренного сустава и через 1 сутки после операции
|
Показатель |
До операции |
Первые сутки после операции |
||||
|
РА |
ОА |
p |
РА |
ОА |
p |
|
|
Лейкоциты (× 103/мкл) |
7,60 [5,92; 9,30] |
6,60 [5,50; 8,50] |
0,354 |
10,20 [9,20; 11,20] |
8,54 [7,50; 10,51] |
0,159 |
|
Нейтрофилы (× 103/мкл) |
4,40 [3,10; 6,36] |
3,98 [3,22; 4,50] |
0,316 |
7,47 [6,89; 8,80] |
6,37 [5,25; 7,91] |
0,212 |
|
Лимфоциты (× 103/мкл) |
2,07 [1,69; 2,94] |
1,93 [1,52; 2,49] |
0,430 |
1,35 [1,13; 1,56] |
1,26 [1,00; 1,49] |
0,475 |
|
Моноциты (× 103/мкл) |
0,54 [0,43; 0,75] |
0,51 [0,40; 0,66] |
0,381 |
0,94 [0,74; 1,05] |
1,02 [0,71; 1,16] |
0,263 |
|
Эозинофилы (× 103/мкл) |
0,08 [0,00; 0,16] |
0,06 [0,00; 0,10] |
0,790 |
0,04 [0,01; 0,11] |
0,03 [0,01; 0,09] |
0,405 |
|
Базофилы (× 103/мкл) |
0,03 [0,00; 0,05] |
0,01 [0,00; 0,02] |
0,233 |
0,02 [0,01; 0,04] |
0,01 [0,01; 0,03] |
0,147 |
|
Эритроциты (× 106/мкл) |
4,37 [4,10; 4,68] |
4,75 [4,30; 4,98] |
0,086 |
3,65 [3,23; 4,01] |
3,71 [3,27; 4,03] |
0,839 |
|
Гемоглобин (г/л) |
133,0 [119,0; 136,0] |
140,0 [124,0; 146,0] |
0,031 |
107,0 [103,0; 113,0] |
107,0 [102,0; 116,0] |
0,228 |
|
Тромбоциты (× 103/мкл) |
257,0 [233,0; 306,0] |
219,0 [178,0; 262,0] |
0,026 |
213,0 [174,0; 267,0] |
170,0 [146,0; 225,0] |
0,025 |
|
MPV (фл) |
8,7 [8,3; 10,0] |
9,9 [9,1; 10,8] |
0,043 |
9,8[8,6; 10,6] |
10,1 [9,5; 10,5] |
0,17 |
Примечание: РА – ревматоидный артрит, ОА – остеоартрит, MPV – средний объем тромбоцитов, p – статистическая значимость различий между группами РА и ОА. Результаты представлены как медиана [интерквартильный интервал].
ОБСУЖДЕНИЕ
По данным литературных источников, анемия наблюдается у 33-60 % пациентов с РА [15, 16] и коррелирует с активностью заболевания [17, 18]. Выявлена связь между анемией и инвалидностью у пациентов с РА [19]. Наиболее часто встречается анемия при хронических заболеваниях и железодефицитная анемия [20–22]. Механизмы развития анемии до конца не ясны, но известно, что воспалительные цитокины, такие как ИЛ6 и ФНО- α , влияют на регуляцию обмена железа, стимулируя продукцию гормона гепсидина, который, в свою очередь, вызывает деградацию трансмембранного белка ферропортина [20]. Кроме того, нарушается эритропоэз, пролиферация предшественников эритроида, продукция эритропоэтина и продолжительность жизни эритроцитов [15, 23]. В нашем исследовании было обнаружено, что у пациентов с РА перед проведением ЭТС уровень эритроцитов и гемоглобина ниже, чем у пациентов с ОА, что объясняется связью с воспалительным процессом при РА и согласуется с данными других авторов [24, 25]. В данной работе у 30,4 % пациентов с РА до операции уровень гемоглобина был ниже 120 г/л, но не ниже 110 г/л. После операции ни у одного из пациентов уровень гемоглобина не опускался ниже 80 г/л.
Современные методы оценки кровопотери включают гравиметрический метод и визуальную оценку, хотя признается, что они недостаточно точны [26]. Кроме того, при эндопротезировании тазобедренного сустава значительная часть крови, истекающей при повреждении сосудов, остается в мягких тканях. В последние годы для снижения риска развития послеоперационной перипротезной инфекции дренажные системы при эндопротезировании крупных суставов не применяются [27–29]. В нашем исследовании дренажи также не устанавливались, поэтому отследить по-слеоперционную кровопотерю по дренажам также не представлялось возможным. Для оценки кровопотери, кроме измерения объема аспирационного содержимого в «Армед 7Е-А» (Россия), мы использовали косвенную оценку потери крови по уровню снижения эритроцитов и гемоглобина. Измерение концентрации гемоглобина для оценки интраоперационной кровопотери предлагается и другими авторами [30, 31]. Полученные нами данные указывают на то, что потеря крови при ЭТС у пациентов с РА не больше, чем у пациентов с ОА. Тенденцию к менее объемной кровопотере у пациентов с РА можно объяснить более активным формированием сгустков, закрывающих повреждения сосудов при хирургическом вмешательстве. Такое предположение основывается на наличии в крови более высокого уровня тромбоцитов, принимающих основное участие в гемостазе. Кроме того, существует тесная корреляционная связь между функциональной активностью тромбоцитов, маркерами воспаления и течением РА [32].
Все исследователи, изучающие морфофункциональные характеристики тромбоцитов при РА, сходятся во мнении, что количество, средний объем тромбоцитов (MPV), тромбокрит (PTC), вариабельность тромбоцитов по объему (PDW) существенно изменяются при РА [33–36]. Вместе с тем, нет единого мнения относительно характера этих изменений. Ранее было показано, что MPV при РА имеет положительную корреляцию с маркерами воспаления и тяжестью заболевания, причем данный показатель снижался после лечения [34]. В противоположность этому, D.A. Kim and T.Y. Kim, сравнивая гематологические показатели пациентов с остеоартритом и РА, показали, что у пациентов с РА существенно выше количество тромбоцитов, но значительно ниже показатели MPV и PDW [35]. B. Kisacik et al. также показали, что у пациентов с РА объем тромбоцитов значительно ниже, чем у пациентов с ОА; после лечения MPV увеличивался, оставаясь, тем не менее, значительно ниже, чем у пациентов с ОА [33]. По данным Işık et al., PTC положительно коррелировал с С-реактивным белком, а показатели MPV и PDW имели отрицательную корреляцию с данным маркером воспаления при РА [36]. Мы обнаружили, что у пациентов с РА наблюдается положительная корреляционная связь между количеством лейкоцитов и PTC (коэффициент корреляции Спирмена rs = 0,48; р < 0,05) и отрицательная корреляционная связь между количеством лейкоцитов и MPV (rs = -0,43; р < 0,05), что также можно объяснить ассоциированностью тромбоцитарных параметров с уровнем воспаления.
Мы обнаружили, что MPV у больных РА существенно ниже, чем у пациентов с обменно-дистрофическим кок-сартрозом. Объем тромбоцитов является очень важным морфофункциональным показателем. Тромбоциты большего объема имеют более высокий прокоагуляционный и провоспалительный потенциал, поскольку содержат в своих гранулах большое количество соответствующих компонентов, которые выделяются при активации [37]. Вместе с тем, активированные тромбоциты продуцируют микрочастицы, которые участвуют в патогенезе РА, играя важную роль в представлении антигена, в воспалении, ангиогенезе, передаче сигналов между клетками и в деградации внеклеточного матрикса суставного хряща [38, 32]. Кроме того, микрочастицы, выделяемые тромбоцитами, несут и активаторы коагуляционного процесса [39]. Снижение объема тромбоцитов у пациентов с РА, обнаруженное нами, может свидетельствовать о повышенной продукции ими микрочастиц, что, в свою очередь, дает возможность более быстро сформировать сгустки, препятствующие потере крови.
D.A. Kim and T.Y. Kim, сравнивая лейкоцитарные показатели пациентов с остеоартритом и РА, показали, что у пациентов с РА существенно выше количество лейкоцитов, в частности, нейтрофилов [35]. Нейтрофилы играют важную роль на начальных этапах заболевания ревматоидным артритом: на ранней стадии они мигрируют в суставную полость, активизируются и включаются в воспалительный процесс. Внеклеточные ловушки нейтрофилов (NETs) принимают участие в выработке аутоантител против цитруллинированных белков, инициирующих иммунную реакцию при ревматоидном артрите. В то же время провоспалительные цитокины стимулируют миграцию нейтрофилов, апоптоз и образование NETs [40, 41]. У пациентов с РА может наблюдаться и нейтропения, которая, как правило, связана с наличием синдрома Фелти или Т-клеточного лейкоза из больших гранулярных лейкоцитов [42, 43]. Вместе с тем, в настоящее время признается, что нейтрофильный лизис играет важную роль в патогенезе РА, поскольку гибель нейтрофильных клеток приводит к стимулированию цитруллинирования, посттрансляционной модификации белка, катализируемой ферментами пептидил аргинин деиминазами, превращающими аргинин в цитруллин [44, 45]. В нашем исследовании пациенты с РА и ОА не имели значимых различий ни по общему количеству лейкоцитов, ни по количеству нейтрофилов.
Эозинофилы – полифункциональные лейкоциты, обладающие широким набором иммуномодулирующих факторов [46]. В настоящее время показано, что при РА они оказывают противовоспалительное действие, поскольку способны индуцировать формирование у макрофагов «противовоспалительного» фенотипа M2 посредством ингибирования сигнального пути I κ B/P38 MAP-киназы [47]. Мы не выявили доопераци-онных различий в уровне лейкоцитов данного типа у пациентов с РА и ОА.
В целом, уровень и соотношение клеток белой крови у больных РА после проведения предоперационной подготовки в ревматологическом отделении ГАУЗ СОКБ № 1 был близок к таковому у пациентов с ОА.
Можно полагать, что и дооперационный уровень воспалительного процесса имел сходную выраженность. Кроме того, у всех больных РА, включенных в исследование, после предоперационного корректирующего лечения уровень гемоглобина был не ниже 100 г/л, что соответствовало анемии легкой степени. Таким образом, отсутствие у пациентов с РА периоперационных гемотрансфузий, клинически выраженных тромбоэмболических, а также других осложнений хирургического лечения можно считать следствием адекватной предоперационной подготовки.
Результаты нашей работы согласуются с исследованиями, которые показывают, что при выполнении ЭТС пациентам с РА в условиях специализированного центра частота осложнений при РА не выше, чем при ОА [9, 11, 48]. В частности, анализ результатов ЭТС более 120 тысяч пациентов с ОА и более 6 тысяч пациентов с РА показал, что пациенты с РА имели эквивалентные периоперационные риски [49].
ВЫВОДЫ
Операция эндопротезирования тазобедренного сустава на сегодняшний день является наиболее эффективным, но в то же время наиболее сложным ортопедическим вмешательством, позволяющим в короткий реабилитационный период восстановить безболезненные движения в пораженном суставе. Особую группу составляют больные с системными заболеваниями соединительной ткани, а именно, ревматоидным артритом с порозными изменениями костной ткани на фоне длительной иммуносупрессивной терапии. Помимо технических проблем имплантации протеза в измененные тазовую и бедренную кости, у больных РА может быть повышен риск развития общих осложнений эндопротезирования на фоне исходной анемии и низкого уровня гемоглобина.
В результате проведенного исследования нами было определено, что гематологические особенности, имею- щиеся у больных РА, прошедших специализированную предоперационную подготовку, не приводят к повышению уровня кровопотери при операции эндопротезирования тазобедренного сустава. Нивелирование лейкоцитарных показателей в дооперационном и раннем послеоперационном периоде может служить свидетельством отсутствия значимого дополнительного влияния РА на послеоперационный воспалительный процесс. Предотвратить развитие тяжелых общих и локальных осложнений при тотальной артропластике тазобедренного сустава возможно тщательным предоперационным обследованием, специализированной медикаментозной подготовкой, направленной на снижение воспаления и коррекцию исходной анемии, технологичным атравматичным выполнением хирургического вмешательства, ранней послеоперационной реабилитацией.
Список литературы Гематологические особенности у больных ревматоидным артритом при эндопротезировании тазобедренного сустава
- Orthopaedic surgery in 255 patients with inflammatory arthropathies: longitudinal effects on pain, physical function and health-related quality of life / H. Osnes-Ringen, T.K. Kvien, J.E. Henriksen, P. Mowinckel, H. Dagfinrud // Ann. Rheum. Dis. 2009. Vol. 68, No 10. P. 1596-1601.
- Волокитина Е.А., Ершов А.С., Хабиб М. Эндопротезирование тазобедренного сустава при протрузионной деформации вертлужной впадины на фоне ревматоидного артрита, осложненного подвертельным переломом бедренной кости. Случай из практики. // Уральский медицинский журнал. 2018. № 4. С. 117-120.
- Influence of preoperative platelet activity on coagulation and blood loss in large orthopedic surgery / I. Antropova, B. Yushkov, I. Shlykov, E. Volokitina // Research and Practice in Thrombosis and Haemostasis. 2018. Vol. 2, No S1. Special Issue: аbstracts of the 64th Annual Meeting of the Scientific Standardization Committee of the International Society on Thrombosis and Haemostasis (July 18-21, 2018). P. 9-10.
- Risk Factors for Transfusions Following Total Joint Arthroplasty in Patients With Rheumatoid Arthritis / E. Salt, A.T. Wiggins, M.K. Rayens, K. Brown, K. Eckmann, A. Johannemann, R.D. Wright, L.J. Crofford // J. Clin. Rheumatol. 2018. Vol. 24, No 8. P. 422-426. DOI: 10.1097/ RHU.0000000000000755.
- Risk Factors Associated With Short-term Clinical Results After Total Hip Arthroplasty for Patients With Rheumatoid Arthritis / T. Imagama, A. Tokushige, K. Seki, T. Seki, H. Ogasa, T. Taguchi // Orthopedics. 2018. Vol. 41, No 6. P. e772-e776. DOI: 10.3928/01477447-20180828-06.
- Mean Platelet Volume and Blood Loss in Total Hip Replacement Surgery / I.P. Antropova, E.A. Volokitina, A. Arkhipova, M.V. Gilev, S.M. Kutepov // Research and Practice in Thrombosis and Haemostasis. 2019. Vol. 3, Special Issue: аbstracts of the XXVII Congress of the International Society on Thrombosis and Haemostasis (July 6-10, 2019). Р. 213-214. https://onlinelibrary.wiley.com/toc/24750379/2019/3/S1.
- Factors that predict short-term complication rates after total hip arthroplasty / N.F. Soohoo, E. Farng, J.R. Lieberman, L. Chambers, D.S. Zingmond // Clin. Orthop. Relat. Res. 2010. Vol. 468, No 9. P. 2363-2371. DOI: 10.1007/s11999-010-1354-0.
- Incidence and risk factors of prosthetic joint infection after total hip or knee replacement in patients with rheumatoid arthritis / T. Bongartz, C.S. Halligan, D.R. Osmon, M.S. Reinalda, W.R. Bamlet, C.S. Crowson, A.D. Hanssen, E.L. Matteson // Arthritis Rheum. 2008. Vol. 59, No 12. P. 1713-1720. DOI: 10.1002/art.24060.
- Lee D.K., Kim H.J., Lee D.H. Incidence of Deep Vein Thrombosis and Venous Thromboembolism following TKA in Rheumatoid Arthritis versus Osteoarthritis: A Meta-Analysis // PLoS One. 2016. Vol. 11, No 12. Р. e0166844. DOI: 10.1371/journal.pone.0166844.
- Patients with Rheumatoid Arthritis have Similar Excellent Outcomes after Total Knee Replacement Compared with Patients with Osteoarthritis / S.M Goodman, B. Johnson, M. Zhang, W.T Huang, R. Zhu, M. Figgie, M. Alexiades, L.A. Mandl // J. Rheumatol. 2016. Vol. 43, No 1. P. 46-53. DOI: 10.3899/jrheum.150525.
- Rheumatoid arthritis does not increase risk of short-term adverse events after total knee arthroplasty: a retrospective case-control study / Z.J. LoVerde, L.A. Mandl, B.K. Johnson, M.P. Figgie, F. Boettner, Y.Y. Lee, S.M. Goodman // J. Rheumatol. 2015. Vol. 42, No 7. P. 1123-1130. DOI: 10.3899/ jrheum.141251.
- Bowman S.J. Hematological manifestations of rheumatoid arthritis // Scand. J. Rheumatol. 2002. Vol. 31, No 5. P. 251-259. DOI: 10.1080/030097 402760375124.
- Hematological Improvement of Patients with Active Rheumatoid Arthritis by p-D-Mannuronic Acid (M2000) as a Novel NSAID with Immunosuppressive Property / H. Ahmadi, A.R. Jamshidi, M. Mahmoudi, F. Gharibdoost, M. Vojdanian, M.J. Fattahi, N. Rastkari, Z. Aghazadeh, A. Mirshafiey // Iran J. Allergy Asthma Immunol. 2017. Vol. 16, No 5. Р. 433-442.
- Mean platelet volume measurement, EDTA or citrate? / M.S. Dastjerdi, T. Emami, A. Najafian, M. Amini // Hematology. 2006. Vol. 11, No 5. P. 317319. DOI: 10.1080/10245330600954163.
- Галушко Е.А. Клиническое значение определения геп-сидина при анемии у больных ревматоидным артритом // Klin. Med. 2014. Vol. 92, No 6. P. 21-27.
- Prevalence and outcomes of anemia in rheumatoid arthritis: a systematic review of the literature / A. Wilson, H.T. Yu, L.T. Goodnough, A.R. Nissenson // Am. J. Med. 2004. Vol. 116, No Suppl. 7A. Р. 50S-57S. DOI: 10.1016/j.amjmed.2003.12.012.
- Association of Anemia with Activities of Daily Living in Chinese Female Centenarian / W. Jia, S. Wang, K. Han, M. Liu, S. Yang, W. Cao, Y. He // J. Nutr. Health Aging. 2020. Vol. 24, No 3. P. 346-351. DOI: 10.1007/s12603-020-1326-3.
- Anaemia in Newly Diagnosed Patients of Rheumatoid Arthritis and its Correlation with Disease Activity / L. Goyal, P.J. Shah, R.N. Yadav, R. Saigal, A. Agarwal, S. Banerjee // J. Assoc. Physicians India. 2018. Vol. 66, No 5. P. 26-29.
- Association of anemia and physical disability among patients with rheumatoid arthritis / C. Han, M.U. Rahman, M.K. Doyle, J.M. Bathon, J. Smolen, A. Kavanaugh, R. Westhovens., E.W. St Clair, D. Baker, M. Bala // J. Rheumatol. 2007. Vol. 34, No 11. P. 2177-2182.
- Гринштейн Ю.И., Шабалин В.В., Кусаев В.В. Анемический синдром при ревматоидном артрите: подходы к диагностике и возможности терапии. Терапевтический архив. 2016. Т. 88б № 5. С. 107-112. DOI: 10.17116/terarkh2016885107-112.
- Agrawal S., Misra R., Aggarwal A. Anemia in rheumatoid arthritis: high prevalence of iron-deficiency anemia in Indian patients // Rheumatol. Int. 2006 Vol. 26, No 12. P. 1091-1095. DOI: 10.1007/s00296-006-0133-4.
- Etanercept improved anemia and decreased hepcidin gene expression in a rat model of rheumatoid arthritis / M.S. Elsheemy, A.H. Hasanin, A. Mansour, S.I. Mehrez, M. Abdel-Bary // Biomed. Pharmacother. 2019. Vol. 112. P. 108740. DOI: 10.1016/j.biopha.2019.108740.
- Anemia of chronic disease in rheumatoid arthritis is associated with increased apoptosis of bone marrow erythroid cells: improvement following anti-tumor necrosis factor-alpha antibody therapy / H.A. Papadaki, H.D. Kritikos, V. Valatas, D.T. Boumpas, G.D. Eliopoulos // Blood. 2002. Vol. 100, No 2. Р. 474-482. DOI: 10.1182/blood-2002-01-0136.
- Tranexamic Acid Does Not Reduce the Risk of Transfusion in Rheumatoid Arthritis Patients Undergoing Total Joint Arthroplasty / K.W. Morse, N.K. Heinz, J.M. Abolade, J.I. Wright-Chisem, L.A. Russell, M. Zhang, S.Z. Mirza, D.E. Orange, M.P. Figgie, P.K. Sculco, S.M. Goodman // J. Arthroplasty. 2020. Vol. 35, No 9. Р. 2367-2374. DOI: 10.1016/j.arth.2020.04.029.
- Factors Associated With Perioperative Transfusion in Lower Extremity Revision Arthroplasty Under a Restrictive Blood Management Protocol / S.S. Rao, Y.P. Chaudhry, S.A. Hasan, V. Puvanesarajah, R.M. Amin, J.K. Oni, R.S. Sterling, H.S. Khanuja // J. Am. Acad. Orthop. Surg. 2021. Vol. 29, No 8. P. e404-e409. DOI: 10.5435/JAAOS-D-20-00185.
- Real-time evaluation of an image analysis system for monitoring surgical hemoglobin loss / G. Konig, J.H. Waters, M. Javidroozi, B. Philip, V. Ting, G. Abbi, E. Hsieh, G. Tully, G. Adams // J. Clin. Monit. Comput. 2018. Vol. 32, No 2. P. 303-331. DOI: 10.1007/s10877-017-0016-0.
- Лычагин А.В., Грицюк А.А., Гасымов А.Ш. Вопросы дренирования раны при первичном эндопротезировании тазобедренного сустава (Литературный обзор) // Кафедра травматологии и ортопедии. 2018. № 1(31). С. 28-33.
- Влияние дренирования послеоперационной раны на частоту трансфузий эритроцитов после первичного эндопротезирования тазобедренного сустава / Н.Д. Гречанюк, А.В. Зверьков, А.В. Овсянкин, Е.Б. Жибурт // Вестник травматологии и ортопедии им. Н.Н. Приорова. 2006. № 4. С. 12-16.
- Скрытая кровопотеря после тотального эндопротезирования коленного сустава на фоне комплексной антикоагулянтной тромбопрофилак-тики / В.Б. Накопия, Н.Н. Корнилов, С.А. Божкова, А.В. Каземирский, М.Ю. Гончаров // Современные проблемы науки и образования. 2017. № 6. С. 97. URL: http://www.science-education.ru/ru/article/view?id =27272 (дата обращения: 10.02.2021).
- Accuracy and Trending of Continuous Noninvasive Hemoglobin Monitoring in Patients Undergoing Liver Transplantation / P.H. Huang, B.F. Shih, Y.F. Tsai, P.C. Chung, F.C. Liu, H.P. Yu, W.C. Lee, C.J. Chang, C.C. Lin // Transplant. Proc. 2016. Vol. 48, No 4. Р. 1067-1070. DOI:10.1016/j. transproceed.2015.12.121.
- Clinical Practice Guidelines From the AABB: Red Blood Cell Transfusion Thresholds and Storage / J.L. Carson, G. Guyatt, N.M. Heddle, B.J. Grossman, C.S. Cohn, M.K. Fung, T. Gernsheimer, J.B. Holcomb, L.J. Kaplan, L.M. Katz, N. Peterson, G. Ramsey, S.V. Rao, J.D. Roback, A. Shander, A.A. Tobian // JAMA. 2016. Vol. 316, No 19. P. 2025-2035. DOI: 10.1001/jama.2016.9185.
- Platelets: Emerging Facilitators of Cellular Crosstalk in Rheumatoid Arthritis / O.O. Olumuyiwa-Akeredolu, M.J. Page, P. Soma, E. Pretorius // Nat. Rev. Rheumatol. 2019. Vol. 15, No 4. P. 237-248. DOI: 10.1038/s41584-019-0187-9.
- Mean platelet volume (MPV) as an inflammatory marker in ankylosing spondylitis and rheumatoid arthritis / B. Kisacik, A. Tufan, U. Kalyoncu, O. Karadag, A. Akdogan, M.A. Ozturk, S. Kiraz, I. Ertenli, M. Calguneri // Joint Bone Spine. 2008. Vol. 75, No 3. P. 291-294. DOI: 10.1016/j. jbspin.2007.06.016.
- The platelet indices in patients with rheumatoid arthritis: mean platelet volume reflects disease activity / S. Yazici, M. Yazici, B. Erer, B. Erer, Y. Calik, H. Ozhan, S. Ataoglu // Platelets. 2010. Vol. 21, No 2. P. 122-125. DOI: 10.3109/09537100903474373.
- Kim D.A., Kim T.Y. Controversies Over the Interpretation of Changes of Mean Platelet Volume in Rheumatoid Arthritis // Platelets. 2011. Vol. 22, No 1. P. 79-80. DOI: 10.3109/09537101003663758.
- Ifik M., §ahin H., Huseyin E. New Platelet Indices as Inflammatory Parameters for Patients With Rheumatoid Arthritis // Eur. J. Rheumatol. 2014. Vol. 1, No 4. P. 144-146. DOI: 10.5152/eurjrheumatol.2014.140023.
- Mean Platelet Volume (MPV): New Perspectives for an Old Marker in the Course and Prognosis of Inflammatory Conditions /A. Korniluk, O.M. Koper-Lenkiewicz, J. Kaminska, H. Kemona, V. Dymicka-Piekarska // Mediators Inflamm. 2019. Vol. 2019. P. 9213074. DOI: 10.1155/2019/9213074.
- Harifi G., Sibilia J. Pathogenic role of platelets in rheumatoid arthritis and systemic autoimmune diseases. Perspectives and therapeutic aspects // Saudi Med J. 2016. Vol. 37, No 4. P. 354-360. DOI: 10.15537/smj.2016.4.14768.
- Role of extracellular vesicles in rheumatoid arthritis / H. Fu, D. Hu, L. Zhang, P. Tang // Mol. Immunol. 2018. Vol. 93. P. 125-132. DOI:10.1016/j. molimm.2017.11.016.
- Neutrophils: Novel key players in Rheumatoid Arthritis. Current and future therapeutic targets / I. Cecchi, I. Arias de la Rosa, E. Menegatti, D. Roccatello, E. Collantes-Estevez, C. Lopez-Pedrera, N. Barbarroja // Autoimmun. Rev. 2018. Vol. 17, No 11. Р. 1138-1149. DOI: 10.1016/j. autrev.2018.06.006.
- Neutrophil Function in an Inflammatory Milieu of Rheumatoid Arthritis. / W. Chen, Q. Wang, Y. Ke, J. Lin // J. Immunol. Res. 2018. Vol. 2018. P. 549329. DOI: 10.1155/2018/8549329.
- Сигидин Я.А., Лукина Г.В., Позднякова Е.С. Синдром Фелти и Т-клеточный лейкоз из больших гранулярных лейкоцитовзакономерное сочетание // Научно-практическая ревматология. 2007. Т. 45, № 3. С. 105-108. URL: https://doi.org/10.14412/1995-4484-2007-696.
- Gazitt T., Loughran T.P. Jr. Chronic neutropenia in LGL leukemia and rheumatoid arthritis // Hematology Am. Soc. Hematol. Educ. Program. 2017. Vol. 2017, No 1. P. 181-186. DOI: 10.1182/asheducation-2017.1.181.
- Immune-mediated pore-forming pathways induce cellular hypercitrullination and generate citrullinated autoantigens in rheumatoid arthritis / V. Romero, J. Fert-Bober, P.A. Nigrovic, E. Darrah, U.J. Haque, D.M. Lee, J. van Eyk, A. Rosen, F. Andrade // Sci. Transl. Med. 2013. Vol. 5, No 209. P. 209ra150. DOI: 10.1126/scitranslmed.3006869.
- Neutrophil extracellular traps enriched in oxidized mitochondrial DNA are interferogenic and contribute to lupus-like disease / C. Lood, L.P. Blanco, M.M. Purmalek, С. Carmona-Rivera, S.S. de Ravin, C.K. Smith, H.L. Malech, J.A. Ledbetter, K.B. Elkon, M.J. Kaplan // Nat. Med. 2016. Vol. 22, No 2. P. 146-153. DOI: 10.1038/nm.4027.
- Эозинофил: современный взгляд на кинетику, структуру и функцию / Ю.В. Колобовникова, О.И. Уразова, В.В. Новицкий, Л.С. Литвинова, С.П. Чумакова // Гематология и трансфузиология. 2012. Т. 57, № 1. С. 30-36.
- Eosinophils attenuate arthritis by inducing M2 macrophage polarization via inhibiting the IkB/P38 MAPK signaling pathway / L. Liu, Y. Zhang, X. Zheng, L. Jin, N. Xiang, M. Zhang, Z. Chen // Biochem. Biophys. Res. Commun. 2019. Vol. 508, No 3. P. 894-901. DOI: 10.1016/j. bbrc.2018.12.010.
- Increased surgeon experience with rheumatoid arthritis reduces the risk of complications following total joint arthroplasty / B. Ravi, R. Croxford, P.C. Austin, S. Hollands, J.M. Paterson, E. Bogoch, H. Kreder, G.A. Hawker // Arthritis Rheumatol. 2014. Vol. 66, No 3. P. 488-496. DOI: 10.1002/ art.38205.
- Rheumatoid Arthritis Versus Osteoarthritis in Patients Receiving Revision Total Knee Arthroplasty in the United States: Increased Perioperative Risks? A National Database-Based Propensity Score-Matching Study / X. Pan, J. Wang, Z. Shi, H. Cheng, Z. Lin, X. Wu, Z. Shi // J. Am. Acad. Orthop. Surg. 2021. DOI: 10.5435/JAAOS-D-20-00979.


