Генетическая инженерия как инструмент модификации состава запасных белков и повышения питательной ценности зерна у злаков
Автор: Эльконин Л.А., Доманина И.В., Итальянская Ю.В.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Обзоры
Статья в выпуске: 1 т.51, 2016 года.
Бесплатный доступ
За последние годы генная инженерия стала одним из методов генетического улучшения возделываемых растений, в том числе эффективным инструментом изменения состава запасных белков зерна у злаковых культур - основного источника продуктов питания для человека. В обзоре описаны разные подходы, используемые в этих исследованиях, а именно введение генетических конструкций, которые обеспечивают синтез белков, отсутствующих у сорта-реципиента; индуцируют РНК-сайленсинг генов, кодирующих белки с низкой питательной ценностью; регулируют пул аминокислот в эндосперме зерновки. Рассматриваются работы, в которых сообщается о введении дополнительных генов высокомолекулярных глютенинов ( 1Dx5, 1Ax1, 1Bx17, 1By18, 1Dy10 и др.) в геномы различных линий и сортов мягкой пшеницы. В этих работах были созданы трансгенные линии с улучшенными хлебопекарными свойствами зерна (повышенная сила муки и эластичность теста). Помимо прикладного значения, такие исследования позволяют понять роль отдельных генов высоко- и низкомолекулярных глютенинов в формировании признаков качества муки. Приводятся примеры получения безмаркерных трансгенных линий пшеницы, экспрессирующих гены 1Dy10 и 1Bx14, а также переноса генов высокомолекулярных глютенинов в геномы других злаковых культур - ржи, кукурузы, сорго. Обсуждаются возможности использования РНК-интерференции для получения информации о механизмах образования белковых телец, стекловидного эндосперма, а также роли различных классов проламинов и глютенинов в технологических свойствах муки и теста. Приводятся примеры создания трансгенной кукурузы с улучшенной питательной ценностью посредством РНК-сайленсинга генов зеинов, подавление синтеза которых ведет к накоплению других белков с более высоким содержанием лизина и триптофана, трансгенного сорго с улучшенной переваримостью белков за счет сайленсинга гена g-кафи-рина (белка, образующего поверхностный слой белковых телец, устойчивого к действию пепсина), трансгенной пшеницы с подавленным синтезом глиадинов, мука которой обладает низкой токсичностью для людей, подверженных целиакии и вынужденных соблюдать безглютениновую диету. Приводится пример природного РНК-сайленсинга: у мутанта риса со сниженным уровнем глютелина в локусе Lgc1 обнаружена делеция между двумя кодирующими последовательностями, одна из которых имеет инвертированную ориентацию. Описываются генно-инженерные подходы для повышения содержания лизина: введение нечувствительных к ретроингибированию генов дигидропиколин-синтазы (DHPS) и аспартаткиназы, усиливающих синтез лизина; подавление экспрессии гена zlkr / sdh, регулирующего его катаболизм; введение генов, контролирующих синтез белков с высоким содержанием лизина (гистонов и др.). Обсуждаются перспективы использования генно-инженер-ных методов создания сортов с улучшенной питательной ценностью зерна, которые связаны с применением безмаркерных технологий, повышением точности встраивания генетических конструкций, применением методов редактирования генома с помощью искусственно сконструированных нуклеаз.
Трансгенные растения, рнк-сайленсинг, проламины, белковые тельца, эндосперм, злаковые культуры
Короткий адрес: https://sciup.org/142133655
IDR: 142133655 | УДК: 633.1:[573.6.086.83:577.21]:58 | DOI: 10.15389/agrobiology.2016.1.17rus
Genetic engineering as a tool for modification of seed storage proteins and improvement of nutritional value of cereal grain
In recent years, genetic engineering has become an effective tool for the genetic improvement of cultivated plants including changes in the composition grain storage proteins of cereal crops that are the main source of nutrition for humans. The review describes the approaches used in these studies: the introduction of genetic constructs (i) providing the synthesis of proteins that are absent in recipient cultivars; (ii) inducing RNA-silencing of genes encoding proteins with low nutritional value, (iii) regulating the pool of amino acids in the endosperm. The studies are referred, which reported on the introduction of additional genes of high molecular weight glutenins ( 1Dx5, 1Ax1, 1Bx17, 1By18, 1Dy10 and others) into the genomes of different lines and cultivars of wheat. In these studies, the transgenic lines with increased dough strength and elasticity were obtained. In addition to the practical importance, these studies allow understanding the role of individual genes of high and low molecular weight glutenins in the formation of wheat flour quality traits. The examples of marker-free transgenic wheat lines expressing 1Dy10 and 1Bx14 genes, as well as transfer of high molecular weight glutenin genes into the genomes of other cereals (rye, corn, sorghum) are given. The possibilities of using the RNAi technology to obtain new information about the mechanisms of development of protein bodies, vitreous endosperm formation, and the role of different classes of prolamins and glutenins in the technological properties of flour and dough are discussed. The examples of the creation of transgenic maize with improved nutritional value via RNA-silencing of prolamin genes, transgenic sorghum with improved protein digestibility (obtained by silencing gene of the g-kafirin, the protein that forms outer layer of the protein bodies, resistant to pepsin digestion), transgenic wheat with suppression of gliadin synthesis, which flour has a low toxicity to humans with celiac disease, forced to comply gluten-free diet, are given. An example of natural RNA-silencing is given Partivularly, in the rice mutant with reduced level of glutelin, a deletion between the two coding sequences, one of which has an inverted orientation has been detected in the Lgc1 locus. The genetic engineering approaches to increase the lysine content are described, e.g. introduction of genes that enhance its synthesis, such as dihydrodipicolinate synthase (DHPS) insensitive to feedback inhibition and aspartate kinase; suppression of zlkr / sdh gene regulating its catabolism; introduction of genes that control the synthesis of proteins with high lysine content (histones and other lysine-rich proteins). The prospects of using genetic engineering methods to create varieties with improved nutritional value are associated with the use of marker-free technologies, increasing accuracy of insertion of genetic constructs, using the methods of genome editing by artificially engineered nucleases.
Текст обзорной статьи Генетическая инженерия как инструмент модификации состава запасных белков и повышения питательной ценности зерна у злаков
Работы, выполненные за последние 20 лет, убедительно доказали, что генная инженерия — это высокоэффективный инструмент генетического улучшения возделываемых растений. Реальность такова, что генная инженерия стала одним из методов селекции, позволившим создать у разных сельскохозяйственных культур значительное число сортов и агроно- мически ценных линий, устойчивых к биотическим и абиотическим стрессовым факторам, с улучшенным качеством получаемой продукции, повышенной интенсивностью фотосинтеза и использования минеральных удобрений .
Среди разнообразных методов генной инженерии агробактериаль-ная трансформация представляется наиболее эффективным и наименее затратным подходом при получении трансгенных растений. В течение длительного времени этот прием слабо использовался у злаковых культур, у которых единственным реальным способом трансгенеза служила дорогостоящая баллистическая трансформация. Однако совершенствование методов регенерации злаковых растений в культуре тканей, разработка разнообразных протоколов агробактериальной трансформации (1, 2) существенно облегчили получение трансгенных растений у злаков, значительно расширив возможности использования генной инженерии в селекции столь важной группы возделываемых культур.
К числу наиболее перспективных направлений генной инженерии относится создание трансгенных растений, улучшенных по питательной ценности, у которых изменен состав запасных белков. Эти исследования особенно актуальны для злаков — основного источника пищевого и кормового белка. Известно, что до 50 % белка (в развивающихся странах — до 70 %) и до 65 % калорий человечество получает от использования зерна злаков, у которых запасные белки составляют до 80 % от общего содержания белка зрелого семени (3-5).
В статье представлен обзор работ по получению трансгенных растений злаков с измененным составом запасных белков. Рассмотрены возможности использования таких растений для изучения развития белковых телец и формирования эндосперма, а также создания линий с более высокой питательной ценностью.
Фракции запасных белков зерна злаков. Запасные белки, согласно широко используемой классификации Т.Б. Осборна, основанной на их растворимости, подразделяются на фракции альбуминов (водорастворимые), глобулинов (солерастворимые), проламинов (спирторастворимые) и глютенинов (щелочерастворимые) (6).
У мягкой пшеницы ( Triticum aestivum L.) — основного хлебного злака — запасные белки представлены глютенинами (50 % от общего пула белков эндосперма) и глиадинами (30 %). Глютенины — это полимерный комплекс, определяющий эластичность муки, в состав которого входят субъединицы с высокой и низкой молекулярной массой (соответственно HMW и LMW). Мягкая пшеница содержит тесно сцепленные пары генов, которые кодирую X- и Y-типы субъединиц, образующих HMW-белки, и локализованы в длинном плече хромосом 1А, 1В и 1D. Глиадины включают α -, γ - и ω -фракции с разной электрофоретической подвижностью (7). Глиадины контролируются тесно сцепленными кластерами генов, именуемых блоками, которые локализованы в 1-й и 6-й хромосомах (4, 8).
Проламины служат основными запасными белками у кукурузы Zea mays L. и сорго Sorghum bicolor (L.) Moench. Проламины кукурузы (зеины) представлены фракциями α - (19 кДа и 22 кДа), β - (15 кДа), γ - (50 кДа, 27 кДа, 16 кДа) и δ - (18 кДа и 10 кДа) зеинов, при этом на α -зеины в эндосперме зерновок кукурузы приходится до 70 % от общего пула белков (5, 6). Зеины содержат незначительное количество ценных аминокислот — лизина, треонина, триптофана, поэтому имеют низкую питательную ценность. В 1960-е годы у кукурузы были получены мутанты opaque-2 ( o2 ) и floury-2 ( fl2 ) со сниженным содержанием α -зеина, в эндосперме которых 18
накапливалось значительное количество незеиновых белков, богатых лизином, а также возрастало содержание свободного лизина и триптофана (6). В зерновках этих мутантов, однако, отсутствовал стекловидный слой эндосперма, что увеличивало хрупкость зерновок, их подверженность инфицированию грибной микрофлорой и, в конечном итоге, затрудняло коммерческое использование таких мутантов. Позднее были получены рекомбинанты со стекловидным эндоспермом и высоким содержанием лизина (QPM — Quality Protein Maize), в зерновках которых происходил компенсаторный синтез незеиновых белков, богатых лизином, а также повышалось содержание γ -зеина (6, 9).
По аналогии с кукурузой, фракции проламинов сорго (кафири-нов) были обозначены как α - (25 и 23 кДа), β - (18.7 кДа) и γ -кафирины (28 кДа) (10-12). Данные о молекулярной массе γ -кафирина в разных работах варьировали — 28 кДа (10) и 20 кДа (13). В соответствии с последней опубликованной классификацией кафирины сорго представлены шестью белками: это α -кафирин 1 (25 кДа), α -кафирин 2 (22 кДа), β -ка-фирин (19 кДа), γ -кафирин 1 (27 кДа), γ -кафирин 2 (50 кДа), δ -кафирин (18 кДа), причем фракция α -кафиринов составляет до 80 % от суммарного количества кафириновых белков (14).
Проламины, синтезируемые в клетках эндосперма, депонируются в высокоспециализированных клеточных органеллах — белковых тельцах с упорядоченной структурой (5). Белковые тельца формируются в виде везикул эндоплазматической сети. Вначале в таких везикулах происходит накопление γ - и β -проламинов. На более поздних этапах развития в них начинают накапливаться α - и δ -проламины, при этом γ - и β -проламины отодвигаются к внешним слоям. Считается, что такая организация белковых телец служит одной из главных причин, обусловливающих более низкую питательную ценность зерна сорго, поскольку γ -кафирин, занимающий периферийное положение, обладает высокой устойчивостью к протеолитическому расщеплению, тем самым препятствуя перевариванию основных запасных белков — α -кафиринов (15, 16).
У риса ( Oryza sativa L.) запасные белки представлены проламинами и глютелинами. Проламины разделяют на три субкласса: 10 кДа, 13 кДа (13a-1, 13a-2, 13b-1 и 13b-2) и 16 кДа. Проламины 13a-1 и 13a-2 относятся к белкам, богатым цистеином, тогда как в 13b-1 и 13b-2 содержание цистенина низкое. Гены, кодирующие 13b-2 проламин, представлены 18 копиями, гены остальных проламинов имеют более низкую копийность (2-4 копии на геном) (17).
В эндосперме зерновок риса проламины и глютелины откладываются в белковых тельцах. Белковые тельца, содержащие проламин, имеют сферическую форму, размер 1-2 мкм и внутреннюю структуру, в которой различаются концентрические круги разной электронной плотности; белковые тельца, содержащие глютелин, имеют неправильную форму, размер 3-4 мкм и они равномерно окрашены (18, 19). Было установлено, что проламин с молекулярной массой 10 кДа расположен в центре белкового тельца, проламины 13a и 16 кДа присутствуют в среднем слое, а 13b образует поверхностный слой и прослойку между внутренним и средним слоем белкового тельца (17).
Трансгенные растения с дополнительными генами запасных белков. Разработка методов генетической трансформации открыла возможность применения генно-инженерных технологий для изменения состава запасных белков у злаков. Для решения этой задачи используются различные подходы: введение генов, контролирующих синтез запасных белков, которые отсутствуют у сорта-реципиента; введение генетиче-19
ских конструкций, индуцирующих РНК-сайленсинг генов, кодирующих белки с низкой питательной ценностью или снижающих разрушение других белков протеазами; введение генов, регулирующих синтез аминокислот.
К настоящему времени в литературе имеется значительное число сообщений о введение генов различных высокомолекулярных глютенинов ( 1Dx5 , 1Ax1 , 1Bx17 , 1By18 , 1Dy10 и др.) в геномы различных линий и сортов мягкой пшеницы. В результате проведенных исследований получены трансгенные линии с улучшенным качеством муки, повышенной подъемной силой и эластичностью теста (20-24). Помимо прикладного значения, эти работы позволяют понять роль отдельных генов высоко- и низкомолекулярных глютенинов в формировании признаков качества муки. Так, у трансгенных линий мягкой пшеницы с усиленной экспрессией генов низкомолекулярных глютенинов наблюдалось снижение показателя SDS-седиментации, а также силы муки (24). Одновременная экспрессия трех генов HMW-GS — 1Ax1 , 1Dx5 и 1Dy10 — увеличивала подъемную силу муки, при этом ген 1Dy10 оказывал значительно более сильный эффект, чем 1Ax1 и 1Dx5 (25).
Сообщалось также о трансгенных растениях твердой пшеницы с генами 1Ax1 или 1Dx5 , кодирующими высокомолекулярные глютенины (26). Из 10 трансгенных линий, полученных посредством баллистической трансформации незрелых зародышей у трех сортов и одной селекционно-ценной линии Triticum turgidum L. var. durum , у пяти наблюдалась экспрессия введенных трансгенов. Как показал анализ миксограмм муки из зерна трех трансгенных линий, у них повышались показатели подъемной силы и стабильности теста, что свидетельствует о возможности использовать генетическую трансформацию для улучшения качества зерна у твердой пшеницы.
В аналогичной работе, выполненной на других сортах твердой пшеницы, также были получены трансгенные линии с генами мягкой пшеницы 1Dx5 и 1Dy10 , кодирующими высокомолекулярные глютенины (27). Примечательно, однако, что у одной из линий трансгены и маркерный ген ( bar ) оказались расположены на разных хромосомах, и в результате расщепления была выделена безмаркерная трансгенная линия, экспрессирующая ген 1Dy10 . Технологический анализ показал, что мука у полученных трансгенных линий обладает улучшенными смесительными свойствами.
Получены также трансгенные растения твердой пшеницы с генами, кодирующими низкомолекулярные глютенины LMW-GS (28), и в результате создана трансгенная линия с повышенной силой муки (29).
Учитывая возможные негативные эффекты маркерного гена bar на здоровье человека, была предпринята работа по получению безмаркерных трансгенных растений мягкой пшеницы с дополнительными генами запасных белков (30). В этом исследовании отбор трансгенных растений с геном 1Bx14 , кодирующим субъединицу высокомолекулярного глютенина, осуществляли с помощью ПЦР. Среди 1219 растений выявили семь трансформантов (частота трансформации 0,28 %), и у трех из них в поколении Т1 наблюдалась экспрессия трансгена.
Следует отметить эксперименты, в которых гены высокомолекулярных глютенинов были перенесены в геномы других злаковых культур. Так, сообщалось о трансгенной линии ржи ( Secale cereale L.) с генами глютенинов мягкой пшеницы Glu-1DX5 и Glu-1Dy10 , у которой количество клейковины возросло в 2-3 раза (31). Созданы также трансгенные растения кукурузы и сорго, в геномы которых введены соответственно гены Glu-1DX5 и 1Dy10 , которые при этом специфически экспрессировались в эндосперме (32, 33).
Использование РНК-интерференции для изменения состава запасных белков. Как известно, технология РНК-интерференции основана на разрушении мРНК целевых генов с помощью генетических конструкций, содержащих инвертированные повторяющиеся последовательности фрагментов этих генов. мРНК, транскрибированная с таких конструкций, образует шпилечную структуру. Возникшая двуспиральная молекула РНК подвергается разрушению, и образуются одноцепочечные фрагменты длиной 21-25 п.н. (короткие интерферирующие РНК), которые за счет комплементарности взаимодействуют с мРНК целевого гена. В результате появляются новые двуспиральные молекулы РНК, которые также подвергаются распаду (34-36).
В последние годы технология РНК-интерференции интенсивно применяется для повышения питательной ценности ряда злаковых культур, в частности кукурузы и сорго, а также для получения новой информации о механизмах образования белковых телец, формирования структуры эндосперма и роли различных классов проламинов и глютенинов в определение технологических свойств муки и теста.
Посредством баллистической трансформации с использованием генетической конструкции, которая содержала последовательности фрагмента гена γ -глиадина в прямой и инвертированной ориентации, разделенные UbiI интроном, у двух линий пшеницы сорта Bobwhite было получено семь трансгенных растений с сайленсингом гена γ -глиадина (37). В дальнейшем конструкцию для РНК-сайленсинга с помощью скрещиваний перенесли в геномы трех других сортов мягкой пшеницы, что привело к увеличению количества высоко- и низкомолекулярных глютенинов и показателя SDS-седиментации вследствие сайленсинга (38). Примечательно, что на генофоне сорта Bobwhite 208 такого эффекта от сайленсинга по гену γ -глиадина не обнаружили.
В других экспериментах с использованием генетических конструкций для РНК-сайленсинга генов α - и ω -глиадинов отмечали репрессию синтеза всех классов глиадинов (до 86,8 % по сравнению с наблюдаемой у исходных нетрансгенных растений) (8). У таких линий были выявлены нарушения в развитии белковых телец (они имели неправильную форму), тогда как подавление синтеза только γ -глиадина не приводило к изменению формы этих образований. У линий, несущих генетическую конструкцию, направленную на сайленсинг генов α - и ω -глиадинов, повышалось содержание глобулинов. Сообщалось также о получении трансгенной пшеницы с сайленсингом гена α -глиадина, которая характеризовалась повышенным показателем силы муки и увеличением объема выпечки (39).
Были получены линии трансгенной пшеницы, несущие генетическую конструкцию для сайленсинга гена ω -5-глиадина (40). У двух линий содержание ω -5-глиадина уменьшалось на 80 %, причем синтез других белков клейковины не нарушался. В то же время у двух других линий наблюдалось полное подавление синтеза ω -5-глиадина, а также снижение экспрессии ω -1,2-глиадинов. При этом у одной из линий также уменьшался синтеза трех белков, относящихся к высокомолекулярным глютенинам, одного низкомолекулярного глютенина (s-type LMW-GS) и одновременно возрастало содержание двух других низкомолекулярных глютенинов (m-type LMW-GS) и нескольких α -глиадинов. Это исследование наглядно демонстрирует, что одна и та же конструкция для РНК-сайленсинга может вызывать различные эффекты в зависимости от генофона.
Следует отметить, что у линий трансгенной пшеницы с подавленным синтезом глиадинов мука менее токсична для людей, подверженных 21
целиакии и вынужденных соблюдать безглютениновую диету. Было показано, что белки клейковины у трансгенных линий пшеницы с сайленсингом генов α -, γ - и ω -глиадинов снижают образование связанных с проявлением целиакии специфических эпитопов (DQ2 и DQ8) (41), которые распознаются Т-лейкоцитами. Следовательно, трансгенная пшеница с подавленным синтезом глиадинов может быть использована для питания людей при целиакии, которые не могут потреблять продукты из обычной муки пшеницы, ржи, ячменя.
У кукурузы с использованием генетических конструкций, содержащих инвертированные повторы генов α -зеинов (19 и 22 кДа), получены трансгенные линии с подавленным синтезом этих белков (42, 43). Оказалось, что репрессия синтеза зеинов, имеющих сравнительно низкую питательную ценность, ведет к накоплению других белков с более высокой питательную ценностью. Растения кукурузы с сайленсингом генов α -зеинов характеризовались удвоенным содержанием незаменимых аминокислот триптофана и лизина в зерновках.
В этих экспериментах было обнаружено, что сайленсинг гена α -зе-ина с молекулярной массой 22 кДа приводил к образованию мучнистого эндосперма. Такое изменение типа эндосперма связывали с отклонениями в формировании структуры белковых телец, а именно с нарушением встраивания α -зеина с массой 19 кДа в центр белкового тельца или модификацией его взаимодействия с β - и γ -зеином (42).
В дальнейшем с помощью РНК-интерференции генов разных фракций зеинов у линии кукурузы QPM со стекловидным эндоспермом получены разнообразные мутанты с различными вариациями структуры белковых телец и типами эндосперма (44, 45). Было показано, что важную роль в формировании мучнистого эндосперма играет сайленсинг гена γ -зеина, в результате которого происходит модификация структуры белковых телец и изменение их связи с крахмальными гранулами (45).
В детальном исследовании разных субклассов зеинов с применением РНК-интерференции выявлена их роль в формировании стекловидного эндосперма и развитии белковых телец у кукурузы (46). Так, установлено, что γ -зеин с молекулярной массой 27 кДа участвует в инициации образования белковых телец. Другие белки, относящиеся к семейству γ -зеинов, функционируют на этапе роста белковых телец. Совместная супрессия двух α -зеинов (19 и 22 кДа) значительно ингибирует разрастание белковых телец, но не вызывает их морфологических аномалий, возникающих при редукции только α -зеина с молекулярной массой 22 кДа. Одновременное подавление всех классов зеинов приводит к снижению числа белковых телец, которые при этом сохраняют нормальный размер и морфологию.
Большой объем экспериментов был выполнен несколькими исследовательскими группами по индукции РНК-сайленинга генов кафиринов у сорго. Основная цель этих экспериментов заключалась в подавлении синтеза труднопереваримого γ -кафирина и создании линий сорго, улучшенных по питательной ценности. РНК-сайленсинг индуцировали генетическими конструкциями, несущими инвертированные повторы нескольких генов кафиринов ( δ 2, γ 1, γ 2 или α 1, δ 2, γ 1, γ 2), разделенных последовательностью интрона ADH1 (гена альдегиддегидрогеназы 1). Эти конструкции управлялись промотором гена α -зеина (19 кДа) кукурузы (14, 47, 48). В другой работе (33) для индукции сайленсинга гена γ -кафирина использовали генетическую конструкцию, включавшую полную последовательность гена γ -кафирина под контролем промотора γ -кафирина, а в качестве терминатора — последовательность гена рибозима (self-cleaving ri-22
bozyme) вируса кольцевой мозаики табака. Сайленсинг α -кафирина индуцировали с помощью конструкции, состоящей из инвертированных повторов α -кафирина, разделенных последовательностью интрона гена арабидоп-сиса, кодирующего белок D1 сплайсосомы; конструкция управлялась α -кафириновым промотором (33). В экспериментах каждой из групп были получены линии трансгенного сорго с мучнистым типом эндосперма и улучшенной переваримостью кафиринов пепсином. К сожалению, мучнистый эндосперм является недостатком этих линий, поскольку отсутствие стекловидного слоя повышает хрупкость зерновок и снижает их устойчивость к поражению грибной микрофлорой.
Нами посредством агробактериальной трансформации с использованием штамма GV3101, несущего генетическую конструкцию pNRKAF-SIL для индукции РНК-сайленсинга гена γ -кафирина, получены линии трансгенного сорго с улучшенной переваримостью запасных белков зерна in vitro и измененным составом аминокислот (повышение относительного содержания лизина) (49). Конструкция pNRKAFSIL, созданная в Центре «Биоинженерия» РАН (г. Москва; авторы Н.В. Равин и А.Л. Ракитин), представляла собой шпилечную вставку, состоявшую из фрагментов гена γ -кафирина в прямой и обратной ориентации, между которыми располагался интрон гена убиквитина кукурузы; конструкция управлялась конститутивным 35S-промотором вируса мозаики цветной капусты (CaMV).
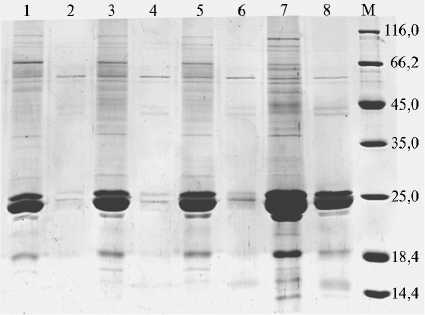
Рис. 1. Электрофоретические спектры белков зерновок у трех трансгенных растений сорго Sorghum bicolor (L.) Moench из поколения Т 3 , несущих генетическую конструкцию для сайленсинга гена γ -кафирина (дорожки 1-6), и контрольного растения исходной нетрансгенной линии сорта Желтозерное 10 (дорожки 7, 8) без обработки (дорожки 1, 3, 5, 7) и после обработки (дорожки 2, 4, 6, 8) пепсином. М (кДа) — маркер молекулярных масс SM0431 («Thermo Scien-tific», Литва).
Анализ переваримости запасных белков в системе in vit- ro показал, что мука из зерновок трансгенных растений характеризуется более высокими показателями по сравнению с мукой исходной линии сорго (сорт Желтозерное 10) (рис. 1). У некоторых трансгенных растений количество белков, которые не расщеплялись пепсином, было в 4,7 раза меньше, а количество нерасщепившихся мономеров кафиринов — в 17,5 меньше, чем у исходной линии. При этом переваримость (общее количество расщепившихся белков) достигала 90-92 % от контроля, не обработанного пепсином, тогда как у исходной нетрансгенной линии — 60-61 % (49). Более высокая переваримость наблюдалась у растений из разных поколений (Т1-Т3), то есть наследовалась в потомстве.
Примечательно, что в наших экспериментах наряду с растениями с мучнистым типом эндосперма были получены формы со стекловидным или модифицированным типом эндосперма, сочетавшие высокую переваримость кафиринов с наличием в эндосперме стекловидного слоя (рис. 2). Выделенные нами трансгенные растения представляют значительный интерес для селекции, поскольку стекловидный слой необходим для защиты зерновки от патогенов и механических повреждений.
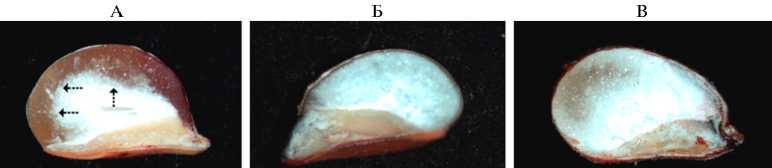
Рис. 2. Текстура эндосперма у трансгенных растений сорго Sorghum bicolor (L.) Moench, несущих генетическую конструкцию для сайленсинга гена γ -кафирина: А — зерновка исходной нетрансгенной линии сорта Желтозерное 10 с толстым слоем стекловидного эндосперма (границы отмечены стрелками); Б — зерновка трансгенного растения с мучнистым эндоспермом; В — зерновка трансгенного растения с модифицированным типом эндосперма, в котором мучнистый эндосперм содержит фрагменты стекловидного эндосперма (StereoDiscovery V12, «Carl Zeiss», Германия). Увеличение ½20,5.
Следует отметить, что структура белковых телец, определяющая переваримость и питательную ценность зерна сорго, изменялась у трансгенных линий с сайленсингом гена α -кафирина. В эндосперме растений обычных линий сорго белковые тельца имеют правильную округлую форму, в то время как у трансгенных линий или мутантов с высокой переваримостью белков форма этих образований неправильная, на их поверхности наблюдаются выпячивания и борозды (14, 50). В то же время при сайленсинге γ -кафирина форма белковых телец не изменялась (33, 47).
Технология РНК-интерфренции использовалась для изучения механизма формирования и структуры белковых телец у риса. С помощью генетической конструкции для сайленсинга гена одного из проламинов, CysR10 (проламин 10 кДа, богатый цистеином), было показано, что этот белок входит в состав содержащих проламин белковых телец: у линии с РНК-сайленсингом белковые тельца утрачивали характерную сферическую конфигурацию (51).
Изменения в форме и размере содержащих проламин белковых телец наблюдали и у трансгенных растений риса с сайленсингом гена проламина 13 кДа (52). У таких трансгенных растений белковые тельца имели меньший размер и были лишены характерной ламеллярной структуры. Кроме того, у таких растений наблюдалось увеличение содержания других белков (проламина 10 кДа, глютелинов, шаперона) и свободного лизина, что повышало питательную ценность зерна. Было также показано, что сайленсинг гена проламина 13 кДа повышает содержание общего лизина до 56 % в результате компенсаторного увеличения синтеза богатых лизином глютелинов, глобулинов и шаперонов (53).
Примечательно, что у риса выявлена природная мутация Lgc1 ( low glutelin content ), снижающая содержание глютелина в зерновках, вероятно, на основе РНК-интерференции. В локусе Lgc1 обнаружена делеция между двумя последовательностями гена глютелина, одна из которых имеет инвертированную ориентацию. Такая структурная организация локуса в процессе его транскрипции может приводить к образованию двуцепочечной молекулы РНК — индуктора РНК-сайленсинга (54). Таким образом, мутация Lgc1 представляет собой наглядный пример РНК-сайленсинга, существующего в природе, и одно из доказательств в пользу того, что генетическая инженерия использует естественные процессы, существующие в природе и происходящие без участия человека.
Изменение содержания важнейших аминокислот. Генно-инженерные подходы весьма перспективны для решения проблемы обогащения зерна злаков незаменимыми аминокислотами — лизином, триптофаном, метионином. Благодаря использованию специфичных для эндосперма промоторов экспрессия нужных генов обеспечивается именно в зерновках, а не в соматических тканях, где повышенное содержание перечисленных аминокислот может приводить к аномалиям развития (55). Однако в настоящее время успешные результаты по изменению аминокислотного состава зерна злаков методами генной инженерии достигнуты только для лизина. Для повышения содержания этой аминокислоты применялись различные генно-инженерные подходы: введение генов, усиливающих его синтез; подавление генов, регулирующих катаболизм лизина; подавление синтеза белков с низким содержанием лизина, вследствие чего в эндосперме инициируется синтез белков, богатых лизином; введение генов, контролирующих синтез белков, богатых лизином.
Биосинтез лизина запускается ферментом дигидродипиколинат-синтазой (dihydrodipicolinate synthase — DHDPS, КФ 4.2.1.52). Его особенность заключается в чувствительности к ингибированию конечным продуктом, что позволяет поддерживать концентрацию лизина в клетках растений на постоянном уровне (55). Однако из бактерии Corynebacterium glutamicum выделен измененный фермент DHDPS, названный CordapA, нечувствительный к ингибированию конечным продуктом (56). Посредством агробактериальной трансформации была получена линия трансгенной кукурузы M27908 с геном CordapA, у которой содержание свободного лизина возросло более чем в 50 раз (57). При скрещивании линий кукурузы с РНК-сайленгом гена α -зеина (19 кДа) с линией М27908, несущей ген CordapA, были получены гибриды F1, у которых содержание общего лизина в зерновках возросло до 6,9-8,5 % от общего содержания аминокислот (в контроле — 3,3-3,4 %) (57). Таким образом, благодаря сочетанию двух подходов (подавление синтеза белков с низким содержанием лизина и введение гена, усиливающего синтез этой аминокислоты) удалось создать гибридную кукурузу с удвоенным содержанием лизина в зерновках.
Катаболизм лизина контролируется двумя ферментами — лизин: α -кетоглуторат-редуктазой (LKR, КФ 1.4.3.2, EC 1.5.1.8) и сахаропиндегид-рогеназой (SDH, EC 1.5.1.9), которые являются продуктами одного гена lkr / sdh (5). С использованием генетической конструкции, индуцирующей РНК-сайленсинг гена zlkr / sdh , у кукурузы были получены трансгенные растения, у которых содержание лизина возросло в 20 раз по сравнению с нетрансгенным контролем (58). В дальнейшем с использованием единой кассеты, в составе которой имелся ген CordapA, усиливающий биосинтез лизина, и генетическая конструкция, индуцирующая РНК-сайленсинг гена zlkr / sdh и, тем самым, снижающая катаболизм лизина, были получены трансгенные растения кукурузы c 40-кратным увеличением количества этой амиокислоты в зерновках (59).
Сообщалось о получении трансгенных растений риса с генами, усиливающими синтез лизина, которые кодируют нечувствительную к ингибированию лизином аспартаткиназу (КФ 2.7.2.4, EC 2.7.2.4) и дигидро-пиколинат-синтазу (EC 4.2.1.52), и конструкциями, индуцирующими РНК-интерференцию гена lkr / sdh , который управляет катаболизмом лизина (60). У этих растений зарегистрировали 60-кратное увеличение содержания свободного лизина в семенах и 12-кратное — в листьях. У растений не проявлялись какие-либо заметные отклонения в развитии и прорастании семян.
Как уже отмечалось, еще один способ обогащения зерновок кукурузы и сорго лизином и триптофаном — подавление синтеза зеинов, в которых содержание этих аминокислот невелико. В результате компенсаторного эффекта в зерновках усиливается синтез незеиновых белков, более богатых лизином и триптофаном (61). Аналогичный процесс наблюдался у трансгенных линий сорго с подавленным синтезом кафиринов, в зерновках которых усиливался синтез некафириновых белков (33, 47).
В последние годы для создания линий злаков с повышенным содержанием лизина стал использоваться подход, основанный на введении генов, контролирующих синтез богатых лизином белков. При этом для обеспечения экспрессии таких генов в эндосперме в состав генетической конструкции включают специфичный для эндосперма промотор и в некоторых случаях сигнальную последовательность, направляющую синтезированный белок в белковые тельца. Так были получены трансгенные растения риса, у которых в семенах наблюдалась усиленная экспрессия генов, кодирующих синтез гистонов RLRH1 и RLRH2 с высоким содержанием лизина. Транскрипция трансгенов обеспечивалась промотором гена глютелина 1 риса. У полученных трансгенных растений содержание лизина возросло на 35 % (62). В другом исследовании ген дикого картофеля ( So-lanum berthaultii ) sb401 , кодирующий богатый лизином белок цитоскелета пыльцы, был введен в геном кукурузы. В результате содержание лизина возросло в потомстве разных трансгенных растений на 16,1-54,8 % по сравнению с исходной нетрансгенной линией, а общее содержание белка — на 11,6-39,0 %, причем увеличение количества лизина и белка стабильно наследовалось в течение шести поколений (63). В другой работе были получены трансгенные растения кукурузы с геном хлопчатника ( Gossipium hirsu-tum L.) GhLRP , контролирующим синтез богатого лизином белка, что позволило увеличить содержание в нем лизина на 65 % по сравнению с нетрансгенным (64). Следует отметить, что потенциальная аллергенность этих белков была исключена до начала работ при помощи теста на гомологичность с известными аллергенными последовательностями.
Обсуждая практические перспективы применения генно-инженерных методов для создания сортов злаковых культур с улучшенной питательной ценностью зерна, следует отметить, что первый трансгенный сорт кукурузы LY038 с повышенным содержанием лизина был выведен на рынок в 2005 году (55). Препятствием для более широкого распространения трансгенных сортов остается негативное общественное мнение и озабоченность возможным вредным влиянием генно-модифицированных продуктов на здоровье человека и окружающую среду. Однако очевидно, что при совершенствовании методов получения трансгенных растений (например, с использованием безмаркерных технологий) (65, 66), повышении точности встраивания генетических конструкций (67), применении методов редактирования генома с помощью искусственно сконструированных нуклеаз (68) число трансгенных сортов злаковых культур, улучшенных по целевым признакам (в частности, по питательной ценности), будет возрастать, поскольку в этих экспериментах используются последовательности ДНК, кодирующие полезные и безопасные для человека продукты, а в основе генно-инженерных методов селекции лежат естественные природные процессы.
Итак, использование методов генетической инженерии открывает большие возможности для модификации состава запасных белков зерна у злаков. Эти исследования важны для решения теоретических проблем, связанных с пониманием закономерностей развития эндосперма, механизмов синтеза и накопления основных питательных веществ — белка и крахмала, реализации генетической информации в онтогенезе. Кроме того, они имеют непосредственный практический выход, поскольку позволяют создавать сорта и селекционно значимые линии, улучшенные по питательной ценности, для использования в пищу и в качестве фуражно-26
го зерна для кормопроизводства.
Список литературы Генетическая инженерия как инструмент модификации состава запасных белков и повышения питательной ценности зерна у злаков
- Hiei Y., Ishida Y., Komari T. Progress of cereal transformation technology mediated by Agrobacterium tumefaciens. Front. Plant Sci., 2014, 5: 628 ( ) DOI: 10.3389/fpls.2014.00628
- Sparks C.A., Doherty A., Jones H.D. Genetic transformation of wheat via Agrobacterium-mediated DNA delivery. Methods Mol. Biol., 2014, 1099: 235-250 ( ) DOI: 10.1007/978-1-62703-715-0_19
- Godwin I.D., Williams S.B., Pandit P.S., Laidlaw H.K.C. Multifunctional grains for the future: genetic engineering for enhanced and novel cereal quality. In Vitro Cell & Dev. Biol.-Plant, 2009, 45(3): 383-399 ( ) DOI: 10.1007/s11627-008-9175-5
- Shewry P.R., Halford N.G. Cereal seed storage proteins: structures, properties and role in grain utilization. J. Exp. Botany, 2002, 53(370): 947-958 ( ) DOI: 10.1093/jexbot/53.370.947
- Gibbon B.C., Larkins B.A. Molecular genetic approaches to developing quality protein maize. Trends in Genetics, 2005, 21(4): 227-233 ( ) DOI: 10.1016/j.tig.2005.02.009
- Holding D.R. Recent advances in the study of prolamin storage protein organization and function. Plant Sci., 2014, 5: 276 ( ) DOI: 10.3389/fpls.2014.00276
- Metakovsky E.V., Novoselskaya A.Y., Sozinov A.A. Genetic analysis of gliadin components in winter wheat using two-dimensional polyacrylamide gel electrophoresis. Theor. Appl. Genet., 1984, 69: 31-37.
- Gil-Humanes J., Piston F., Shewry P.R., Tosi P., Barro F. Suppression of gliadins results in altered protein body morphology in wheat. J. Exp. Bot., 2011, 62(12): 4203-4213 ( ) DOI: 10.1093/jxb/err119
- Prasanna B.M., Vasal S.K., Kassahun B., Singh N.N. Quality protein maize. Curr. Sci., 2001, 81: 1308-1319.
- Shull J.M., Watterson J.J., Kirleis A.W. Proposed nomenclature for the alcohol soluble proteins (kafirins) of Sorghum bicolor (L. Moench) based on molecular weight, solubility, and structure. J. Agric. Food Chem., 1991, 39(1): 83-87.
- Belton P.S., Delgadillo I., Halford N.G., Shewry P.R. Kafirin structure and functionality. J. Cereal Sci., 2006, 44: 272-286 ( ) DOI: 10.1016/j.jcs.2006.05.004
- De Mesa-Stonestreet N.J., Alavi S., Bean S.R. Sorghum proteins: the concentration, isolation, modification, and food applications of kafirins. J. Food Sci., 2010, 75: 90-104 ( ) DOI: 10.1111/j.1750-3841.2010.01623.x
- Wong J.H., Marx D.B., Wilson J.D., Buchanan B.B., Lemaux P.G., Pedersen J.F. Principal component analysis and biochemical characterization of protein and starch reveal primary targets for improving sorghum grain. Plant Sci., 2010, 179: 598-611 ( ) DOI: 10.1016/j.plantsci.2010.08.020
- Grootboom A.W., Mkhonza N.L., Mbambo Z., O’Kennedy M.M., da Silva L.S., Taylor J., Taylor J.R.N., Chikwamba R., Mehlo L. Co-suppression of synthesis of major α-kafirin sub-class together with γ-kafirin-1 and γ-kafirin-2 required for substantially improved protein digestibility in transgenic sorghum. Plant Cell Rep., 2014, 33: 521-537 ( ) DOI: 10.1007/s00299-013-1556-5
- Oria M.P., Hamaker B.R., Shull J.M. Resistance of sorghum α-, β-and γ-kafirins to pepsin digestion. J. Agric. Food Chem., 1995, 43: 2148-2153.
- Duodu K.G., Taylor J.R.N., Belton P.S., Hamaker B.R. Factors affecting sorghum protein digestibility. J. Cereal Sci., 2003, 38: 117-131 ( ) DOI: 10.1016/S0733-5210(03)00016-X
- Saito Y., Shigemitsu T., Yamasaki R., Sasou A., Goto F., Kishida K., Kuroda M., Tanaka K., Morita S., Satoh S., Masumura T. Formation mechanism of the internal structure of type I protein bodies in rice endosperm: relationship between the localization of prolamin species and the expression of individual genes. The Plant J., 2012, 70: 1043-1055 ( ) DOI: 10.1111/j.1365-313X.2012.04947.x
- Takemoto Y., Coughlan S.J., Okita T.W., Satoh H., Ogawa M., Kumamaru T. The rice mutant esp2 greatly accumulates the glutelin precursor and deletes the protein disulfide isomerase. Plant Physiol., 2002, 128: 1212-1222 ( ) DOI: 10.1104/pp.010624
- Takaiwa F., Hirose S., Takagi H., Yang L., Wakasa Y. Deposition of a recombinant peptide in ER-derived protein bodies by retention with cysteine-rich prolamins in transgenic rice seed. Planta, 2009, 229: 1147-1158 ( ) DOI: 10.1007/s00425-009-0905-7
- Barro F., Rooke L., Bekes F., Gras P., Tatham A.S., Fido R., Lazzeri P.A., Shewry P.R., Barcelo P. Transformation of wheat with high molecular weight subunit genes results in improved functional properties. Nat. Biotechnol., 1997, 15: 1295-1299 ( ) DOI: 10.1038/nbt1197-1295
- Rakszegi M., Bekes F., Lang L., Tamas L., Shewry P.R., Bedo Z. Technological quality of transgenic wheat expressing an increased amount of a HMW glutenin subunit. J. Cereal Sci., 2005, 42: 15-23 ( ) DOI: 10.1016/j.jcs.2005.02.006
- Rakszegi M., Pastori G., Jones H.D., Bekes F., Butow B. Technological quality of field grown transgenic lines of commercial wheat cultivars expressing the 1A61 HMW glutenin subunit gene. J. Cereal Sci., 2008, 47: 310-321 ( ) DOI: 10.1016/j.jcs.2007.04.010
- Blechl A., Lin J., Nguyen S., Chan R., Anderson O.D., Dupont F.M. Transgenic wheats with elevated levels of Dx5 and/or Dy10 high-molecular-weight glutenin subunits yield doughs with increased mixing strength and tolerance. J. Cereal Sci., 2007, 45: 172-183 ( ) DOI: 10.1016/j.jcs.2006.07.009
- Masci S., D’Ovidio R., Scossa F., Patacchini C., Lafiandra D. Production and characterization of a transgenic bread wheat line over-expressing a low molecular-weight glutenin subunit gene. Mol. Breed., 2003, 12(3): 209-222 ( ) DOI: 10.1023/A:1026346823301
- Leon E., Marin S., Gimenez M.J., Piston F., Rodriguez-Quijano M., Shewry P.R., Barro F. Mixing properties and dough functionality of transgenic lines of a commercial wheat cultivar expressing the 1A61, 1D65 and 1Dy10 HMW glutenin subunit genes. J. Cereal Sci., 2009, 49: 148-156 ( ) DOI: 10.1016/j.jcs.2008.08.002
- He G.Y., Rooke L., Steele S., Bekes F., Gras P., Tatham A.S., Fido R., Barcelo P., Shewry P.R., Lazzeri P. Transformation of pasta wheat (Triticum turgidum L. var. durum) with high-molecular-weight glutenin subunit genes and modification of dough functionality. Mol. Breed., 1999, 5(4): 377-386 ( ) DOI: 10.1023/A:1009681321708
- Gadaleta A., Blechl A.E., Nguyen S., Cardone M.F., Ventura M., Quick J.S., Blanco A. Stably expressed D-genome derived HMW glutenin subunit genes transformed into different durum wheat genotypes change dough mixing properties. Mol. Breed., 2008, 22: 267-279 ( ) DOI: 10.1007/s11032-008-9172-8
- Tosi P., D’Ovidio R., Napier J.A., Bekes F., Shewry P.R. Expression of epitope-tagged LMW glutenin subunits in the starchy endosperm of transgenic wheat and their incorporation into glutenin polymers. Theor. Appl. Genet., 2004, 108: 468-476 ( ) DOI: 10.1007/s00122-003-1459-x
- Tosi P., Masci S., Giovangrossi A., D’Ovidio R., Bekes F. Modification of the low molecular weight (LMW) glutenin composition of transgenic durum wheat: Effects on glutenin polymer size and gluten functionality. Mol. Breed., 2005, 16: 113-126 ( ) DOI: 10.1007/s11032-005-5912-1
- Liu X., Jin W., Liu J., Zhao H., Guo A. Transformation of wheat with the HMW-GS 1Bx14 gene without markers. Russ. J. Genet., 2011, 47(2): 182-188 ( ) DOI: 10.1134/S1022795411010066
- Altpeter F., Vasil V., Srivastava V., Vasil I.K. Integration and expression of the high-molecular-weight glutenin subunit 1A61 gene into wheat. Nat. Biotechnol., 1996, 14: 1155-1159 ( ) DOI: 10.1038/nbt0996-1155
- Sangtong V., Moran L., Chikwamba R., Wang K., Woodman-Clikeman W., Long J., Lee M., Scott P. Expression and inheritance of the wheat Glu-1DX5 gene in transgenic maize. Theor. Appl. Genet., 2002, 105(6-7): 937-945 ( ) DOI: 10.1007/s00122-002-1036-8
- Kumar T., Dweikat I., Sato S., Ge Z., Nersesian N., Elthon T., Bean S., Ioerger B.P., Tiley M., Clemente T. Modulation of kernel storage proteins in grain sorghum (Sorghum bicolor (L.) Moench). Plant Biotechnol. J., 2012, 10: 533-544 ( ) DOI: 10.1111/j.1467-7652.2012.00685.x
- Ali N., Datta S.K., Datta K. RNA interference in designing transgenic crops. GM Crops, 2010, 1(4): 207-213 ( ) DOI: 10.4161/gmcr.1.4.13344
- Katoch R., Thakur N. Advances in RNA interference technology and its impact on nutritional improvement, disease and insect control in plants. Appl. Biochem. Biotechnol., 2013, 169(5): 1579-1605 ( ) DOI: 10.1007/s12010-012-0046-5
- Younis A., Siddique M.I., Kim C.-K., Lim K.-B. RNA Interference (RNAi) induced gene silencing: a promising approach of hi-tech plant breeding. Int. J. Biol. Sci., 2014, 10(10): 1150-1158 ( ) DOI: 10.7150/ijbs.10452
- Gil-Humanes J., Piston F., Hernando A., Alvarez J.B., Shewry P.R., Barro F. Silencing of γ-gliadins by RNA interference (RNAi) in bread wheat. J. Cereal Sci., 2008, 48: 565-568 ( ) DOI: 10.1016/j.jcs.2008.03.005
- Gil-Humanes J., Piston F., Gimenez M.J., Martın A., Barro F. The introgression of RNAi silencing of γ-gliadins into commercial lines of bread wheat changes the mixing and technological properties of the dough. PLoS ONE, 2012, 7(9): e45937 ( ) DOI: 10.1371/journal.pone.0045937
- Wieser H., Koehler P., Folck A., Becker D. Characterization of wheat with strongly reduced α-gliadin content. 9th Annual Gluten Workshop, 14-16 September, 2006, San Fransisco, California, USA/G.L. Lookhart, P.K.W. Ng (eds.). AACC, St Paul, MN, 2006: 13-16.
- Altenbach S.B., Tanaka C.K., Allen P.V. Quantitative proteomic analysis of wheat grain proteins reveals differential effects of silencing of omega-5 gliadin genes in transgenic lines. J. Cereal Sci., 2014, 59: 118-125 ( ) DOI: 10.1016/j.jcs.2013.11.008
- Gil-Humanes J., Pistón F., Tollefsen S., Sollid L.M., Barro F. Effective shutdown in the expression of celiac disease-related wheat gliadin T-cell epitopes by RNA interference. PNAS USA, 2010, 107(39): 17023-17028 ( ) DOI: 10.1073/pnas.1007773107
- Segal G., Song R., Messing J. A new opaque variant of maize by a single dominant RNA-interference-inducing transgene. Genetics, 2003, 165: 387-397.
- Huang S., Frizzi A., Florida C.A., Kruger D.E., Luethy M.H. High lysine and high tryptophan transgenic maize resulting from the reduction of both 19-and 22-kD α-zeins. Plant Mol. Biol., 2006, 61: 525-535 ( ) DOI: 10.1007/s11103-006-0027-6
- Wu Y., Messing J. RNA interference-mediated change in protein body morphology and seed opacity through loss of different zein proteins. Plant Physiol., 2010, 153: 337-347 ( ) DOI: 10.1104/pp.110.154690
- Wu Y., Holding D.R., Messing J. g-Zeins are essential for endosperm modification in quality protein maize. PNAS USA, 2010, 107(29): 12810-12815 ( ) DOI: 10.1073/pnas.1004721107
- Guo X., Yuan L., Chen H., Sato S.J., Clemente T.E., Holding D.R. Non-redundant function of zeins and their correct stoichiometric ratio drive protein body formation in maize endosperm. Plant Physiol., 2013, 162: 1359-1369 ( ) DOI: 10.1104/pp.113.218941
- Da Silva L.S., Jung R., Zhao Z.Y., Glassman K., Grootboom A.W., Mehlo L., O’Kennedy M.M., Taylor J., Taylor J.R.N. Effect of suppressing the synthesis of different kafirin sub-classes on grain endosperm texture, protein body structure and protein nutritional quality in improved sorghum lines. J. Cereal Sci., 2011, 54: 160-167 ( ) DOI: 10.1016/j.jcs.2011.04.009
- Da Silva L.S., Taylor J., Taylor J.R.N. Transgenic sorghum with altered kafirin synthesis: kafirin solubility, polymerization and protein digestion. J. Agric. Food Chem., 2011, 59: 9265-9270 ( ) DOI: 10.1021/jf201878p
- Эльконин Л.А., Доманина И.В., Итальянская Ю.В., Ракитин А.Л., Равин Н.В. Трансгенное сорго с улучшенной перевариваемостью запасных белков и модифицированным типом эндосперма, полученное с помощью агробактериальной трансформации в культуре in vitro. Мат. V Всерос. симп. «Трансгенные растения: технология создания, биологические свойства, применение, безопасность». М., 2014: 239-242.
- Oria M.P., Hamaker B.R., Axtell J.D., Huang C.P. A highly digestible sorghum mutant cultivar exhibits a unique folded structure of endosperm protein bodies. PNAS USA, 2000, 97: 5065-5070 ( ) DOI: 10.1073/pnas.080076297
- Nagamine A., Matsusaka H., Ushijima T., Kawagoe Y., Ogawa M., Okita T.W., Kumamaru T. A role for the cysteine-rich 10 kDa prolamin in protein body I formation in rice. Plant Cell Physiol., 2011, 52(6): 1003-1016 ( ) DOI: 10.1093/pcp/pcr053
- Kim H.-J., Lee J.-Y., Yoon U.-H., Lim S.H., Kim Y.-M. Effects of reduced prolamin on seed storage protein composition and the nutritional quality of rice. Int. J. Mol. Sci., 2013, 14: 17073-17084 ( ) DOI: 10.3390/ijms140817073
- Kawakatsu T., Hirose S., Yasuda H., Takaiwa F. Reducing rice seed storage protein accumulation leads to changes in nutrient quality and storage organelle formation. Plant Physiol., 2010, 154: 1842-1854 ( ) DOI: 10.1104/pp.110.164343
- Kusaba M., Miyahara K., Lida S., Fukuoka H., Takario T., Sassa H., Nishimura M., Nishio T. Low glutenin content 1: a dominant mutation that suppresses the glutenin multigene family via RNA silencing in rice. Plant Cell, 2003, 15: 1455-1467 ( ) DOI: 10.1105/tpc.011452
- Ufaz S., Galili G. Improving the content of essential amino acids in crop plants: goals and opportunities. Plant Physiol., 2008, 147(3): 954-961 ( ) DOI: 10.1104/pp.108.118091
- Falco S.C., Keeler S.J., Rice J.A. Chimeric genes and methods for increasing the lysine and threonine content of the seeds of plants. US Patent 5,773,691. A01H 5/00. E. I. Du Pont de Nemours and Company. Appl. No.: 474,633. Filed: Jun. 7, 1995. Date of Patent: Jun. 30, 1998.
- Huang S., Kruger D.E., Frizzi A., D’Ordine R.L., Florida C.A., Adams W.R., Brown W.E., Luethy M.H. High-lysine corn produced by the combination of enhanced lysine biosynthesis and reduced zein accumulation. Plant Biotechnol. J., 2005, 3: 555-569 ( ) DOI: 10.1111/j.1467-7652.2005.00146.x
- Houmard N.M., Mainville J.L., Bonin C.P., Huang S., Luethy M.H., Malvar T.M. High-lysine corn generated by endosperm-specific suppression of lysine catabolism using RNAi. Plant Biotechnol. J., 2007, 5: 605-614 ( ) DOI: 10.1111/j.1467-7652.2007.00265.x
- Frizzi A., Huang S., Gilbertson L.A., Armstrong T.A., Luethy M.H., Malvar T.M. Modifying lysine biosynthesis and catabolism in corn with a single bifunctional expression/silencing transgene cassette. Plant Biotechnol. J., 2008, 6(1): 13-21 ( ) DOI: 10.1111/j.1467-7652.2007.00290.x
- Long X., Liu Q., Chan M., Wang Q., Sun S.S.M. Metabolic engineering and profiling of rice with increased lysine. Plant Biotechnol. J., 2012, 11(4): 490-501 ( ) DOI: 10.1111/pbi.12037
- Huang S., Frizzi A., Florida C.A., Kruger D.E., Luethy M.H. High lysine and high tryptophan transgenic maize resulting from the reduction of both 19-and 22-kD α-zeins. Plant Mol. Biol., 2006, 61: 525-535 ( ) DOI: 10.1007/s11103-006-0027-6
- Wong H.W.,·Liu Q.,·Sun S.S.M. Biofortification of rice with lysine using endogenous histones. Plant Mol. Biol., 2015, 87: 235-248 ( ) DOI: 10.1007/s11103-014-0272-z
- Yu P., Zhang Z., Zhu S., Liu A. Seed-specific expression of the lysine-rich protein gene sb401 significantly increases both lysine and total protein content in maize seeds. Mol. Breed., 2004, 14(1): 1-7 ( ) DOI: 10.1023/B:MOLB.0000037990.23718.d6
- Yue J., Li C., Zhao Q., Zhu D., Yu J. Seed-specific expression of a lysine-rich protein gene, GhLRP, from cotton significantly increases the lysine content in maize seeds. Int. J. Mol. Sci., 2014, 15(4): 350-365 ( ) DOI: 10.3390/ijms15045350
- Рукавцова Е.Б., Лебедева А.А., Захарченко Н.С., Бурьянов Я.И. Пути создания биобезопасных трансгенных безмаркерных растений. Физиология растений, 2012, 60(1): 17-30.
- Tuteja N., Verma S., Sahoo R.K., Raveendary S., Reddy IN B.L. Recent advances in development of marker-free transgenic plants: Regulation and biosafety concern. J. Biosci., 2012, 37: 167-197 ( ) DOI: 10.1007/s12038-012-9187-5
- De Paepe A., De Buck S., Nolf J., Van Lerberge E., Depicker A. Site-specific T-DNA integration in Arabidopsis thaliana mediated by the combined action of CRE recombinase and fC31 integrase. Plant J., 2013, 75: 172-184 ( ) DOI: 10.1111/tpj.12202
- Bortesia L., Fischer R. The CRISPR/Cas9 system for plant genome editing and beyond. Biotechnol. Adv., 2015, 33: 41-52 ( ) DOI: 10.1016/j.biotechadv.2014.12.006


