Генетическое разнообразие Bos grunniens, разводимого в Тянь-Шане Кыргызской Республики
Автор: Исакова Ж.Т., Чекиров К.Б., Кипень В.Н., Ирсалиев М.И., Мукеева С.Б., Курманбекова Г.Т., Айтбаев К.А., Иманбердиева Н.А.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Генетическая структура популяций
Статья в выпуске: 4 т.60, 2025 года.
Бесплатный доступ
Массивы высокогорных пастбищ, занимающие 90 % территории Кыргызской Республики, благоприятствуют развитию яководства, поскольку яки ( Bos grunniens ) - это исключительно пастбищные животные, приспособленные к обитанию в условиях высокогорного сурового климата. В мире считаные страны занимаются яководством. В Кыргызской Республике яки разводятся с глубокой древности, при этом расселение яка в горах Тянь-Шаня шло с юга на север. В процессе эволюции в горах Тянь-Шаня и Памиро-Алая сформировался определенный тип высокогорного яка, у которого выделено 8 типов мастей, от черной и бурой до пестрой и светло-бурой. В этой связи возникла необходимость выяснения генетической структуры у имеющегося поголовья яков для составления предварительной генетической референсной группы уникальных животных. В настоящей работе с помощью микросателлитных маркеров ДНК впервые определен молекулярно-генетический статус яков, разводимых в высокогорном регионе Тянь-Шаня Кыргызской Республики. Выявлены специфические характеристики, которые отличают кыргызскую популяцию яков от других географических групп этих животных, что вносит существенный вклад в понимание ее генетических особенностей. Полученные данные также дают возможность оценить генетическое разнообразие и риски инбридинга в популяциях яков Тянь-Шаня, что имеет большое значение для разработки стратегий сохранения и рационального использования этих животных. Цель нашего исследования - оценка генетического разнообразия популяции домашнего яка, разводимого в высокогорном регионе Тянь-Шаня Кыргызской Республики с использованием микросателлитных маркеров ДНК. Работа проводилась в 2021-2023 годах на базе НИИ молекулярной биологии и медицины (г. Бишкек, Кыргызская Республика) и в Институте генетики и цитологии (г. Минск, Республика Беларусь). Материалом для исследования служили образцы крови, взятые у взрослого поголовья 55 домашних яков, разводимых в высокогорном регионе Калмак-Ашуу (Кочкорский р-н, Нарынская обл., Кыргызская Республика). Образцы были генотипированы по 15 микросателлитным локусам: ETH3, INRA023, TGLA227, TGLA126, TGLA122, SPS115, ETH225, TGLA53, BM2113, BM1824, ETH10, BM1818, CSSM66, ILSTS006 и CSRM60. ПЦР проводили с использованием Multiplex PCR Master («Jena Bioscience GmbH», Германия) в мультилокусном формате согласно рекомендациям производителя. Далее продукты амплификации объединяли и подвергали фрагментному анализу. Анализ результатов ПЦР осуществляли методом капиллярного электрофореза с помощью автоматического генетического анализатора с лазериндуцированной флуоресцентной детекцией Applied Biosystems 3500 («Thermo Fisher», США). Контролем служили образцы, валидированные с использованием набора COrDIS Cattle (ООО «ГОРДИЗ», РФ). Анализ популяционно-генетических параметров, а также степень дифференциации на основании матрицы генетических дистанций проводили с использованием программного обеспечения GenAlEx 6.503 с последующей визуализацией дендрограмм по алгоритму Neighbor joining в программе Past v.4.03. Генетическую структуру исследуемой выборки яков оценивали посредством кластеризации в программе STRUCTURE 2.3.4. Оптимальное число кластеров (ΔK) определяли с использованием веб-приложения POPHELPER v1.0.10. В 15 аутосомных STR-локусах исследованной выборки было выявлено 89 аллелей, из них 32 - редкие (с частотой встречаемости менее 5,0 %). По результатам оценки генетико-популяционных параметров Na (5,933±0,316), Ne (3,015±0,235), Ho (0,617±0,049), PIC (0,581±0,130) сделано заключение о высоком уровне генетического разнообразия исследуемой выборки яков. Для формирования референсной группы яков, характеризующих их генетическое разнообразие в регионе, создана электронная база генотипов особей. Селекционные схемы при разведении домашнего яка в высокогорном регионе Тянь-Шаня сбалансированы и способствуют сохранению генетического разнообразия. Сравнительный анализ результатов представленного молекулярно-генетического исследования с результатами других аналогичных работ позволяет сделать заключение о значительном генетическом разнообразии домашних яков ( Bos grunniens ), разводимых в Тянь-Шане Кыргызской Республики.
Днк, микросателлитные маркеры, генотипирование
Короткий адрес: https://sciup.org/142246203
IDR: 142246203 | УДК: 636.293.3:575.174.015.3 | DOI: 10.15389/agrobiology.2025.4.641rus
Genetic diversity of Bos grunniens bred in the Tien Shan of the Kyrgyz Republic
The mountain range pastures, which occupy 90 % of the territory of the Kyrgyz Republic, are highly favorable for the development of yak breeding. Yaks ( Bos grunniens ) are exclusively pasture-based animals that are well-adapted to living in harsh high-mountain climatic conditions. Only a few countries in the world engage in yak breeding, and the Kyrgyz Republic has been breeding yaks since ancient times. The migration of yaks in the Tien Shan Mountains proceeded from south to north. During the evolutionary process in the Tien Shan and Pamir-Alai Mountains, a specific type of high-mountain yak was formed, exhibiting eight distinct coat colors, ranging from black and brown to variegated and light brown. It became necessary to clarify the genetic structure of the existing yak population in order to compile a preliminary genetic reference group of unique animals. In this study, the molecular genetic status of yaks bred in the high-mountain region of the Tien Shan of the Kyrgyz Republic was determined for the first time using microsatellite DNA markers. Specific characteristics that distinguish the Kyrgyz yak population from other geographic groups of these animals were identified, significantly contributing to the understanding of its genetic features. The obtained data also enable an assessment of genetic diversity and inbreeding risks in Tien Shan yak populations, which is crucial for developing conservation strategies and rational utilization of these animals. The aim of our research is to assess the genetic diversity of the domestic yak population bred in the highland region of the Tien Shan in the Kyrgyz Republic using DNA microsatellite markers. The study was conducted in 2021-2023 at the Research Institute of Molecular Biology and Medicine (Bishkek, Kyrgyz Republic) and the Institute of Genetics and Cytology (Minsk, Republic of Belarus). The research material was blood samples collected from an adult herd of 55 domestic yaks bred in the highland region of Kalmak-Ashuu (Kochkor district, Naryn region, Kyrgyz Republic). The samples were genotyped for 15 microsatellite loci: ETH3, INRA023, TGLA227, TGLA126, TGLA122, SPS115, ETH225, TGLA53, BM2113, BM1824, ETH10, BM1818, CSSM66, ILSTS006, and CSRM60. PCR was performed using Multiplex PCR Master (Jena Bioscience, Germany) in a multilocus format according to the manufacturer’s recommendations. The amplification products were then combined and subjected to fragment analysis. The PCR results were analyzed by capillary electrophoresis using an automatic genetic analyzer with laser-induced fluorescence detection, Applied Biosystems 3500 (Thermo Fisher, USA). Samples validated using the COrDIS Cattle kit (GORDIZ LLC, Russian Federation) served as controls. The analysis of population genetic parameters and the degree of differentiation based on the genetic distance matrix was performed using GenAlEx 6.503 software, with subsequent visualization of dendrograms using the Neighbor-joining algorithm in the Past v.4.03 program. The genetic structure of the studied yak sample was assessed by clustering in the STRUCTURE 2.3.4 program. The optimal number of clusters (ΔK) was determined using the POPHELPER v1.0.10 web application. In the 15 autosomal STR loci of the studied sample, 89 alleles were identified, 32 of which were rare (with an occurrence frequency of less than 5.0 %). Based on the assessment of genetic and population parameters (Na = 5.933±0.316, Ne = 3.015±0.235, Ho = 0.617±0.049, PIC = 0.581±0.130), a conclusion was made about the high values of genetic diversity in the studied yak sample. An electronic database of individual genotypes was created to form a reference group of yaks characterizing their genetic diversity in the region. The breeding schemes for domestic yaks in the high-mountain region of the Tien Shan are balanced and contribute to the preservation of genetic diversity. A comparative analysis of the results of this molecular genetic study with those of other similar works allows us to conclude that domestic yaks ( Bos grunniens ) bred in the Tien Shan of the Kyrgyz Republic exhibit significant genetic diversity.
Текст научной статьи Генетическое разнообразие Bos grunniens, разводимого в Тянь-Шане Кыргызской Республики
Работа выполнена в рамках государственного задания Министерства образования и науки Кыргызской Республики (Договор № 30-21 от 15/02/2021 №129/1).
Кыргызская Республика — горная страна, около 90 % территории сельскохозяйственных угодий которой занимают огромные массивы высокогорных пастбищ, что благоприятствует развитию яководства. Яки ( Bos grunniens ) — это исключительно пастбищные животные, приспособленные к обитанию в условиях высокогорного сурового климата, где почти нет других одомашненных продуктивных животных (1, 2). Обитая в мало затронутых антропогенным влиянием высокогорных районах (от 2700 до 5200 м над уровнем моря) при среднегодовой температуре 4 ° C, як дает экологически чистую продукцию и сырье (молоко, мясо, пух, шерсть). Мясо и молоко яка можно отнести к продуктам геронтологического питания повышенной пищевой ценности (2). В связи с этим в настоящее время, когда наблюдается спад мировой экономики, вопрос увеличения поголовья яков приобретает важное значение, тем более что их разведение всегда занимало важную нишу в жизни кыргызов, проживающих в обширных высокогорных районах, обеспечивая их необходимыми для жизни продуктами питания и сырьем для удовлетворения бытовых потребностей (2, 3).
В мире насчитывается около 15 млн яков. Китай — ведущая яко-водческая страна, в которой сосредоточено более 85 % мирового поголовья яков. Другие яководческие страны — Непал, Бутан, Индия, США, Пакистан, Афганистан, Кыргызстан, Таджикистан и Монголия (4). Считанные страны в мире имеют оптимальные природные условия для разведения яка, что позволяет им получать уникальную продукцию и сырье.
Архивные материалы свидетельствуют о том, что в Кыргызской Республике яки разводятся с глубокой древности, при этом расселение яка в горах Тянь-Шаня шло с юга на север (4). Тянь-Шаньский як, скорее всего, пришел из Тибета, а не из Монголии. В те времена южнее Кыргызстана, а именно в Кашгарских горах и Кокшалтау, жили кыргызы, занимающиеся яководством (5, 6). В процессе эволюции в горах Тянь-Шаня и Памиро-Алая сформировался определенный тип высокогорного яка, у которого выделено восемь типов мастей: от черной и бурой до пестрой и светло-бурой.
Систематический статистический учет численности яков начал проводиться с 1951 года, когда в республике насчитывалось около 3,8 тыс. яков, численность которых уже к 1978 году достигла 79,2 тыс. гол. (7). В связи с реформой в сельском хозяйстве в конце XX века их численность сократилась более чем в четыре раза, но уже по состоянию на 2021 год она составляет около 54 тыс. гол. (8).
В этой связи возникла необходимость выяснения генетической структуры у имеющегося поголовья яков для составления предварительной генетической референсной группы уникальных животных, хорошо приспособленных к суровым высокогорным климатогеографическим условиям Кыргызстана. Для исследований мы выбрали высокогорный регион Тянь-Шаня Калмак-Ашуу (высота местности 3000-3500 м над уровнем моря), где издавна занимались разведением яков.
В настоящей работе впервые определен молекулярно-генетический статус яков, разводимых в высокогорном регионе Тянь-Шаня Кыргызской Республики, с помощью микросателлитных маркеров ДНК. Выявлены специфические характеристики, которые отличают кыргызскую популяцию яков от других географических групп этих животных, что вносит существенный вклад в понимание ее генетических особенностей. Полученные данные также дают возможность оценить генетическое разнообразие и риски инбридинга в популяциях яков Тянь-Шаня, что имеет большое значение для разработки стратегий сохранения и рационального использо- вания этих животных.
Цель нашего исследования — оценка генетического разнообразия популяции домашнего яка, разводимого в высокогорном регионе Тянь-Шаня Кыхргызской Республики с использованием микросателлитных маркеров ДНК.
Методика. Работа проводилась в 2021-2023 годах на базе НИИ молекулярной биологии и медицины (г. Бишкек, Кыргызская Республика) и в Институте генетики и цитологии (г. Минск, Республика Беларусь). Материалом для исследования служили образцы крови, взятые у взрослого поголовья 55 домашних яков, разводимых в высокогорном регионе Кал-мак-Ашуу (Кочкорский р-н, Нарынская обл., Кыргызская Республика, координаты 42.134536N, 75.584365E, 2021-2022 годы). Были соблюдены все международные, национальные и институциональные принципы ухода и использования животных.
ДНК выделяли методом фенол-хлороформной экстракции (9). Образцы были генотипированы по 15 микросателлитным локусам (short tandem repeat, STR). Из анализируемых STR-локусов 12 составляли стандартную панель маркеров, рекомендованную Международным обществом генетики животных (International Society of Animal Genetics, ISAG): ETH3, INRA023, TGLA227, TGLA126, TGLA122, SPS115, ETH225, TGLA53, BM2113, BM1824, ETH10, BM1818. Дополнительно проанализировали микросателлитные локусы CSSM66, ILSTS006 и CSRM60. Последовательности олигонуклеотидов («Люмипроб Рус», Россия), температура отжига (Tотж.), флуоресцентные красители представлены ниже:
Праймер-F (5' ^ 3')
Праймер-R (5 ' ^ 3')
STR-локус
5 Т°тж'’ Ссылка метка oC
|
CSSM662 |
AATTTAATGCACTGAGGAGCTTGG |
ACACAAATCCTTTCTGCCAGCTGA |
FAM |
59 |
(10) |
|
BM18241 |
GAGCAAGGTGTTTTTCCAATC |
CATTCTCCAACTGCTTCCTTG |
ROX |
58 |
|
|
SPS1152 |
AAAGTGACACAACAGCTTCACCAG |
AACCGAGTGTCCTAGTTTGGCTGTG |
R6G |
59 |
(11) |
|
CSRM601 |
AAGATGTGATCCAAGAGAGAGGCA |
AGGACCAGATCGTGAAAGGCATAG |
ROX |
58 |
|
|
BM18181 |
AGCTGGGAATATAACCAAAGG |
AGTGCTTTCAAGGTCCATGC |
FAM |
58 |
(12) |
|
ILSTS0063 TGTCTGTATTTCTGCTGTGG |
ACACGGAAGCGATCTAAACG |
FAM |
56 |
(13) |
|
|
TGLA2274 GGAATTCCAAATCTGTTAATTTGCT |
ACAGACAGAAACTCAATGAAAGCA |
R6G |
56 |
(14) |
|
|
TGLA1264 CTAATTTAGAATGAGAGAGGCTTCT TTGGTCCTCTATTCTCTGAATATTCC |
R6G |
56 |
|||
|
TGLA1223 AATCACATGGCAAATAAGTACATAC |
CCCTCCTCCAGGTAAATCAGC |
R6G |
56 |
||
|
TGLA533 |
GCTTTCAGAAATAGTTTGCATTCA |
ATCTTCACATGATATTACAGCAGA |
TMR |
56 |
|
|
ETH32 |
GAACCTGCCTCTCCTGCATTGG |
ACTCTGCCTGTGGCCAAGTAGG |
FAM |
59 |
(15) |
|
ETH102 |
GTTCAGGACTGGCCCTGCTAACA |
CCTCCAGCCCACTTTCTCTTCTC |
ROX |
59 |
|
|
ETH2251 |
GATCACCTTGCCACTATTTCCT |
ACATGACAGCCAGCTGCTACT |
TMR |
58 |
(16) |
|
BM21132 |
GCTGCCTTCTACCAAATACCC |
CTTCCTGAGAGAAGCAACACC |
ROX |
59 |
|
|
INRA0233 |
GAGTAGAGCTACAAGATAAACTTC |
TAACTACAGGGTGTTAGATGAACTC |
FAM |
56 |
(17) |
|
Приме |
ч а н и е. В надстрочном формате приведен номер мультиплексной ПЦР. |
||||
ПЦР проводили с использованием Multiplex PCR Master («Jena Bioscience GmbH», Германия) в мультилокусном формате согласно рекомендациям производителя (число циклов — 35, объем реакционной смеси — 50 мкл, финальная концентрация праймеров — 300 нМ). Всего было проведено четыре реакции для каждого животного. Далее продукты амплификации объединяли и подвергали фрагментному анализу. Анализ результатов ПЦР осуществляли методом капиллярного электрофореза с помощью автоматического генетического анализатора с лазериндуцирован-ной флуоресцентной детекцией Applied Biosystems 3500 («Thermo Fisher», США). Контролем служили образцы, валидированные с использованием набора COrDIS Cattle (ООО «ГОРДИЗ», Россия).
Анализ популяционно-генетических параметров (среднее число аллелей на локус Na, эффективное число аллелей Ne, уровень ожидаемой и наблюдаемой гетерозиготности Ho/He, коэффициент Fis, а также стандартные отклонения для них), а также классификацию на основании мат- рицы генетических дистанций проводили с использованием программного обеспечения GenAlEx 6.503 (18) с последующей визуализацией дендрограмм по алгоритму Neighbor joining (Boot N = 10000) в программе Past v.4.03 (19). Коэффициенты информационного полиморфизма PIC (рoly-morphism information content) рассчитывали с использованием веб-приложения Gene-Calc (20).
Нарушение генетического равновесия оценивали с использованием соотношения Харди-Вайнберга (Hardy-Weinberg Equilibrium, HWE), отклонения считали значимыми при p < 0,05.
Генетическую структуру исследуемой выборки яков анализировали методом кластеризации в программе STRUCTURE 2.3.4 (21) с применением смешанной модели (число предполагаемых кластеров K — от 3 до 10; длина burn-in периода — 50K; модель Марковских цепей Монте-Карло — 5K). Для каждого значения K выполнялось по 10 итераций. Оптимальное число кластеров ( A K) определяли с использованием веб-приложения POPHELPER V1.0.10 по методу, предложенному G.S. Evanno с соавт. (22). Графическая интерпретация результатов, полученных в STRUCTURE v.2.3.4, была выполнена с помощью веб-приложения POPHELPER V1.0.10 (23).
Результаты. В 15 аутосомных STR-локусах исследованной выборки животных. 1).

Рис. 1. Яки ( Bos grunniens ), разводимые в высокогорном регионе Тянь-Шаня Калмак-Ашуу Коч-корского района Нарынской области Кыргызской Республики (2021 год) . Высота местности 3000-3500 м над уровнем моря.
1. Генетическая характеристика домашних яков ( Bos grunniens ) по результатам генотипирования 15 STR-локусов ( n = 55; высокогорный регион Тянь-Шаня Калмак-Ашуу, Кочкорский р-н, Нарынская обл., Кыргызская Республика, 2021-2022 годы)
|
STR-локус |
1 Na 1 |
Ne |
I Ho |
| He |
1 PIC I |
F is |
|
ETH3 |
4 |
1,577 |
0,291 |
0,366 |
0,321 |
0,205 |
|
CSSM66 |
7 |
3,965 |
0,800 |
0,748 |
0,696 |
- 0,070 |
|
INRA023 |
6 |
3,513 |
0,655 |
0,715 |
0,677 |
0,085 |
|
BM1818* |
6 |
1,676 |
0,400 |
0,403 |
0,357 |
0,008 |
|
ILSTS006 |
4 |
2,526 |
0,691 |
0,604 |
0,552 |
- 0,144 |
|
TGLA127* |
8 |
4,400 |
1,000 |
0,773 |
0,739 |
- 0,294 |
|
TGLA126 |
6 |
2,612 |
0,673 |
0,617 |
0,573 |
- 0,090 |
|
TGLA122 |
7 |
3,372 |
0,709 |
0,703 |
0,670 |
- 0,008 |
|
SPS115 |
6 |
4,080 |
0,709 |
0,755 |
0,614 |
0,061 |
|
CSRM60 |
6 |
3,103 |
0,564 |
0,678 |
0,613 |
0,168 |
|
BM2113 |
8 |
3,317 |
0,673 |
0,699 |
0,663 |
0,037 |
|
BM1824 |
5 |
1,995 |
0,527 |
0,499 |
0,445 |
- 0,057 |
|
ETH10* |
6 |
3,689 |
0,764 |
0,729 |
0,683 |
- 0,048 |
Продолжение таблицы 1
|
ETH225* |
5 |
1,931 |
0,327 |
0,482 |
0,442 |
0,321 |
|
TGLA53* |
5 |
3,473 |
0,473 |
0,712 |
0,662 |
0,336 |
|
Среднее ( M) |
5,933 |
3,015 |
0,617 |
0,632 |
0,581 |
0,034 |
|
Стандартное отклонение (±SD) |
0,316 |
0,235 |
0,049 |
0,034 |
0,130 |
0,044 |
Примечание. Na — число выявленных аллелей, Ne — число эффективных аллелей, H o — наблюдаемая гетерозиготность, H e — ожидаемая гетерозиготность, PIC — величина информационного полиморфизма, F IS — индивидуальный индекс фиксации.
* Выявлены статистически значимые отклонения от равновесия Харди-Вайнберга.
Число аллелей в каждом локусе варьировало от 4 до 8 при среднем значении 5,933±0,316 на локус. Наибольшее число аллелей имели аутосомные маркеры BM2113 и TGLA127 — по 8 аллелей. Обнаружены 32 редких аллеля (с частотой встречаемости менее 5,0 %), что составляло 35,96 % от общего числа выявленных аллелей. Наибольшее число редких аллелей выявлено для STR-локусов BM1818 (4 аллеля) и TGLA122 (3 аллеля).
Для некоторых STR-маркеров с большим числом наблюдаемых аллелей (например, для ETH3, BM1818, ETH225 и BM1824) были характерны относительно невысокие значения Ne. Это явление объясняется наличием в локусах редких аллелей с частотой встречаемости менее 5,0 %. При этом число эффективных аллелей в STR-маркерах значительно варьировало — от 1,577 (ETH3) до 4,400 (TGLA127). Показатель наблюдаемой гетерозиготности H o находился в диапазоне от 0,291 (ETH3) до 1,0 (TGLA127) при среднем значении 0,617±0,049. Для семи STR-маркеров показатель H o был выше ожидаемого H e (см. табл. 1).
Нарушение генетического равновесия было выявлено по семи мик-росателлитным локусам: INRA023 (ChiSq = 25,13; DF =15; p < 0,05), TGLA122 (ChiSq = 36,18; DF = 21; p < 0,05), TGLA53 (ChiSq = 39,05; DF = 10; p < 0,001), ETH225 (ChiSq = 45,47; DF = 10; p < 0,001), BM1818 (ChiSq = 110,68; DF = 15; p < 0,001), ETH10 (ChiSq = 114,93; DF = 15; p < 0,001) и TGLA127 (ChiSq = 160,44; DF = 28; p < 0,001).
При введении поправки на множественные сравнения статистически значимые различия для STR-локусов INRA023 и TGLA122 нивелировались. Для остальных STR-маркеров статистически значимых отклонений от равновесия Харди-Вайнберга не выявили (p > 0,05).
Величина PIC определяется способностью STR-маркера устанавливать полиморфизм в популяции в зависимости от числа обнаруживаемых аллелей и распределения их частот (24). Показатель PIC зависит от числа известных аллелей, а также распределения их частот и тем самым эквивалентен генетическому разнообразию. Для 11 STR-локусов в нашем исследовании PIC превышал значение 0,5, что свидетельствует о высокой информативной ценности использованных STR для дифференциации животных между собой. Наибольшие показатели PIC имели STR-локусы ETH10 (0,683), cSsM66 (0,696) и TGLA127 (0,739). Наименьшие значения показателя информативности отмечали у локусов ETH3 (0,321), BM1818 (0,357), ETH225 (0,442) и BM1824 (0,445).
Fis — индивидуальный индекс фиксации, который указывает на редукцию гетерозиготности из-за неслучайного спаривания и означает меру отклонения генотипических частот от таковых при HWE внутри субпопуляций с точки зрения недостатка или избытка гетерозигот. Дефицит гетерозиготных особей (родственное спаривание), то есть Fis > 0 показан для восьми STR-локусов (BM1818, BM2113, SPS115, INRA023, CSRM60, ETH3, ETH225 и TGLA53). Для оставшихся семи STR-локусов значение Fis < 0, то есть наблюдался избыток гетерозигот (неродственное спаривание). Среднее значение Fis (0,034±0,044) (см. табл. 1) позволяет сделать заключение о наличии незначительного сдвига в сторону процессов инбридинга для исследуемой выборки Bos grunniens.
Для оценки генетической подразделенности всей выборки c использованием программы STRUCTURE v.2.3.4 по методу J.K. Pritchard соавт. (21) был проведен расчет критерия Q, который характеризует принадлежность каждого отдельного животного к соответствующему кластеру. Выраженная генетическая подразделенность отсутствовала, а значит, выборка животных была довольно однородной.
В программе Past v.4.03 с использованием алгоритма Neighbour joining (Boot N = 10000) на основании генетических дистанций между особями построили дендрограмму, графически отображающую степень их схожести (рис. 2). По результатам кластеризации можно выделить два кластера, которые все же оказались незначительно удалены друг от друга. Дифференциация между кластерами была обусловлена, в первую очередь, частотой распространенности аллелей в STR-локусах TGLA53, ETH225, ETH10, CSRM60, SPS115 и ETH3.
Генетическая дистанция, отн. ед.
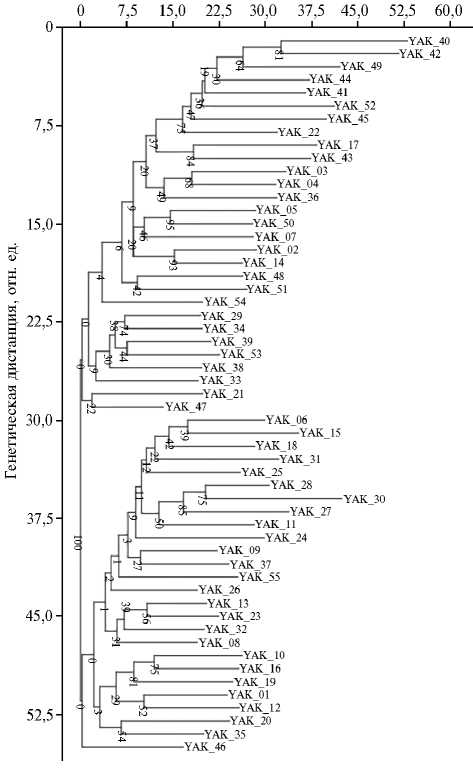
Рис. 2. Дендрограмма на основе парных генетических дистанций между особями из выборки Bos grunniens ( n = 55; высокогорный регион Тянь-Шаня Калмак-Ашуу, Кочкорский р-н, Нарын-ская обл., Кыргызская Республика, 2021-2022 годы). Расчет методом Neighbour joining, Boot N = 1000, адаптировано из PAST v.4.03.
Также мы провели сравнительный анализ параметров Na и Ho для выборок Bos grunniens с географической локализацией особей в Китае (25, 26), Монголии (26, 27), России (25, 27), Пакистане (28) и Швейцарии (29). Для всех исследований минимальное число STR-локусов составило 15, для сравнения приведены значения Na и Ho (табл. 2). Параметр Ne и частоты распространенности аллелей, как правило, не приводились, что не позволило проанализировать значения Ne вместо Na.
Установлено, что для изученных нами особей Bos grunniens из Кыргызстана среднее значение параметра Na (в контексте исследуемых в настоящей работе STR-маркеров) было одним из наибольших и составило 5,93±0,32; лишь для выборок из Китая (провинции Сычуань, Ганьсу, Синьцзян, Тибет, Цинхай и Юньнань) и Северного Хангая (Монголия) этот параметр был выше. При усреднении значений по странам Na оказался выше только для выборок из Китая.
Этот факт может свидетельствовать как о значительной полиморф-ности анализируемых нами STR-маркеров, так и о высоком генетическом разнообразии выборки Bos grunniens из Кыргызстана. Рассчитанный показатель H o в нашей работе также оказался одним из самых высоких и был сопоставим со значениями, полученными для выборок из Китая (25), Монголии (25) и России (25, 27). В целом, при совокупном анализе показателей Na и H o выборка Bos grunniens из Кыргызстана оказалась одной из наиболее генетически разнообразных.
2. Генетическая характеристика домашних яков ( Bos grunniens ) по результатам генотипирования STR-локусов ( M ±SD)
|
Страна |
Географическая локализация (число особей, n ) |
STR |
Na |
H o |
Ссылка |
|
Китай |
Цзяли (50) |
15 |
5,87±2,26 |
0,684±0,017 |
(25) |
|
MW, Сычуань (59) |
16 |
6,06 |
0,6 |
(26) |
|
|
TW, Ганьсу (60) |
16 |
6,13 |
0,551 |
||
|
XJ, Синьцзян (60) |
16 |
6,13 |
0,595 |
||
|
TH, Тибет (61) |
16 |
6,25 |
0,579 |
||
|
JL, Сычуань (60) |
16 |
6,31 |
0,55 |
||
|
PL, Тибет (62) |
16 |
6,31 |
0,59 |
||
|
SB, Тибет (57) |
16 |
6,31 |
0,61 |
||
|
QP, Цинхай (60) |
16 |
6,50 |
0,608 |
||
|
ZD, Юньнань (60) |
16 |
7,06 |
0,574 |
||
|
Китай (589) |
6,29±0,32 |
0,590±0,040 |
|||
|
Монголия |
Ubs (30) |
15 |
4,33±1,11 |
0,625±0,023 |
(25) |
|
Южный Гоби (20) |
15 |
4,90±0,36 |
0,600±0,050 |
(27) |
|
|
Хубсугул (20) |
15 |
5,10±0,44 |
0,590±0,053 |
||
|
Ховсгол (40) |
15 |
5,27±1,44 |
0,639±0,020 |
(25) |
|
|
Южный Гоби (38) |
15 |
5,47±1,88 |
0,669±0,022 |
||
|
Гоби Алтай (38) |
15 |
5,60±1,84 |
0,705±0,019 |
||
|
Северный Хангай (38) |
15 |
6,20±1,74 |
0,676±0,017 |
||
|
Монголия (224) |
5,27±0,59 |
0,640±0,040 |
|||
|
Россия |
Адарган, Тува (58) |
15 |
3,90±0,41 |
0,530±0,051 |
(27) |
|
Малчан, Тува (59) |
15 |
3,90±0,34 |
0,630±0,049 |
||
|
Алтай (20) |
15 |
4,10±0,33 |
0,590±0,035 |
||
|
Моген-Бурен, Тува (58) |
15 |
4,30±0,53 |
0,580±0,049 |
||
|
Арыг-Хем, Тува (60) |
15 |
4,60±0,58 |
0,570±0,050 |
||
|
Бурятия (40) |
15 |
4,73±1,83 |
0,641±0,020 |
(25) |
|
|
Сайзырал, Тува (69) |
15 |
4,80±0,57 |
0,530±0,051 |
(27) |
|
|
Россия (364) |
4,33±0,38 |
0,580±0,040 |
|||
|
Пакистан |
(300) |
27 |
5,11±2,33 |
0,482±0,305 |
(28) |
|
Швейцария |
Вале (51) |
25 |
5,56±1,89 |
0,583±0,162 |
(29) |
|
Кыргызстан |
Калмак-Ашуу (55) |
15 |
5,93±0,32 |
0,617±0,049 |
Настоящее исследование |
Примечание. Na — число выявленных аллелей, H o — наблюдаемая гетерозиготность. MW, TW, XJ, TH, JL, PL, SB, QP, ZD — обозначения пород (26).
Таким образом, результаты оценки генетико-популяционных параметров Na, Ne, Ho, He, PIC, Fis для домашних яков (Bos grunniens), разводимых в высокогорном регионе Тянь-Шаня Калмак-Ашуу Кыргызской Республики, свидетельствуют о высоком генетическом разнообразии исследуемой выборки, которое при сравнении с аналогичными данными других исследований в большинстве случаев также остается одним из наибольших. По четырем микросателлитным локусам — ETH3, CSRM60, ETH225 и TGLA53 показаны высокие значения Fis, которые сдвигают среднее значение этого параметра в положительную область (Fis = 0,034±0,044), в то же время смещение генетического равновесия в сторону процессов инбридинга оказалось несущественным. Среднее значение коэффициента информационного полиморфизма PIC составило 0,581±0,130, а для девяти STR его значение превысило 0,6. Для формирования референсной группы яков, характеризующих их генетическое разнообразие в регионе, создана электронная база генотипов особей. Селекционные схемы при разведении домашнего яка в высокогорном регионе Тянь-Шаня сбалансированы и способствуют сохранению генетического разнообразия (динамика последнего будет изучаться в среднесрочной перспективе).


