Генотоксический мониторинг морских лагун залива Петра Великого
Автор: Слободскова В.В., Солодова Е.Е., Челомин В.П.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Природопользование и мониторинг
Статья в выпуске: 1-6 т.13, 2011 года.
Бесплатный доступ
В работе представлены результаты исследования по выявлению генотоксичности среды обитания Corbicula japonica населяющей лагуны Тихая и Лебяжья залива Петра Великого. Для выявления генотоксических эффектов был использован метод ДНК-комет. Выяснено, что моллюски, обитающие в лагуне Тихая, находятся под влиянием антропогенного загрязнения, т.к. 1/3 молекулы ДНК жаберных клеток C. japonica имеет ярко выраженные деструктивные изменения.
Мониторинг, морская лагуна, метод днк-комет
Короткий адрес: https://sciup.org/148199870
IDR: 148199870 | УДК: 577.1:577.41
Genotoxical monitoring of sea lagoons peter the great bay
In work results of research on revealing gene toxicity of Corbicula japonica inhabitancy in occupying lagoon Tikhaya and Lebyazhaya from Peter the Great bay are presented. For revealing genetoxical effects the method of DNA-comets has been used. It is found out that the mollusks living in Tikhaya lagoon, are under the influence of anthropogenous pollution, since 1/3 molecules of DNA of branchiate cages C. japonica has strongly pronounced destructive changes.
Текст научной статьи Генотоксический мониторинг морских лагун залива Петра Великого
В морских лагунах залива Петра Великого сформировались наиболее высокопродуктивные водные экосистемы, в состав которых входит ряд хозяйственно важных и ценных видов растений и животных. В связи с этим состояние уникальных экосистем морских лагун требует комплексных исследований, направленных на сохранение среды обитания гидробионтов. Экосистемы морских лагун характеризуются уязвимостью, они испытывают сильные воздействия внешних факторов среды и постоянно изменяются при незначительных колебаниях уровня моря. Это объясняется тем, что при функционировании любой приливно устьевой области формируется собственный режим сезонной и короткопериодной циркуляции вод и биогеохимических характеристик. Помимо этого, они в значительной степени подвержены антропогенному влиянию. Вариабельность абиотических факторов может изменять биодоступность и токсичность поллютантов. Концентрация большого количества органического вещества в этих акваториях обычно приводит к истощению кислорода, что неблагоприятно сказывается на гидробионтах.
В нашей работе мы провели генотоксический мониторинг морских лагун залива Петра Великого с использованием метода ДНК-комет
Ранее метод применялся только в медицинских исследованиях на клетках млекопитающих, но в середине 90-х гг. стал широко использоваться в экологическом мониторинге [6-10]. Данный подход служит для оценки раннего проявления повреждающего действия негативных факторов среды и, по своей сути, является сигналом возникновения угрозы развития патологических процессов. Основное преимущество метода заключается в его способности регистрировать повреждения на уровне отдельной эукариотической клетки практически любого происхождения. Для анализа образца методом ДНК-комет необходимо наличие всего нескольких тысяч клеток. Также привлекает быстрота проведения экспериментов и относительная простота лабораторного протокола.
Цель работы: выявить генотоксические эффекты среды обитания на степень повреждения молекулы ДНК жаберных клеток двустворчатого моллюска Corbicula japonica методом ДНК-комет.
Материалы и методы исследования. В работе использовали половозрелых особей (размер 30-34 мм) двустворчатого моллюска Corbicula japonica . Вид распространен в Японском море от Восточно-Корейского залива до западного побережья Сахалина. Обитает в солоноватых водах эстуариев рек, приморских лагун и озер, соединяющихся с морем протоками. Отбор моллюсков проводился в весеннее время при температуре воды примерно 14-15оС в лагунах Лебяжья и Тихая водолазным способом (рис. 1). Выловленных моллюсков доставляли в лабораторию в течение 2-х часов. После 2-х дневной адаптации при температуре 16-18ºС проводили исследование степени повреждения молекулы ДНК жаберных клеток
C. japonica , обитающей в разных лагунах залива Петра Великого. В работе использовали щелочной вариант кометного анализа, адаптированного к морским организмам [2].
Исходя из классификации, предложенной Коллинзом с коллегами [5], клетки жабр моллюсков обитающих в лагуне Лебяжья, в большинстве, образуют кометы класса С1. Принад-
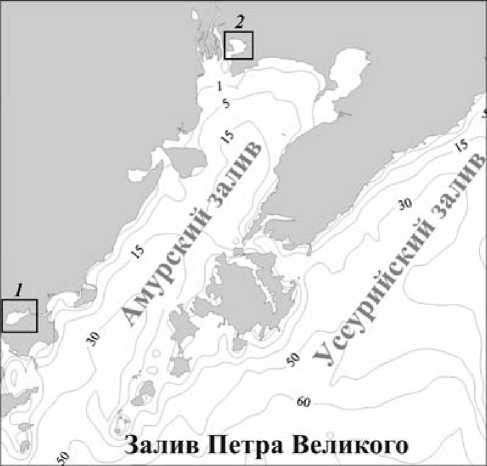
Рис. 1. Места сбора проб моллюсков: 1 – лагуна Лебяжья; 2 – лагуна Тихая
лежность комет к данному типу характерна для неповрежденных и жизнеспособных клеток. Кометы, формируемые клетками жабр корбикулы, населяющей устье реки Раздольная, можно отнести преимущественно к классу С3, что свидетельствуют о высоком уровне фрагментации молекулы ДНК. В таблице мы привели усредненные параметры полученных комет (доля ДНК в хвосте кометы – %DNAt, длина хвоста кометы – Lt), отражающие степень повреждения ДНК клеток жабр C. Japon-ica (см. таблицу).
Таблица. Основные параметры ДНК-комет клеток жабр моллюсков C. japonica, собранных в разных районах залива Петра Великого
|
Места сбора моллюсков |
Lt |
% DNAt |
|
лагуна Лебяжья |
36,25±14,92 |
20,79±8,40 |
|
Лагуна Тихая |
91,18±38,1 |
40,90±12,05 |
Результаты и обсуждение. На рис. 2
представлены микрофотографии комет, формируемые клетками жабр С. japonica собранной с разных лагун залива Петра Великого (рис. 2). При визуальном анализе полученных изображений, видно, что молекула ДНК клеток жабр C. japonica собранной в лагуне Лебяжьей практически не имеет деструктивных изменений (рис. 2 а ), т.к. ДНК образует симметричное яркое ядро с незначительным количеством повреждений. В то же время, в клетках жабр моллюсков, отобранных в лагуне Тихая, молекула ДНК образует хорошо выраженные кометы, что, очевидно, обусловлено глубокой деградацией генома и миграцией низкополимер-ных фрагментов ДНК (рис. 2 б ).
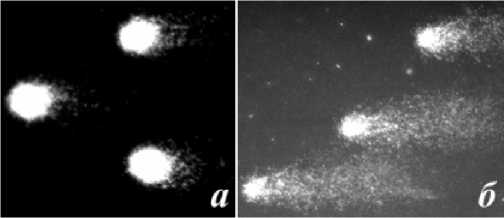
Рис. 2. Микрофотографии комет, формируемые клетками жабр C. Japonica собранных с разных лагун залива Петра Великого: а – лагуна Лебяжья; б – лагуна Тихая
При анализе этих данных отчетливо видно, что в клетках жабр у животных собранных в лагуне Тихая, значения указанных параметров существенно выше, чем у животных обитающих в лагуне Лебяжья (см. таблицу). Для наглядности, полученные экспериментальные данные, из которых были рассчитаны усредненные значения (таблица), были представлены на рис. 3 в виде зависимости между % ДНК и длиной «хвоста» кометы. Этот вид бивари-антного распределения обычно используется для характеристики популяций и наглядно демонстрирует пределы значений параметров, характеризующих кометы, и их взаимосвязь. При этом доля ДНК, мигрирующей из ядра кометы, в клетках моллюсков, обитающих в лагуне Лебяжья, не превышает 10 и 15%, тогда как в клетках корбикул, полученных из лагуны Тихой, этот показатель для основной массы комет составляет 40-45%. Также обращает на себя внимание высокая вариабельность данных параметров, что свидетельствует о гетерогенности всех выборок комет и обусловлено влиянием негативных факторов среды. Похожая картина была отмечена авторами при аккумуляции кадмия клетками жабр C. japonica и Mizuhopecten yessoensis [2, 11].
На основе проведенного генотоксического мониторинга морских лагун, находящихся в разных районах залива Петра Великого, можно судить об уровне антропогенной нагрузки на водные экосистемы данных акваторий. Наши данные позволяют сделать вывод о том, что моллюски, обитающие в лагуне Тихая, находятся под давлением мощного антропогенного прессинга, т.к. практически 1/3 часть молекулы ДНК жаберных клеток имеет повреждения.
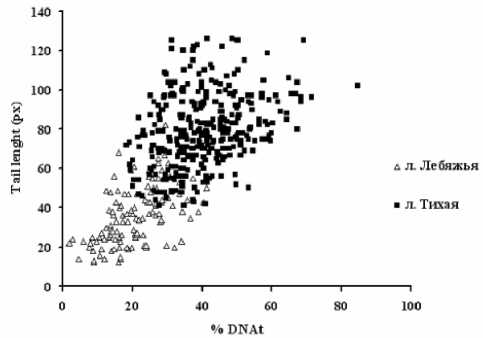
Рис. 3. Корреляция между % мигрированной ДНК (%DNAt) и длиной хвоста (Lt) комет, формируемых клетками жабр моллюсков обитающих в лагунах Лебяжья и Тихая
сопровождается эвтрофикацией водоема [1]. На это также указывает разрушенный периост-ракум моллюсков, населяющих данную акваторию, что говорит о неблагоприятных (кислых) условиях среды [4]. Следует отметить, что периостакум моллюсков, собранных в лагуне Тихой, разрушен не был.
Выводы: любое вмешательство человека в окружающую среду откладывает свой отпечаток на функционирование биологических систем. Наше исследование показало, что не только загрязнение водной среды, но и бездумная «перекройка» прибрежных акваторий определяют условия обитания гидробионтов. При этом неблагополучная среда обитания может инициировать серьезные нарушения в структуре молекулы ДНК, которые могут привести к возникновению мутаций и злокачественных трансформаций клетки. Учитывая исключительную роль генома в функционировании биологической системы, выявленные повреждения в структуре молекулы ДНК следует отнести к наиболее важным проявлениям неблагоприятного воздействия среды. Потенциальные экологические последствия такого влияния на отдельные особи могут реализовываться через нарушение динамики на популяционном уровне и уровне сообществ. Генотоксический мониторинг прибрежных акваторий с использованием метода ДНК-комет является объективным критерием оценки качества среды, так как позволяет фиксировать изменения на ранних этапах развития необратимых патологий.
Работа выполнена при поддержке гранта Правительства Российской Федерации № 11.G34.31.0010.
Список литературы Генотоксический мониторинг морских лагун залива Петра Великого
- Раков, В.А. Современное состояние, перспективы использования и сохранения экосистем морских лагун и эстуариев юга Дальнего Востока//Природа без границ: Материалы I Международного экологического форума. Ч. 1. Владивосток, 2006. С. 267-270.
- Слободскова, В.В. Оценка генотоксичности кадмия в клетках жабр двустворчатого моллюска Corbicula japonica с помощью метода ДНК-комет/В.В. Слободскова, Е.Е. Солодова, Е.Н. Слинько, В.П. Челомин//Биология моря. 2010. Т. 36, № 4. С. 303-308.
- Слободскова, В.В. Применение генотоксического анализа для мониторинга прибрежной зоны залива Петра Великого/В.В. Слободскова, Е.Е. Солодова, В.П. Челомин//Современные проблемы физиологии и биохимии водных организмов. Том. 1. Экологическая физиология и биохимия водных организмов. сборник научных статей -Петрозаводск: Карельский научный центр РАН, 2010. С. 272-277.
- Явнов, С.В. Корбикула/С.В. Явнов, В.А. Раков. -Владивосток: ТИНРО-центр, 2002. 145 с.
- Collins, A.R. The kinetics of repair of oxidative DNA damage (strand breaks and oxidized pyrimidine) in human cells/A.R. Collins, A.G. Ma, S.J. Duthie//Mutation Res. 1995. V. 336. P. 69-77.
- Mitchelmore, C.L. Detection of DNA strand breaks in isolated mussels (Mytilus edulis) digestive gland cells using the "Comet" assay/C.L. Mitchelmore, C. Birmelin, D.R. Livingstone, J.K. Chipman//Ecotoxicology and Environmental Safety. 1998. Vol. 41. P. 51-58.
- Mitchelmore, C.L. Assessing DNA damage in cnidarians using the Comet assay/C.L. Mitchelmore, S. Hyatt//Mar. Environ. Res. 2004. Vol. 58. P. 707-711.
- Nacci, D.E. Detection of DNA damage in individual cells from marine organisms using the single cell gel assay/D.E. Nacci, S. Cayula, E. Jackim//Aquat. Toxicol. 1996. Vol. 35. P. 197-210.
- Regoli, F. Time-course variations of oxyradical metabolism, DNA integrity and lisosomal stability in mussels, Mytilus galloprovincialis, during a field translocation experiment/F. Regoli, G. Frenzili, R. Bocchetti et al./Aquat. Toxicol. 2004. Vol. 68. P. 167-178.
- Shugart, L.R. DNA damage as a biomarker of exposure//Ecotoxicology. 2000. Vol. 9. P. 329-340.
- Slobodskova, V.V. DNA damage (Comet assay) as biomarker of Cd exposure in marine seed scallops Mizuhopecten yessoensis age 1 year/V.V. Slobodskova, E.E. Solodova, V.P. Chelomin//Journal of environ. Scien. and Engineer. 2010. V. 4. № 10. P. 63-69.


