Гетерогенный катализ этерификации адипиновой кислоты фосфатом титана, активированным SOCl2
Автор: Михаил Евгеньевич Ханов, Антон Дмитриевич Абрамян, Наталья Михайловна Тарасова, Данил Андреевич Манько, Олег Игоревич Большаков
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
Современные тенденции в разработке экологичных полимерных материалов, в частности биоразлагаемых и биосовместимых полимеров, стимулируют активные поиски пластификаторов, обладающих аналогичным комплексом свойств. В качестве перспективной альтернативы токсичным фталатным пластификаторам, доминирующим на рынке, выступают диалкиловые эфиры алифатических дикарбоновых кислот, такие как производные адипиновой и себациновой кислот. Их ключевые преимущества — биоразлагаемость, низкая миграционная способность и минимальная экотоксичность. Однако существенным технологическим барьером остается их синтез, который до сих пор преимущественно основан на применении гомогенных минеральных кислот в качестве катализаторов этерификации. Это сопряжено с фундаментальными недостатками: высокой коррозионной активностью, необходимостью нейтрализации и промывки, образованием больших объемов токсичных солей и сточных вод, что прямо противоречит принципам «зеленой» химии и устойчивого развития. Гетерогенные катализаторы рассматриваются как стратегически важное решение, позволяющее минимизировать негативное воздействие на окружающую среду за счет возможности регенерации и организации поточных процессов. В отличие от гомогенных систем, они содержат стабильные кислотные центры Бренстеда или Льюиса, закрепленные на развитой поверхности термостойкой неорганической подложки. Несмотря на значительный прогресс в повышении их активности и селективности, ключевым технологическим ограничением для широкого внедрения остается сравнительно низкая кинетика этерификации длинноцепочечных субстратов. В данной работе предложен метод бескислотной активации фосфата титана с помощью тионилхлорида. Этот подход позволяет трансформировать инертные поверхностные гидроксильные группы в высокоактивные хлоридные центры Льюиса. Показано, что каталитическая активность в реакции этерификации коррелирует с остаточным содержанием поверхностных -OH групп на поверхности, которые в ходе активации конвертируются в хлориды, существенно усиливая кислотные свойства материала. Интересно, что наиболее активными как до, так и после обработки оказались аморфные образцы TiP, лишенные выраженной кристаллической структуры и морфологических особенностей, что, вероятно, связано с большей удельной поверхностью.
Этерификация, адипиновая кислота, гетерогенный катализатор, фосфат титана
Короткий адрес: https://sciup.org/147252530
IDR: 147252530 | УДК: 544.47 | DOI: 10.14529/chem250418
Heterogeneous catalysis of adipic acid esterification by titanium phosphate activated with SOCL₂
Current trends in the development of environmentally friendly polymer materials, in particular biodegradable and biocompatible polymers, naturally stimulate active research for plasticizers with a similar set of properties. Dialkyl esters of aliphatic dicarboxylic acids, such as derivatives of adipic acid and sebacic acid, act as a promising alternative to toxic phthalate plasticizers that dominate the market. Their key advantages are biodegradability, low migration capacity, and minimal ecotoxicity. However, their synthesis remains a significant technological barrier, as it is still mainly based on the use of homogeneous mineral acids in the role of esterification catalysts. This is associated with fundamental disadvantages: high corrosive activity, the need for neutralization and flushing, as well as formation of large volumes of toxic salts and wastewater, which directly contradicts the principles of "green" chemistry and sustainable development. Heterogeneous catalysts are considered as a strategically important solution that minimizes the negative impact on the environment due to possibilities of regeneration and organization of flow processes. Unlike homogeneous systems, they contain stable Bronsted or Lewis acid centers fixed on the developed surface of a heat-resistant inorganic substrate. Despite significant progress in increasing their activity and selectivity, the key technological limitation for widespread adoption remains the relatively low kinetics of esterification of long-chain substrates. In this paper, a method of acid-free activation of titanium phosphate using thionyl chloride is proposed. This approach makes it possible to transform inert surface hydroxyl groups into highly active Lewis chloride centers. It is shown that catalytic activity in the esterification reaction correlates with the residual content of the -OH groups on the surface, which are converted into chlorides during activation, significantly enhancing acidic properties of the material. Interestingly, amorphous TiP samples, devoid of pronounced crystalline structure and morphological features, are the most active both before and after treatment, which is probably due to the higher specific surface area.
Текст научной статьи Гетерогенный катализ этерификации адипиновой кислоты фосфатом титана, активированным SOCl2
Пластификаторы представляют собой добавки к полимерным материалам, модифицирующие их основные свойства: пластичность и вязкость. Эти соединения выполняют функцию молекулярных разбавителей, внедряясь в структуру полимера и ослабляя межмолекулярные взаимодействия между цепями, что приводит к снижению жесткости и увеличению пластичности и эластичности. Годовой объем производства пластификаторов оценивается в несколько миллионов тонн. Наиболее совместимыми с полимерами считаются сложные эфиры дикарбоновых кислот, содержащие длинные алкильные цепи.
Наиболее распространенными и доступными пластификаторами являются эфиры фталевой кислоты, на долю которых приходится свыше 85 % мирового рынка [1, 2]. Однако применение фталатов связано с повышенными рисками для здоровья человека [3, 4], поскольку они легко мигрируют из полимерных композитов. Данный факт обусловливает необходимость ужесточения контроля и сокращения их использования [5–7].
Перспективной альтернативой считаются экологически безопасные пластификаторы нового поколения – диэфиры адипиновой, себациновой и янтарной кислот с длинными алифатическими цепями [8–11]. К их преимуществам относятся биоразлагаемость, термическая стабильность, а также сниженная склонность к миграции из полимерной матрицы [12].
Получение диалкиладипатов и диалкилсебацинатов обычно включает реакцию этерификации адипиновой или себациновой кислот спиртами C 4 –C 8 в кислой среде. Процесс проводят при повышенных температуре и давлении для смещения равновесия в сторону образования эфира. Традиционно используемый катализатор – серная кислота – требует дополнительных стадий промывки продукта щелочными растворами и больших объемов воды [8]. В связи с этим разработка эффективных, экономичных и экологически безопасных катализаторов остается актуальной научно-технологической задачей.
Постепенное присоединение длинных алкильных остатков к дикарбоновым кислотам кинетически затруднено [13–15]. Для компенсации низкой скорости реакции используют избыток спирта и высокие температуры [16–18]. Дополнительную проблему представляет высокая вязкость высших спиртов, кислот и их смесей. Для ее снижения и улучшения кинетики этерификации в систему вводят растворители. Современное производство пластификаторов основано на применении сильных минеральных кислот и их производных [19–22]. Однако такая технология требует использования коррозионно-стойких реакторов и стадий нейтрализации, сопровождающихся образованием опасных отходов [23]. Данный устаревший подход увеличивает капитальные и эксплуатационные затраты, делая процесс дорогостоящим и экологически неблагоприятным.
Эффективной альтернативой минеральным кислотам в катализе этерификации являются кислоты Льюиса. В частности, успешно применяются соли металлов, их гидраты и комплексы, а также алкоксиды переходных металлов [24–26], позволяющие проводить реакцию в менее жестких условиях без использования и выделения агрессивных веществ. Однако основные недостатки металлсодержащих катализаторов – остаточное содержание металлов в реакционной смеси и высокая стоимость.
В этом контексте гетерогенные катализаторы представляют более перспективную альтернативу, доказавшую свою эффективность в промышленных процессах [23, 27]. Они позволяют проводить многократные циклы реакции без потери каталитической активности, а также адаптировать процесс к поточным технологиям. Кислотные гетерогенные катализаторы этерификации получают введением кислотных центров на поверхность подложки. Кислотные центры Бренстеда могут быть закреплены на поверхности носителя методом хемосорбции или ковалентного связывания, тогда как центры Льюиса создаются путем допирования ионами металлов [28–30].
Индивидуальные оксиды редко используются в катализе, выполняя преимущественно роль пористых носителей для сульфатов [31], алкилсульфонатов, гетерополикислот [32] и ионов металлов [33]. Более эффективными считаются смешанные оксиды, поскольку их неоднородная структура создает дополнительные дефекты кристаллической решетки, выступающие кислотными центрами или участками адсорбции. Для повышения каталитической активности смешанные оксиды подвергают модификации: импрегнации сильными кислотами, допированию ионами металлов, нанесению наночастиц, введению функциональных групп.
Фосфат титана – широко изученный материал, нашедший применение как сорбент, фотокатализатор, гетерогенный катализатор и протонный проводник [34–37]. Наличие в составе фосфатных групп создает предпосылки формирования Бренстедовских кислотных центров, необходимых для проведения реакции этерификации. Вместе с тем силы этих кислотных центров недостаточно для кинетически затрудненной этерификации адипиновой кислоты. Для решения этой проблемы нами предложена модификация поверхности фосфата титана путем введения Льюи-совксих центров кислотности реакцией с тионилхлоридом (SOCl 2 ) – известного дегидратирующего [38] и хлорирующего агента [39]. Данный подход позволил получить поверхностно-хлорированные титановые центры, значительно повысив каталитическую активность в синтезе октилового эфира адипиновой кислоты – перспективного заменителя фталатных пластификаторов.
Аммиак (NH 4 OH, 32%-ный водный раствор), тионилхлорид (SOCl 2 ) и перекись водорода (H 2 O 2 , 60 %) были приобретены в AO «ВЕКТОН» (Санкт-Петербург, Россия). Миндальная кислота (100 %, Bingospa), H 3 PO 4 (НеваРеактив) были использованы без предварительной очистки. Порошок титана (Ti), метилстеарат и диоктиладипинат были приобретены Sigma-Aldrich, Merck KGaA (Драмштадт, Германия). Адипиновая кислота была приобретена в Radici Group (Зельбиц-Хохфранкен, Бавария, Германия). Бутанол, хлороформ, изо-бутанол, октанол, 1-гексанол, изооктанол, 2-бутоксиэтанол были приобретены в ООО «Реарус» (Москва, Россия). П-толуолсульфокислота была приобретена в Компонент-Реагент (Москва, Россия).
Методы
Морфологию и элементный состав полученных образцов анализировали с помощью энергодисперсионной рентгеновской спектроскопии (ЭДС) на сканирующем электронном микроскопе с полевой эмиссией JEOL JSM 7001F (JEOL, Япония), оснащенном энергодисперсионным спектрометром Oxford INCA Xmax 80. Ускоряющее напряжение электронной пушки было установлено на уровне 20 кВ, что является оптимальным для анализа ЭДС.
Кристаллические фазы синтезированных материалов определяли методом рентгенографии. Рентгенограммы регистрировали с помощью дифрактометра Rigaku Ultima IV (Rigaku Corporation, Япония) с использованием излучения CuKα (λ = 1,541 Å) при ускоряющем напряжении 40 кВ. Сканирование проводилось в диапазоне от 5 до 90 2θ° со скоростью 5 2θ°/мин.
Определение удельной поверхности и пористости проводились методом низкотемпературной адсорбции азота на приборе ASAP Micromeritics 2020. Навеска образца составляла 100 мг. Стадии измерения предшествовала стадия дегазации, проводимая при температуре 200 °С в течение 2 часов. Определение удельной поверхности осуществлялось на основе метода многослойной адсорбции БЭТ при изменении относительного давления N 2 (P/P 0 ). Объем мезопор и распределение их по размерам рассчитан на основании модели Барретта-Джойнера-Халенды (БДХ/БЭТ).
Количественный и качественный анализ продуктов реакции проводили с помощью газового хромато-масс-спектрометра Shimadzu GCMS-QP2010 Ultra, оснащенного колонкой GsBP-1MS, работающей при ионизации 70 эВ в режиме сбора данных FASST (Fast automated Scan/SIM mode).
Потерю массы и тепловые эффекты оценивали с помощью синхронного термического анализатора NETZSCH STA 449 F3 Jupiter (NETZSCH, Германия), позволяющего проводить одновременную дифференциальную сканирующую калориметрию (DSC) и термогравиметрический анализ (TGA).
Элементный состав образцов был проанализирован с помощью оптико-эмиссионной спектроскопии с индуктивно-связанной плазмой (ОЭС-ИСП) на приборе Perkin Elmer ORAS OPTIMA 7300 DV для определения содержания титана и фосфора. Определение содержания титана (Ti) и фосфора (P) проводили по спектральным линиям 336,121 нм (Ti) и 213,617 нм (P). Калибровочные кривые для элементов показали значительную линейность (R2 = 0,9999). Перед анализом твердые образцы растворяли в 5 мл 35%-ной перекиси водорода (H 2 O 2 ) с постепенным нагреванием от 100 до 180 °С, избегая сильного кипячения. После полного растворения добавляли 5 мл концентрированной серной кислоты (H 2 SO 4 ) и нагревали смесь при температуре 150–250 °С до обесцвечивания. Затем температуру увеличивали до 350 °С и раствор выпаривали до появления густых паров H2SO4. После охлаждения остаток растворяли и доводили до метки в мерной колбе объемом 50 мл.
Синтез Ti-комплекса с DL-миндальной кислотой. Согласно ранее опубликованной методике [40] 0,41 г (8,5 ммоль) порошка титана диспергировали в 5 мл NH 4 OH (25 %), затем добавляли 40 мл перекиси водорода (37 %) для растворения металла, контролируя температуру смеси в диапазоне 5–10 °С. Полученный светло-желтый раствор пероксокомплекса смешивали с раствором DL-миндальной кислоты (2,6 г, 17 ммоль) в 5 мл воды. Полученный водный раствор выпаривали при пониженном давлении на роторном испарителе при 30–40 °С, получая титановый комплекс в виде светло-желтого порошка.
Синтез микроструктурированного фосфата титана гидротермальным методом. Раствор комплекса титана с миндальной кислотой (0,69 г, 1,66 ммоль) в 20 мл воды помещали в тефлоно- вый вкладыш, затем добавляли фосфорную кислоту (98 %) в количестве, соответствующем исходному мольному соотношению элементов Ti:P, который варьировался от 1/8 до 1/4. Приготовленные водные растворы затем герметично закрывали в автоклаве из нержавеющей стали с тефлоновым вкладышем и нагревали. Полученные осадки декантировали и промывали дистиллированной водой с последующим центрифугированием. Наконец, осадки сушили в вакууме при 90 °С в течение ночи. В табл. 1 приведены условия получения, состав, размер и шифры образцов, полученных при различных условиях.
Таблица 1
Условия и характеристики образцов TiP
|
№ |
T, °С |
Время, ч |
Начальное соотношение Ti:P |
Выход, мг |
Соотношение элементов Ti:P в осадке (ОЭС-ИСП) |
|
TiP |
120 |
4 |
1/5 |
105 |
0,85 |
|
TiP_MS_I |
180 |
4 |
1/8 |
275 |
0,82 |
|
TiP_MS_II |
140 |
24 |
1/5 |
280 |
0,86 |
|
TiP_R |
120 |
72 |
1/4 |
258 |
0,86 |
Тионилирование фосфата титана. Навеска прокаленного фосфата титана помещалась в колбу с магнитным якорем, после чего добавлялось рассчитанное из необходимой концентрации количество хлороформа и тионила хлористого. После добавления реагентов содержимое перемешивалось под обратным холодильником заданное время. По завершении реакции смесь количественно переносилась в центрифужные пробирки и центрифугировалась (6000 об./мин), после чего промывалась хлороформом и снова центрифугировалась. После завершения обработки образцы сушились при 60 °С под вакуумом в течение 18 часов.
Определение содержания хлоридов
20 мг образца обрабатывали ультразвуком (200 Вт, 40 кГц) в течение 5 мин в 1 мл деионизированной воды, разбавляли деионизированной водой до объема 30 мл и титровали потенциометрически раствором AgNO 3 (0,01 моль/л) с использованием хлоридсеребряного электрода.
Определение максимальной концентрации кислоты (МКК)
20 мг катализатора диспергировали 3 мин в УЗ-ванне в 1 мл ацетонитрила. Доводили аликвоту до 30 мл ацетонитрилом и тировали раствором бутиламина в ацетонитриле используя рН-электрод для неводных сред.
Методика проведения этерификации адипиновой кислоты
Начальные эксперименты по этерификации проводили в следующих условиях: в виалу на 4 мл помещали 146 мг (1 ммоль) адипиновой кислоты, 635 мкл (4 ммоль) октанола и 14,6 мг катализатора (10 масс. % кислоты). Реакционные смеси нагревали до заданной температуры, после чего охлаждали до комнатной температуры и анализировали методом газовой хроматографии с масс-спектрометрическим детектированием. Количественный анализ продукта и исходных компонентов проводился на основе калибровочных кривых, построенных с использованием внутреннего стандарта (метилстеарата). Эксперименты проводились в 2 параллелях.
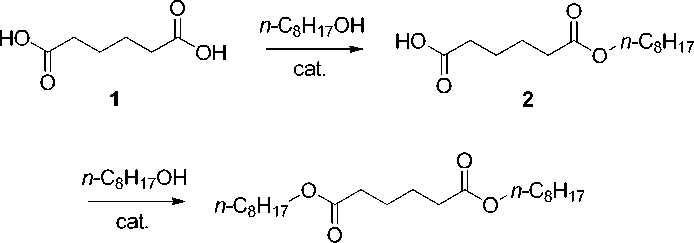
Схема 1. Каталитическая этерификация адипиновой кислоты октанолом
Реакционная смесь была количественно перенесена в мерную пробирку и доведена до 5 мл метанолом. Катализатор отделяли центрифугированием, после чего отбирали аликвоту в 1 мл, которую разбавляли до 30 мл и титровали потенциометрически с помощью раствора КОН (0,1 моль/л) в изопропиловом спирте в присутствии рН-электрода для неводных сред. Степень конверсии адипиновой кислоты рассчитывали по формуле
ACD, % = z n* x 100 %, где 2 – исходное количество карбоксильных групп (ммоль),
n x 103, ммоль = 5 x C(KOH) x f x V (КОН)экв, где 5 – объем пробы (мл), С (KOH) – концентрация титранта (моль/л), V (KOH)экв – объем раствора KOH в точке эквивалентности (мл), f = 0,769 – поправочный коэффициент, определенный при титровании 0,1 моль/л водного раствора гидрофталата калия.
Описание катализаторов
Продукты гидротермального синтеза фосфата титана, как потенциального катализатора реакции этерификации, демонстрируют три типа морфологии в зависимости от продолжительности времени синтеза, температуры и исходного соотношения реагентов: водорастворимого комплекса и фосфорной кислоты. При малом времени выдержки, относительно низком содержании фосфорной кислоты и низкой температуре формируется аморфный осадок (TiP). СЭМ-микрофотография продукта TiP не показала отчетливых структурных особенностей и представляет собой изображение набора бесформенных агрегатов (рис. 1а). Рентгенограмма продукта показывает аморфное гало, без видимых рефлексов. Важно отметить, что при более низких концентрациях фосфорной кислоты (ФК) осадка не образуется.
Микросферы фосфата титана представленные двумя типоразмерами частиц (рис. 1а), которые формируются в широком диапазоне параметров, и при строгом контроле условий, приобретают правильную форму с узким распределением по размерам. Их структура представляет собой сферически упорядоченные агрегаты микрочешуек. Продолжительный синтез (≥ 48 ч) приводит к рекристаллизации микросфер в термодинамически стабильные микростержни TiP_R (рис. 1а). ЭДС-анализ подтверждает равномерное распределение элементов Ti, P и O (рис. 1б). Рентгенофазовый анализ выявил эволюцию состава от аморфного TiP (4 ч) через двухфазную систему Ti(HPO 4 ) 2 ·0,5H 2 O/Ti 6 O 3 (H 2 O) 3 (PO 4 ) 7 ·(H 3 O) 3 ·H 2 O (12 ч) до монокристаллической фазы Ti 6 O 3 (H 2 O) 3 (PO 4 ) 7 ·(H 3 O) 3 ·H 2 O (≥ 48 ч) (рис. 1в). Очевидно, увеличение степени кристалличности образцов по мере увеличения времени гидротермальной обработки.

а)
б)
в)
Рис. 1. SEM-изображения TiP, микросфер TiP_MS_I, TiP_MS_II и микростержней TiP_R (а); элементное картирование микросферических частиц TiP (б);
рентгенофазовый анализ для всех исследованных типов морфологии TiP (в)
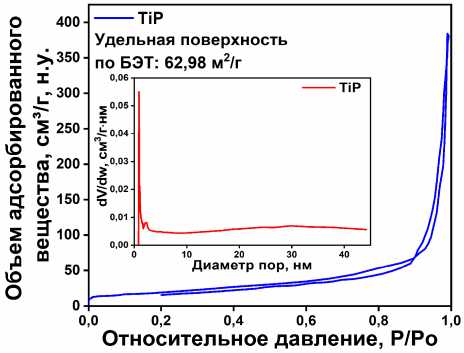
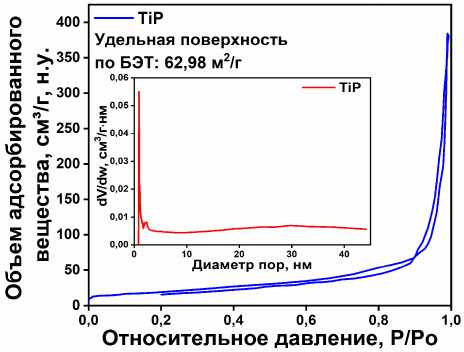
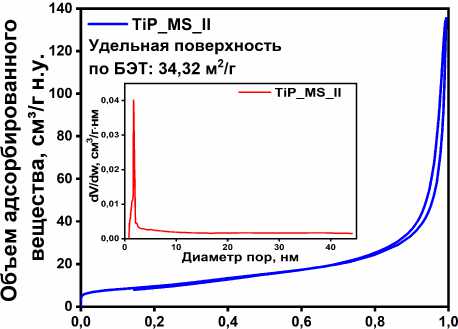
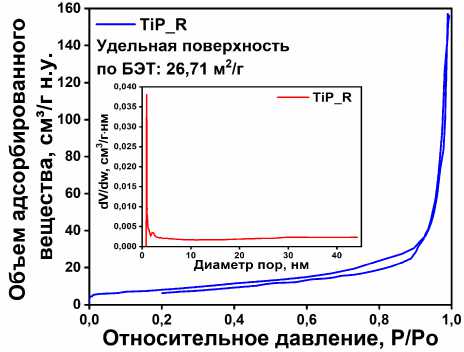
Изотермы адсорбции-десорбции азота образцов фосфата титана (рис. 2 а–г), относятся к I типу по классификации IUPAC. Исследуемые образцы характеризуется развитой микропористой структурой. Значения удельной поверхности (S уд ), рассчитанные методом БЭТ, демонстрируют значительный разброс: S уд = 62,98 м²/г для TiP, для TiP_MS_I S уд = 40,34 м²/г, S уд = 34,32 м²/г для TiP_MS_II и TiP_R с S уд = 26,71 м²/г. Такой широкий диапазон значений S уд , указывает на сложную структурные измерения по мере изменения морфологии. Вместе с тем, нельзя не заметить характерное равномерное уменьшение удельной площади поверхности при переходе от аморфного состояния (TiP) в высококристаллическое (TiP_R). Относительно высокие значения удельной площади поверхности полученных образцов фосфата титана создают предпосылки для формирования на их основе гетерогенных катализаторов.
б)
Относительное давление, Р/Ро
в)
г)
Рис. 2. Кривые изотерм адсорбции-десорбции азота для TiP (а), микросфер TiP_MS_I (б), TiP_MS_II (в) и микростержни TiP_R (г)
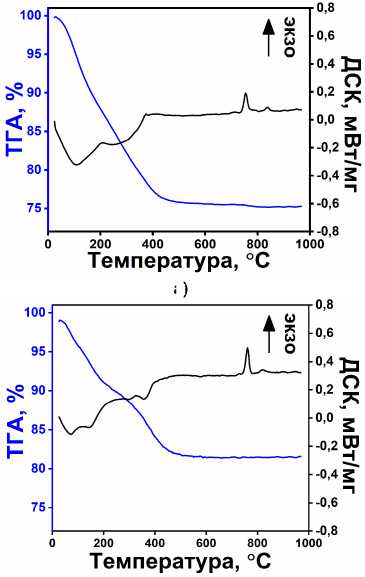
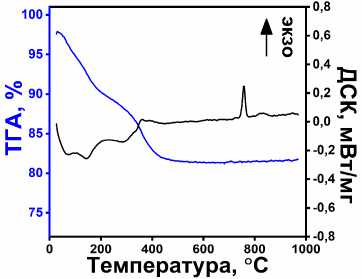
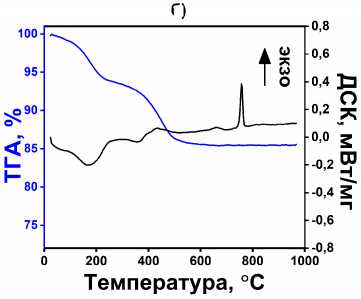
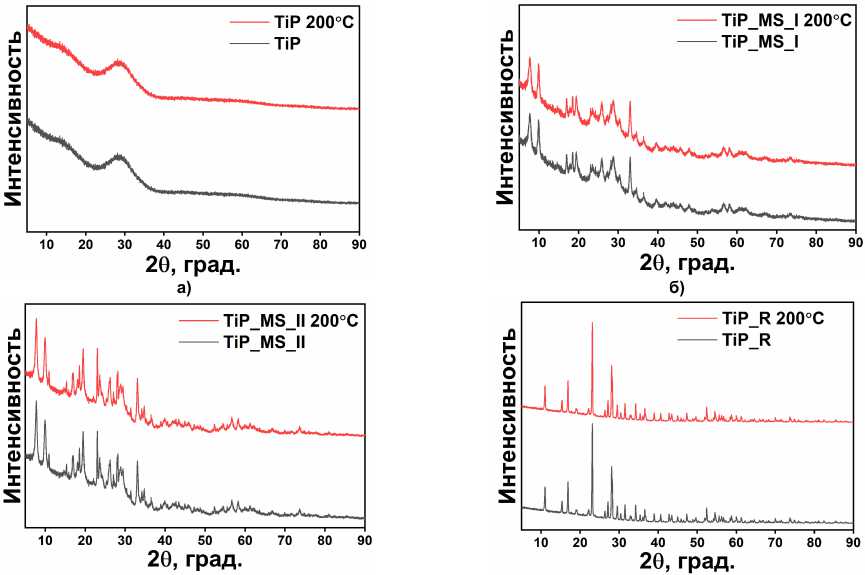
Порошкообразные твердые образцы фосфата титана были проанализированы методом ТГА (рис. 3). Для всех четырех типов образцов характерны следующие термические эффекты. На первом этапе (30–200 °С) высвобождаются молекулы физически и химически адсорбированной воды, при котором потеря массы составляет ≈ 6–10 %. На некоторых термограммах можно дифференцировать эндотермические пики, соответствующие потере обоих типов связанной воды. Стоит заметить, что потери воды обратно-пропорциональны степени кристалличности. Кроме того, данный этап не сопровождается существенными изменениями кристаллической решетки, что подтверждается данными порошковой дифрактометрии, из которых видно, что профиль дифрак-тограмм образцов до и после прокаливания при 200 °С не изменился (рис. 4).
Второй этап прокаливания (200–525 °С) подразумевает последовательное высвобождение молекул воды за счет конденсации гидрофосфатных групп (структурных групп PO3-OH) в фосфаты или конденсация гидроксильных групп соседних атомов титана или титана-фосфора с фор- мированием мостиковых кислородных связей. Потеря массы на данном этапе составляет ≈ 9 % [41–43]. К тому же на всех термограммах явно виден экзотермический пик кристаллизации фосфата титана, в узком диапазоне 760–780 °С, ранее описанный нашей группой [44].
а)
в)
б)
г)
Рис. 3. Термоаналитические кривые ТГА-ДСК для TiP (а), микросфер TiP_MS_I (б), TiP_MS_II (в) и микростержни TiP_R (г)
в)
г)
Рис. 4. Данные порошковой диффрактометрии до и после прокаливания при 200 °С для TiP (а), микросфер TiP_MS_I (б), TiP_MS_II (в) и микростержней TiP_R (г)
Структура фосфата титана представлена разупорядоченными и частично гидратированными тетраэдрическими фосфатными и октаэдрическими титанатными фрагментами в соотношении примерно 7 к 6, согласно данным порошковой дифрактометрии и данным ИСП-ОЭС. Очевидно, что наличие фосфатных групп в структуре фосфата титана создает предпосылки к наличию на поверхности материала гидро- и дигидрофосфатных групп, как потенциальных кислотных центров, что делает фосфат титана перспективным катализатором для этерификации. Опираясь на рост востребованности экологически безопасных пластификаторов, диоктиладипинат был выбран в качестве целевого продукта катализа этерификации.
Для определения каталитических свойств материалов на основе фосфата титана был выбран ряд образцов с различной морфологией. Содержащаяся в образцах вода негативно влияет на равновесие реакции этерификации, что требует предварительного нагревания для её удаления. Было проведено сопоставление температуры предварительной обработки. Температуры были выбраны с учетом данных термоанализа исходя из этапности потерь физисорбирован-ной/хемосорбированной и кристаллогидратной/хемосорбированной воды (см. рис. 3). Первичные эксперименты по этерификации проводились по стандартной методике, приведенной в разделе Методы . Рассматривая полученные данные становится очевидным, что кислотной силы поверхностных гидро- и дигидрофосфатных групп, рассматриваемых в качестве потенциальных кислотных центров, оказывается недостаточно, для полной конверсии адипиновой кислоты в соответствующий эфир (табл. 2). Прокаливание при 500 °С всего ряда фосфатов титана незначительно увеличило выход этерификации. Данный опыт показывает, что Бренстедовская кислотность гидрофосфатных групп не является решающей в катализе процесса, следственно каталитическая активность определяется скорее Льюисовской кислотностью.
Таблица 2
Выход реакции этерификации с использованием в качестве катализатора прокаленных образцов с различной морфологией
|
Образцы |
Температура прокаливания, °С |
|
|
200 |
500 |
|
|
TiP |
31,5 |
29,5 |
|
TiP_MS1 |
29,3 |
30,4 |
|
TiP_MS2 |
20,0 |
32,4 |
|
TiP_R |
21,3 |
26,2 |
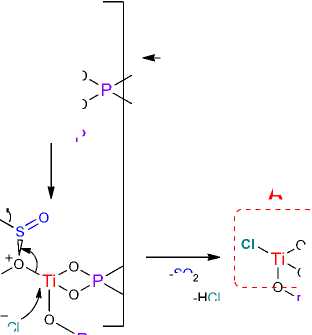
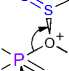
Нами был применен подход активации поверхности с помощью тионила хлористого. Этот реагент давно известен благодаря своим дегидратирующей [38] и хлорирующей способностям [39]. Он также активно используется как реагент превращающий оксидные и окси-гидроксидные соединения металлов в соответствующие хлориды. Мы предполагаем, что обработка хлористым тионилом приводит к замещению экспонируемых титанатными и фосфатными фрагментами гидроксильных групп в соответствующие хлориды через известный механизм замещения SN2 с образованием хлорсульфитных интермедиатов [45] (схема 2). Получаемые таким образом хлорированные фрагменты поверхности могут представлять собой высокореакционные и каталитически активные центры.
Можно предположить, что хлорированный фрагмент тетракоординированного титана A будет обладать выраженной Льюисовской кислотностью. Во-первых, тетракоординированный титан обладает свободной d-орбиталью для взаимодействия с неподеленной парой электронов основания, во-вторых, замещение гидроксильной функции, как сильного основания на хлорид, как более слабое основание существенно усиливает кислотность металла. Мы можем предположить наличие также и дихлор- и трихлор-производных тетракоординированного титана на поверхности, тем более, что аналогичные частицы уже были постулированы при описании гетерогенного катализатора на основе комплекса полистирола и тетрахлорида титана [46]. Гексакоординиро-ванные хлорированные фрагменты титана Льюисовской кислотностью не обладают, поскольку все орбитали титана в них заполнены. Вместе с тем, они могут легко диссоциировать с образованием хлорид аниона и пентакоординированного атома титана – потенциального кислотного центра (схема 2) [47].
Cl
O O
H Ti O
I O
O P
Cl
Cl O
S <
SOCl2 HO O
Ti С '
I O
O
P
Cl
H
A
-SO2
Cl
O X O
P' /Ti / P
O I O
O
OH
OX 1.xO
P< /Ti ^
O I O
O
O
O
P
C
-
OH
O и O OH
P \ " Ti P^
O I " O O
O
SOCl2
O Cl
S
OH 1 V иO Oн
Ti с P H
I OO
O
SOCl2
O
O
Cl
I.' O Cl
Ti P
I ' OO
O
-SO2
-HCl
OH иO
Ti
I O
O
Cl
O
г Cl
H
Cl
Cl O O^/ O
Ti с P Ti с '
I OO I " O O"P O
Cl
O O / Cl
P Ti ' ^P
O I OO
O
Схема 2. Пути хлорирования поверхности фосфата титана тионилом хлористым
Согласно данным табл. 3 выход продукта прокаленных образцов после тионилирования существенно вырос по сравнению с серией не подвергшейся обработке SOCl 2 . Более того, прокаленные при 200 °С образцы фосфата титана оказались более эффективны, чем образцы, прокаленные при 500 °С. Видимо, наличие поверхностных гидроксильных групп увеличивает степень замещения их хлоридами, и формирования, таким образом, Льюисовских кислотных центров.
Таблица 3
Выход реакции этерификации с использованием в качестве катализатора прокаленных образцов с различной морфологией после обработки тионилхлоридом
|
Образцы |
Температура прокаливания, °С |
|
|
200 |
500 |
|
|
TiP |
80,3 |
58,0 |
|
TiP_MS1 |
59,7 |
54,0 |
|
TiP_MS2 |
56,9 |
45,9 |
|
TiP_R |
27,6 |
26,9 |
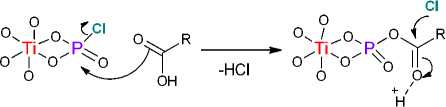
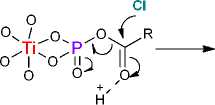
Хлорпроизводные соединения фосфора на поверхности, пример которого приведен на схеме 2 (фрагмент B ), в настоящей работе не представляет интереса в качестве каталитического центра, так как напрямую реагируют с карбоксильной функцией формируя хлорангидрид кислоты по известному механизму. Хлорангидрид адипиновой кислоты может участвовать в последующей реакции этерификации со спиртом, хотя при этом фосфорный фрагмент поверхности остается нефункциональным (схема 3).
о
0Х I ^Ск
О I о о
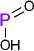
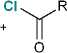
Схема 3. Образование хлорангидрида кислоты из поверхностного оксихлорида фосфора
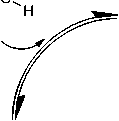
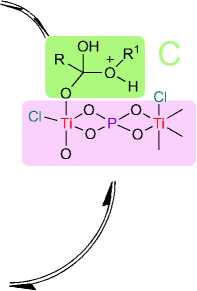
Повышенная каталитическая активность образцов фосфата титана, обработанного тионил-хлоридом, может быть объяснена схемой 4. Здесь атомы хлорированного титана с увеличенной Льюисовской кислотностью координируют карбонильный кислород адипиновой кислоты и, таким образом, повышают электрофильность углерода карбонила, в то время как мостиковые ки- слороды, окружающие титан, образуют стабильную водородную связь со спиртом. Такое пространственное расположение способствует образованию тетракоординированного sp3-гибридизованного промежуточного продукта С и его протонированной формы D, которые легко образуют стабильную эфирную группу целевого сложного эфира.
R
OH
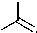
acid
R 1
O alcohol
Cl
OH
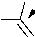
R1
O
H Cl
Cl O / O I
Ti P < Ti
IOO"Г
O
Cl O O I
Ti _ P Ti
TOi O P O Ti
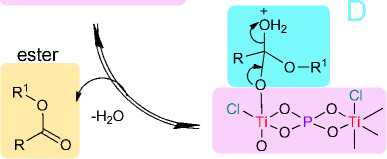
Схема 4. Катализ реакции этерификации хлорированным титаном на поверхности фосфата титана
Таким образом, наивысшую каталитическую способность проявил образец TiP, представляющий собой аморфный смешанный оксид титана-фосфора, прокаленный при 200 °С и обработанный тионилхлоридом. Двукратная разница активности обработанного и необработанного материала стимулировала дальнейшее изучение влияния обработки тионилхлоридом для достижения максимальной активности материала. Было изучено влияние концентрации тионилхлорида, времени и нагревания при обработке на каталитическую активность фосфата титана (рис. 5).
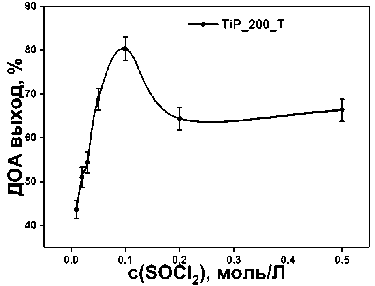
а)
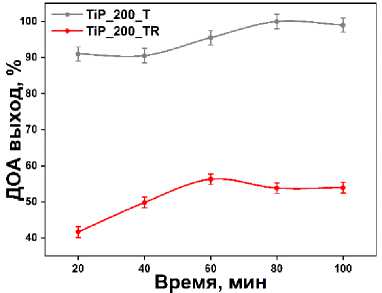
б)
Рис. 5. Графики оптимизации условий обработки тионилхлоридом: а) концентрации тионилхлорида при комнатной температуре, б) времени обработки при комнатной температуре TiP_200_T и нагревании при 60 °С TiP_200_TR
Лучшие результаты этерификации были достигнуты при применении раствора SOCl2 с концентрацией 0,1 моль/л. Как видно из графика, дальнейшее увеличение концентрации тионилхло-рида приводит к снижению выхода реакции. Зависимость от времени обработки показывает оптимальную точку на 60 минутах. Однако, при сопоставлении катализаторов после обработки при комнатной температуре и нагревании, наблюдается существенное снижение эффективности материала, обработанного при нагревании, что, как и снижение эффективности при высоких концентрациях тионилхлорида, может быть объяснено вымыванием титана с поверхности катализа- тора в виде TiCl4. Тем более, что аналогичный пример вымывания был опубликован ранее [48]. Факт снижения активности при вымывании металла потенциально указывает на его ключевую роль в катализе этерификации [49]. Потенциометрическое титрование раствором азотнокислого серебра образца, тионилированного по оптимизированной методике, показало удельное содержание хлоридов в количестве 0,34 ммоль на грамм катализатора.
Оценка влияния обработки SOCl2 потребовала дополнительного исследования путем оценки кислотных свойств оптимального катализатора. Общее количество кислотных центров было оценено методом потенциометрического титрования н -бутиламином в ацетонитриле. Начальный потенциал кривой титрования при потенциометрическом титровании характеризует кислотную силу титруемого материала, а выход кривой титрования на плато указывает на заполнение всех кислотных участков основанием, независимо от их типа и концентрации [50–52]. Оказалось, кислотность материала обработанного тионилхлоридом существенно выше (327,3 мВ), чем у необработанного материала (282,9 мВ).
Вместе с тем, общее количество кислотных центров при обработке тионилхлоридом убывает: 1,41 против 1,83 мг-экв/г. Скорее всего, при обработке материала SOCl 2 , происходит конверсия дигидрофосфатных фрагментов в соответствующие дихлорпроизводные фосфора с соответствующим превращением двух центров Бренстедовской кислотности в один центр Льюисовской кислотности. Кратное превышение кислотных центров над общим содержанием хлоридов на поверхности указывает на преобладание более слабых по силе кислотных центров в виде остаточных гидрофосфатных фрагментов, протонов, связанных с мостиковым кислородом или поверх-ностых пентакоординированных атомов титана [47].
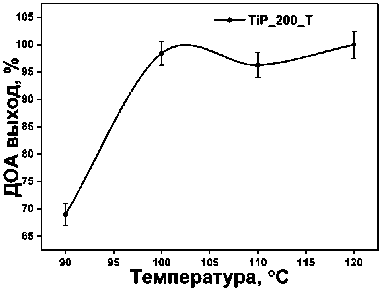
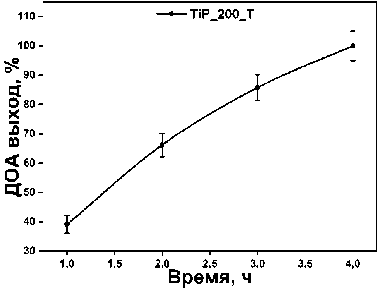
Наилучший образец TiP_200_T был использован для дополнительной оптимизации условий проведения реакции этерификации (рис. 6). Найденные условия включали 15 масс. % катализатора (относительно кислоты), трехкратный избыток октанола, 4 часа проведения реакции при 100 °С.
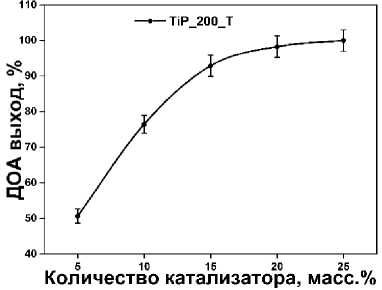
а)
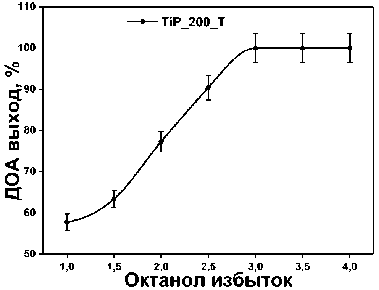
б)
в)
Рис. 6. Графики оптимизации этерификации: а) избыток катализатора (1 ммоль адипиновой кислоты и 4 ммоль октанола, 4 часа); б) избыток октанола (21,9 мг катализатора, 1 ммоль адипиновой кислоты, 4 часа); в) температура проведения реакции (21,9 мг катализатора, 1 ммоль адипиновой кислоты, 6 ммоль октанола, 4 часа);
г) время проведения реакции (21,9 мг катализатора, 1 ммоль адипиновой кислоты, 6 ммоль октанола)
г)
Также был проведен эксперимент по сопоставлению каталитической силы полученного фосфата титана с гетерогенными катализаторами, ранее описанными в литературе [31, 53–57]. Результаты, приведенные на рис. 7 наглядно показывают превосходство TiP_200_Т над большинством систем за исключением катионообменной смолы Dowex. Однако сравнение на более глубоком уровне показывает, что применение катионообменной смолы в синтезе пластификаторов является неудачным решением ввиду низкой термостабильности и высокой стоимости производства в сравнении с фосфатом титана.
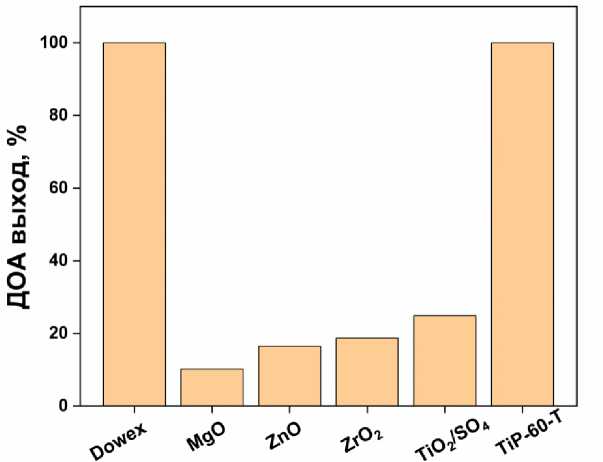
Рис. 7. Сравнение TiP_200_T с различными каталитическими системами в оптимизированных условиях
Далее, для подтверждения эффективности разработанного материала для синтеза различных диэфиров адипиновой кислоты был расширен ряд спиртов. Степень конверсии этерификации оценивали с помощью потенциометрического титрования аликвоты реакционной смеси 0,1 моль/л раствором КОН (табл. 4). Мы можем сделать вывод, что в случае с бутанолом и изобутанолом степень конверсии кабоксильных COOH-групп была достигнута на высоком уровне – до 89 %. Реакция со спиртами с более длинной цепью (гексанол-1 и бутоксиэтанол) приводит к снижению степени конверсии (58 и 53 % соответственно). В случае изооктанола в реакции не образовывался диэфир, согласно данным ГХ-МС. Адипиновая кислота превращалась в моноэфир с конверсией в 31,8 %.
Таблица 4
Конверсия адипиновой кислоты в этерификации с различными спиртами в присутствии катализатора TiP_200_T в оптимизированных условиях
|
Спирты |
V (KOH)экв, мл |
n, ммоль COOH |
Конв. кисл., % |
|
|
1 |
Гексанол-1 |
2,264 |
0,0008 |
58,0 |
|
2 |
Изооктанол |
3,678 |
0,0014 |
31,8 |
|
3 |
Бутоксиэтанол |
2,493 |
0,0009 |
53,8 |
|
4 |
Бутанол-1 |
1,3287 |
0,0005 |
75,4 |
|
5 |
Изо-бутанол |
0,5905 |
0,0002 |
89,0 |
Кинетически затрудненный процесс этерификации адипиновой кислоты октанолом решается в промышленности применением сильных кислот при повышенной температуре, что осложнено как производственными издержками, так и экологическими проблемами, связанными с утилиза- цией кислотных отходов. Поиск гетерогенных катализаторов с выраженными кислотными свойствами рассматривается как перспективное решение. В данной работе были опробованы различные типы фосфата титана, полученные гидротермальной обработкой водорастворимого комплекса титана в присутствии фосфорной кислоты. Полученные образцы при сходстве химического состава отличались морфологическими и кристаллохимическими свойствами, которые оказали существенное влияние на катализ этерификации. Неожиданно аморфный образец оказался наилучшим как после термообработки, так и после обработки тионилом хлористым. Вероятно, это связано, с существенно более высокой, по сравнению с морфологически-структурированными образцами, удельной поверхностью. Сравнение температур термообработки показало, что наличие гидроксильных групп на поверхности фосфата титана необходимо для катализируемой Брен-стедовскими кислотными центрами этерификации. Также гидроксильные группы играют важную роль при тионилировании поверхности фосфата титана, так как они увеличивают вероятность замещения на хлорид-анионы и, как следствие, формирование потенциальных Льюисовских центров кислотности. Оптимизация условий тионилирования фосфата титана и ступенчатая оптимизация условий этерификации позволили получить каталитический материал, по свойствам, не уступающим ранее опубликованным кислотным катализаторам. Оптимизированная методика этерификации адипиновой кислоты с использованием разработанного катализатора была убедительно расширена на ряд иных спиртов.


