Гипотракционные технологии в резекционной хирургии желудка
Автор: Власов А.П., Власов П.А., Рубцов О.Ю.
Журнал: Хирургическая практика @spractice
Рубрика: Оригинальные исследования
Статья в выпуске: 4, 2017 года.
Бесплатный доступ
В эксперименте на 36 собаках и в клинике у 56 больных язвенной болезнью желудка и двенадцатиперстной кишки при резекции желудка применена гипотракционная технология (патент), заключающаяся в наложении дополнительных слизисто-подслизистых или серозно-мышечных швов в 1-2 см от линии анастомоза, благодаря которым происходит сближение анастомозированных отделов, что снижает нагрузку на основные швы соустья. В экспери- менте доказана эффективность разработанной технологии в условиях существенного натяжения (2,5-3,6 Н - 245-350 г) культи желудка и культи двенадца- типерстной кишки. Доказано, что уменьшение напряжения в основных швах по линии анастомоза способствует меньшим расстройствам трофики тканей регенерирующих структур, что установлено по повышению в них редокс-потенциала, снижению интенсивности липопероксидации и фосфолипазной ак- тивности. В клинике применение гипотракционных и эвертированного швов при резекции желудка позволили до минимума свести послеоперационные осложнения. Несостоятельности швов гастродуоденального анастомоза не было. Отмечено существенное уменьшение анастомозита до 1,8%, послеопера- ционного панкреатита - до 3,6%.
Резекция желудка, гипотракционные швы, регенерация, послеоперационные осложнения
Короткий адрес: https://sciup.org/142221827
IDR: 142221827 | УДК: 616.34
Hypotensive technology in the resection surgery of the stomach
In the experiment on 36 dogs and in the clinic, 56 patients with gastric ulcer and duodenal ulcer stomach resection hypotrachyna applied technology (patent pending), consisting in the imposition of additional muco-submucosal or serous-muscular sutures 1-2 cm from the anastomosis, which occurs due to the convergence anastomosing departments, which reduces the load on the main seams of the anastomosis. In the experiment the efficacy of the developed technologies under conditions of significant tension (2,5-3,6 N - 245-350 g) of the stump of the stomach and duodenal stump. It is proved that the reduction of tension in the major joints along the line of the anastomosis contributes to a smaller disorders of the trophic tissue regenerating structures that are installed for increasing the redox potential, reduction in the intensity of lipid peroxidation and leading to phospholipase activity. In the clinic application hypotensive and overthrowing sutures in resection of the stomach allowed us to minimize postoperative complications. Failure of sutures gastroduodenal anastomosis was not. A marked decrease in the maintenance of anastomositis to 1.8%, postoperative pancreatitis to 3.6%.
Текст научной статьи Гипотракционные технологии в резекционной хирургии желудка
Материал и методы
В основу работы положены результаты экспериментальных исследований и клинических наблюдений.
Экспериментальный раздел
Применялись следующие методики: макроскопия на аутопсии, световая микроскопия при окраске препаратов гематокси-лин-эозином, определение окислительно-восстановительного потенциала (редокс-потенциала) для изучения электрогенеза тканей, определение в тканях соустья содержания ТБК-активных продуктов и активности фосфолипазы А2, определение физической герметичности швов (пневмопрессия) и индекса стенозирования (степень сужения) анастомоза.
Клинический раздел
Результаты и их обсуждение
При макро- и микроскопической оценке состояния тканей по линии соустья выявлено, что заживление анастомоза происходило без осложнений по типу первичного натяжения с минимальными явлениями анастомозита.
Отметим, что ранний послеоперационный период у животных протекал тяжело. В трех случаях зарегистрирована несостоятельность швов. В остальных наблюдениях процесс репарации сопровождался выраженными воспалительными явлениями в тканях соустья (анастомозит), что существенно снижало его прочность. Сила биологической консолидации тканей в контрольных точках периода наблюдения была существенно (на 26,3-41,2%) ниже, чем в контроле. Наибольшие патоморфологические явления отмечены в области шовного материала, где были регистрированы язвенные процессы, с наложениями гноя и фибрина, что приводило к сужению просвета (существенный (на 42,3%) рост индекс стенозирования) в области соустья.
В третьей группе объем операции и технические приемы при ее выполнении были аналогичными второй группы. Однако после формирования гастродуоденального соустья с целью уменьшения напряжения в основных швах нами применен способ уменьшения натяжения швов анастомоза (патент № 2049429 от 10.12.1995), при котором на расстоянии более 1,0 см от края анастомозируемых отделов накладывались дополнительные узловые гипотракционные слизисто-подслизистые или серозно-мышечные швы, равномерно распределяя их по окружности, с помощью которых подтягивали и фиксировали отрезки друг к другу на расстоянии, позволяющем предотвратить натяжение основных швов анастомоза. Количество швов определяется диаметром анастомозируемых отделов, степенью натяжения при их сближении друг к другу. В наших опытах их было 4.
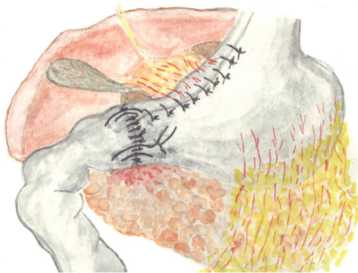
Рис. 1. Внешний вид гастродуоденального анастомоза с гипотракционными швами
В этой группе животных послеоперационный период протекал без осложнений и во многом соответствовал таковому контрольной (первой) группы. Отличия заключались лишь в том, что через 1-3 суток после операции происходило прорезывание дополнительных швов с одного из анастомозированных отделов с формированием точечного дефекта в области серозно-мышечной оболочки. Однако этот процесс существенно не влиял на заживление анастомоза, который в целом был аналогичен первой группы и сопровождался минимальными воспалительными явлениями по линии основных швов.
Таким образом, при помощи дополнительных гипотракци-онных швов достигается возможность приблизить и удержать анастомозируемые отделы при их натяжении. Удерживающую способность швы сохраняют 1-3 суток, затем прорезываются. Этого времени вполне достаточно для адаптация анастомозированных отделов к изменившимся условиям и «первичного склеивания» тканей по линии анастомоза, что в целом и обеспечивает надежность основных швов и благоприятное заживление анастомоза.
Нами установлено, что в основе патогенеза несостоятельности швов гастродуоденального соустья при натяжении анастомозируемых отделов лежат существенные нарушения трофики тканей, которые регистрируются уже незамедлительно после создания соустья. Так, редокс-потенциал в тканях гастродуоденального соустья после его формирования в контрольной группе падал до -42,3 1,3 мВ, тогда как при натяжении анастомозированных отделов (вторая группа) снижался на 34,0% до -56,7 1,5 мВ (р<0,05). Такого рода динамика отмечена и в раннем послеоперационном периоде (табл. 1).
Следует отметить, что вне зависимости от исследуемой группы в тканях гастродуоденального соустья в раннем послеоперационном периоде сохраняются выраженные нарушения трофики. Так, в контрольной группе редокс-потенциал через 1 и 3 суток после операции падал на 62,3 и 32,9% (р<0,05) соот- ветственно. При этом в тканях регистрировалась интенсификация перекисного окисления липидов, о чем свидетельствовал рост уровня ТБК-активных продуктов на 32,1 и 36,6% (р<0,05) соответственно. Отметим факт повышения и фосфолипазной активности на 150,9 и 135,3% (р<0,05) соответственно (табл. 1).
Таким образом, даже в неосложненных ситуациях в тканевых структурах кишечного анастомоза в самые ранние сроки создаются условия для угнетения репаративного процесса. Об этом свидетельствуют все регистрированные показатели. Отметим особую патофизиологическую значимость интенсификации перекисного окисления липидов и повышения фосфолипазной активности в силу того, что они обладают крайне нежелательным мембранодеструктивным действием, существенно снижая репаративный потенциал регенерирующих структур.
Подчеркнем, что при натяжении анастомозированных отделов регистрированные биохимические и биофизические показатели состояния тканевых структур гастродуоденального анастомоза претерпевали более значимые изменения. Так, редокс-потенциал через 1 и 3 суток после операции падал на 93,2 и 101,4% (р<0,05), уровень ТБК-активных продуктов повышался на 69,9 и 80,4% (р<0,05), фосфолипазная активность – на 272,4 и 330,2% соответственно. При этом их уровень был достоверно изменен по отношению к контролю в 1 и 3 сутки на 19,0 и 51,6%, 28,6 и 32,0%, 48,5 и 82,8% соответственно. Отметим и то, что при напряжении в швах в динамике отмечено ухудшение трофики тканей, что явилось важнейшим обстоятельством в возникновении несостоятельности швов анастомоза.
Таблица 1
Некоторые биохимические и биофизические показатели состояния тканевых структур гастродуоденального анастомоза (M±m)
|
Показатель |
Норма |
Группа |
Этапы послеоперационного наблюдения, сутки |
||
|
1 |
3 |
5 |
|||
|
Электрогенез тканей, мВ |
–35,3±1,1 |
I |
–57,3±1,2* |
–46,9±1,14* |
–36,7± 1,3 |
|
II |
–68,2±1,3* |
–71,1±1,4* |
– |
||
|
III |
–61,6±1,3*^ |
–48,7±1,5*^ |
–37,3±1,4 |
||
|
Содержание ТБК-активных продуктов, нмоль/г белка |
3,52±0,21 |
I |
4,65±0,23* |
4,81±0,22* |
3,77±0,27 |
|
II |
5,98±0,31* |
6,35±0,44* |
– |
||
|
III |
5,23±0,25*^ |
5,01±0,26*^ |
3,81±0,21 |
||
|
Активность фосфолипазы А2, мкмоль/с/г белка (*10-2) |
1,16±0,07 |
I |
2,91±0,12* |
2,73±0,15* |
1,28±0,14 |
|
II |
4,32±0,22* |
4,99±0,31* |
– |
||
|
III |
3,88±0,21*^ |
3,23± 0,19*^ |
1,45±0,16 |
||
Примечание: I – первая (контрольная) группа, II – вторая (опытная) группа; III – третья (опытная) группа; * – достоверность по отношению к норме при р<0,05; жирный шрифт – достоверность по отношению к контролю при р<0,05; ^ – достоверность по отношению к второй группе при р<0,05
рой группе, и во многом приближалось к контрольному уровню. Так, редокс-потенциал через 1 и 3 суток после операции был снижен по сравнению с нормой на 74,5 и 31,6% (р<0,05), уровень ТБК-активных продуктов повышался на 48,6 и 42,3% (р<0,05), фосфолипазная активность – на 234,5 и 178,4% (р<0,05) соответственно. При этом их уровень был достоверно изменен по отношению к контролю только в первые сутки на 7,5, 12,5 и 33,3% соответственно (активность фосфолипазы А2 была выше контроля и на 3-и сутки на 18,3% (р<0,05)). Отметим, что по сравнению с результатами второй группы зареги- стрированы достоверные положительные сдвиги исследованных показателей. Так, редокс-потенциал через 1 и 3 суток после операции был выше на 9,7 и 14,7% (р<0,05), содержание ТБК-активных продуктов ниже12,6 и 21,1% (р<0,05), фосфолипазная активность падала на 10,2 и 35,3% (р<0,05) соответственно (табл. 1).
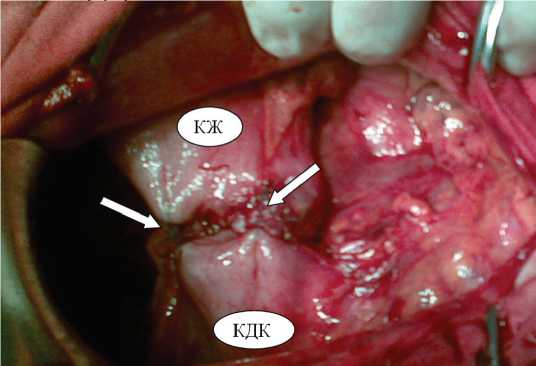
Рис. 2. Интраоперационное фото.
Таблица 2
|
Осложнения |
Способ формирования гастродуоденального анастомоза |
|||
|
Классический двухрядный Ламбера-Альберта (n=52) |
Однорядный эвертированный с гипотракционными швами (n=56) |
|||
|
Анастомозит |
9 |
17,3% |
1 |
1,8% |
|
Панкреатит |
6 |
11,5% |
2 |
3,6% |
|
Несостотель-ность швов |
4 |
7,7% |
– |
– |
|
Абсцесс брюшной полости |
1 |
1,9% |
– |
– |
|
Парез кишечника |
8 |
15,4% |
2 |
3,6% |
|
Нагноение раны |
3 |
5,8% |
2 |
3,6% |
|
Всего: |
31 |
59,6% |
7 |
12,5% |
Наиболее значимые результаты такого рода операций заключаются в развитии тяжелых осложнений, и в первую очередь, возникновения несостоятельности швов гастродуоденального анастомоза. При применении разработанной тех- нологии такого рода осложнений не было, тогда как при классическом двухрядном шве оно возникло у 4 больных (7,7%). Этим пациентам выполнены повторные операции, в том числе реконструктивные, после которых на фоне прогрессирующего перитонита 2 (3,9%) больных погибли.
При использовании разработанных технологий отмечено существенное уменьшение и других осложнений, в частности анастомозита (в первой группе 1,8%, во второй – 17,3%), послеоперационного панкреатита (в первой группе 3,6%, во второй – 11,5%), что, безусловно, связано с особенностью разработанных операций, в частности с щадящим отношением к анастомозируемым отделам и минимальной травматизацией поджелудочной железы при мобилизации двенадцатиперстной кишки.
Эндоскопический контроль в раннем послеоперационном периоде за течением репаративного процесса гастродуоденального анастомоза, формированного по разработанным технологиям, показал, что по линии швов отмечается быстрая регрессия воспалительного процесса и ускоренная эпителизация раневого дефекта слизистой оболочки, что вы-ступали профилактическими факторами возникновения анастомозита.
Список литературы Гипотракционные технологии в резекционной хирургии желудка
- Абдуллажанов Б.Р., Абдирайимов Б.А., Бозоров Н.Э., Ниша-нов М.Ф. Первичная резекция желудка при перфоративных язвах двенадцатиперстной кишки//Гастроэнтерология Санкт-Петербурга. 2011. № 2-3. С. 1-2
- Брехов Е.И., Мизин С.П., Репин И.Г., Шипова А.А. Обоснование способа восстановления непрерывности желудочно-кишечного тракта после резекции желудка//Хирургия. Журнал им. Н.И. Пирогова. 2013. № 6. С. 8-13
- Власов А.П., Кукош М.В., Сараев В.В., Степанов Ю.П. Резекционная хирургия желудка. Н. Новгород: Изд-во НГМА, 2005. 360 с
- Волостников Е.В., Линченко В.И., Шопен Г.Н. Ишемический некроз культи желудка после субтотальной дистальной резекции желудка Хирургия. Журнал им. Н.И. Пирогова. 2013. № 11. С. 61-62
- Зайцев О.В., Тарасенко С.В., Натальский А.А., Морозов К.С. Технические аспекты выполнения резекции желудка в условиях труд-ной дуоденальной язвы//Тихоокеанский медицинский журнал. 2011. № 3. С. 75-79
- Куликов Е.П., Мерцалов С.А. Применение резекции желудка с сохранением привратника у больных раком желудка//Онкология. Журнал им. П.А. Герцена. 2013. Т. 1. № 6. С. 18-21
- Лубянский В.Г., Насонов С.В. Острый панкреатит после резекции желудка при низкорасположенных дуоденальных язвах//Хирургия. Журнал им. Н.И. Пирогова. 2001. № 3. С. 8-11
- Сажин В.П., Наумов И.А., Климов Д.Е., Нуждихин А.В. Лапароскопическая резекция желудка по Бильрот-1//Хирургия. Журнал им. Н.И. Пирогова. 2005. № 1. С. 21-24
- Тарасенко С.В. Зайцев О.В., Копейкин А.А., Карюхин И.В. Способ оценки результатов оперативного лечения заболеваний желудка и двенадцатиперстной кишки.//Вестник новых медицинских технологий. -2009. -Т. XVI. -№ 2. -С. 169171
- Федосеев А.В., Лузгин Д.А. Качество жизни больных с осложненным течением язвенной болезни желудка и двенадцатиперстной кишки после резекции желудка. Паллиативная медицина и реабилитация. 2005. № 2. С. 28
- Шестопалов С.С., Совцов С.А., Михайлова С.А. Использование электростимуляции в профилактике моторно-эвакуаторных нарушений после гастрэктомии и субтотальной резекции желудка//Новые технологии в онкологической практике. Барнаул, 2005. С. 191-192
- Skarstein A. Hoisaeter P.A. Perforated peptic ulcer: a comparison of long term results following partial gastric resection or simple closure//British Journal of Surgery. -2005. -Т. 63. -№ 9 -С. 700-703


