Гистологические изменения в печени крыс при экспериментальном отравлении препаратами на основе имидокарба и диминазина
Автор: Бойко Т.В., Гонохова М.Н., Кошкарев М.В., Веретенникова В.С., Кузьмин С.С.
Журнал: Вестник Омского государственного аграрного университета @vestnik-omgau
Рубрика: Ветеринария и зоотехния
Статья в выпуске: 1 (33), 2019 года.
Бесплатный доступ
Представлены результаты сравнительной оценки гистологических изменений в печени крыс при введении терапевтических и токсических доз пироплазмоцидных препаратов производных имидазола - «Бабезан» (4%-ный раствор для инъекций) и «Пиро-Стоп», а также производных диминазина - «Неозидин М». Препараты животным вводили двукратно согласно инструкции по применению. Взятие образцов печени для гистологического исследования осуществляли через 3 и 10 сут. Через 3 сут после введения препаратов в терапевтической дозе наибольшие изменения в печени регистрировали при введении препарата «Пиро-Стоп», которые характеризовались зернистой дистрофией гепатоцитов, полнокровием центральных вен и расширением синусоидных капилляров, участками некроза гепатоцитов, пролиферацией соединительной ткани вокруг крупных сосудов. Через 10 сут изменения в печени сохранялись. У животных, получавших токсическую дозу лекарственных препаратов, в оба срока наблюдений отмечали полнокровие центральных вен и сосудов триад, морфологические признаки гидропической дистрофии гепатоцитов, лимфоплазмоцитарные инфильтраты. После введения препаратов «Неозидин» и «Пиро-Стоп» на фоне вышеперечисленных изменений в органах регистрировали участки некроза и разрастание рыхлой соединительной ткани. Проведенные исследования указывают на гепатотропный характер действия препаратов на основе имидокарба и диминазина, что необходимо учитывать в комплексном лечении бабезиозов у домашних животных.
Экспериментальное исследование, печень, морфология, противопаразитарные средства, имидокарб, диминазин, отравление
Короткий адрес: https://sciup.org/142220537
IDR: 142220537 | УДК: 619:615.9
Histological changes in rat liver at experimental poisoning with drugs based on imidocarb and diminazine
The article presents the results of a comparative evaluation of histological changes in the liver of rats with the administration of therapeutic and toxic doses of pyroplasmicidal preparations of imidazole derivatives - Babesan 4% injection and Pyro-Stop, as well as diminazene derivatives - Neozidin M. Preparations for animals were administered twice according to the instructions for use. Liver samples for histological examination were taken after 3 and 10 days. Three days after the administration of the drugs at the therapeutic dose, the greatest changes in the liver were recorded with the administration of Pyro-Stop, characterized by granular dystrophy of hepatocytes, central vascular congestion and dilated sinusoidal capillaries, hepatocyte necrosis, proliferation of connective tissue around large vessels. After 10 days, changes in the liver persisted. In animals who received a toxic dose of drugs, in both periods of observation, the congestion of central veins and vessels of triads as well as the morphological signs of hydropic dystrophy of hepatocytes, and lymphoplasmocytic infiltrates were noted...
Текст научной статьи Гистологические изменения в печени крыс при экспериментальном отравлении препаратами на основе имидокарба и диминазина
Проблема заболеваемости животных бабезиозом стоит остро в разных странах мира [1]. Являясь тяжело протекающим, с полиморфизмом клинических проявлений, трансмиссивным заболеванием, бабезиоз представляет серьезную опасность для здоровья животных в связи с развитием тяжелой анемии и тромбоцитопении с летальным исходом [2]. Для решения этой проблемы фармацевтическими компаниями разработаны и зарегистрированы химиотерапевтические препараты, обладающие специфическим действием на возбудителей болезни из семейства Babesiidae . Ассортимент пироплаз-моцидных средств представлен двумя действующими веществами – имидокарба дипропионатом («Пиро-стоп®», «Фортикарб®» и др.) и диминазина диацетуратом («Неози-дин® М», «Диминазен-70» и др.). В основе механизма действия пироплазмоцидных средств лежит нарушение энергетических процессов кровепаразитов, что приводит к их
гибели [3]. Имидокарб блокирует поступление инозитола – витаминоподобного вещества, что приводит к нарушению образования и использования паразитами полиаминов, необходимых для их роста, развития и размножения. Механизм действия диминазина основан на ингибировании у кровепаразита процессов аэробного гликолиза и синтеза ДНК, разрушении их клеточной структуры и гибели [4]. Лекарственные препараты на основе имидокарба и диминазина имеют разные фармакокинетические характеристики. Так, после парентерального введения терапевтическая концентрация диминазина в крови достигается через 3–5 ч и удерживается в течение суток. Терапевтическая концентрация имидокарба дипропионата в крови после парентерального введения препарата достигается только через 18–24 ч и удерживается на пироплазмостатическом уровне в течение 4–6 нед. Накапливаются имидокарб и диминазин преимущественно в почках и печени, а выводятся из организма преимущественно с мочой. У лактирующих животных возможно выведение с молоком [5].
Сравнительной оценке терапевтической эффективности препаратов с разными действующими веществами при бабезиозе животных посвящены работы многих ученых [6]. В базе данных научной электронной библиотеки Elibrari.ru зарегистрировано 62 источника по этой проблеме [7]. Следует отметить, что существуют разнообразные мнения о степени эффективности и безопасности при назначении пироплазмоцидных средств животным [8]. Согласно инструкции по применению, лекарственные препараты «Неозидин М» и «Пиро-стоп» относятся к умеренно опасным веществам (3-й класс опасности по ГОСТ 12.1.007–76) и в рекомендуемых дозах не оказывают местнораздражающего, эмбриотоксического, тератогенного и мутагенного действий [9]. Однако в литературе описаны серьезные нежелательные реакции у животных при применении препаратов на основе диминазина, которые проявлялись рвотой, отеками, потерей зрения, судорогами, гиперкинезией и атаксией, вплоть до летальных случаев. Применение препаратов на основе имидакарба не вызывало подобных явлений [5].
Безусловно, проявление нежелательных эффектов пироплазмоцидных средств обусловлено не только химической структурой самого препарата, но и физиологическим состоянием животного, поступившего в клинику. Именно поэтому сведения о характере влияния лекарственных веществ на организм животных, полученные в условиях эксперимента, позволят оценить степень повреждающего действия на органы и ткани, что необходимо учитывать при выборе лекарственного средства для терапии бабезиоза у животных с разной степенью тяжести течения заболевания и своевременного назначения корректирующей терапии данных состояний. При анализе литературы сведения о влиянии имидокарба дипропионата и диминазина диацетурата на ткани печени не были отмечены.
Цель исследования – изучение гистологических изменений в печени при экспериментальном введении препаратов на основе имидокарба и диминазина в токсической и терапевтической дозах.
Материалы и методы
В эксперименте использовали белых беспородных крыс самцов, подобранных по принципу аналогов со средней массой тела 300,0 г. Содержание, уход и кормление экспериментальных животных осуществляли согласно ГОСТ 33215–2014 «Руководство по содержанию и уходу за лабораторными животными» [10]. Для исследования были отобраны препараты – производные имидазола – «Бабезан» (4%-ный раствор для инъекций) (АВЗ, Московская область), «Пиро-Стоп» (ООО НПО «АПИ-САН», Московская область), а также на основе диминазина – «Неозидин® М» (ООО «NITA-FARM», г. Саратов). Для оценки влияния препаратов на печень животных испытывали две дозы – терапевтическую и токсическую. Крысам контрольной группы (n = 6) двукратно, с интервалом 24 часа, подкожно вводили 0,9%-ный раствор натрия хлорида в дозе 0,5 мл. Опытным группам (n = 12) лекарственные препараты вводили внутримышечно в терапевтической дозе согласно инструкции по применению и двукратно превышающие терапевтические дозы на фоне обычного пищевого режима двукратно с интервалом 24 часа до кормления. Дозы препарата «Бабезан» (4%) составили 4 и 8 мг/кг соответственно, препарата «Неозидин-М» - 2,5 и 5 мг/кг, препарата «Пиро-стоп» - 6 и 12 мг/кг. В течение экспериментального периода осуществляли ежедневное наблюдение за крысами, а именно: оценивали активность животных, состояние шерстного покрова, по-едаемость корма и потребление воды, степень сформированности фекальных болюсов. По окончании исследований выведение животных из эксперимента осуществляли путем обескровливания на фоне инъекционного наркоза препаратом «Золетил». Сразу после наступления биологической смерти проводили патологоанатомическое вскрытие. Для гистологического исследования были отобраны образцы печени, которые фиксировали в 4%-ном нейтральном растворе формальдегида. Для приготовления микропрепаратов использовали стандартные гистологические методики. Полученные препараты окрашивали гематоксилином и эозином. Микрофотосъемку гистологических препаратов проводили на микроскопе «Альтами БИО 1» с использованием цифровой окулярной USB-камеры USMOSO3100KPA. Результаты, полученные при проведении гистологического исследования препаратов печени, сравнивали с результатами, полученными от животных контрольной группы. Для проведения статистического анализа использовали критерий Стьюдента.
Результаты исследований
При гистологическом исследовании ткани печени у крыс контрольной группы отмечали дольчатое строение, синусоидные капилляры печени были обычного размера, выстланы эндотелиальными клетками. В центре долек визуализируются центральные вены, часть которых была заполнена эритроцитами. Границы между дольками прослеживаются нечетко вследствие слабо развитой соединительной ткани. Большинство гепатоцитов одноядерные, редко встречались двуядерные клетки. Ядерный хроматин и цитоплазма гепатоцитов однородно окрашены. Между дольками располагались типичного строения триады и собирательные вены.
На фоне введения терапевтических доз препаратов через 3 и 10 сут после инъекции регистрировали однотипные изменения разной степени выраженности. Так, на фоне введения «Неозидина » отмечали сохранение нормального строения печени у всех животных. Большинство сосудов триад были запустевшие, синусоидные капилляры не расширены. При визуализации препаратов обращали внимание на увеличение числа макрофагов в ткани печени (рис. 1). Иную картину отмечали на фоне введения терапевтических доз «Пиро-стоп » и «Бабезана ». Признаки зернистой дистрофии гепатоцитов и скопления мононуклеаров вокруг крупных сосудов и в ткани печени наблюдали в обеих экспериментальных группах (рис. 2, 3). Помимо вышеперечисленных признаков после введения « Пиро-стоп » через 3 сут на фоне дистрофических процессов отмечали ограниченные участки некроза паренхимы, в этих местах находили большое число двуядерных гепатоцитов, вокруг крупных сосудов регистрировали участки с разрастанием рыхлой соединительной ткани (рис. 4).
Гистологическая картина ткани печени крыс экспериментальных групп, получавших препараты в токсических дозах (двукратная терапевтическая доза), через 3 сут: на фоне введения «Неозидина» - сохранением долькового строения печени. Цитоплазма большинства гепатоцитов была монохромна, в некоторых зонах отмечали наличие зерен хроматина, что указывает на развитие зернистой дистрофии. Имели место участки некроза гепатоцитов, сопровождающиеся дископлектацией печеночных балок, на месте отдельных полностью разрушенных клеток обнаруживали мелкие полости без содержимого (рис. 5), вокруг которых регистрировали двуядерные клетки. Вокруг сосудов регистрировали скопление мононуклеаров (рис. 6). Внутридольковые синусоидные капилляры были обычных размеров. После введения «Пиро-стоп» и «Бабезана» в том же режиме отмечали признаки зернистой дистрофии печени, расширение синусоидных капилляров, дольчатое строение органа было сохранено (рис. 7, 8). При введении «Пиростоп» и «Бабезана» наблюдали единичные участки скопления мононуклеаров в паренхиме органа (рис. 9, 10). Через 10 сут после введения испытуемых препаратов в токсических дозах у всех экспериментальных животных наблюдали признаки гидропической дистрофии гепатоцитов, степень выраженности которой была выше на фоне введения «Пиро-стоп», клетки печени практически не имели цитоплазмы (рис. 9). На фоне дистрофических процессов отмечали ограниченные участки некроза паренхимы после введения «Неозидина», рядом с погибшими клетками регистрировали большое число двуядерных клеток. У всех животных отмечали разную степень полнокровия сосудов и появление очагов скопления мононуклеаров, как в паренхиме печени, так и вокруг крупных сосудов.
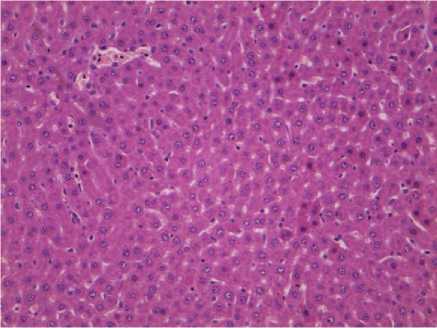
Рис. 1. Паренхима печени крыс после двукратного введения « Неозидина » в дозе 2,5 мг/кг через 3 сут. Окраска гематоксилином и эозином. Ув.×300
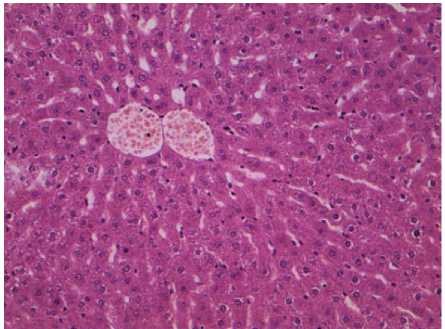
Рис. 2. Паренхима печени крыс после двукратного введения « Бабезана » в дозе 4 мг/кг через 3 сут. Зерна хроматина в цитоплазме гепатоцитов.
Окраска гематоксилином и эозином. Ув.×300
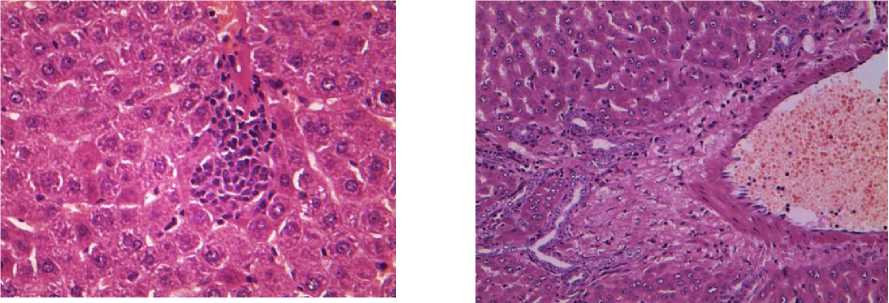
Рис. 3. Зернистая дистрофия гепатоцитов, периваскулярное скопление мононуклеаров, гиперемия вены триады у крыс после двукратного введения « Пиро-стоп » в дозе 6 мг/кг через 3 сут. Окраска гематоксилином и эозином. Ув.×600
Рис. 4. Волокна соединительной ткани вокруг крупных сосудов в печени крыс после двукратного введения « Пиро-стоп » в дозе 6 мг/кг через 3 сут.
Окраска гематоксилином и эозином. Ув.×300
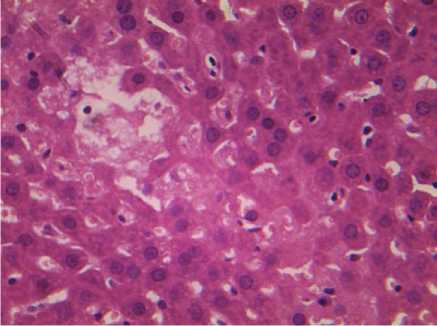
Рис. 5. Участок некроза гепатоцитов и двуядерные гепатоциты после двукратного введения « Неозидина » в дозе 5 мг/кг через 3 сут. Окраска гематоксилином и эозином. Ув.×600
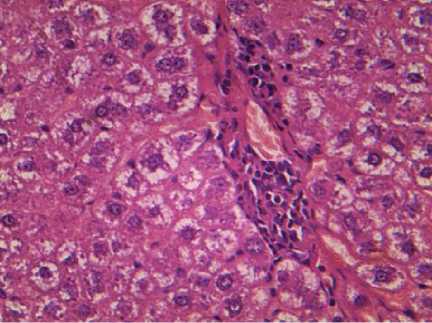
Рис. 6. Гидропическая дистрофия гепатоцитов, периваскулярное скопление мононуклеаров после двукратного введения « Неозидина » в дозе 5 мг/кг через 10 сут. Окраска гематоксилином и эозином.
Ув.×600
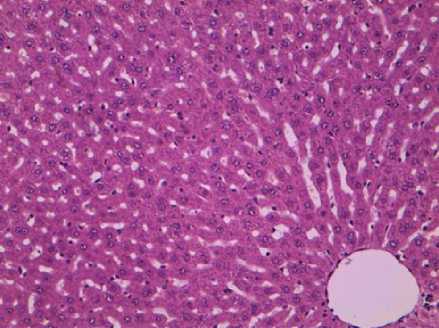
Рис. 7. Расширение синусоидных капилляров в ткани печени крыс после двукратного введения « Пиро-стоп » в дозе 12 мг/кг через 3 сут. Окраска гематоксилином и эозином. Ув.×300
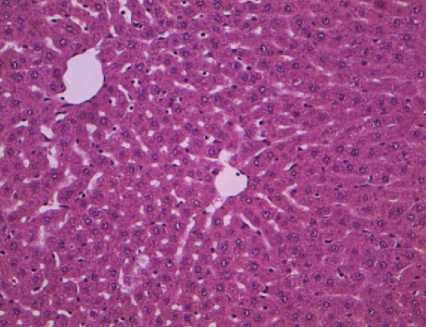
Рис. 8. Паренхима печени крыс после двукратного введения « Бабезана » в дозе 8 мг/кг через 3 сут. Расширение синусоидных капилляров. Окраска гематоксилином и эозином. Ув.×300
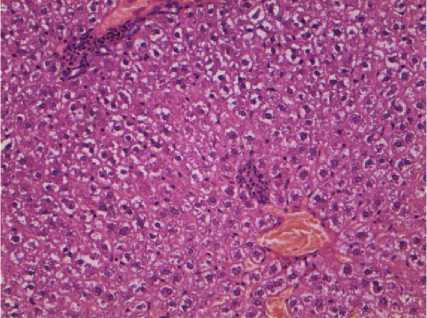
Рис. 9. Гидропическая дистрофия гепатоцитов, скопление мононуклеаров, гиперемия сосудов печени у крыс после двукратного введения « Пиро-стоп » в дозе 12 мг/кг через 10 сут. Окраска гематоксилином и эозином. Ув.×300
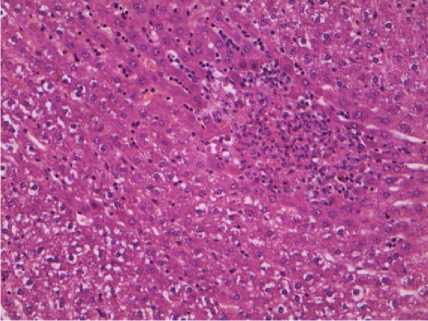
Рис. 10. Скопление мононуклеаров и гидропическая дистрофия в печени крыс после двукратного введения « Бабезана » в дозе 8 мг/кг через 10 сут.
Окраска гематоксилином и эозином. Ув.×300
В целом изменения в печени у животных опытных групп выглядели следующим образом (таблица).
Гистологические изменения в паренхиме печени у крыс опытных групп, получавших «Неозидин», «Бабезан» и «Пиро-стоп» через 10 сут, % животных в группе
|
Признак |
Препарат в терапевтической и токсической дозах, мг/кг |
|||||
|
«Неозидин» |
«Бабезан» |
«Пиро-стоп» |
||||
|
2,5 |
5,0 |
4,0 |
8,0 |
6,0 |
12,0 |
|
|
Полнокровие центральных вен |
— |
100 |
100 |
100 |
70 |
100 |
|
Расширение синусоидных капилляров |
– |
– |
– |
– |
100 |
100 |
|
Полнокровие сосудов триад |
— |
60 |
— |
— |
60 |
100 |
|
Зернистая дистрофия |
80 |
— |
100 |
— |
100 |
— |
|
Гидропическая дистрофия |
– |
100 |
– |
100 |
– |
100 |
|
Некрозы |
– |
100 |
– |
– |
100 |
100 |
|
Двуядерные клетки |
– |
100 |
– |
100 |
– |
|
|
Скопления мононуклеаров |
– |
100 |
100 |
100 |
100 |
100 |
|
Соединительнотканные элементы |
– |
– |
– |
– |
60 |
100 |
Для полного понимания патогенеза ассоциированной пироплазмоцидными лекарственными препаратами гепатопатии и разработки путей патогенетической коррекции обнаруженные изменения требуют дальнейшего изучения с применением усовершенствованных методов гистологической диагностики.
Заключение
При экспериментальном моделировании фармакотерапии с использованием препаратов на основе имидокарба и диминазина отмечали патоморфологические изменения в печени, характерные для токсического поражения органа. Через 3 сут после введения препаратов в терапевтической дозе наибольшие изменения в печени регистрировали при введении « Пиро-стоп »: зернистая дистрофия гепатоцитов, полнокровие центральных вен и расширение синусоидных капилляров, участки некроза гепатоцитов, пролиферация соединительной ткани вокруг крупных сосудов. Через 10 сут изменения в печени сохранялись. У животных, получавших токсическую дозу лекарственных препаратов, в оба срока наблюдений отмечали полнокровие центральных вен и сосудов триад, морфологические признаки гидропической дистрофии гепатоцитов, лимфоплазмоцитарные инфильтраты. После введения « Неозидина » и « Пиро-стоп» на фоне вышеперечисленных изменений в органах регистрировали участки некроза и разрастание рыхлой соединительной ткани. Наименьшие изменения в гепатоцитах отмечали при введении крысам « Бабезана » в терапевтической дозе, однако превышение дозы в два раза ведет к развитию дистрофических и воспалительных процессов в органе.
Таким образом, проведенные исследования свидетельствует о гепатотропном характере действия препаратов на основе имидокарба и диминазина, что необходимо учитывать в комплексном лечении бабезиозов у домашних животных.
T.V. Boyko, M.N. Gonokhovа, M.V. Koshkarev, V.S. Veretennikova, S.S. Kuzmin Omsk State Agrarian University named after P.A. Stolypin, Omsk
Histological changes in rats, liver at experimental poisoning with drugs based on imidocarb and diminazine
Список литературы Гистологические изменения в печени крыс при экспериментальном отравлении препаратами на основе имидокарба и диминазина
- Parasitological and molecular diagnostic of a clinical Babesia caballi outbreak in Southern Romaniaonita M, Nicorescu M, Pfister K, Mitrea IL.//Parasitol Res. -2018. -May 15. -Режим доступа: https://www.ncbi.nlm.nih.gov/pubmed/29766270 DOI: 10.1007/s00436-018-5899-2
- A four year epidemiological and chemotherapy survey of babesiosis and theileriosis, and tick vectors in sheep, cattle and goats in Dehgolan, IranHasheminasab SS1, Moradi P2, Wright I3. Ann Parasitol. 2018; 64(1): 43-48. -Режим доступа: https://www.ncbi.nlm.nih.gov/pubmed/29717573 DOI: 10.17420/ap6401.131
- Efficacy, safety and tolerance of imidocarb dipropionate versus atovaquone or buparvaquone plus azithromycin used to treat sick dogs naturally infected with the Babesia microti-like piroplasm/R. Checa et al.//Parasit Vectors. -2017. -Mar 13; 10(1): 145 DOI: 10.1186/s13071-017-2049-0
- Распространение бабезиоза собак в центральном районе Российской Федерации и рациональные схемы лечения/С.В. Енгашев, Э.Х. Даугалиева, М.Д. Новак, О.Ю. Мазитова//Теория и практика борьбы с паразитарными болезнями. -2015. -№ 16. -С. 136-139.
- Акимов Д.Ю. Сравнительная оценка эффективности препаратов на основе имидокарба и диминазина при бабезиозе /Д.Ю. Акимов, Е.М. Романова, Л.А. Шадыева. -Режим доступа: file:///C:/Users/ZALMAN/Downloads/sravnitelnaya-otsenka-effektivnosti-preparatov-na-osnove-imidokarba-i-diminazina-pri-babezioze% 20(1).pdf.
- Шмыголь О.В. Сравнительная эффективность препаратов при пироплазмозе собак/О.В. Шмыголь, Л.В. Бычкова//Актуальные проблемы инвазионной и незаразной патологии животных: материалы междунар. науч.-практич. конф., посвящ. 100-летию со дня рождения С.Н. Никольского. -Ставрополь, 2003. -С. 145-146.
- Научная электронная библиотека Elibrary.ru . -Режим доступа: https://elibrary.ru/query_results.asp.
- Инструкция по применению «Неозидина® М» для лечения и профилактики кровепаразитарных болезней животных . -Режим доступа: http://www.nita-farm.ru/upload/iblock/c6d/c6db9b2df796afb6053a5394744c1af9.pdf.
- Инструкция по применению «Пиро-стоп» для лечения и профилактики кровепаразитарных болезней у животных . -Режим доступа: http://www.vetlek.ru/directions/?id=661http://www.vetlek.ru/directions/?id=661.
- ГОСТ 33215-2014. Руководство по содержанию и уходу за лабораторными животными. Правила оборудования помещений и организации процедур . -Режим доступа: http://docs.cntd.ru/document/1200127789.


