Гистоновый код и эпигенетическая регуляция гена PTEN в злокачественных глиомах
Автор: Семенова Е.В., Волницкий А.В., Филатов М.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 3 (51), 2012 года.
Бесплатный доступ
Представлен анализ транскрипционной активности PTEN в 7 первичных культурах глиом с помощью 2 эпигенетических мар- керов посттрансляционных модификаций гистона Н3: Н3К9me3 и Н3К4ас. Продемонстрировано наличие маркера подавления транскрипционной активности Н3К9me3 вблизи сайтов инициации транскрипции гена PTEN (1-й экзон) в подавляющем боль- шинстве (6 из 7) исследованных клеточных линий. Маркер активной транскрипции Н3К4ас в области 1-го экзона нами обнаружен только в одной клеточной линии. В области гена PTEN, кодирующей фосфотазный домен (5-й экзон), модификация Н3К9me3 зафиксирована во всех проанализированных линиях глиом. Анализ статуса ацетилирования гистона Н3 в данной области PTEN показал полное отсутствие модификации Н3К4ас. Полученные результаты указывают на подавление транскрипционной активности гена PTEN в абсолютном большинстве (6 из 7) клеточных линий глиом посредством измененного гистонового кода. Кроме того, по всей видимости, они свидетельствуют о значительной универсальности эпигенетических механизмов регуляции экспрессии антионкогена PTEN в глиомах.
Белок-онкосупрессор pten, гистоновый код, глиомы, метод иммунопреципитации хроматина, эпигенетические механизмы
Короткий адрес: https://sciup.org/14056226
IDR: 14056226 | УДК: 616-006.484:575.113
Histone code and epigenetic regulation of PTEN gene in malignant gliomas
To analyse the transcriptional activity of PTEN in 7 primary cultures of gliomas we have used two epigenetic markers of histone H3 posttranlational modifications: H3K9me3 and H3K4ac, which are typical for active and repressed chromatin, respectively. The presence of suppression marker of transcriptional activity (H3K9me3) near the transcriptional initiation site (exon I) was found in 6 of 7 cell lines investigated, and only one line shown to contain the acetylated H3K4ac form in this region of PTEN. Additional analysis of histone signature in exon 5 region of the gene has revealed the only H3K9me3 marker in all 7 cell cultures. The data obtained indicate the suppression of transcriptional activity of PTEN in most analysed gliomas through altered histone code, which seems to be an universal mechanism of epigenetic regulation of PTEN expression in gliomas.
Текст научной статьи Гистоновый код и эпигенетическая регуляция гена PTEN в злокачественных глиомах
Нарушение по той или иной причине нормального функционирования гена PTEN – характерная черта злокачественных глиом [18, 20], соответственно, уровень экспрессии PTEN – важнейший показатель злокачественной трансформации глиом [1, 6, 7, 9, 11, 18]. Соматические мутации PTEN – достаточно частое явление для глиобластом (IV степень злокачественности глиом по классификации ВОЗ) [12, 19, 27]. Кроме того, генетические изменения PTEN обнаружены в незначительной группе (менее 10 %) анапластических астроцитом и анапластических олигодендроглиом (III степень злокачественности глиом по классификации ВОЗ), но они практически отсутствуют в глиомах более низких степеней злокачественности [6, 12, 27]. По всей видимости, появление мутаций PTEN – относительно позднее событие в злокачественной прогрессии глиом. Однако существенное изменение экспрессионного профиля PTEN зафиксировано в значительной части не только глиобластом, но и глиом более низких степеней злокачественности, и этот показатель намного превосходит частоту встречаемости мутаций PTEN [6, 26]. Эти данные указывают на существование альтернативных механизмов инактивации гена PTEN в злокачественных глиомах. По-видимому, таковыми являются эпигенетические нарушения, в том числе промоторное метилирование ДНК и изменение гистонового кода. Действительно, публикации последних лет подтверждают важную роль ДНК-метилирования в регуляции экспрессии PTEN в глиомах [9, 12, 14, 16, 26]. Однако нам не удалось обнаружить в литературе сведений об изучении транскрипционной активности PTEN в глиомах с помощью анализа посттрансляционных модификаций коровых гистонов, так называемого гистонового кода.
Целью исследования является определение эпигенетических изменений гена PTEN в клеточных линиях глиом посредством посттрансляционных модификаций гистона Н3. Используя метод иммунопреципитации хроматина с дальнейшим ПЦР-анализом, мы исследовали трансрипционную активность PTEN в 7 первичных культурах глиом с помощью 2 эпигенетических маркеров: маркера транскрипционной инертности Н3К9me3 и маркера активно транскрибируемого хроматина Н3К4ас.
Материал и методы
Первичные культуры глиом . Исследовали 7 первичных культур глиом человека, полученных в нашей лаборатории из хирургического материала пациентов Российского научно-исследовательского нейрохирургического института им. проф. А.Л. Поленова. Образцы опухолевых тканей были идентифицированы как глиомы III (анапластическая астроцитома) и IV (глиобластома мультиформная) степени по классификации ВОЗ с помощью морфологического и гистологического анализов (две глиомы № 4 и № 7 – III степени, остальные – IV степени злокачественности). Клетки культивировали в среде DMEM и DMEM/F-12 (1:1) с добавлением 10 % сыворотки крови плодов коровы (БиолоТ, Россия), 0,1 % L-глутамина (Invitrogen, Великобритания), 100 ед/мл пенициллина и 0,1 мг/мл стрептомицина и снимали с помощью 0,02 % раствора Версена (БиолоТ, Россия).
Процедура иммунопреципитации хроматина (CHIP). Процедура CHIP (Chromatin Immunoprecipitation Assay) была строго стандартизирована. В каждом эксперименте использовался хроматин, полученный из 3×106 клеток. С целью образования ковалентных сшивок между ДНК и гистонами клетки 10 мин инкубировали с 1 % формальдегидом при комнатной температуре. Реакция останавливалась добавлением 2,5 М глицина (1/20 объема реакционной смеси) с последующей инкубацией на льду в течение 20 мин. Клетки осаждались 5 мин центрифугированием при 4ºС на 1500g, дважды про- мывались в холодном растворе РВС. После этого клетки инкубировались по 10 мин в промывочных растворах 1 (0,25 % Triton X-100, 10 mM EDTA, 10 mM Hepes; pH 7Ю5) и 2 (0,2 M NaCl, 1,5 M EDTA, 10 mM Hepes; pH 7,5) с добавлением ингибиторов протеаз: PMSF и коктейля ингибиторов протеаз (Thermo scientific,США). Затем в течение 20 мин клетки лизировали на льду в 600 μl буфера, содержащего 150 mM NaCl; 25 mM Tris-HCl, pH 7,5; 5 mM EDTA; 1 % Triton X-100; 0,1 % SDS; 0,5 % sodium deoxycholate и ингибиторы протеаз. Лизат «озвучивали» на дезинтеграторе УЗДН-2Т 8×10 сек, после чего центрифугировали при 13000 g в течение 15 мин при 4ºС. Супернатант разводили 1:5 буфером, содержащим 25 mM Tris-HCl, pH 7,5; 1 mM EDTA; 1 % Triton X-100 и ингибиторы протеаз, и делили на 3 равные части. Первая часть использовалась в качестве негативного контроля, ко второй части добавляли анти-Н3К9me3 антитела (Upstate, США), к третьей – анти-Н3К4ас (Upstate, США) и при постоянном вращении инкубировали ночь при 4ºС. Затем иммунокомплексы адсорбировали на протеин А-агарозу в течение 1 ч. После нескольких промывок агарозы иммунокомплексы элюировали буфером, содержащим 1 % SDS и 0,1 M NaHCO3. Затем элюаты инкубировали в течение 6 ч при 65ºС. в присутствии 200 mM NaCl для разрушения сшивок между ДНК и гистонами. После обработки элюатов РНКазой (конечная концентрация 50 мкг/мл) и протеиназой К (Fisher, США) (конечная концентрация 100 мкг/мл) осуществляли экстракцию ДНК смесью фенол-хлороформ с последующим осаждением этанолом по стандартной методике. Выделенную ДНК ресуспендировали в 20 мкл H2O и использовали для ПЦР-анализа. Для каждой линии глиом выполнено по три независимых процедуры CHIP.
ПЦР-анализ . Полимеразную цепную реакцию проводили в 20 мкл смеси, содержащей: 62 мМ Tris-HCl, pH 8,5; 1,5 мM MgCl2; 35 мМ КCl; 0,01 мМ EDTА; 10 мM 2-меркаптоэтанол; 0,15 % Triton X-100; 0,1 мМ DTT; 5 % глицерин; по 250 мМ каждого из четырех dNTP (Медиген, Россия); по 10 пМ каждого праймера (НПО «Синтол», Россия); фиксированный объем выделенной в процессе CHIP ДНК (5 мкл); 1 ед. Taq-полимеразы (НПО «СибЭнзим», Россия). В работе использовались праймеры к 1-му и 5-му экзонам гена PTEN (табл.1).
Таблица 1
Праймеры к 1-му и 5-му экзонам гена PTEN
|
Последовательность праймера |
Температура отжига |
Размер продукта, п.н |
Локализация в геноме |
|
F: 5`-CAAGCGGCGGACGAGCGAGG-3` R: 5`-AGGTCAAGTCTAAGTCGAATC-3` |
57ºС |
210 |
1-й экзон гена PTEN |
|
F: 5`-CTTATTCTGAGGTTATCTTTTTTACC-3` R: 5`-CTCAGAATCCAGGAAGAGGA-3` |
58ºС |
304 |
5-й экзон гена PTEN |
Таблица 2
Результаты исследования транскрипционной активности гена PTEN в первичных культурах глиом с помощью 2 эпигенетических маркеров посттрансляционных модификаций гистона Н3: Н3К9me3 и Н3К4ас
|
Порядковый номер клеточной линии |
Наличие модификации Н3К9me3 в 1-м экзоне PTEN |
Наличие модификации Н3К4ас в 1-м экзоне PTEN |
Наличие модификации Н3К9me3 в 5-м экзоне PTEN |
Наличие модификации Н3К4ас в 5-м экзоне PTEN |
|
1 |
+ |
- |
+ |
- |
|
2 |
- |
+ |
+ |
- |
|
3 |
+ |
- |
+ |
- |
|
4 |
+ |
- |
+ |
- |
|
5 |
+ |
- |
+ |
- |
|
6 |
+ |
- |
+ |
- |
|
7 |
+ |
- |
+ |
- |
Последовательности праймеров для 1-го экзона взяты из литературы [15]. Последовательности праймеров для 5-го экзона собственного дизайна. При конструировании праймеров использовались данные о структуре гена PTEN , полученные из международной базы данных NCBI (США).
ПЦР-продукты разделяли электрофоретически в 6 % акриламидном геле.
Фрагменты ДНК визуализировали с помощью окрашивания азотнокислым серебром AgNO3.
Результаты и обсуждение
Белок PTEN считается специфическим молекулярным маркером патогенеза глиом [1, 6, 18, 24]. В 60–70 % глиобластом утрачена нормальная функция PTEN вследствие генетических и эпигенетических нарушений [10, 27]. Изменение экспрессионного уровня PTEN коррелирует со степенью злокачественности глиом и, как следствие, с продолжительностью жизни пациентов, страдающих опухолями головного мозга данного типа [9, 19, 27].
Наше исследование посвящено определению эпигенетических изменений гена PTEN посредством посттрансляционных модификаций корового гистона Н3 в клеточных линиях глиом. Ацетилирование и метилирование – два наиболее хорошо изученных к настоящему времени типа модификаций коровых гистонов. Ацетилирование связывают с транскрипционно активным эухроматином, деацетилирование способствует образованию транскрипционно инертных гетерохроматиновых структур. Метилирование гистонов может быть связано как с транскрипционной активностью, так и с подавлением таковой, в зависимости от типа гистонов, порядкового номера аминокислотных остатков, по которым происходит метилирование, и количества присоединенных метильных групп [2, 3, 8]. Известно, что модификация Н3К4ас является эпигенетическим маркером активной транскрипции, а модификация Н3К9me3 – маркером транс-крипционно инертного хроматина [2, 3, 13]. Для определения транскрипционной активности антионкогена PTEN в глиомах мы проанализировали 1-й экзон PTEN в 7 первичных культурах глиом с помощью антител к этим двум противоположным по своим функциям модификациям гистона Н3. Для этих целей была применена процедура иммунопреципитации хроматина с последующим ПЦР-анализом выделенных фрагментов ДНК.
Было показано, что в 6 из 7 проанализированных клеточных линиях область вблизи сайтов инициации транскрипции PTEN (1-й экзон) обогащена маркером стабильной генной репрессии Н3К9me3. Уровень ацетилирования гистона Н3 в области 1-го экзона PTEN, определяемый с помощью маркера активной транскрипции Н3К4ас, оказался ниже порога чувствительности используемого метода также в 6 из 7 исследованных клеточных культурах. При этом в области 1-го экзона PTEN модификация транскрипционной активности Н3К4ас обнаружена именно в той клеточной линии (№ 2), в которой отсутствовала модификация Н3К9me3. Данные этого анализа на примере 3 клеточных линий глиом представлены на рис. 1А. Полученные результаты свидетельствуют о подавлении транскрипционной активности PTEN с помощью эпигенетических механизмов в абсолютном большинстве исследованных клеточных линий глиом. Кроме того, нами обнаружено антагонистическое распределение двух противоположных по своим функциям посттрансляционных модификаций гистона Н3 (Н3К9me3 и Н3К4ас) вблизи сайтов инициации транскрипции PTEN. В ряде исследований также указывается на необходимость деацетилирования гистона Н3 для поддержания определенного уровня Н3К9 метилирования в гетерохроматине [17, 25].
Модификации Н3К9me3, Н3К27me1 и Н4К20me1 являются маркерами транскрипционно инертного хроматина [5, 22], однако в ряде работ зафиксировано наличие данных модификаций в кодирующих областях транскрипционно активных генов [4, 21, 23, 25]. То есть позитивно регулирующие промоторную активность модификации коровых гистонов не всегда сохраняют высокую степень обогащения вдоль всей транскрибируемой области, замещаясь модификациями, связанными с генной репрессией. Анализ области гена, кодирующей коровый домен липидной фосфатазной активности белка PTEN (5-й экзон) во всех исследованных нами клеточных линиях глиом, показал наличие маркера транскрипционной инертности Н3К9me3. Ацетилирование гистона Н3 в области 5-го экзона PTEN (модификация Н3К4ас) нами не обнаружено (рис.1Б). То есть, по-видимому, для поддержания определенного уровня Н3К9 метилирования в кодирующей области гена PTEN необходимо удаление модификации Н3К4ас. Обобщенные результаты исследования представлены в табл. 2.
Таким образом, эпигенетический маркер стабильной генной репрессии Н3К9me3 зафиксирован нами вблизи промоторной области гена PTEN (1-й
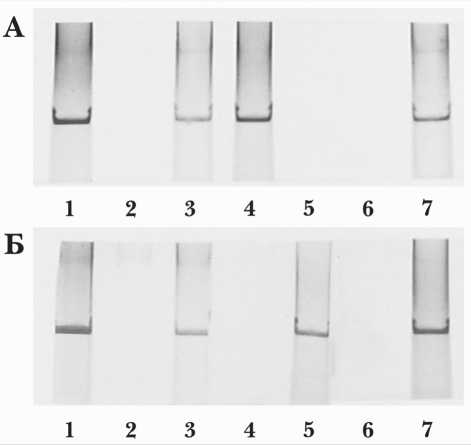
Рис. 1. Анализ транскрипционной активности гена PTEN в 3 первичных культурах глиом с помощью посттрансляционных модификаций гистона Н3: маркера активной транскрипции Н3К4ас и маркера генной репрессии Н3К9me3. Примечание: А – Результаты, полученные для области 1-го экзона гена PTEN в глиомах № 1
(дорожки 2, 3), № 2 (дорожки 4, 5) и № 3 (дорожки 6, 7); Б – Результаты, полученные для области 5-го экзона гена PTEN в глиомах № 1 (дорожки 2, 3), № 2 (дорожки 4, 5) и № 3 (дорожки 6, 7).
Дорожка 1 – результат амплификации геномной ДНК (контроль); дорожки 2, 4, 6 – результат амплификации ДНК, полученной в результате процедуры иммунопреципитации хроматина с анти-Н3К4ас антителами; дорожки 3, 5, 6 – результат амплификации
ДНК, полученной в результате процедуры иммунопреципитации хроматина с анти-Н3К9me3 антителами экзон) в абсолютном большинстве проанализированных клеточных линий, и в области гена, кодирующей фосфатазный домен белка PTEN (5-й экзон), во всех без исключения проанализированных клеточных линиях, что, по всей видимости, свидетельствует о значительной универсальности эпигенетических механизмов регуляции экспрессии антионкогена PTEN в глиомах. Полученные данные об измененном «гистоновом коде» гена PTEN в 6 из 7 исследованных клеточных линиях глиом (подавление транскрипционной активности посредством эпигенетического механизма регуляции экспрессии) подтверждают важность инактивации этого антионкогена для процессов злокачественной трансформации глиом.


