Гормональный и липидный дисбаланс в формировании миопической хориоретинальной неоваскуляризации у женщин
Автор: Григорьева А.В., Щуко А.Г., Курсакова Ю.В., Иванова Е.И., Самсонов Д.Ю.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Глазные болезни
Статья в выпуске: 2 т.15, 2019 года.
Бесплатный доступ
Цель: определить роль гормонального и липидного дисбаланса в формировании миопической хориоретинальной неоваскуляризации у женщин. Материал и методы. В первую клиническую группу включены результаты исследования пациенток с активной формой хориоретинальной неоваскуляризации (ХНВ), во вторую - результаты исследования их парного глаза. Отдельно сформированы группы контроля. Всем пациенткам и лицам групп контроля проведено всестороннее обследование офтальмологического и соматического статуса. Результаты. Установлено повышение уровня пролактина до 501,7±28,2 мМЕ/мл, в группе контроля до 272,9±33,4 мМЕ/мл; уровня фолликулостимулирующего гормона до 13,0±0,1 мМЕ/мл, в группе контроля до 4,6±1,2 мМЕ/мл. Концентрация эстрадиола снижена до 35,2±3,1 пг/л, прогестерона до 2,8±0,1 нмоль/л, в сравнении с группой контроля, где значения данных гормонов составили соответственно 66,8±8,1 и 6,3±1,1 нмоль/л. Выявлено повышение уровня острофазовых белков: фибриногена в 3,8 (14,0±0,5) и С-реактивного белка в 2 раза (5,7±2,3) по сравнению с группой контроля, где значения данных белков составило соответственно 3,6±0,5 и 2,5±0,7. Наблюдалось повышение уровня липопротеина (а) до 50,2±1,2 г/л и АпоВ/АпоА до 0,6±0,1 г/л по сравнению с группой контроля, где данные показатели составили 9,1±1,1 и 0,4±0,1 г/л. Заключение. Полученные данные подтверждают патогенетическую значимость системных факторов риска в развитии хориоидальной дисфункции и, как следствие, формирование хориоретинальной неоваскуляризации.
Гипоэстрогенемия, миопия, оптическая когерентная томография
Короткий адрес: https://sciup.org/149135321
IDR: 149135321 | УДК: 617.753:612.018
Hormonal and lipid imbalances in the formation of myopic chorioretinal neovascularization in women
Purpose: to determine the role of hormonal and lipid imbalance in the formation of myopic chorioretinal neovascularization in women. Material and Methods. The frst clinical group includes the results of the study of patients with the active form of myopic chorioretinal neovascularization, the second - the results of the study of their paired eyes. The control groups were formed separately. Ophthalmologic and somatic status of all patients and people in the control groups were thoroughly examined. Results. An increase in the level of prolactin to 501.7±28.2 mlU/ml was established, in the control group to 272.9±33.4 mlU/ml, the level of follicle-stimulating hormone 13±0.1 mlU/ml, the control group 4,6±1.2 mlU/ml. The concentration of estradiol is reduced 35.2±3.1 pg/l, progesterone 2.8±0.1 nmol/l, compared to the control group 66.8±8.1 and 6.2±1.1 nmol/l respectively. An increase in the level of acute-phase proteins was revealed: fibrinogen 3.8 (14.0±0.5) and C-reactive protein 2 times (5.72±2.30) compared with the control group 3.6±0.5 and 2.5±0.7. Increased lipoprotein level (a) 50.2±1.2 g/l and ApoB/ApoA 0.6±0.1 compared with the control group 9.1±1.1 et 0.4±0.1 g/l. Conclusion. The fndings confrm the pathogenetic signifcance of systemic risk factors in the development of choroidal dysfunction and, as a
Текст научной статьи Гормональный и липидный дисбаланс в формировании миопической хориоретинальной неоваскуляризации у женщин
корригированная миопия создает трудности при выполнении зрительной работы, снижает профессиональную адаптацию и ухудшает качество жизни [1]. По оценкам T. Y. Wong (2014), патологическая миопия поражает до 3% населения мира [2].
Основной причиной необратимого снижения зрительных функций у пациентов с близорукостью является формирование дегенеративных процессов центральных отделов сетчатки на фоне хориоидальной неоваскуляризации. Распространенность миопической хориоретинальной неоваскуляризации (мХНВ) достигает 5,2% и в 34% случаев поражает оба глаза [3]. В 35% случаев отмечено двустороннее развитие
ХНВ у пациентов с миопией, парный глаз поражался в течение 8 лет [4]. Миопическая ХНВ составляет до 62% от всех видов ХНВ, возникающих у этих пациентов [5], и демографические исследования подтверждают, что это чаще заболевание среднего, чем пожилого возраста [6].
Золотым стандартом лечения мХНВ является своевременное интравитреальное введение ингибиторов ангиогенеза. Однако механизмы анти-VEGF-терапии при этом заболевании до сих пор до конца не выяснены. Отсутствуют единые схемы лечения и прогностические критерии, определяющие эффективность и резистентность терапии, возможность формирования рецидивов и развития патологического процесса на парном глазу.
Цель: определить роль гормонального и липидного дисбаланса в формировании миопической хориоретинальной неоваскуляризации у женщин.
Материал и методы. Исследование проведено в соответствии с Хельсинкской декларацией Всемирной медицинской ассоциации «Этические принципы проведения научных медицинских исследований с участием человека» (1964 г., с поправками 2000 г.) и «Правилами клинической практики в Российской Федерации» (приказ Минздравсоцразвития РФ №266 от 19.06.2003 г.). Письменное информированное согласие получено от всех пациентов. Работа состояла из двух этапов. Первый этап: ретроспективный анализ историй болезни пациентов с диагнозом «миопия», обратившихся за диагностикой и лечением в ИФ МНТК «Микрохирургия глаза» с 2006 по 2017 г. Второй этап: проспективное нерандомизированное обследование пациентов с диагнозом «миопическая хориоретинальная неоваскуляризация».
В первую клиническую группу включены пациентки с активной формой ХНВ (n=25), средний возраст 33,5±5,1 года. Вторую клиническую группу составили результаты обследования парного глаза в том случае, если в нем отсутствовали признаки хориоретинальной неоваскуляризации (n=15), средний возраст 33,5±5,1 года. В связи с тем что в 25% случаев наблюдался двусторонний процесс, количество объектов исследования в первой и второй группах отличалось. Отдельно сформированы группы контроля. Участники первой группы контроля были сопоставимы с основной клинической группой по возрасту и степени миопии: n=21, средний возраст 33,6±4,7 года. Вторую группу контроля составили женщины с эмметропией (n=22), средний возраст 33,6±0,5 года. Все пациентки с мХНВ получали анти-VEGF-терапию в режиме «по потребности». Наблюдение проводилось в течение 12 месяцев.
Для всесторонней оценки структурно-функционального состояния зрительной системы применялись стандартные офтальмологические исследования, а также оптическая когерентная томография (ОКТ) и оптическая когерентная томография в сосудистом режиме (ОКТА) (RTVue XR Avanti; Optovue, USA), флюоресцентная ангиогафия (FA Topcon TRС-50DX, Japan).
Для исследования центральных отделов сетчатки использовали протокол сканирования Retina Map, с помощью которого оценивали толщину сетчатки от ретинального пигментного эпителия (РПЭ) до внутренней пограничной мембраны (ВПМ). Структуру хориоидеи оценивали в протоколе Сross Line, выполненном через центр фовеа в горизонтальном и вертикальном меридианах. Измерения проводили в 5 точках по стандартной методике от наружной границы пигментного эпителия до внутренней границы склеры в проекции фовеа, пара-фовеа и перифовеа с шагом в 500 мкм с назальной и темпоральной сторон.
Структуру хориоидеи оценивали с учетом сегментации на 3D-сканах и En Face [7]. Площадь мХНВ измеряли вручную с использованием стандартных функций прибора ОКТА. Данные флюоресцентной ангиографии и ОКТА использовали в качестве основных критериев диагностики ХНВ, определения ее активности и показаний к лечению.
Изучение концентрации гормонов проводилось с целью оценки уровня стрессорных реакций и гормональных изменений, определяющих нарушение репродуктивных функций. Исследование гормонального статуса включало определение концентрации соматотропного (СТГ), фолликулостимулирующего (ФСГ), лютеинизирующего (ЛГ), тиреотропного (ТТГ) гормонов, пролактина, тестостерона, 17-ОН прогестерона, прогестерона, эстрадиола, трийодтиронина (Т3), тироксина или тетрайодтиронина (Т4). Исследование проводили методом твердофазного ИФА (Im-munochem-2100 Microplate Reader, USA). Кроме того, изучали липидограмму второго уровня с определением липопротеина (а), соотношения АпоА/АпоВ (Accent-200 Cormay, Poland), коагулограммы (Helena C-2, UK), показателей окислительного стресса (Formplus Callegari, Italy). Забор крови для исследования проводился из локтевой вены у женщин с сохраненным менструальным циклом с 5-го по 9-й день.
Статистический анализ полученных результатов исследования проводился с использованием пакета прикладных программ Statistica 6.0 и включал дескриптивный и корреляционный анализ. Показатели групп проверены на нормальное распределение по критерию Колмогорова — Смирнова. Рассчитывали среднее значение (М), стандартное отклонение (s), ошибку средней (m). Вариационные ряды сравнивались с применением критерия Манна — Уитни, критерия Уилкоксона и Z-критерия. Выбранный критический уровень значимости равнялся 5% (
P
<0,05). Корреляционный анализ по методу Спирмена позволил определить фактическую степень параллелизма между двумя количественными рядами изучаемых признаков и оценить тесноту установленной связи с помощью количественно выраженного коэффициента. Сила, степень или теснота корреляционной связи определялись по абсолютному значению коэффициента корреляций и не зависели от ее направленности. При коэффициенте r>0,7 связь считалась высокой, при 0,5
Результаты. Установлено, что группу больных составляли в преобладающем большинстве женщины репродуктивного возраста (91,8%). Это послужило основанием включить в основную клиническую группу исследования пациентов именно женского пола, изучая у них концентрации основных гормонов.
Результаты сравнительного анализа показали, что у пациенток основной клинической группы длина глазного яблока варьировалась от 26,5 до 30,0 мм, но в 75% случаев преобладала выраженная элонгация глазного яблока более 28 мм.
Формирование мХНВ закономерно сопровождалось снижением центральной корригированной остроты зрения в среднем до 0,3±0,9, что в 2 раза ниже значений парного «условно здорового» глаза, в 2,6 раза ниже значений группы контроля у лиц с миопической рефракцией и в 3,3 раза ниже контроля с эмметропией (рис. 1).
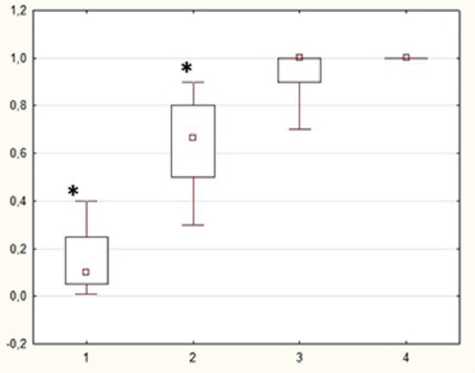
Рис. 1. Изменение корригированной остроты зрения: МКОЗ — максимальная корригированная острота зрения; 1 — основная клиническая группа; 2 — группа сравнения (парный «условно здоровый» глаз); 3 — контроль (миопическая рефракция); 4 — контроль (эмметропия); * — p<0,01
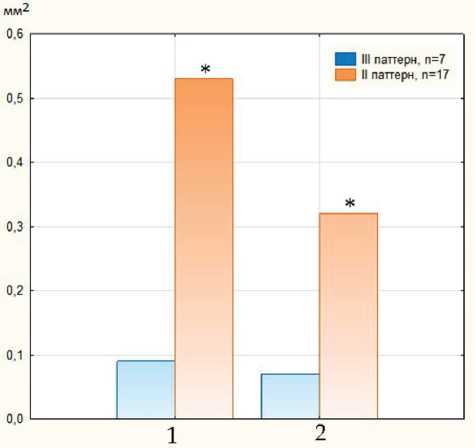
Рис. 2. Оценка площади хориоретинальной неоваскулярной мембраны: 1 — выделенная область (select area); 2 — выделенный сосуд (select vessel); * — p<0,01
Всесторонняя оценка структуры хориоретинального комплекса позволила выявить следующее: в 24% случаев пациенты с мХНВ имели так называемый мозаичный, или паркетный, тип глазного дна, причиной формирования которого является частичная утрата пигментного эпителия и хориокапилляр-ного слоя. У пациентов группы контроля при миопической рефракции такие изменения встречались лишь в 5% случаев, а у эмметропов не выявлены ни в одном случае. Кроме того, у пациенток основной клинической группы как на больном в 72% случаев, так и на парном «условно здоровом» глазу в 66,7% случаев офтальмоскопировались так называемые «лаковые трещины», происхождение которых связано с механическим повреждением комплекса «пигментный эпителий — стекловидная пластинка — хориокапилляры». У группы контроля с миопией такие изменения выявлены лишь у 5% пациентов, а при эмметропии также отсутствовали. При офтальмоскопии на глазах с мХНВ визуализировался небольшой очаг, расположенный в 95% случаев юкстафовеолярно, активность которого подтверждалась данными ФАГ.
Обращало на себя внимание выраженное уменьшение толщины хориоидеи, как на глазах с ХНВ, так и на парных «условно здоровых» глазах. В основной клинической группе практически в 3 и 4 раза по сравнению с группами контроля (p=0,01), на парном глазу в 2 раза по сравнению с контролем. У каждой 8-й пациентки основной клинической группы толщина хори-оидеи не превышала 50 мкм, что свидетельствовало о серьезных дистрофических процессах, лежащих в основе хориоретинальной ишемии.
Оценка относительной плотности сосудистого сплетения в режиме ОКТ-ангио продемонстрировала отсутствие статистически достоверных отличий данного показателя в поверхностном сосудистом сплетении, как у лиц основной клинической группы, так и лиц групп сравнения. В то же время установлено уменьшение относительной плотности глубокого сосудистого сплетения на глазах с мХНВ на 20% и более чем на 30% по сравнению с группами контроля с миопией и эмметропией соответственно в проекции парафовеолярной области.
У всех пациенток с мХНВ на уровне хориокапил-ляров и наружной сетчатки диагностирована классическая субретинальная неоваскулярная мембрана (II типа). В ходе исследования установлено, что в преобладающем большинстве случаев ХНВ соответствовала 2-му типу паттернов так называемой «sea fan» по классификации Elsa Bruyère (2018), для которого характерно наличие фидерного сосуда и хорошо визуализирующиеся сосудистые петли, которые окаймлены темным ореолом, соответствующим зонам ишемии хориокапилляров. Менее чем в 30% случаев строение ХНВ соответствовало третьему типу паттерна и имело вид «tree-in-bud», для которого характерна плотная сосудистая сеть, при котором фидерный сосуд и ореол не визуализировались или слабо визуализировались. При этом площадь так называемой выделенной области, соответствующая СНМ и выделенной площади сосудов при втором типе паттерна, превышала соответствующее значение третьего типа паттерна практически в 5 раз (рис. 2).
Тщательный сбор анамнеза vitae, исследование концентрации гормонов и биохимических показателей крови позволили установить, что пациентки основной клинической группы имели выраженные нарушения менструально-овариального цикла по типу опсо- и олигоменореи. Сравнительный анализ концентрации изучаемых гормонов в сыворотке крови обнаружил отсутствие патологических изменений в показателях тиреотропных гормонов, кортизола и СТГ, ЛГ, тестостерона.
В то же время установлены значимые изменения половых гормонов: пролактина в 1,5 раза, а ФСГ в 3 раза превышал значения групп контроля.
Концентрация эстрадиола была снижена в полтора раз и прогестерона в 2 раза, что свидетельствует о дисбалансе основных половых гормонов у пациенток с ХНВ (табл. 1).
Анализ биохимических показателей крови установил у пациенток с мХНВ повышение уровня острофазовых белков, являющихся лабораторными маркерами воспаления и тканевого повреждения: фибриногена в 3,8 раза и С-реактивного белка в 2,5 раза по сравнению с группами контроля.
Таблица 1
Сравнительный анализ концентрации гипофизарных и половых гормонов в сыворотке крови, M±m
|
Показатель |
Миопическая ХНВ1, n=25 |
Контроль, миопия, рефр. 2, n=21 |
Контроль, эмметропия, рефр. 3, n=22 |
Критерий Манна–Уитни, р |
|
Пролактин, мМЕ/мл |
501,7±28,2 |
341,0±81,1 |
272,9±33,4 |
р 1–2, 2–3, 1–3 =0,001 |
|
ФСГ, мМЕ/мл |
13,0±0,1 |
5,6 ±1,4 |
4,6±1,2 |
р 1–2, 2–3, 1–3 =0,001 |
|
Эстрадиол, пг/л |
35,2±3,1 |
59,0±5,1 |
66,8±8,1 |
р 1–2, 2–3, 1–3 =0,001 |
|
Прогестерон, нмоль/л |
2,8±0,1 |
4,0±1,7 |
6,2±1,1 |
р 1–2, 2–3, 1–3 =0,001 |
|
Таблица 2 |
||||
|
Сравнительный анализ концентрации острофазовых белков и липопротеинов 2-го уровня в сыворотке крови, M±m |
||||
|
Показатель |
Миопическая ХНВ1, n=25 |
Контроль, миопия, рефр. 3, n=21 |
Контроль, эмметропия рефр. 4, n=22 |
Критерий Манна–Уитни, р |
|
Фибриноген, г/л |
14,0±0,5 |
3,6±0,5 |
3,6±1,1 |
р 1-2 =0,04; p 2-3 =0,5; p1-3=0,04 |
|
С-реактивный белок, г/л |
5,7±2,3 |
2,5±0,7 |
1,9±0,7 |
р 1-2 =0,05; p 2-3 =0,6; p1-3=0,04 |
|
Липопротеин (а), г/л |
50,2±1,2 |
13,7±0,9 |
9,1±1,1 |
p 1-2 <0,01; p 2-3 =0,3; p1-3<0,01 |
|
АпоВ/АпоА, г/л |
0,6±0,1 |
0,4±0,1 |
0,4±0,1 |
p 1-2 =0,01; p 2-3 =0,5; р1-3=0,001 |
Таблица 3
Корреляционный анализ показателей, характеризующих изменения липидного и гормонального профиля и аксиальной длины глазного яблока у больных с мХНВ
|
Показатель |
ПЗО |
Толщина хориоидеи, мкм |
Пролактин, мМЕ/л |
Эстрадиол, пг/мл |
Прогестерон, нмоль/л |
Липопр. (а), г/л |
АпоВ/АпоА, г/л |
Фибриноген, г/л |
|
ПЗО |
1,00 |
–0,44 |
–0,06 |
0,03 |
0,35 |
0,00 |
–0,11 |
0,40 |
|
Толщина хориои-деи, мкм |
–0,44 |
1,00 |
–0,43 |
0,40 |
–0,06 |
0,09 |
–0,23 |
–0,03 |
|
Пролактин, мМЕ/л |
–0,06 |
–0,43 |
1,00 |
–0,64 |
–0,58 |
0,06 |
0,58 |
–0,07 |
|
Эстрадиол, пг/мл |
0,03 |
0,40 |
–0,64 |
1,00 |
0,11 |
–0,64 |
–0,60 |
–0,45 |
|
Прогестерон, нмоль/л |
0,35 |
–0,06 |
–0,58 |
0,11 |
1,00 |
0,13 |
–0,05 |
0,37 |
|
Липопр. (а), г/л |
0,00 |
0,09 |
0,06 |
–0,64 |
0,13 |
1,00 |
–0,26 |
0,63 |
|
АпоВ/АпоА, г/л |
0,32 |
–0,23 |
0,58 |
–0,60 |
–0,05 |
–0,26 |
–0,01 |
–0,09 |
|
Фибриноген, г/л |
0,40 |
–0,03 |
–0,07 |
–0,45 |
0,37 |
0,63 |
–0,09 |
1.00 |
П р и м еч а н и е : ПЗО — переднезадняя ось (аксиальная длина глазного яблока); желтым цветом выделены корреляции с r>0,4 (p<0,001).
На современном этапе еще одними высокочувствительным маркёрами и предикторами наследственной предрасположенности к сердечно-сосудистым и микрососудистым заболеваниям являются липопротеин (а) и аполипопротеины.
У больных с мХНВ выявлено практически шестикратное повышение концентрации липопротеина (а) и умеренное повышение соотношения АпоВ/АпоА (табл. 2).
Корреляционный анализ между показателем, характеризующим степень миопии (длина глазного яблока), толщиной хориоидеи и основными критериями исходной реактивности организма, показал наличие достоверных взаимосвязей у больных с мХНВ между толщиной хориоидеи, концентрацией пролактина, эстрадиола и их взаимосвязь с липопротеином (а), соотношением АпоВ/АпоА и фибриногеном, что отсутствовало у пациенток групп контроля (табл. 3).
Полученные данные подтверждают патогенетическую значимость не только местных, но и системных факторов риска в развитии хориоидальной дисфункции и, как следствие, формирование ХНВ.
Обсуждение. Выявлены выраженная дезорганизация хориоидеи, нарушение сегментации, изменение калибра и хода сосудов среднего и крупного калибра. Сегментация хориоидеи на парном «условно здоровом» глазу была частично сохранена. В группах контроля подобные изменения отсутствовали. Такое нарушение толщины и топографии сосудистой сети является важным фактором, позволяющим говорить о выраженных гемодинамических расстройствах у больных с мХНВ, которые обусловливали грубые дистрофические изменения ретинального пигментного эпителия, наружных слоев сетчатки.
Таким образом, выявленные изменения у пациенток основной клинической группы как на глазу с ХНВ, так и на парном «условно здоровом» глазу можно рассматривать как местные факторы риска и особенности формирования данного заболевания.
Известно, что недостаточность эстрогена запускает процессы эндотелиальной дисфункции и инициирует явления вазоспазма. В то же время эстроген снижает уровень воспалительных процессов в сосудистой стенке, стимулирует релаксацию сосудов путем стимуляции и высвобождения оксида азота и воздействует непосредственно на гладкую мускулатуру сосудистой стенки [8].
Результаты, полученные в работах K. Kobayashi (2002), показали наличие рецепторов эстрогена в СНМ у больных с миопией [9]. Следовательно, ги-поэстрогенемия и гормональный дисбаланс в целом являются важным механизмом сосудистых изменений формирования ХНВ.
Сходство строения липопротеина (а) и белков острой фазы позволяет рассматривать его как специфический белок, характеризующий наличие и степень воспалительных процессов в сосудистой стенке. При этом повышение данных показателей и изменения соотношения АпоВ/АпоА-1 характеризует повышенный риск развития атеросклерза и ишемических инсультов даже при низких уровнях ЛПНП и холестерина крови.
Заключение. Таким образом, результаты проведенного исследования показали, что к ключевым местным факторам риска формирования ХНВ у больных с миопией можно отнести наличие дефектов комплекса «пигментный эпителий — стекловидная пластинка — хориокапилляры» на фоне элонгации глазного яблока. Кроме того, одним из основных звеньев патогенеза данного заболевания является выраженная хориоидальная дисфункция, выявленная на обоих глазах у пациентов с мХНВ. Данные структурные и гемодинамические изменения обусловливают дистрофические изменения пигментного эпителия и нейросенсорной сетчатки. В то же время отсутствие подобных изменений у лиц контрольной группы с миопической рефракцией указывает на то, что триггером к формированию данных изменений является исходно измененная реактивность организма, о чем свидетельствуют высокий уровень липопротеина (а) и соотношение аполипротеинов.
Гипоэстрогенемия и дисбаланс половых гормонов являются серьезными предрасполагающими факторами формирования васкулярных осложнений: с одной стороны, формирования эндотелиальной дисфункции, а с другой — длительного вазоспазма. При этом хориоидея выступает органом-мишенью в реализации патологического процесса, а хориоидальная ишемия инициирует формирование СНМ, которая, как было вы- яснено, преимущественно протекает по второму типу с формированием паттерна «seafan».
Список литературы Гормональный и липидный дисбаланс в формировании миопической хориоретинальной неоваскуляризации у женщин
- Юрьева Т. Н., Григорьева А. В., Пятова Ю. С. Миопия и ее осложнения. Бюллетень Восточно-Сибирского научного центра Сибирского отделения Российской академии медицинских наук 2015; 6 (106): 75-82
- Wong T Y, Ferreira A, Hughes R, et al. Epidemiology and disease burden of pathologic myopia and myopic choroidal neovascularization: an evidence-based systematic review. Am J Ophthalmol 2014; 157: 9-25
- Ohno-Matsui T. Myopic Choroidal Neovascularization. In: Ophthalmology: Ocular Angiogenesis: Diseases, Mechanisms, and Therapeutics. Springer Nature Switzerland, 2006; p. 430-86
- Ohno-Matsui K, Yoshida T, Futagami S, et al. Patchy atrophy and lacquer cracks predispose to the development of choroidal neovascularization in pathological myopia. Br J Ophthalmol 2003; 87: 570-3
- Silva R. Myopic maculopathy: a review. Ophthalmologica 2012; 228: 197-213
- Wolf S, Balciuniene VJ, Laganovska G, et al. Radiance: a randomized controlled study of ranibizumab in patients with choroidal neovascularization secondary to pathologic myopia. Ophthalmology 2014; 121: 682-92
- Аверьянов Д. А., Алпатов С. А., Жукова С. И. и др. Оптическая когерентная томография в диагностике глазных болезней. М.: ГЭОТАР-Медиа, 2010; 128 c.
- Григорьева А. В., Юрьева Т. Н., Курсакова Ю. В., Иванова Е. И. Роль изменения гормонального статуса в формировании миопической хориоретинальной неоваскуляризации. Современные технологии в офтальмологии 2017; 4: 61-4
- Kobayashi K, Mandai M, Suzuma I, et al. Expression of Estrogen Receptor in the Choroidal Neovascular Membranes in Highly Myopic Eyes. Retina 2002; 22: 418-22.


