Градиентный феномен экспрессии генов множественной лекарственной устойчивости в опухоли молочной железы при проведении неоадъювантной химиотерапии: связь с прогрессированием заболевания
Автор: Литвяков Н.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 4 (58), 2013 года.
Бесплатный доступ
Обследовано 106 больных раком молочной железы (РМЖ), получавших неоадъювантную химиотерапию (НАХТ). При помощи количественной ПЦР с обратной транскрипцией в режиме реального времени изучена экспрессия 8 генов множественной лекарственной устойчивости (МЛУ) ABCB1, АВСВ2, ABCC1, ABCC2, АВСС5, ABCG1, ABCG2 и MVP в биопсийном материале до лечения и в операционном материале после НХТ. Установлено, что у 75 % больных наблюдается однонаправленное изменение экспрессии 5 генов МЛУ ABCB1, ABCC1, ABCC2, ABCG1 и ABCG2 в соответствии с эффектом НАХТ: снижение экспрессии при хорошем ответе и повышение экспрессии при отсутствии клинического эффекта предоперационной химиотерапии, которое было названо градиентным феноменом. У 25 % больных изменение экспрессии генов было разнонаправленным и не коррелировало с непосредственным эффектом НАХТ, при этом констатировали отсутствие градиентного феномена. Показано, что наличие градиентного феномена является благоприятным прогностическим признаком, 5-летняя безметастатическая выживаемость у таких пациенток составила 73 %, против 39 % у больных без градиентного феномена (log-rank test p=0,0018). Предполагается, что градиентный феномен является маркером наличия или отсутствия в опухолевых клетках сбалансированной системы генной регуляции и реактивности на химиопрепараты. С практической точки зрения сочетание оценки эффекта предоперационной химиотерапии и изменения экспрессии генов МЛУ в процессе НАХТ может существенно повысить эффективность прогнозирования исхода заболеваний у больных РМЖ.
Гены множественной лекарственной устойчивости, рак молочной железы, неоадъювантная химиотерапия, безметастатическая выживаемость
Короткий адрес: https://sciup.org/14056351
IDR: 14056351 | УДК: 618.19-006.6-036.17:575.113:615.28
Gradient phenomenon of multidrug resistance gene expression in breast cancer during neoadjuvant chemotherapy is related to disease progression
The paper examined 106 patients with breast cancer (bC) treated with neoadjuvant chemotherapy (NАС). In the biopsy material, derived from primary tumor before NAC and surgical samples after chemotherapy the expression of 8 multidrug resistance genes (MDR) ABCB1, АВСВ2, ABCC1, ABCC2, АВСС5, ABCG1, ABCG2 и MVP was evaluated using quantitative RT-PCR. During the NAC course 75 % of patients manifested gradient phenomenon for gene expression that means a unidirectional change in the expression of all five MDR genes ABCB1, ABCC1, ABCC2, ABCG1 и ABCG2 closely associated with the NAC efficacy: the reduction in MDR gene expression was related to good response to NAC while the expression increase associated with poor response to NAC. In 25% of patients there was no such change in studied gene expression that means the lack of a gradient phenomenon. The objective was to study whether gradient phenomenon for MDR gene expression during NAC is related to disease free survival in breast cancer patients. Five-year metastasis-free survival in patients having a gradient phenomenon was 73 % versus 39 % in patients who lack a gradient phenomenon (log-rank test p=0,0018). So, the presence of a gradient phenomenon in patients is appeared to be associated with a good disease prognosis. It is assumed that the gradi
Текст научной статьи Градиентный феномен экспрессии генов множественной лекарственной устойчивости в опухоли молочной железы при проведении неоадъювантной химиотерапии: связь с прогрессированием заболевания
В опухолевых клетках в ответ на действие даже одного цитостатика может развиться множественная лекарственная устойчивость (МЛУ) к большому количеству других препаратов, еще не воздействовавших на опухоль. В эксперименте показано, что МЛУ обусловлена работой ABC-транспортеров (ATP-Binding Cassette) лекарств, осуществляющих выброс цитостатических и тар-гетных препаратов из опухолевых клеток против градиента их концентрации, с затратой энергии АТФ [18, 21]. В клинических исследованиях предпринимались попытки связать исходный уровень экспрессии генов и белков ABC-транспортеров с эффектом химиотерапии и прогрессированием заболевания, но их результаты оказались крайне противоречивыми и не позволили сделать однозначные выводы о роли АВС-транспортеров в реализации химиорезистентности опухоли [7, 11, 12, 20, 21].
Нами было показано, что эффективность неоадъювантной химиотерапии (НАХТ), в том числе при раке молочной железы, связана с направлением изменения экспрессии индивидуальных генов МЛУ в опухоли в процессе лечения, а не с исходным уровнем экспрессии каждого из этих генов. Уменьшение экспрессии (или отрицательный градиент) генов МЛУ в опухоли молочной железы после НАХТ по сравнению с биопсийными образцами до лечения ассоциировалось с хорошим ответом на НАХТ. Повышение экспрессии (или положительный градиент) этих генов связано с отсутствием непосредственного эффекта НАХТ. Направление изменения экспрессии отдельных генов МЛУ в опухоли молочной железы при НАХТ имеет значение не только для ответа на химиотерапию, но и ассоциировано с безметастатической выживаемостью. Ранее также было установлено, что снижение экспрессии любого из генов ABCB1 , ABCC2 или ABCG1 в процессе НАХТ является благоприятным прогностическим фактором, а повышение экспрессии – неблагоприятным фактором [3]. Следует отметить, что формирование МЛУ – это процесс, который обусловлен комплексной работой нескольких ключевых генов МЛУ [8, 18].
Целью исследования явилось изучение изменения экспрессии комплекса основных генов МЛУ в процессе НХТ больных раком молочной железы и оценка связи этих изменений с безметастатической выживаемостью.
Материал и методы
Было обследовано 106 больных с морфологически верифицированным раком молочной железы IIA–IIIC стадий (T1–4N0–3M0), в возрасте 28–68 лет (средний возраст – 47,43 ± 0,78 года), получавших лечение в клинике ФГБУ «НИИ онкологии СО РАМН» в 2006–2010 гг. Исследование проходило в соответствии с Хельсинкской декларацией 1964 г. (исправленной в 1975 и 1983 гг.) и с разрешения локального этического комитета института. Были получены информированные согласия пациентов. Более 85 % больных имели инвазивный протоковый рак, у 75 % размер опухоли составил 2–5 см (Т2) и у 64 % пациенток были лимфогенные метастазы. Иммуногистохимическое исследование включало оценку экспрессии рецепторов эстрогена, прогестерона и HER2/neu на опухолевых клетках.
Все больные получили 2–4 курса неоадъювантной химиотерапии по схемам FAC (фторурацил, доксорубицин, циклофосфан), CAX (циклофосфан, доксорубицин, кселода) или монотерапию таксотером [19]. Через 3–5 нед после НАХТ проводилась операция в объеме радикальной мастэктомии, радикальной резекции или секторальной резекции с аксиллярной лимфаденэктомией, затем больным проводили 4 курса адъювантной химиотерапии по схеме FAC. Лучевая терапия и/или гормонотерапия назначались по показаниям.
Эффективность предоперационной химиотерапии оценивали по критериям ВОЗ с помощью УЗИ и маммографии, которые проводили до лечения, после 2 курсов НАХТ и перед операцией. Регистрировали полную регрессию, частичную регрессию (уменьшение объема опухоли более чем на 50 %), стабилизацию (снижение объема менее чем на 50 % или увеличение не более чем на 25 %) и прогрессирование (увеличение объема опухоли более чем на 25 %). Для оценки экспрессии генов МЛУ были использованы биопсийные опухолевые об-
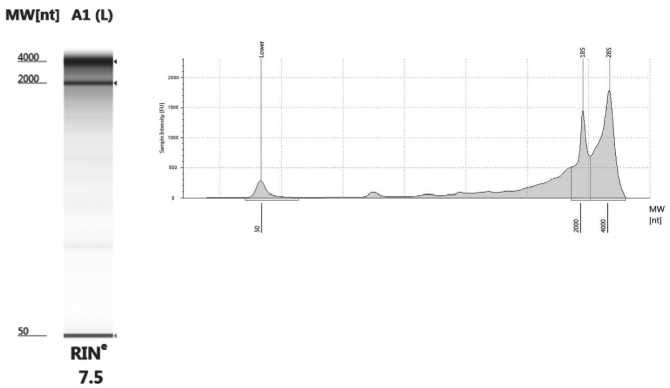
Рис. 1. Электрофореграмма и денситограмма тотальной РНК, выделенной из опухоли молочной железы при помощи набора Rneasy Mini Kit Plus (Qiagen, Germany). Капиллярный электрофорез выполнен на приборе TapeStation (Agilent Technologies, USA). Видны бенды 28S и 18S рибосомальной РНК, показатель целостности РНК – RIN (RNA Integrity Number) составил 7,5.
Спектрофотометрические показатели этого образца РНК – А260/280=1,95, А260/230=2,34; концентрация – 153 нг/мкл
разцы (~10 мм3), взятые до лечения под контролем УЗИ, а также операционный материал (~60–70 мм3). Больные, у которых в процессе НАХТ была достигнута полная морфологическая регрессия, не были включены в исследование, поскольку не представлялось возможным оценить уровень экспрессии генов МЛУ в опухоли после терапии. Частичная регрессия отмечена у 58 больных, стабилизация – у 39, прогрессирование – у 9 пациенток.
Исследуемые образцы помещали в раствор RNAlater (Ambion, USA) и сохраняли при температуре –80ºС (после 24-часовой инкубации при +4ºС) для дальнейшего выделения РНК. Тотальная РНК была выделена с помощью набора RNeasy mini Kit Plus, содержащего ДНК-азу I (Qiagen, Germany) с использованием ингибитора РНК-аз Ribolock (Fermentas, Lithuania). Качество выделенной РНК проверяли при помощи капиллярного электрофореза на приборе TapeStation (Agilent Technologies, USA), и RIN (RNA Integrity Number) составил 5,6–7,6 (рис. 1). Для получения кДНК на матрице РНК проводили реакцию обратной транскрипции с помощью набора RevertAid™ (Fermentas, Lithuania) со случайными гексануклеотидными праймерами в соответствии с инструкцией к набору. Остальные манипуляции, последовательность праймеров и методика оценки относительной экспрессии генов МЛУ описаны ранее [13]. В качестве результата оценивался уровень экспрессии 8 генов МЛУ:
ABCB1 , АВСВ2 , ABCC1 , ABCC2 , АВСС5 , ABCG1 , ABCG2 и MVP относительно гена-рефери GAPDH и нормальной ткани молочной железы, вычисляемый по методу Pfaffl (2001) [16] в биопсии до лечения и операционном материале после НАХТ. Сравнивая уровень экспрессии генов МЛУ до лечения и после НАХТ, определяли направление ее изменения: повышение или снижение в процессе НАХТ.
Для проверки гипотезы о значимости различий по частоте признака использовали критерий χ2 («STATISTICA 8.0», StatSoft Inc., США) и , показатель относительного риска – RR с 95 % доверительным интервалом (CI) вычислялся на калькуляторе http://vassarstats. net/ Для анализа безметастатической выживаемости использовались кривые выживаемости, построенные по методу Каплана–Майера [10]. Оценка значимости различий между группами производилась с помощью log-rank теста («STATIS-TICA 8.0», StatSoft Inc., США).
Результаты и обсуждение
На первом этапе были изучены закономерности изменения экспрессии комплекса основных генов МЛУ в процессе НАХТ и отмечено интересное явление: у большинства пациенток – 80 (75 %) случаев – экспрессия 5 из 8 изучаемых генов МЛУ (ABCB1, ABCC1, ABCC2, ABCG1 и ABCG2) изменялась в одном направлении и в строгом со- ответствии с эффектом НАХТ, т.е. наблюдалось снижение экспрессии всех 5 генов при хорошем ответе на НАХТ, либо повышение их экспрессии при отсутствии ответа. Это явление однонаправленного изменения экспрессии комплекса 5 генов МЛУ ABCB1, ABCC1, ABCC2, ABCG1 и ABCG2 в строгом соответствии с эффектом НХТ было названо нами градиентным феноменом. Примечательно, что вектор изменения экспрессии в процессе НАХТ именно этих генов показал наибольшую связь с эффективностью НАХТ [13]. У 25 % (26 из 106) больных не наблюдалось однонаправленного изменения экспрессии генов МЛУ в соответствии с эффектом НАХТ. Изменение экспрессии 2 или более из 5 выявленных генов МЛУ было разнонаправленным и не соответствовало эффекту НАХТ. По-видимому, у этих пациенток при проведении НАХТ происходило разобщение регуляции комплекса 5 генов МЛУ, и градиентный феномен не наблюдался.
Для того чтобы установить патогенетическую значимость градиентного феномена, была изучена его связь с безметастатической выживаемостью. Всех больных в зависимости от наличия/отсутствия градиентного феномена при проведении НАХТ разделили на две группы: 1-ю группу составили 80 больных с наличием феномена, 2-ю группу – 26 больных с его отсутствием. Сравниваемые группы больных не различались по основным клиникопатологическим параметрам (таблица). Можно отметить только тенденцию к увеличению частоты всречаемости отрицательного рецепторного статуса (ER- и PR-) у больных без градиентного феномена. Также группы не различались по среднему уровню экспрессии генов ABCB1 , ABCC1 , ABCC2 , ABCG1 и ABCG2 в биопсийном образце опухоли до лечения и операционном материале после НАХТ (данные не представлены). Это дает основания полагать, что наличие/отсутствие градиентного феномена не ассоциировано с основными клиникопатологическими параметрами, в том числе и молекулярными подтипами РМЖ, и позволяет корректно провести сравнение показателей безме-тастатической выживаемости в обеих группах.
На следующем этапе была изучена связь градиентного феномена с показателями безметаста-тической выживаемости. В общей группе из 106 обследованных пациентов отдаленные метастазы развились у 35 (33 %) больных в сроки 3–48 мес от момента постановки диагноза. Трехлетняя безметастатическая выживаемость составила 72 %, 5-летняя – 65 %. При наличии градиентного феномена 5-летняя безметастатическая выживаемость составила 73 % против 39 % у больных без градиентного феномена (log-rank test p=0,0018) (рис. 2А). Частота метастазирования – 25 % и 58 % соответственно (р=0,0021, критерий χ2). Это позволяет рассматривать наличие градиентного феномена у пациентов в качестве благоприятного прогностического фактора. При отсутствии градиентного феномена относительный риск развития гематогенных метастазов RR=1,77 (95% CI 1,11–2,83, уровень доверительной значимости с поправкой Йетса р=0,005).
Градиентный феномен является независимым прогностическим фактором, который успешно работает и позволяет дифференцировать больных по возможному исходу заболевания в таких, казалось бы, клинически «однородных» группах, как пациентки с местным распространением опухоли, соответствующей Т2 (рис. 2Б) (RR=2,32 (95 % CI 1,19–4,52), р=0,001), с наличием лимфогенного метастазирования (рис. 2В) (RR=2,45 (95 % CI 1,12–5,36), р=0,01) и больные с люминальным РМЖ (рис. 2Г) (RR=1,74 (95 % CI 0,90–3,38), р=0,03).
Таким образом, градиентный феномен имеет выраженную связь с прогрессией заболевания при раке молочной железы. Примечательно, что безме-тастатическая выживаемость была высокой (73 %) у больных РМЖ с наличием градиентного феномена при проведении НАХТ вне зависимости от того, достигнута частичная регрессия, стабилизация или прогрессирование. Низкая безметастатическая выживаемость (39 %) у больных с отсутствием градиентного феномена также не зависела от эффекта НАХТ (таблица). Это в определенной мере объясняет результаты исследования N. Wolmark et al. (2001) [22], которые показали, что только достижение полной морфологической регрессии при проведении НАХТ является благоприятным прогностическим фактором, а группы с частичной регрессией, стабилизацией или прогрессированием значимо не различались по показателям общей и безметастатической выживаемости.
Учитывая высокую прогностическую значимость градиентного феномена, можно предположить, что его наличие при проведении НАХТ является маркером сохранения в опухолевых клетках «нормальной» (сбалансированной) системы генной регуляции и клеточного ответа на химиопрепараты. Все 5 генов МЛУ локализованы в разных хромосомах (АВСВ1 – 7q21.12; ABCC1 – 16p13.11; ABCC2 – 10q24.2; ABCG1 – 21q22.3; ABCG2 – 4q22.1 http://www. , соответственно, они не являются сцепленными, но имеют общие сигнальные и метаболические пути [18]. Однонаправленность из- менений экспрессии этого комплекса 5 генов МЛУ показывает сохранение интактности системы их регуляции и, по всей вероятности, свидетельствует о сохранности в опухолевых клетках баланса многих систем жизнеобеспечения, реактивности и гибели.
Отсутствие градиентного феномена при проведении НАХТ предположительно является маркером серьезных нарушений в реакции на химиопрепараты (включая такие процессы, как
Таблица
Клинико-патологические параметры в группах больных рМж с наличием и отсутствием градиентного феномена
|
Клинико-патологические параметры |
Градиентный феномен |
p-value |
|
|
Есть |
Нет |
||
|
≤45 лет |
26 (33 %) |
10 (38 %) |
0,577 |
|
>45 лет |
54 (67 %) |
16 (62 %) |
|
|
Пременопауза |
45 (56 %) |
17 (65 %) |
0,412 |
|
Постменопауза |
35 (44 %) |
9 (35 %) |
|
|
т . 1–2 |
71 (89 %) |
21 (81 %) |
0,296 |
|
T3–4 |
9 (11 %) |
5 (19 %) |
|
|
N 0 |
32 (40 %) |
7 (27 %) |
0,229 |
|
N1–3 |
48 (60 %) |
19 (73 %) |
|
|
Инвазивный протоковый рак |
68 (85 %) |
23 (88 %) |
0,660 |
|
Другие гистотипы |
12 (15 %) |
3 (12 %) |
|
|
1-я степень злокачественности |
3 (5 %) |
1 (4 %) |
0,455 |
|
2-я степень злокачественности |
55 (87 %) |
19 (79 %) |
|
|
3-я степень злокачественности |
5 (8 %) |
4 (17 %) |
|
|
ER+ |
44 (59 %) |
10 (40 %) |
0,105 |
|
ER- |
31 (41 %) |
15 (60 %) |
|
|
PR+ |
46 (61 %) |
10 (40 %) |
0,063 |
|
PR- |
29 (39 %) |
15 (60 %) |
|
|
HER2 (- или +) |
53 (71 %) |
18 (72 %) |
0,971 |
|
HER2 (++ или +++) |
21 (29 %) |
7 (28 %) |
|
|
Люминальный |
52 (66 %) |
11 (44 %) |
0,129 |
|
Трижды негативный |
15 (19 %) |
9 (36 %) |
|
|
HER2 позитивный |
12 (15 %) |
5 (20 %) |
|
|
Уницентрический |
57 (71 %) |
15 (58 %) |
0,198 |
|
Мультицентрический |
23 (29 %) |
11 (42 %) |
|
|
НХТ по схемам CAX или FAC |
60 (75 %) |
22 (85 %) |
0,308 |
|
НХТ по схеме таксотер |
20 (25 %) |
4 (15 %) |
|
|
Частичная регрессия |
45 (56 %) |
13 (50 %) |
0,587 |
|
Стабилизация + прогрессирование |
35 (44 %) |
13 (50 %) |
|
Примечание: p-value – уровень статистической значимости различий по критерию χ2, в группе люминальный рак – в основном больные с люминальным В подтипом.
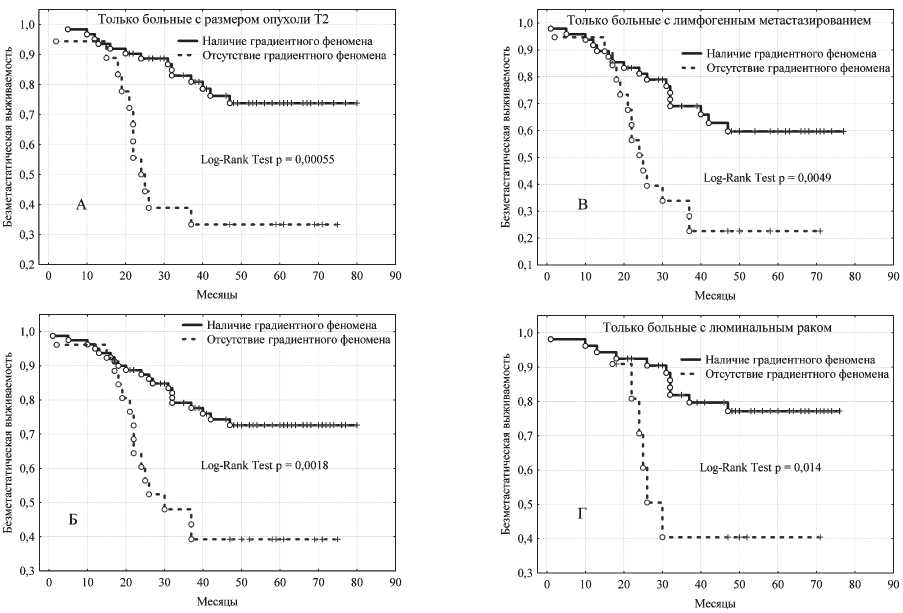
Рис. 2. Безметастатическая выживаемость больных РМЖ в зависимости от наличия/отсутствия градиентного феномена. А – общая группа, Б – больные с опухолью Т2, В – больные с лимфогенным метастазированием, Г – больные с люминальным раком молочной железы
метаболическая активация, детоксикация и удаление ксенобиотиков, остановка клеточного цикла, репарация и апоптоз) и в системе генной регуляции (дизрегуляция и дисбаланс) опухолевых клеток, показывая их высокий агрессивный потенциал. В отсутствие градиентного феномена при НАХТ могут играть роль такие нарушения процесса апоптоза, индуцируемого лекарственными средствами, как неадекватность ответа на химиопрепараты, вплоть до стимуляции пролиферации вместо апоптоза. Возможны нарушения в трансдукции сигнала вплоть до реверсии реактивности клеточных рецепторов адгезии (кадхеринов, интегринов, катенинов), рецепторов факторов роста, frizzled (G-белок связанных) рецепторов и др. [8]. Высокая внутриопухолевая гетерогенность, свойственная РМЖ, с большим числом клонов, несущих разные первичные и вторичные драйверные мутации и мутации-«пассажиры» [4, 23], может вносить вклад в формирование градиентного феномена. Например, драйверные мутации гена-супрессора опухо- левого роста ТР53 могут приводить к инактивации или парадоксальной реализации (активации вместо ингибирования и наоборот) многих клеточных функций, таких как апоптоз, репарация, регуляциия экспрессии множества генов, в том числе и генов МЛУ [1, 5, 6, 9, 14, 17]. При этом интересно, что частота мутаций ТР53 при РМЖ составляет 25 % [15], и это совпадает с частотой отсутствия у больных градиентного феномена (25 %). Полученные результаты свидетельствуют об актуальности дальнейшего исследования механизмов, определяющих наличие/отсутствие градиентного феномена, и его значения для клеточной регуляции.
Заключение
Установлен новый потенциальный прогностический фактор, не зависящий от основных клиникопатологических факторов прогноза – наличие или отсутствие градиентного феномена, который наблюдается при проведении НАХТ и характеризуется однонаправленными изменениями экспрессии генов МЛУ ABCB1 , ABCC1 , ABCC2 , ABCG1 и
ABCG2 в строгом соответствии с эффектом НАХТ. Наличие у больной РМЖ градиентного феномена является благоприятным прогностическим признаком независимо от клинического ответа на химиотерапию. Если градиентный феномен не наблюдался при проведении НАХТ, то у таких пациенток почти в 2 раза увеличивался относительный риск гематогенного метастазирования (RR=1,77). Предполагается, что градиентный феномен является маркером наличия или отсутствия в опухолевых клетках сбалансированной системы генной регуляции и реактивности на химиопрепараты. Это требует дальнейших исследований, актуальность которых обусловлена прогностической значимостью градиентного феномена. С практической точки зрения сочетание оценки эффекта предоперационной химиотерапии и градиента экспрессии генов МЛУ в процессе НАХТ может существенно повысить эффективность прогноза при раке молочной железы.
Работа поддержана грантом ФЦП «Научные и научно-педагогические кадры инновационной России на 2009–2013 гг.» по теме «Оптимизация стратегии химиотерапии рака молочной железы на основе факторов химиорезистентности и химиочувствительности», соглашение № 8291 от 27 августа 2012 г.
Автор выражает глубокую признательность за помощь в выполнении работы сотрудникам ФГБУ «НИИ онкологии» СО РАМН Н.В.Чердынцевой, Е.М. Слонимской, М.М. Цыганову, Е.Ю. Гарбукову, Е.В. Денисову, М.В. Завьяловой, В.М. Перельмутеру.


