Характер изменений вегетативной регуляции по вариабельности сердечного ритма при лапароскопических оперативных вмешательствах с использованием напряженного карбоксиперитонеума
Автор: Голубев Александр Александрович, Зуева Вера Александровна, Еремеев А.Г., Шпак Леда Викторовна, Кононова Алла Геннадьевна
Журнал: Хирургическая практика @spractice
Рубрика: Оригинальные исследования
Статья в выпуске: 3, 2013 года.
Бесплатный доступ
Целью исследования явилось изучение степени стрессорности напряженного карбоксиперитонеума в ходе лапароскопических оперативных вмешательств. Использовался метод кардиоинтервалографии. Кардиоинтервалограммы снимались на следующих этапах оперативного вмешательства: до наложения карбоксиперитонеума, перед десуфляцией, через 5 и 15 минут после десуфляции. Изучались статистические, временные и частотные показатели вариабельности сердечного ритма с анализом скаттер- и гистограмм. Как показали результаты исследования, исходные показатели характеризовались состоянием вегетативной нормотонии. На высоте карбоксиперитонеума выявлялась избыточность центральных (гипоталамических) и симпатических влияний на регуляцию сердечного ритма. Через 5 минут после десуфляции отмечалось снижение симпатического доминирования. Через 15 минут после десуфляции выявлен сдвиг вегетативного равновесия в парасимпатическую сторону с развитием у некоторых пациентов нарушений сердечного ритма. Обнаруженные изменения кардиоинтервалограмм связаны с расстройством газового состава крови и кислотно-щелочного равновесия, а также перераспределением крови в кровеносном русле, вызванным влиянием напряженного карбоксиперитонеума. Необходим поиск путей минимизации этого негативного влияния.
Напряженный карбоксиперитонеума, негативный эффект, вариабельность ритма сердца
Короткий адрес: https://sciup.org/142211525
IDR: 142211525 | УДК: 617-089
The nature of the changes of autonomic regulation on heart rate variability in laparoscopic operative interventions using a busy carboxyperitoneum
Aim of investigation was to study the stressful effect of tension carboxyperitoneum done in laparoscopic operative manipulations. Cardiointervalography method is used. Cardiointervalograms were taken during operation with the use of tension carboxyperitoneum at the following steps of operative manipulation: till obtaining carboxyperitoneum, before desufflation, after 5 and 15 minutes of desufflation. Statistical, temporary and frequent indications were studied with the analysis of scattergrams and gistograms. According to these indications conditions of vegetative balance is characterized. At the peak of carboxyperitoneum: was found abundant central (hypothalamic) and sympatheh,c effect on regulation of cardiac rhythm. After 5 minutes of desufflation: decrease of sympathetic effect was marked. After 5 minutes of desufflation: sympatho-parasympathetic effect changed into vagus dominance with occurrence of arrhythmia in some patients. The obtained characteristic changes of cardiointervalogram is related with the changes in gas composition, acid-base balance of blood, misdistribution of blood in vascular circuit which occurred under the effect of tension carboxyperitoneum. It is necessary to search ways for minimization of these negative effects.
Текст научной статьи Характер изменений вегетативной регуляции по вариабельности сердечного ритма при лапароскопических оперативных вмешательствах с использованием напряженного карбоксиперитонеума
Негативное влияние напряженного карбоксиперитонеума (НКП) на различные системы и органы при лапароскопических вмешательствах стало изучаться сравнительно недавно [1–6]. Известно, что в ходе выполнения лапароскопических операций с использованием НКП нарушается кислотнощелочной и газовый состав крови, происходит перераспределение объема циркулирующей крови в бассейнах нижней и верхней полых вен, сдавление нижней полой вены и нарушение кровотока в артериях и венах брюшной полости и забрюшинного пространства [3, 7–13]. При НКП страдает церебральный кровоток, повышается давление в спинномозговом канале и желудочках головного мозга [14–17]. При этом лапароскопические операции чаще всего проводятся пациен- там с уже имеющейся сопутствующей сердечно-сосудистой и бронхолегочной патологией [6, 18–20], поэтому необходимо минимизировать негативные эффекты применения НКП [1, 2, 6, 11, 20, 21]. Вместе с тем недостаточно изученными остаются вегетативные нарушения, развивающиеся у пациентов при наложении НКП, до настоящего времени не исследовались временные и частотные составляющие вариабельности сердечного ритма, не известны условия возникновения и длительность аритмогенной готовности миокарда в ходе лапароскопического вмешательства.
Целью исследования явилось изучение вегетативных нарушений и степени стрессорности напряженного карбоксипе-ритонеума при лапароскопических оперативных вмешательствах.
Материалы и методы
В условиях хирургического стационара ГБУЗ «Областная клиническая больница» г. Твери обследовано 90 пациентов (мужчин – 6, женщин – 84; средний возраст – 49±2 года). Всем больным проводилась лапароскопическая холецистэктомия с наложением НКП. Состояние вегетативной регуляции изучалось методом кардиоинтервалографии (прибор «КАД – 03», фирма «ДНК и К», Тверь) [23]. Кардиоинтервалограммы (КИГ) снимались в ходе операций с применением НКП на уровне 12 мм рт. ст. на следующих этапах оперативного вмешательства: исходно – до наложения НКП, перед десуфляцией, через 5 и 15 минут после десуфляции. Анализировалась выборка из 250 RR-интервалов, полученная при 10–15 минутной записи электрокардиограммы. Изучались статистические, временные и частотные показатели вариабельности сердечного ритма (ВСР) с визуальным анализом скаттер- и гистограмм [23]. Статистические параметры включали: частоту сердечных сокращений (ЧСС), дисперсию интервала QT (QTd), моду (Mo – наиболее часто встречающаяся величина кардиоинтервала RR (NN, с), амплитуду моды (AMo, % – количество наиболее часто встречающихся интервалов RR (NN) динамического ряда и характеризующий преимущественно активность симпатического отдела вегетативной нервной системы (ВНС); вариационный размах (ВР, ΔХ, с – разница между максимальным и минимальным значениями длительности кардиоинтервала, отражающий преимущественно парасимпатическую направленность регуляторных влияний), индекс напряжения (ИН, условных единиц (усл. ед.) – соотношение Мо, АМо и ΔХ – суммарный показатель напряженности регуляторных систем, чувствительный к усилению тонуса симпатического отдела ВНС), индекс вегетативного равновесия (ИВР, усл. ед. – отражает соотношение между активностью симпатического и парасимпатического отделов ВНС); вегетативный показатель ритма (ВПР, усл. ед. – позволяет судить о вегетативном балансе по активности автономного контура); показатель активности регуляторных процессов (ПАПР, усл. ед. – комплексная величина оценки ВСР, которая отражает степень централизации управления сердечным ритмом). Определялись показатели временного анализа: стандартное отклонение усредненных интервалов NN (SDNN, мс), квадратный корень из средней суммы квадратов разностей между последовательными NN интервалами (RMSSD, мс), пропорция NN интервалов между смежными, превосходящими 50 мс к общему количеству NN интервалов (рNN50, %), триангуляционный индекс ВСР (HRVtr, интеграл плотности распределения, отнесенный к максимуму плотности распределения). Из показателей частотного анализа оценивались: общая спектральная мощность реализации интервалов NN (TF, мс2), мощность сверхнизкочастотного компонента вариабельности ритма (VLF, мс2) и низкочастотного компонента (LF, мс2), мощность спектра высокочастотного компонента (HF, мс2), а также отношение низкочастотной к высокочастотной составляющей в абсолютных единицах (LF/HF, усл. ед., отражающее вагусносимпатический баланс) [1, 2, 23]. Достоверность полученных результатов оценивалась с помощью методов вариационной статистики с использованием t-критерия Стьюдента.
Результаты
Исходные показатели ВСР в группе наблюдения характеризовались нормальными ЧСС (76±5,0) и QTd (табл. 1), а математические, временные и частотные величины указывали на усиление вегетативной регуляции с незначительной активацией симпатического (увеличение АМо, ИН, ПАПР, ИВР при уменьшении SDNN, pNN50, HRVtr, HF) и парасимпатического (некоторое повышение по сравнению с нормой Мо, ВР, ВПР, RMSSD, TF при снижении LF) звеньев без явного преобладания каждого из них. Одновременное увеличение Мо с ВР и АМо с ИН при уменьшении соотношения LF/HF также подтверждало разнонаправленную симпатико-вагусную активацию. Полученные результаты, вероятно, объясняются формированием функционального антагонизма на фоне операционного стресса и премедикации. Усредненная скаттерграмма имела вид развернутого овала (нормотония), а график гистограмм чаще имел симметричную нормотоническую мономодальную форму. Таким образом, исходно суммарный эффект регуляции характеризуется вегетативным равновесием с устойчивым (тормозным) состоянием гуморально-гормонально-вегетативных звеньев регуляции и стабильностью тонуса блуждающего и симпатического нервов.
На высоте НКП регистрировалась синусовая тахикардия (ЧСС – 110±3,1 в мин.), укорочение QTd и признаки выраженной гиперсимпатикотонии (табл. 1) – уменьшение Мо при увеличении АМо и особенно значительно – ИН, ПАПР, ВПР, и ИВР (табл. 1). Это отражало преимущественно центральные (гипоталамические) и симпатические влияния на сердечный ритм. При этом практически полностью подавлялся автономный контур регуляции сердечного ритма (увеличение АМо и ИН в сочетании с многократным уменьшением ΔХ; р<0,001). Временные показатели отражали предельное напряжение регуляторных систем с вероятным риском сердечно-сосудистых осложнений: уменьшение SDNN, RMSSD, HRVtr (р<0,01). Известно, что снижение SDNN менее 50 мс и рNN50% ниже 1% и HRVtr менее 15 усл. ед. являются предикторами сердечных аритмий [1, 14], поэтому полученные данные подтверждали предположение об аритмогенном влиянии НКП. Частотный анализ обнаруживал значительное уменьшение вариабельности сердечного ритма, общей мощности спектра (TF) за счет практически исчезновения доли очень низкочастотных волн (VLF; р<0,001) и низкочастотных волн (LF; р<0,001), что отражало активацию гипоталамического (межсистемного) уровня центрального контура регуляции и свидетельствовало о напряжении механизмов гомеостаза. Усредненная скаттерграмма имела вид узкой точки, отражая ригидный ритм на фоне гипер-симпатикотонии, а график гистограмм у всех больных приобретал узкую мономодальную симпатотоническую (эксцессивную) форму. Таким образом, перед десуфляцией выявлена избыточность центральных (гипоталамических) и симпатических вли-
Динамика показателей ВСР у при лапароскопической холецистэктомии с применением НКП 12 мм рт. ст. (М+m)
Таблица 1
|
Показатели КИГ |
Период исследования |
|||
|
исходно |
Перед десуфляцией |
Через 5 минут после десуфляции |
Через 15 минут после десуфляции |
|
|
Математические |
||||
|
Mо, с |
0,97±0,005 |
0,56±0,012* |
0,45±0,01** |
0,49±0,36*** |
|
АМо, % |
42,0±4,1 |
98,0±3,2* |
87,3±3,2** |
81,6±11,2 |
|
ВР, с |
646,4±7,2 |
16,1±1,9* |
14,0±1,3** |
524,0±11,9 |
|
ИН, усл. ед. |
120,0±3,0 |
9091,1±21,5* |
6534,2±19,8** |
164,2±5,2 |
|
ПАПР, усл. ед. |
79,3±4,2 |
154,2±5,2* |
159,1±4,6** |
145,0±2,3 |
|
ВПР, усл. ед. |
13,6±0,2 |
201,5±0,85* |
189,6±0,36** |
13,9±0,4 |
|
ИВР, усл. ед. |
248,0±6,5 |
567,3±67,4* |
2693,0±54,6** |
196,2±9,3 |
|
Временные |
||||
|
SDNN, мс |
62,0±0,5 |
152,1±4,5* |
14,6±2,7** |
76,3±4,3 |
|
RMSSDмс |
32,1±0,7 |
16,4±0,45 |
1,2±0,3** |
93,5±1,5 |
|
pNN50% |
3,8±0,1 |
1,5±0,02* |
1,35±0,06** |
15,6±1,3*** |
|
HRVtr, усл. ед. |
12,1±1,2 |
4,3±0,12 |
3,9±0,01** |
2,6±0,04*** |
|
Частотные |
||||
|
TF, мс2 |
4678,0±45,9 |
4,21±1,51* |
5,3±1,5** |
6935,0±15,3 |
|
VLF, мс2 |
2166,2±15,2 |
1,23±0,01* |
3,3±0,003** |
1863,3±6,9 |
|
LF, мс2 |
814,3±19,8 |
0,98±0,02* |
0,93±0,09** |
1236,0±16,3 |
|
HF, мс2 |
301,2±25,6 |
4,53±0,15* |
0,99±0,26** |
3496,3±14,6 |
|
LF/HF |
2,02±0,015 |
0,74±0,12* |
0,97±0,32** |
0,45±0,09*** |
Достоверность различий (р<0,05-0,001) указана между периодами: перед десуфляцией (*), через 5 (**) и 15 (*** ) минут после десуфляции и исходными показател ями
яний на сердечный ритм, автономно – центральный вариант перенапряжения вегетативной регуляции с блокадой парасимпатических влияний, значительным уменьшением вариабельности сердечного ритма и формированием акцентированного симпатического синергизма, на пределе функциональных возможностей поддерживающего межсистемные гомеостатические механизмы.
Через 5 минут после десуфляции на фоне синусовой тахикардии (ЧСС – 119±2,1 в мин.) несколько улучшилась длительность QTd (табл. 1). Сохранялась выраженная симпатикотония (высокие значения ИН, АМо, ПАПР, ИВР, хотя и меньшие, по сравнению с предыдущим периодом исследования; р<0,05). Снижение ВПР отражало незначительное нарастание парасимпатической активности. Следовательно, уже в первые 5 минут после десуфляции выявлено ослабление степени централизации управления системы кровообращения и сохранение сдвига симпато-парасимпатического баланса в симпатическую сторону, несмотря на некоторое усиление вагусных влияний. Временные показатели практически не изменились (RMSSD, pNN50; р>0,05), оставаясь резко сниженными, указывая на сохраняющуюся ригидность сердечного ритма при очень незначительном увеличении SDNN и HRVtr. Частотный анализ ВСР показал недостоверное (р>0,05) увеличение общей мощности спектра (TF) за счет наибольшей доли очень низких частот (VLF – 65% от TF), подтверждало сохранение симпати-котонии. При этом увеличение доли высокочастотной составляющей мощности спектра (HF с 46 до 56%; р<0,02) свидетельствовало об усилении вагусной регуляции сердечного ритма. Вагосимпатический баланс был несколько ближе к равновесию (LF/HF=0,97; р>0,05), однако усредненная скаттерграмма также оставалась в виде сжатого (симпато-тонического) авторегрессивного «облака», а гистограмма также имела мономодальную (эксцессивную) форму. Таким образом, через 5 минут после десуфляции отмечается незначительное ослабление гиперсимпатикотонии и усиление вагусных влияний, свидетельствующие о сохраняющейся напряженности регуляторных систем с возможным срывом адаптации и переходом на автономный контур регуляции сердечного ритма, что создает условия для развития сердечных аритмий.
Через 15 минут после десуфляции (табл. 1) у 9 (10%) больных на фоне уменьшения тахикардии (ЧСС 98±1,3 в мин.) были выявлены нарушения сердечного ритма: желудочковая экстрасистолия – у 6 (в том числе бигеминия – у 3), предсердная экстрасистолия – у 3 пациентов. Повышался, но не достигал нормы QTd, а статистический анализ выявил нормальные значения ВПР и стремящийся к норме ИН, при этом высокие значения ПАПР (в 3 раза), АМо (в 2 раза) и ИВР свидетельствовали об ослабленной, но сохраняющейся централизации управления сердечным ритмом и выраженном напряжении гомеостаза. С другой стороны, временные показатели в виде увеличения RMSSD (в 3 раза) pNN50 (в 2 раза), при сниженных значениях HRVtr и, SDNN указывают на парасимпатическое доминирование. Выявленную разнонаправленность вегетативных влияний подтверждают частотные характеристики нарушения стационарности сердечного ритма. Резкое увеличение общей мощности спектра (TF; р<0,001 по сравнению с предыдущим периодом наблюдения), повышение до 50% доли высокочастотной вагусной составляющей спектра (HF) и сохраняющееся снижение LF/HF (до 0,45) отражало нарастающую дискоор-динацию в функционировании сердечно-сосудистой системы, наступающую на фоне мощных эфферентных парасимпатических влияний. Следовательно, через 15 мин. после десуфляции, симпатическое доминирование сменяется парасимпатическим, с угрозой развития нарушений сердечного ритма на пике ваго-тонии. Критериями прогностического риска в этих случаях являются признаки нарастающего парасимпатического доминирования (увеличение DX, RMSSD, pNN50, TF, HF при снижении ИН). Усредненная скаттерграмма приобретала вид рассеянного «облака», что также подтверждает усиление вагусных влияний, а гистограмма чаще имела полимодальную (ваготоническую) форму.
Как показал дальнейший анализ полученных результатов, описанные нарушения ВСР при использовании карбоксипе-ритонеума 12 мм рт. ст., регистрировались не только у пожилых, но и у лиц среднего и молодого возраста. Статистических различий показателей ВРС в возрастных группах получено не было (р>0,05).
Клинический пример: Пациентка З. Возраст – 57 лет, индекс массы тела (ИМТ) – 36. Сопутствующие заболевания: варикозное расширение вен нижних конечностей, ожирение экзогенно-конституциональное II степени. Уровень КП – 12 мм рт. ст. Длительность операции – 40 минут.
Исходно (рис. 1): нормальная ЧСC и QTd сочетаются с математическими признаками вегетативного равновесия (Mo, AMo, ВР, ИН, ВПР и ИВР соответствуют норме) с устойчивым состоянием вегетативной регуляции и стабильностью тонуса симпатического и блуждающего нервов, что, возможно, связанно с адекватной премедикацией. Этому соответствуют данные временного анализа ВСР: SDNN, RMSSD, pNN50 и HRVtr указывают на то, что суммарный эффект регуляции соответствует вегетативной эйтонии. Согласно частотному анализу, суммарный уровень активности отражает отсутствие напряженности регуляторных систем (TF, VLF в норме) и сниженную активность симпатического (LF) компонента и парасимпатического (HF) отдела ВНС с некоторым преобладанием симпатического (LF/HF=2,1).
Скаттерграмма имеет вид «облака» овальной формы, а гистограмма – нормотонический мономодальный тип. Таким образом, у пациентки исходно выявляется вегетативное равновесие со стабильностью тонуса блуждающего и симпатического нервов с некоторым преобладанием симпатического отдела.
Перед десуфляцией (рис. 2): регистрируется синусовая тахикардия (ЧСС – 110 в мин.), укорочение QTd в 11 раз (до 15 мс) и синдром выраженной симпатикотонии (уменьшение Мо при увеличении АМо и особенно значительно – ИН (в 139 раз), ПАПР (в 3 раза), ВПР (в 57), и ИВР (в 100 раз), указывая на избыточность центральных и симпатических влияний на сердечный ритм. При этом резкое увеличение АМо и ИН в сочетании с многократным уменьшением ΔХ (практически до 0) указывают на развитие автономно-центрального варианта перенапряжения вегетативной регуляции с возможным риском сердечно-сосудистых нарушений. Временные показатели также отражают предельное напряжение регуляторных систем, когда главную роль играют высокие уровни управления с полным подавлением активности автономного контура и блокадой парасимпатических влияний (уменьшение SDNN в 60 раз, RMSSD – в 20 раз, HRVtr – в 13 раз), при этом резкое снижение SDNN и HRVtr являются предиктором сердечных аритмий. Частотный анализ обнаруживает значительное уменьшение вариабельности сердечного ритма (RRd=6 мс), общей мощности
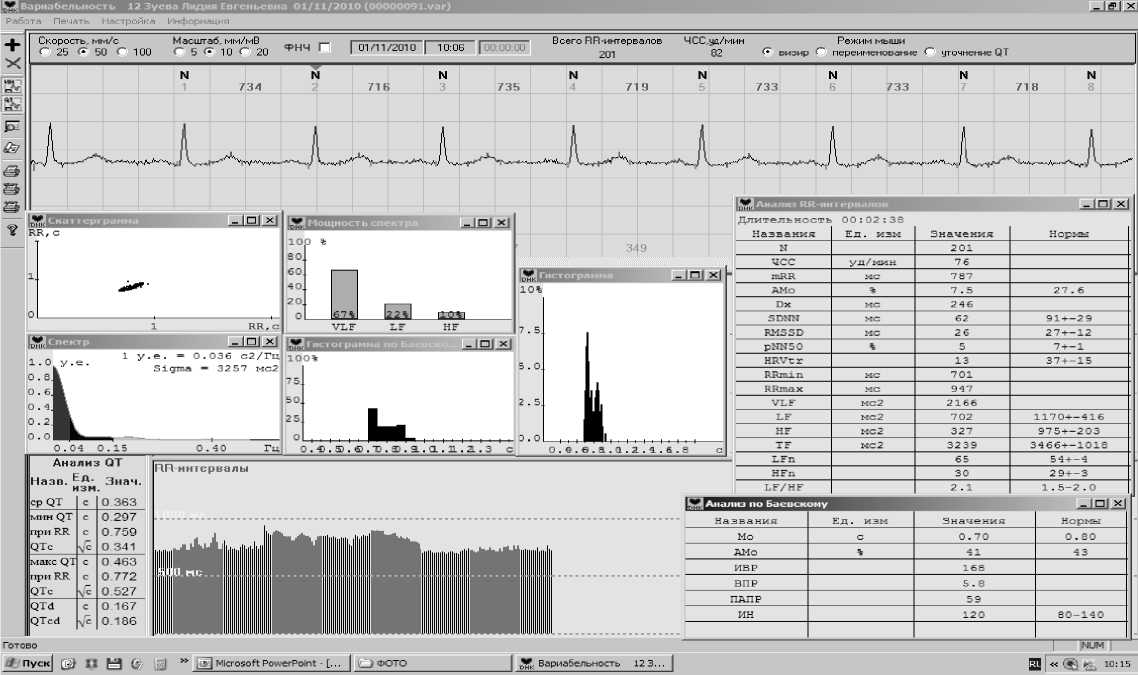
Рис. 1. Исходная кардиоинтервалограмма
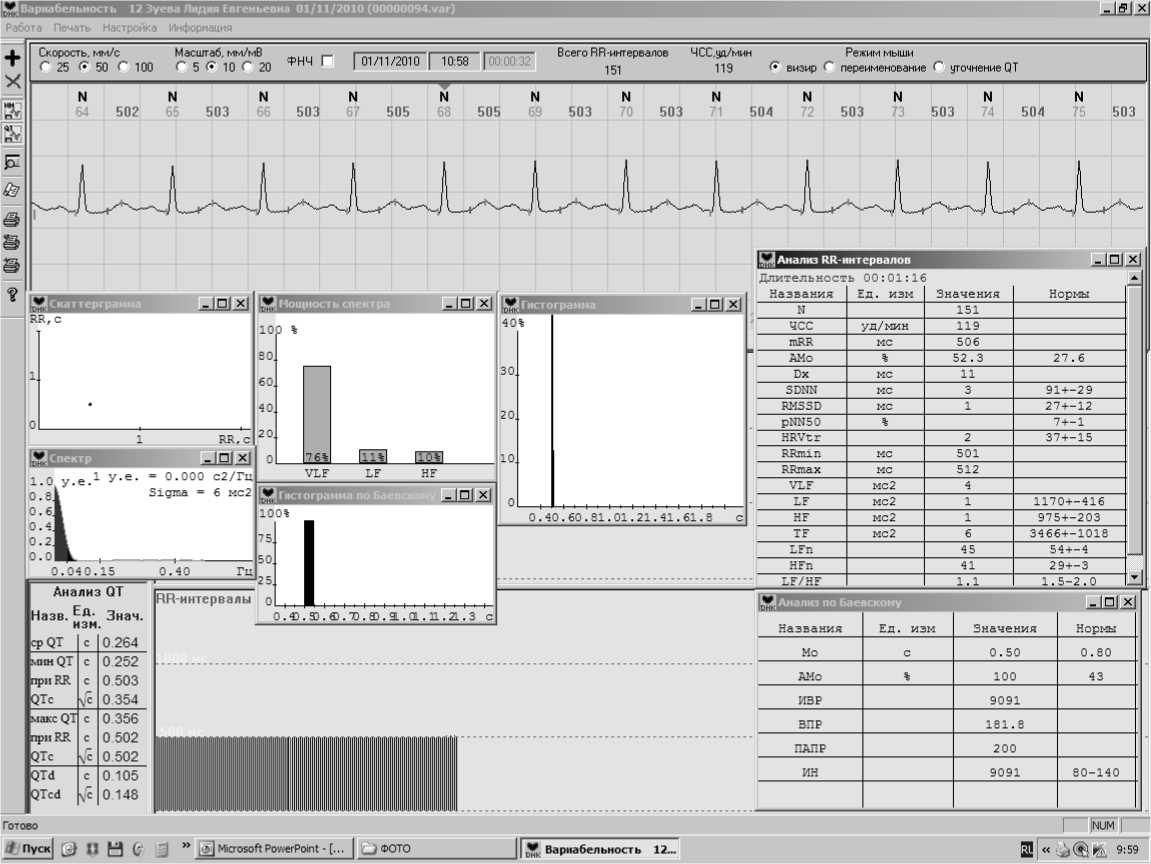
Рис. 2. Кардиоинтервалограмма перед десуфляцией
спектра (TF=1,0) за счет уменьшения доли очень низкочастотных волн (VLF – 14% от TF), что отражает активацию гипоталамического (межсистемного) уровня центрального контура регуляции и свидетельствует о напряжении механизмов гомеостаза. Усредненная скаттерграмма имеет вид точки, отражая ригидный ритм на фоне высокой симпатической активности, а гистограмма приобретает симпатотоническую (эксцессив-ную) форму. Таким образом, перед десуфляцией у больной подтвержден синдром выраженной симпатикотонии с преобладанием центрального контура регуляции сердечного ритма и блокадой вагусных влияний с формированием аритмогенной готовности миокарда.
Через 5 мин. после десуфляции (рис. 3), несмотря на увеличение тахикардии (119 в мин.), несколько улучшилась длительность QTd (0,105 c). Остаются без изменения влияния гуморального канала регуляции и выраженность симпатикотонии
(уменьшение Мо и увеличение АМо). Снизился (на 55%), но остается увеличенным ИН, указывая на ослабление степени централизации управления системы кровообращения, чему соответствует уменьшение ПАПР (так же на 54%). При этом снижение ВПР отражает некоторое нарастание парасимпатической активности. Следовательно, уже в первые 5 минут после десуфляции уменьшается напряженность надсегментарных структур, стимулирующих сердечно-сосудистую систему, но сохраняется сдвиг симпатопарасимпатического баланса в симпатическую сторону, несмотря на некоторое усиление вагусных влияний. Временные и частотные показатели остаются на низком уровне, отражая снижающуюся способность синусового узла отвечать на вегетативную стимуляцию. При этом временные характеристики практически не изменяются (RMSSD, pNN50), оставаясь резко сниженными и указывая на сохраняющуюся ригидность сердечного ритма при некотором увеличе-
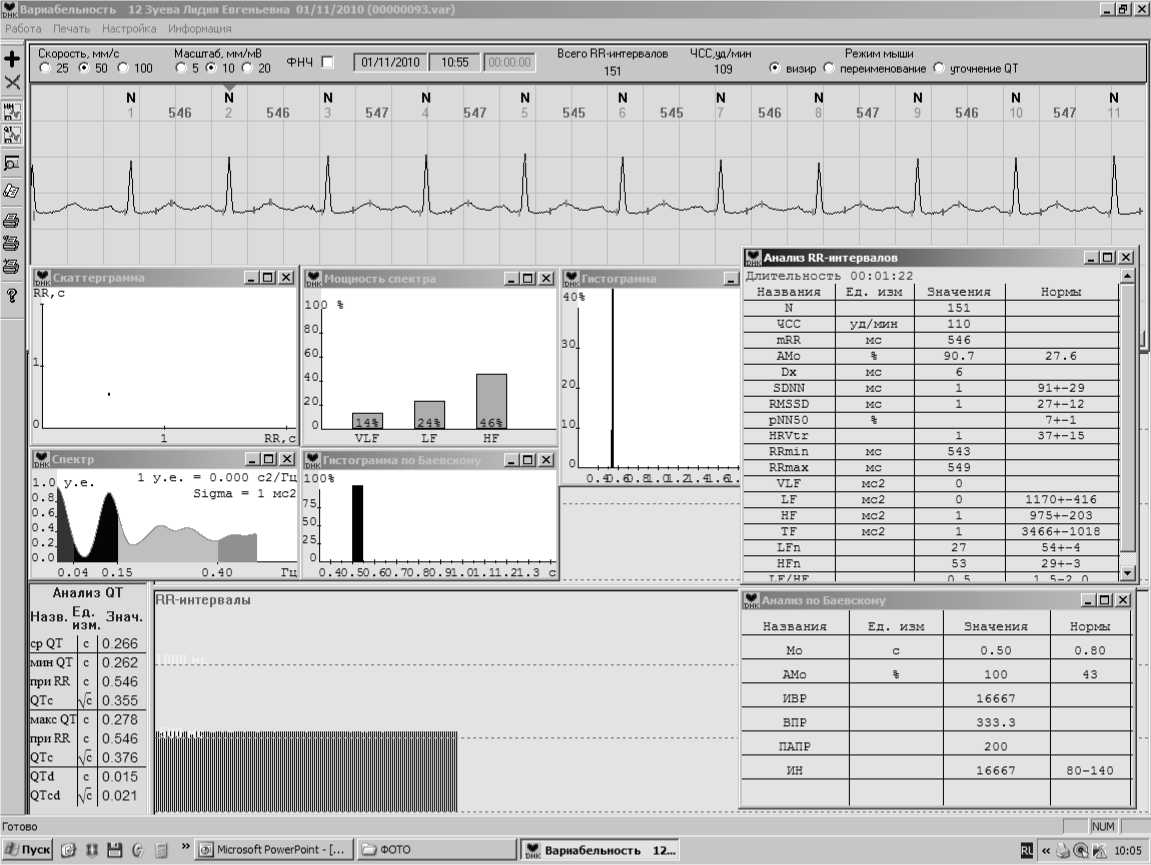
Рис. 3. Кардиоинтервалограмма через 5 минут после десуфляции
нии SDNN и HRVtr. Частотный анализ ВСР свидетельствует о слабом, но все же увеличении общей мощности спектра (TF) за счет наибольшей доли очень низких частот (VLF – 76% от TF), механизм появления которых состоит в снижении восприимчивости органа-мишени к насыщающим влияниям усиленной симпатикотонии на синусовый узел и в меньшей мере – сдвигом в сторону низкочастотной части спектра (доля HF снизилась с 46% до 10% от TF). Этому соответствует слабое преобладание симпатических влияний с приближением вагосимпатического баланса к равновесию (LF/HF=1,1). Тем не менее, скаттерграмма остается в виде сжатого (симпатотонического) авторегрессивного «облака», а гистограмма также имеет симпатотоническую (эксцессивную) форму. Следовательно, через 5 минут после десуфляции отмечается ослабление центральных (гипоталамических) влияний на сердечный ритм и реакции синусового узла на симпатическую стимуляцию, что создает относитель- ное усиление вагусных влияний и приближение реципрокных отношений к равновесию (LF/HF=1,1).
Через 15 минут после десуфляции (рис. 4) зарегистрировано урежение ЧСС (82 в мин.) и появление желудочковой бигеминии, которые сменяются тахикардией (106 в мин., а затем – восстановлением регулярного синусового ритма. Увеличение ВСР и, следовательно, дыхательных парасимпатических волн высокой частоты подтверждается удлинением RRd и восстановлением до нормы QTd. При этом статистический анализ выявляет однозначность сдвигов всех показателей в сторону парасимпатикото-нии: слабое увеличение Мо, значительное – ΔХ и многократное снижение ИВР (в 85 раз), ВПР (в 60 раз), ИН (в 94 раза) и ПАПР (в 1,5 раза), что указывает на сдвиг вегететативного равновесия в парасимпатическую сторону и усиление автономного контура регуляции при недостаточности центральных и симпатических влияний на синусовый узел. Однонаправленное изменение всех
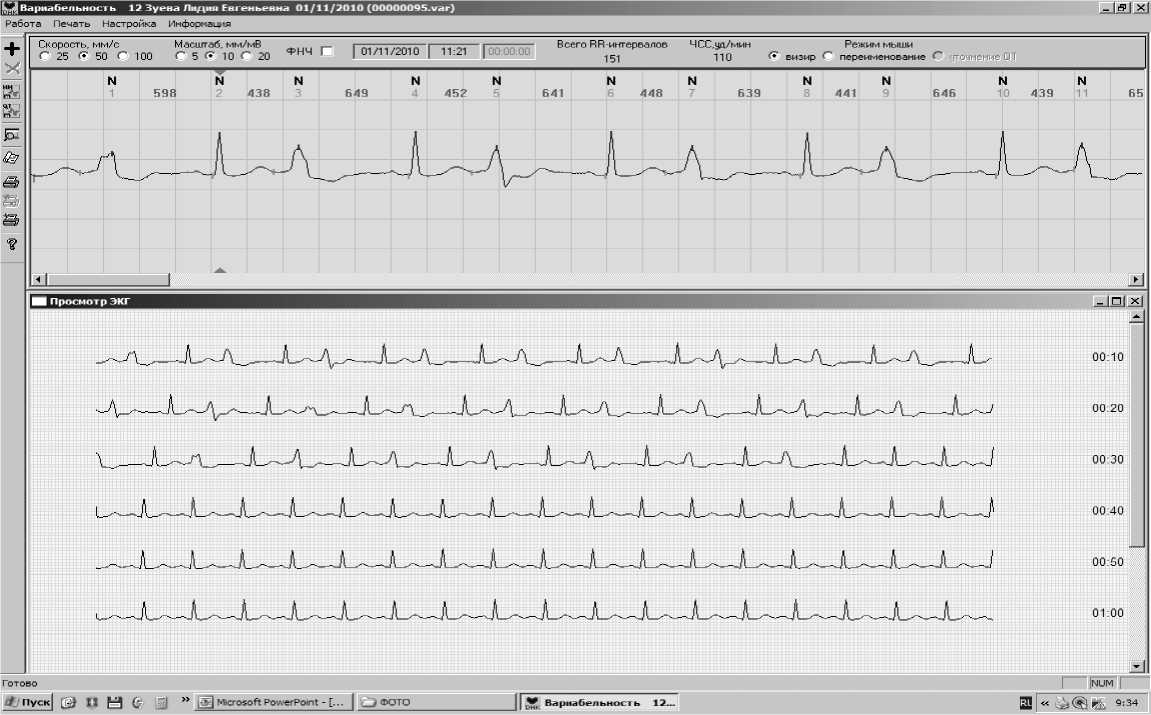
Рис. 4. Кардиоинтервалограмма через 15 минут после десуфляции
временных показателей в виде увеличения SDNN (в 33 раза), RMSSD (в 12 раз) и pNN50 (в 30 раз) при слабой симпатической активности также указывает на парасимпатическое доминирование. Механизм этого вегетативного сдвига раскрывает частотные характеристики нарушения стационарности сердечного ритма. Значительное увеличение общей мощности спектра (TF в 3,5 раза больше нормы и почти в 2000 раз больше показателей при синусовом ритме и 5-минутного периода десуфляции) в связи с увеличением вариабельности ритма, и наибольшей среди всех периодов исследования доли высокочастотной вагусной составляющей спектра (HF – 42%). Увеличение VLF даже в 2 раза имеет самостоятельное значение для оценки межсистемного гипоталамического уровня регуляции, а увеличение в 2000 раз отражает нарастающую дискоординацию в функционировании сердечно-сосудистой системы, наступающую на фоне мощных эфферентных парасимпатических влияний (увеличение HF в 2 раза по сравнению с нормой и снижение LF/HF до 0,5). Следовательно, через 15 мин. после десуфляции симпатическое доминирование сменяется парасимпатическим с нарушением сердечного ритма и развитием желудочковой бигеминии. Скат-терграмма приобретает вид рассеянного ваготонического «облака», а гистограмма становится широкой полимодальной.
Выводы
-
1. При лапароскопической холецистэктомии с наложением НКП исходная вегетативная нормотония «на высоте» использования карбоксиперитонеума перед десуфляцией сменяется гиперсимпатикотонией, а затем – нарастающей ваготонией, отражая срыв механизмов адаптации.
-
2. У ряда пациентов (9%) применение НКП может привести к срыву регуляции сердечного ритма и развитию аритмий.
-
3. Динамические изменения кардиоинтервалограмм на этапах выполнения лапароскопической холецистэктомии при использовании НКП свидетельствуют, что аритмогенная готовность миокарда возникает перед десуфляцией и максимальна – через 15 минут после десуфляции, что требует обязательного интраоперационного и периоперационного мониторирования сердечного ритма.
-
4. Критериями прогностического риска сердечных аритмий при НКП являются признаки нарастающего парасимпатического доминирования: увеличение DX, RMSSD, pNN50, TF, HF при снижении ИН.
-
5. Выраженные нарушения ВСР при использовании карбок-сиперитонеума 12 мм рт. ст. регистрируются не только у пожилых, но и у лиц среднего и молодого возраста.
-
6. Проблема негативного влияния карбоксиперитонеума диктует необходимость поиска способов минимизации этого влияния у пациентов, оперируемых с применением лапароскопических методик.
КЛИНИЧЕСКИЕ СЛУЧАИ. ДИСКУССИИ
Список литературы Характер изменений вегетативной регуляции по вариабельности сердечного ритма при лапароскопических оперативных вмешательствах с использованием напряженного карбоксиперитонеума
- Голубев А.А. Способ создания контролируемого ненапряженного карбоксиперитонеума, снижающего неблагоприятные влияния высокого внутрибрюшного давления на регуляцию сердечного ритма//Альманах института хирургии имени А.В. Вишневского. Материалы XIV Съезда Общества Эндоскопических хирургов России. М.: ООО «Вими реклама», 2011. Т. 6, №1 (1). С 16.
- Голубев А.А., Шпак Л.В., Зуева В.А. и др. Вариабельность сердечного ритма в зависимости от уровня давления в брюшной полости при лапароскопической холецистэктомии//Альманах института хирургии имени А.В. Вишневского. Материалы XIV Съезда Общества Эндоскопических хирургов России. М.: ООО «Вими реклама», 2011. Т. 6, №1 (1), С 17.
- Сердаров Н.О. Изменение функции внешнего дыхания при лапароскопической холецистэктомии//Материалы XI съезда хирургов Российской федерации. Волгоград, 25-27 мая 2011. С. 307-308.
- Сало В.Н., Маликов Я.В. Изучение внутрибрюшного давления в эксперименте и клинике//Материалы XI съезда хирургов Российской федерации. Волгоград, 25-27 мая 2011. С. 299-300.
- Коссович М.А., Бирюков А.Ю., Кузовахо В.В. Использование техники выполнения лапароскопической холецистэктомии в традиционной хирургии как фактор улучшения результатов лечения пациентов с холелитиазом.//Материалы XI съезда хирургов Российской федерации. Волгоград, 25-27 мая 2011. С. 174-175.
- Касумьян С.А., Некрасов А.Ю., Зубарев В.В. и др. Применение веерообразного лапаролифта в лечении острого холецистита у лиц пожилого и старческого возраста//Материалы XI съезда хирургов Российской федерации. Волгоград, 25-27 мая 2011. C. 158-159.
- Lindberg F., Bergqvist D., Rasmussen I. Incidence of thromboembolic complications after laparoscopic cholecystectomy: review of the literature//Surg. Endosc. 1997. Vol. 11.
- Мальчиков А.Я., Сигал З.М. Интраорганная гемопульсомоторо-оксидинамика при лапароскопических операциях//Эндоскопическая хирургия. Материалы IX Всероссийского съезда по эндоскопической хирургии. М.: Медиасфера, 2006. С. 81-82.
- Баулин А.А. Спорные вопросы профилактики послеоперационной тромбоэмболии легочной артерии//Альманах института хирургии имени А.В. Вишневского. Материалы XIV Съезда Общества Эндоскопических хирургов России. М.: ООО «Вими реклама», 29011. Т. 6, №1 (1). С. 13-14.
- Сердаров Н.О. Влияние карбоксиперитонеума на функцию внешнего дыхания//Альманах института хирургии имени А.В. Вишневского. Материалы XIV Съезда Общества Эндоскопических хирургов России. М.: ООО «Вими реклама», 2011. Т. 6, №1 (1). С. 23.
- Зуева В.А., Голубев А.А. и др. О проблемах тромбоэмболии легочной артерии при лапароскопической холецистэктомии//Сборник научных работ шестой научно-практической конференции врачей г. Твери, Тверской области и центрального Федерального округа России с участием ведущих специалистов Российской Федерации. г. Тверь, 1-2 апреля 2011. С. 53-56.
- Голубев А.А. и др. Тромбоэмболические осложнения при лечении желчекаменной болезни//Эндоскопическая хирургия. 2006. Т. 12, №2. С. 33-34.
- Голубев А.А., Еремеев А.Г., Волков С.В и др. Влияние напряженного карбоксиперитонеума на газовый состав и КЩС крови пациентов при выполнении лапароскопической холецистэктомии//ЦентральноАзиатский медицинский журнал. 2010. Т. XVI, Прил. 3. С. 22-24.
- Rosenthal R.J. et al. Intracranial pressure: effects ofpneumoperitoneum in a large-animal model//Surg. Endosc. 1997. Vol. 11. P 376-380.
- Halverson A. Evaluation of mechanism of increased intracranial pressure with insufflation//Surg. Endosc. 1998. Vol. 12. P. 266-269.
- Lindberg F., Bergqvist D., Rasmussen I. Laparoscopy and major retroperitoneal vascular injuries (MRVI)//Surg. Endosc. 1997. Vol. 11.
- Токин А.Н. Новые технологии как средство профилактики послеоперационных осложнений при лапароскопической холецистэктомии//Материалы XI съезда хирургов Российской федерации. Волгоград, 25-27 мая 2011. С. 337.
- Малоштан О.В. Особливоси виконання лапароскошчних втручань у хворих iз супровщною патолопею сердцево-судинно! системи//Шпитальна хiрургiя. 2001. № 3. С. 45-47.
- Хитарьян А.Г. и соавт. Пути прогнозирования и профилактики послеоперационных осложнений лапароскопической холецистэктомии у больных с сопутствующей кардио-респираторной патологией//Эндоскопическая хирургия. Материалы XIV Всероссийского съезда по эндоскопической хирургии. М.: Медиасфера, 2011. С. 56.
- Голубев А.А., Еремеев А.Г. и др. Использование малоинвазивных технологий в лечении пациентов с калькулезным холециститом//Центрально-Азиатский медицинский журнал. 2010. Т. XVI, Прил. 3. С. 24-26.
- Дазаев Р.С. Оптимизация современных методов хирургического лечения желчнокаменной болезни и ее осложнений. М., 2000. 305 c.
- Измайлов С.Г., Рябков М.Г., Лукоянычев Е.Е. Возможности хирургической коррекции интраабдоминальной гипертензии в послеоперационном периоде при закрытой лапаротомной ране//Материалы XI съезда хирургов Российской федерации. Волгоград, 25-27 мая 2011. C. 141.
- Л.В.Шпак. Кардиоинтервалография и ее клиническое значение. Учебно-методическое пособие для врачей, интернов, ординаторов, аспирантов, терапевтов, кардиологов. Тверь: Издательство «Фактор», 2002. 232 с.


