Характеристика микрофлоры пациентов онкологического профиля с постоперационными инфекционными осложнениями
Автор: Правосудова Наталья Александровна, Мельников Виктор Львович, Итяева Людмила Николаевна, Пантелеева Елена Николаевна
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 4, 2022 года.
Бесплатный доступ
Исследована микрофлора патологического материала пациентов с послеоперационными инфекциями и проведен анализ устойчивости выделенных штаммов к противомикробным препаратам. Оценку биологических свойств и антибактериальную чувствительность выделенных бактериальных штаммов осуществляли по общепринятым методикам, регламентирующим работу микробиологической лаборатории. В исследование были включены 83 пациента отделения абдоминальной онкологии, проходивших хирургическое лечение в 2017-2021 гг. В патологическом материале преобладала грамотрицательная микрофлора (р
Микрофлора, послеоперационные инфекции, устойчивость к противомикробным препаратам
Короткий адрес: https://sciup.org/147239295
IDR: 147239295 | УДК: 579.61 | DOI: 10.17072/1994-9952-2022-4-294-299
Microflora characteristics of oncological patients with postoperative infectious complications
The microflora of the pathological material from patients with postoperative infections was studied and the resistance of isolated strains to antimicrobial agents was analyzed. The biological properties and antibacterial sensitivity of the bacterial strains isolated during the studies was assessed according to generally accepted methods that regulate the work of a microbiological laboratory. The study included 83 patients of the abdominal oncology department who underwent surgical treatment in 2017-2021. During this period, gram-negative micro-flora prevailed in the pathological material (p
Текст научной статьи Характеристика микрофлоры пациентов онкологического профиля с постоперационными инфекционными осложнениями
Инфекции, связанные с оказанием медицинской помощи (ИСМП), – это любые клинически выраженные заболевания микробного происхождения, которые поражают больного в результате его поступления в больницу или обращения за медицинской помощью вне зависимости от появления симптомов заболевания у пациента во время пребывания в стационаре или после его выписки [Тутельян, Акимкин, Марьин, 2019]. Особенно остро проблема ИСМП стоит в отделениях хирургического профиля. В Пензенской обл. в 2020 г. зарегистрировано 837 случаев инфекций, связанных с оказанием медицинской помощи, из них 37.8% – в хирургических стационарах [О состоянии …, 2021].
Бактерии обладают высокой пластичностью и способностью быстро приспосабливаться к различным условиям обитания. В медицинских учреждениях различного профиля возможно формирование определенного микроценоза, представители которого способны вызывать инфекционные осложнения у пациентов. На формирование микроценоза лечебных учреждений влияет микрофлора пациентов, сотрудников лечебных учреждений и объектов окружающей среды. Необходимо учитывать, что в отделениях разной направленности формируется определенный набор микроорганизмов, зависящий от вида хирургического вмешательства [Правосудова и др., 2016; Кудлай и др., 2022]. Кроме того, микрофлора лечебных учреждений постоянно подвергается воздействию антимикробных препаратов. В связи с этим микробный пейзаж отделения, устойчивость бактерий к антимикробным препаратам могут меняться. Мониторинг микрофлоры в отделениях лечебных учреждений является обязательным методом профилактики ИСПМ [Светличная и др., 2014; Захватова и др., 2022].
Цель настоящей работы - анализ микрофлоры пациентов с постоперационными инфекционными осложнениями.
Материал и методы исследований
Работа выполнена на базе отделения абдоминальной онкологии Онкологического диспансера г. Пензы. С 2017 по 2021 г. было зарегистрировано 83 случая послеоперационных осложнений в этом отделении. У пациентов были изучены мазки из ран, брюшной полости, трахеи и дренажей.
Посев клинического материала проводили на плотные питательные среды (кровяной агар, агар Эндо, Сабуро, ЖСА, ЦПХ-агар) и в среды обогащения (глюкозный бульон, полужидкую модифицированную среду СКС-199).
Оценку биологических свойств и антибактериальную чувствительность выделенных бактериальных штаммов осуществляли по общепринятым методикам, регламентирующим работу микробиологической лаборатории [Определение чувствительности …, 2015, 2018]. В процессе идентификации штаммов использованы наборы реагентов «Пластина биохимическая, дифференцирующая энтеробактерии (ПБДЭ)» (ООО «НПО «Диагностические системы», Россия), «Пластина биохимическая, дифференцирующая стафилококки (ПБДС)» (ООО «НПО «Диагностические системы», Россия) и микробиологический анализатор VITEK 2 – compact («bioMérieux», Франция). Определение чувствительности к антибактериальным препаратам диско-диффузионным методом проводили на среде Мюллера–Хинтона с помощью аппарата для определения стандарта мутности бактериальной взвеси (DensiChek plus «bioMérieux», Франция) и дисков с антибиотиками (BIOANALYSE, Турция и Mast Group Ltd., Великобритания).
Статистическую обработку данных выполняли, используя ᵪ2.
Результаты и их обсуждение
Распределение различных групп микроорганизмов в патологическом материале у пациентов отделения абдоминальной онкологии в течение 2017-2021 гг. представлено на рис. 1. В указанный период в патологическом материале преобладала грамотрицательная микрофлора (р<0.05). Повышение числа выделенных штаммов микроорганизмов в 2018 г. связано не только с ростом количества пациентов с постоперационными осложнениями (ПОИ) (см. рис. 1), но и c формированием полиинфекций (таблица).
Количество случаев послеоперационных осложнений и полиинфекций в 2017-2021 гг. [The number of postoperative complication and polyinfection cases in 2017-2021]
|
Показатель |
2017 |
2018 |
2019 |
2020 |
2021 |
|
Количество случаев ПОИ |
18 |
25 |
11 |
7 |
22 |
|
Количество полиинфекций |
5 |
17 |
6 |
3 |
11 |
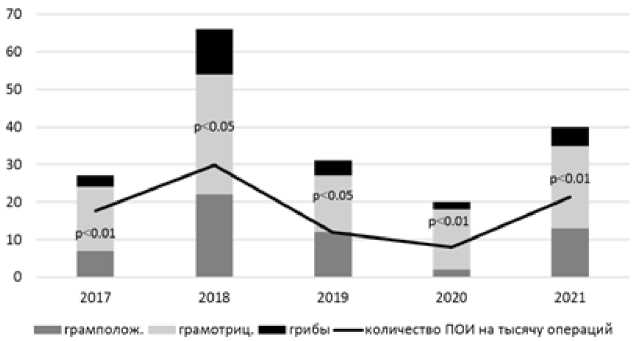
Рис. 1. Распределение микрофлоры (%) в патологическом материале у пациентов отделения абдоминальной онкологии в течение 2017-2021 гг.
[Distribution of microflora in 2017-2021]
В обследованном материале грамотрицательные бактерии были представлены следующими видами: Acinetobacter baumannii , Citrobacter braakii , Enterobacter asburiae , E. cloacae , Escherichia coli , Klebsiella pneumoniae , Pseudomonas aeruginosa , P. putida , Proteus mirabilis , Serratia liquefaciens , Stenotrophomonas maltophilia . В 2017 г. доминировали представители Kl. pneumoniae (35%, р < 0.01) и E. coli (23%, р < 0.01), в 2018 г. – Kl. pneumoniae (47%, р < 0.01) и E. coli (34%, р < 0.01), в 2019 г. – E. coli (40%, р < 0.01) и A. baumannii (20%, р < 0.01), в 2020 г. – E. coli (31%, р < 0.05) и Kl. pneumoniae (25%, р < 0.05), в 2021 г. – E. coli (45,5%, р < 0.01) и A. baumannii (18%, р < 0.01).
Грамположительная микрофлора в 2017-2021 гг. была представлена в основном энтерококками ( E. faecalis , E. faecium и E. gallinarum ) и стафилококками ( S. hominis , S. haemolyticus , S. sciuri , S. epidermidis , S. aureus ) (рис. 2). Кроме того, были выделены Corynebacterium xerosis , Streptococcus parasangunis .
Формирование микробиоценоза в отделении абдоминальной хирургии объясняется тем, что при операциях на брюшной полости представители нормальной микрофлоры кишечника (энтерококки, энтеробактерии) могут выйти за пределы своего обычного ареала. Присутствие Kl. pneumoniae ассоциировано прежде всего с аппаратами искусственной вентиляции легких, и представители данного вида встречаются у пациентов, переведенных в отделение реанимации.
Полученные за пять лет данные позволяют предположить, что в дальнейшем ведущими патогенами у пациентов этого отделения могут стать грамотрицательные микроорганизмы из семейства Enterobacteriaceae .
На формирование микроценозов в лечебных учреждениях влияют различные антибактериальные препараты, которые используются как для лечения, так и для профилактики инфекций. Главной чертой госпитальных штаммов бактерий является множественная резистентность к различным группам антимикробных препаратов [Сухорукова и др., 2019]. В связи с этим нами был проведен анализ чувствитель- ности к антимикробным препаратам у штаммов E. coli, которые выделялись у пациентов этого отделения в течение каждого года.
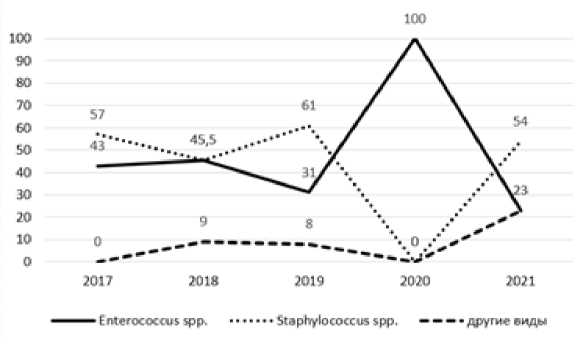
Рис. 2. Распределение грамположительной микрофлоры (%) в патологическом материале у пациентов отделения абдоминальной онкологии в течение 2017-2021 гг.
[Distribution of gram-positive microflora (%) in 2017-2021]
На рисунке 3 представлено количество резистентных штаммов (в %) к определенному антибактериальному препарату. В анализ включены препараты из группы цефалоспоринов (цефтазидим, цефтази-дим/авибактам), пенициллинов (ампициллин, амоксициллин/клавуланат), карбапенемов (меропенем), сульфаниламидов (триметоприм/сульфаметоксазол), тетрациклинов (тайгециклин) и фторхинолонов (ципрофлоксацин).
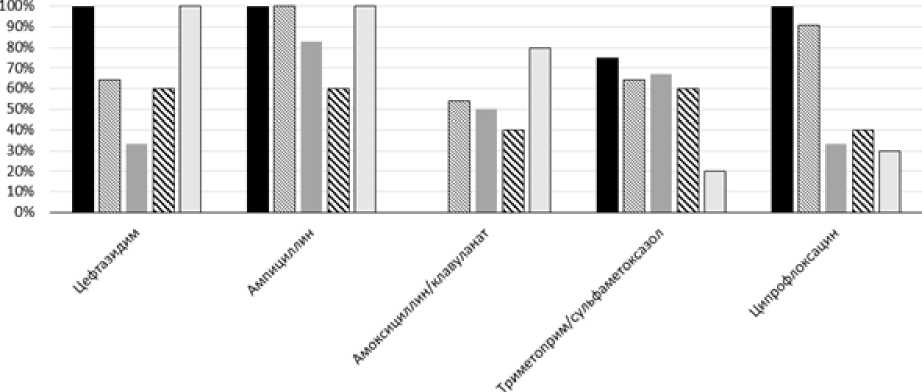
■ 2017 132018 12019 Я2О2О 02021
Рис. 3. Количество (%) выделенных штаммов E. coli , резистентных к антимикробным препаратам [Number (%) of E. coli strains resistant to antimicrobials]
В течение изученного периода сохранялась чувствительность выделенных штаммов E. coli к цефтази-диму/авибактаму, представляющим собой комбинированное антибактериальное средство, сочетающее антибиотик – цефтазидим и ингибитор бета-лактамаз – авибактам. Синтез бета-лактамаз – ферментов, которые разрушают бета-лактамное кольцо антибиотика и инактивируют его, является наиболее часто встречающимся механизмом антибиотикорезистентности [Осипов и др., 2013]. Кроме того, у выделенных штаммов E. coli сохранялась чувствительность к тайгециклину и меропенему. Соответственно, эти препараты рекомендованы для лечения и профилактики постоперационных осложнений в отделении абдоминальной онкологии.
Выводы
-
1. В отделении абдоминальной онкологии в течение 2017-2021 гг. из патологического материала от пациентов с послеоперационными осложнениями преимущественно выделялись грамотрицательные бактерии.
-
2. Представители Kl. pneumoniae , E. coli и A. baumannii являлись ведущими патогенами.
-
3. Выделенные штаммы E. coli были резистентны к воздействию цефтазидима, ампициллина, амокси-циллина/клавуланата, триметоприм/сульфаметоксазола, ципрофлоксацина и чувствительны к тайгецик-лину, меропенему и цефтазидим/авибактаму.
-
4. Для профилактики постоперационных осложнений в отделении абдоминальной онкологии необходимо продолжить микробиологический мониторинг, усилить контроль за грамотрицательной микрофлорой (так как предполагается, что она будет оставаться ведущим этиологическим агентом ПОИ в этом отделении) и использовать для лечения и профилактики послеоперационных осложнений, вызванных E. coli , тайгециклин, меропенем и цефтазидим/авибактам.
Список литературы Характеристика микрофлоры пациентов онкологического профиля с постоперационными инфекционными осложнениями
- Захватова А.С. и др. Микробиологический мониторинг антимикробной резистентности потенциальных возбудителей инфекций кровотока // Инфекция и иммунитет. 2022. №. 1 (12). С. 185-192.
- Кудлай Д.А. и др. Оценка микробиологического пейзажа и уровня антибиотикорезистентности в многопрофильном стационаре // Туберкулёз и болезни лёгких. 2022. № 8(100). С. 43-53.
- О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2020 г. по Пензенской области: материалы гос. доклада. Пенза, 2021. 243 с.
- Определение чувствительности микроорганизмов к антимикробным препаратам: клинич. рекомендации. Версия-2015-02. 162 с.
- Определение чувствительности микроорганизмов к антимикробным препаратам: клинич. рекомендации EUCAST. Версия-2018-03. 206 с.
- Осипов В.А. и др. Металло-бета-лактамазы грамотрицательных бактерий: растущая проблема в мире и в Беларуси // Медицинские новости. 2013. № 2. С. 84-88.
- Правосудова Н.А. и др. Особенности послеоперационных осложнений в отделении онкоурологии и онкогинекологии // Медицинский альманах. 2016. № 3(43). С. 32-35.
- Светличная Ю.С. и др. Микробиологический мониторинг в системе эпидемиологического надзора за госпитальными инфекциями // Эпидемиология и вакцинопрофилактика. 2014. № 1(74). С. 9-14.
- Сухорукова М.В. и др. Антибиотикорезистентность нозокомиальных штаммов Enterobacterales в стационарах России: результаты многоцентрового эпидемиологического исследования МАРАФОН 2015-2016 // Клиническая микробиология и антимикробная химиотерапия. 2019. Т. 21, № 2. С. 147-159.
- Тутельян А.В., Акимкин В.Г., Марьин Г.Г. От внутрибольничных инфекций до инфекций, связанных с оказанием медицинской помощи: научное развитие проблемы // Эпидемиология и инфекционные болезни. Актуальные вопросы. 2019. Т. 9, № 1. С. 14-22.


