Характеристика структурно-функционального состояния сердечно-сосудистой системы у носителей мутации гена HFE
Автор: Лауар М., Мусаев Н.Д., Родюкова И.С., Григорьевская А.С., Маршала С.Н., Семенякин И.В., Резник Е.В.
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Оригинальные статьи
Статья в выпуске: 4, 2025 года.
Бесплатный доступ
Цель. Охарактеризовать состояние сердечно-сосудистой системы (ССС) у пациентов носителей мутаций гена HFE в РФ. Материалы и методы. Проведен ретроспективный анализ медицинской документации 39 пациентов с генетически подтвержденными мутациями в гене HFE. Результаты. Нарушения структурно-функционального состояния ССС выявлены у 20 (51,3%) пациентов с мутациями гена HFE. У 11 (28,21%) пациентов отмечалась артериальная гипертензия, у 3 (7,69%) – инфаркт миокарда в анамнезе, у 2 (5,13%) – острое нарушение мозгового кровообращения. У 5 (12,82%) пациентов диагностирована сердечная недостаточность неишемического генеза. У 14 (35,9%) пациентов отмечены нарушения проводимости: атриовентрикулярная блокада, блокада левой и/или правой ножки пучка Гиса, нарушение внутрижелудочковой проводимости, укорочение интервала PQ, удлинение интервала QT. У 1 (2,56%) пациента - пароксизмальная форма фибрилляции предсердий. Заключение. У половины пациентов с мутациями гена HFE выявлены различные изменения со стороны сердечно-сосудистой системы. В связи с этим пациентам с кардиологической патологией неясной этиологии необходим скрининг для своевременной диагностики гемохроматоза и совместное ведение пациентов с подтвержденным гемохроматозом гематологами, кардиологами и гепатологами для профилактики кардиоваскулярных осложнений.
Гемохроматоз, сердечно-сосудистой системы, сердечная недостаточность, диастолическая дисфункция левого желудочка, нарушения проводимости, аритмии, гипертрофия левого желудочка
Короткий адрес: https://sciup.org/143185098
IDR: 143185098 | УДК: 616.12-008.1+575.224 | DOI: 10.38109/2225-1685-2025-4-74-80
Characteristics of the structural and functional state of the cardiovascular system in carriers of the HFE gene mutations
Objectives. To characterize the state of the cardiovascular system in patients carrying the HFE gene mutations in the Russian Federation. Materials and methods. An evaluation of 39 cases of HFE gene mutations confirmed by biochemical and genetic methods was carried out. Results. When analyzing the medical records of 39 patients with HFE gene mutations, changes in the structural and functional state of the cardiovascular system were detected in 20 (51.3%) patients. There was a history of arterial hypertension in 11 (28.21%) patients. Acute cerebrovascular accident was indicated in the anamnesis in 2 (5.13%) patients. A history of myocardial infarction was detected in 3 (7.69%) patients. Heart failure of non-ischemic genesis was diagnosed in 5 (12.82%) patients. In 14 (35.9%) patients in the form of atrioventricular block, left bundle branch block, right bundle branch block, intraventricular conduction disturbances, shortening of the PQ interval and prolongation of the QT interval, in 1 (2.56%) patient a paroxysmal form of atrial fibrillation was noted. Conclusion. Half patients with HFE gene mutations had various changes in the cardiovascular system. In this regard, patients with cardiac pathology of unclear etiology require screening for timely diagnosis of hemochromatosis and joint management of patients with confirmed hemochromatosis by hematologists, cardiologists and hepatologists to prevent cardiovascular complications.
Текст научной статьи Характеристика структурно-функционального состояния сердечно-сосудистой системы у носителей мутации гена HFE
Данная статья распространяется на условиях «открытого доступа», в соответствии с лицензией CC BY-NC-SA 4.0 («Attribution-NonCommercial-ShareAlike» / «Атрибуция-Не-коммерчески-Сохранение Условий» 4.0), которая разрешает неограниченное некоммерческое использование, распространение и воспроизведение на любом носителе при условии указания автора и источника. Чтобы ознакомиться с полными условиями данной лицензии на русском языке, посетите сайт: by-nc-sa/4.0/
This is an open access article distributed under the terms of the Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International (CC BY-NC-SA 4.0). License , which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited.
Гемохроматоз – это заболевание, характеризующееся системной перегрузкой железом и отложением железа в различных органах, включая сердце. Существует 2 типа гемохроматоза: первичный и вторичный. Первичный гемохроматоз – это наследственное заболевание, вторичный гемохроматоз – это результат длительного приема препаратов железа или частых переливаний крови при анемии или заболевании печени [1].
Первичный гемохроматоз – это наследственное аутосомнорецессивное заболевание, обусловленное снижением уровня регуляторного гормона гепсидина, который контролирует концентрацию железа, или снижением связывания гепсидин-ферропортин. Гепсидин регулирует активность ферропортина, который является единственным известным экспортером клеточного железа. Это приведет к повышению концентрации железа в плазме и накоплению железа в паренхиматозных органах и тканях, таких как сердце и кардиомиоциты, что приведет к развитию фиброза и недостаточности этих органов. Наиболее распространенная форма гемохроматоза вызвана гомозиготными мутациями в гене HFE (Homeostatic Iron Regulator – регулятор гомеостаза железа), в частности, мутацией p.Cys282Tyr, которая встречается более чем у 80% пациентов с данной формой заболевания. Гораздо реже встречаются формы гемохроматоза, связанного с мутациями в других генах: гепсидин противо-микробного пептида ( HAMP ), или гемоювелина ( HJV ), или рецептора трансферрина 2 ( TFR2 ), или ферропортина ( SLC40A1 ), которые предотвращают связывание гепсидин-ферропортин. Как HFE -ассоциированный, так и не- HFE -ассоциированный гемохроматоз приводят к снижению синтеза гепсидина, повышенному поступлению железа из клеток тонкого кишечника и макрофагов селезенки в плазму [2].
Гомозиготность по варианту p.Cys282Tyr в гене HFE встречается при гемохроматозе более чем у 80 % лиц европейского происхождения. Гомозиготность же по мутации p.His63Asp среди пациентов с гомозиготным гемохроматозом, отличным от p.Cys282Tyr, встречается не чаще. Общая распространенность компаунд-гетерозигот p.Cys282Tyr/p.His63Asp среди пациентов с клинически явным гемохроматозом составляет 4,1 % [3]. Однако компаунд-гетерозиготности p.Cys282Tyr/p.His63Asp самой по себе недостаточно, чтобы вызвать гемохроматоз. Только если этот генотип совпадает с дополнительными генетическими или экологическими факторами риска заболевания печени, развивается фенотипический гемохроматоз [4].
В многочисленных исследованиях изучалась частота гемохроматоза и его генетическая причина в различных популяциях. Показано, что распространенность наиболее известных мутаций HFE (а именно p.Cys282Tyr и p.His63Asp), которые могут вызывать гемохроматоз, варьирует в зависимости от этнических групп [5]. Безусловно, наиболее распространенной причиной гемохроматоза является гомозиготность по замене p.Cys282Tyr. Среди людей с диагнозом гемохроматоз в Австралии, Бретани, Франции она составляет 96 %, в то время как в Италии на их долю приходится только 62 %, а в Греции – 39 %.
Гемохроматоз, связанный с мутацией в гене HFE может протекать бессимптомно в течение >30 лет (часто >40 лет у мужчин и >50 лет у женщин). При гемохроматозе, не связанном с HFE , симптомы могут проявиться в возрасте 20–30 лет. В целом симптоматика вариабельна, что объясняет позднюю диагностику [6]. Отложение избыточного количества железа в паренхиматозных тканях приводит к клеточной дисфункции и клиническим проявлениям заболевания. Чаще всего поражаются печень, поджелудочная железа, суставы, кожа, гипофиз и сердце.
Гемохроматоз сердца, или первичная кардиомиопатия с перегрузкой железом, является важной и потенциально предотвратимой причиной сердечной недостаточности. Кардиомиопатия с перегрузкой железом – это систолическая или диастолическая дисфункция сердца, вызванная избыточным отложением железа, проявляющаяся хронической сердечной недостаточностью [7]. По данным литературы, клинические проявления гемохроматоза сердца можно разделить на три группы: аритмии, хроническая сердечная недостаточность (ХСН) из-за систолической дисфункции или диастолической дисфункции [8].
Медиана выживаемости нелеченных больных с гемохроматозом и тяжелой сердечной недостаточностью не превышает года. Однако при раннем и агрессивном лечении выживаемость приближается к таковой у больных с сердечной недостаточностью другой этиологии [8].
В связи с вышеизложенным, цель настоящего исследования: охарактеризовать состояние сердечно-сосудистой системы (ССС) у пациентов носителей мутаций гена HFE в РФ.
МАТЕРИАЛЫ И МЕТОДЫ
Для оценки структурно-функционального состояния сердечнососудистой системы проведено ретроспективное исследование данных медицинской документации с января 2021 года до апреля 2024 года у 39 пациентов с генетически подтвержденными мутациями в гене HFE (32 (82,1%) мужчины, 7 (17,9%) женщин). Медиана (здесь и далее в скобках указаны 25-й и 75-й процентили) возраста пациентов с мутациями в гене HFE составила 50 (38; 61) лет. Клинико-инструментальными критериями вовлечения сердечно-сосудистой системы считали наличие утолщения стенки левого желудочка (ЛЖ) и/или дилатации ЛЖ неустановленной этиологии, клапанных аномалий, нарушений ритма сердца и/или проводимости.
Критерии включения в исследование:
-
1. Генетически подтвержденные мутации в гене HFE ,
-
2. Возраст 18 лет и старше.
Критерии невключения:
-
1. Наличие в анамнезе злокачественного новообразования любой системы органов,
-
2. Трансплантация сердца, почек, печени в анамнезе.
Пациенты были набраны из ФГБУ «Национальный медицинский исследовательский центр гематологии» и поликлиники № 212 в городе Москве. Исследование проводилось в ГКБ № 31 им. Акад. Г.М. Савельевой Департамента Здравоохранения Москвы, Москва.
Этническая принадлежность пациентов в нашем исследовании не учитывалась из-за отсутствия информации.
Статистический анализ. Статистический анализ проведен с помощью непараметрических методов программы IBM SPSS Statistics 2017 версия 25. Количественные значения представлены в виде медианы (Ме) и интерквартильного интервала (Q1 и Q3), где Q1 – 25 процентиль, Q3 – 75 процентиль. При анализе нормальности распределения выборки, который определялся с помощью метода Колмогорова-Смирнова и критерия Шапиро-Уилка, все данные имели ненормальное распределение. При сравнительном анализе групп по количественным признакам использовали непараметрический U-критерий Манна-Уитни (р<0,05).
РЕЗУЛЬТАТЫ
Среди наших пациентов у 27 (69,23%) обнаружена гомозиготность по мутации p.His63Asp в гене HFE . Гомозиготность по варианту p.Cys282Tyr в гене HFE встречалась у 9 (23,08%) пациентов, в то время как гетерозиготность по варианту p.His63Asp в гене HFE наблюдалась – у 3 (7,69%) пациентов.
Медиана времени от дебюта симптомов заболевания до постановки диагноза составила 4,3 (1,8; 8,6) года, max – 12 лет. 1 (2,56%) пациент получал хелатор (Деферазирокс), еще 1 (2,56%) – курсы флеботомии, у 37 пациентов информации о получаемой патогенетической терапии в медициской документации не было представлено.
У 11 (28,21%) пациентов в анамнезе имелась артериальная гипертензия (АГ): у 6 (15,38%) пациентов была АГ 1 степени, у 3 (7,69%) – АГ 2 степени и у 2 (5,13%) – АГ 3 степени (табл. 1).
Дислипидемия отмечена у 20 (51,28%) пациентов. Общий холестерин составил 5,5 (4,9; 6,6) ммоль/л, (95% Доверительный интервал (ДИ) 5,17-6,99), холестерин липопротеидов низкой плотности (ЛПНП) – 3,8 (3,2; 4,4) ммоль/л, ДИ (3,41-4,25), у 17 (43,59%) уровень ЛПНП составил более 3 ммоль/л. Сывороточный ферритин (СФ) составил 423,2 (302; 582) мкг/л, ДИ (365,99-510,63).
При физикальном обследовании бронзовая окраска кожи отмечена у 6 (15,38%) пациентов. Жалобы пациентов отражены на рисунке 1.
У 5 (12,82%) пациентов без инфаркта миокарда (ИМ) в анамнезе была указана в диагнозе ХСН. Больные с ХСН были старше пациентов без ХСН: 57 (38; 68) лет и 49 (38; 61) лет соответственно, p=0,035. ХСН I функционального класса по классификации Нью-Йоркской кардиологической ассоциации (NYHA) отмечена – у 2 (5,13%), II класса – у 2 (5,13%), III класса – у 1 (2,56%) пациента.
По результатам эхокардиографии, фракция выброса левого желудочка (ФВ ЛЖ, по Симпсону) составила >50% у 34 (87,18%), от 40% до 50% – у 5 (12,82%) пациентов, ФВ ЛЖ <40% – не было ни у одного пациента. У всех пациентов с умеренно сниженной ФВ ЛЖ в диагнозе была указана ХСН. Диффузный гипокинез миокарда ЛЖ выявлен у 3 (7,69%) пациентов, у всех из них наблюдалось умеренное снижение ФВ ЛЖ. Утолщение стенки ЛЖ отмечено у 9 (23,08%) пациентов без АГ в анамнезе (рис. 2). Обструкции выходного тракта ЛЖ и/или переднего систолического движения передней створки митрального клапана (МК) не выявлено. Утолщение стенки правого желудочка (ПЖ) выявлено у 2 (5,13%) пациентов. У 17 (43,59%) пациентов при эхокардиографии выявлена недостаточность клапанного аппарата: митральная – у 17 (43,59%), трикуспидальная – у 16 (41,03%), легочная – у 11 (28,21%), аортальная – у 7 (17,95% пациентов. Пролапс МК был выявлен у 2 (5,13%) пациентов: передней створки – у 1 (2,56%), задней – у 1 (2,56%) пациента. В эхокардиографическом заключении описана кальцификация и/или утолщение створок аортального клапана – у 13 (33,33%), МК – у 10 (25,64%), трикуспидального клапана – у 4 (10,26%) пациентов.
Неинвазивные признаки легочной гипертензии выявлены у 5 (12,82%) пациентов. Перикардиальный выпот не верифицирован ни у одного пациента.
Диастолическая дисфункция ЛЖ выявлена у 4 (10,26%) пациентов: у всех – 1-го типа (нарушения релаксации).
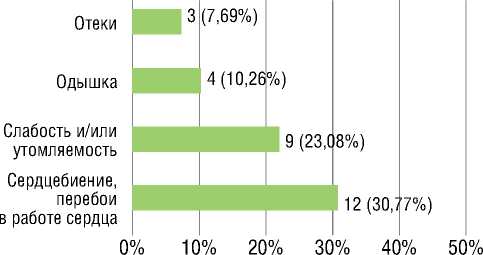
Рисунок 1. Наиболее частые жалобы пациентов с генетически подтвержденными мутациями в гене HFE [собственные данные]
Симметричная гипертрофия 6 (15,4%)

Асимметричная гипертрофия
3 (7,6%)
Рисунок 2. Утолщение стенки ЛЖ у пациентов с генетически подтвержденными мутациями в гене HFE и поражением сердца [собственные данные]
Без гипертрофии 30 (77%)
Септальная 2 (5%)
-
Figure 1. The Most common complaints of patients with genetically confirmed mutations in the HFE gene [own data]
-
Figure 2. Thickening of LV wall in patients with genetically confirmed mutations in the HFE gene and cardiac involvement [own data]
Таблица 1. Сравнительная характеристика мужчин и женщин носителей мутаций в гене HFE [собственные данные]
Table 1. Comparative characteristics of men and women carriers of mutations in the HFE gene [own data]
Показатели
Общая группа (n=39, 100%)
Мужчины (n=32, 82,1%) Женщины (n=7, 17,9%)
Возраст (лет), медиана; 25-й и 75-й процентили
50 (38; 61)
50 (39; 61)
36 (34; 64)
Время от клинической манифестации до диагностики заболевания (годы), медиана; 25-й и 75-й процентили
4,3 (1,8; 8,6)
4,1 (1,6; 7,8)
4,5 (1,9; 8,7)
Нарушения структурно-функционального состояния сердца, n (%)
20 (51,3%)
19 (48,72%)
1 (2,56%)
ХБП, n (%)
15 (38,46%)
13 (33,33%)
2 (5,13%)
АГ, n (%)
11 (28,21%)
6 (15,38%)
5 (12,82%)
СД 2 типа, n (%)
2 (5,13%)
1 (2,56%)
1 (2,56%)
Транзиторная ишемическая атака/инсульт в анамнезе,
n (%) 2 (5,13%)
2 (5,13%)
0 (0)
ИМ в анамнезе, n (%)
3 (7,69%)
2 (5,13%)
1 (2,56%)
Примечание/Notе: АГ – артериальная гипертензия (AH – arterial hypertension), СД – сахарный диабет (DM – diabetes mellitus), ИМ – инфаркт миокарда (MI – myocardial infarction), ХБП – хроническая болезнь почек (CKD – chronic kidney disease).
При анализе ЭКГ, вольтажные признаки гипертрофии левого желудочка (ГЛЖ) (по индексу Соколова-Лайона), выявлены у 8 (20,51%) пациентов, низкоамплитудные комплексы QRS (амплитуда комплекса QRS менее 5 мм во всех отведениях от конечностей и менее 10 мм во всех прекордиальных отведениях) – у 6 (15,38%) пациентов. Среди пациентов без ИМ в анамнезе патологический зубец Q выявлен у 4 (10,26%) пациентов: у 2 (5,13%) – в отведениях от нижней стенки ЛЖ, у 2 (5,13%) – в передне-перегородочной области ЛЖ. Также отмечены нарушения сердечного ритма (рис. 3).
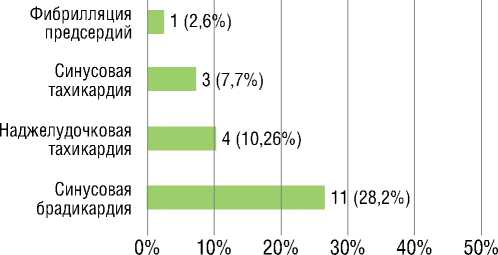
Рисунок 3. Нарушения ритма сердца у пациентов с генетически подтвержденными мутациями в гене HFE и поражением сердца [собственные данные]
-
Figure 3. Heart rhythm abnormalities in patients with genetically confirmed mutations in the HFE gene and cardiac involvement [own data]
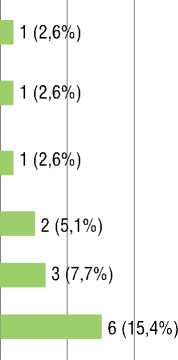
Нарушения проводимости выявлены у 14 (35,9%) пациентов, они обобщены в рисунке (рис. 4).
Синдром удлиненного интервала QT
Синдром предвозбуждения желудочков
Нарушение внутрижелудочковой проводимости
Блокада левой ножки пучка Гиса
Блокада правой ножки пучка Гиса
Атриовентрикулярная блокада
0% 10% 20% 30%
40%
50%
Рисунок 4. Нарушения проводимости у пациентов с генетически подтвержденными мутациями в гене HFE и поражением сердца [собственные данные]
-
Figure 4. Conduction disorders in patients with genetically confirmed mutations in the HFE gene and cardiac involvement [own data]
ОБСУЖДЕНИЕ
По данным литературы, распространенность наиболее известных мутаций гена HFE (а именно p.Cys282Tyr и p.His63Asp), которые могут вызывать гемохроматоз, варьирует в зависимости от этнических групп. Гомозиготность по варианту p.Cys282Tyr в гене HFE встречается при гемохроматозе более,
78 ЕВРАЗИЙСКИЙ КАРДИОЛОГИЧЕСКИЙ ЖУРНАЛ, 4, 2025
чем у 80% лиц европейского происхождения. Гомозиготность по мутации p.His63Asp среди пациентов с гемохроматозом, отличным от p.Cys282Tyr, встречается реже. Общая распространенность компаунд-гетерозигот p.Cys282Tyr/p.His63Asp среди пациентов с клинически явным гемохроматозом составляет 4,1% [3].
Среди проанализированных нами пациентов превалировала гомозиготность по мутации p.His63Asp в гене HFE (69,23%), хотя, по данным литературы, у людей европейского происхождения доминирует гомозиготность по варианту p.Cys282Tyr в гене HFE . Это может отражать особенности Российской популяции.
Гемохроматоз встречается как у мужчин, так и у женщин, хотя дебют клинической симптоматики у женщин наблюдается в более позднем возрасте [9]. В нашем исследовании преобладали мужчины в соотношении 4,57:1.
Диагостика гемохроматоза в ряде случаев затруднена. Поражение сердца при гемохроматозе обычно развивается не сразу, протекает бессимтомно и остается недиагностированным в течение длительного времени [10]. В нашем исследовании медиана времени от появления симптомов до постановки диагноза составила 4,3 года, максимум – 12 лет. Ошибочные диагнозы и несвоевременная диагностика могут приводить к прогрессированию необратимых изменений в различных органах, в т.ч. в сердце.
Насыщение трасферрина железом было определено лишь у 12 (30,77%) пациентов, повышенное насыщение трансферрина железом наблюдалось у 6 (15,39%), а гиперферритинемия присутствовала у 22 (56,41%) пациентов. Важно проводить скрининг на гемохроматоз (лабораторные тесты), среди пациентов с патологией внутренних органов неясной этиологии, особенно тех, у кого в анамнезе были гемотрансфузии или прием препаратов железа с целью лечения анемии, включающий определение уровня железо, коэффициент насыщения трансферрина железом (КНТЖ) и СФ. Повышенный КНТЖ является самым ранним биохимическим нарушением при гемохроматозе, отражающим повышенную абсорбцию железа. Также важно тщательно собирать анамнез и информировать врачей об особенностях гемохроматоза. Семейный скрининг важен для тех, у кого подтвержден диагноз первичного гемохроматоза.
По данным литературы, сахарный диабет и/или бронзовая окраска кожи (бронзовый диабет) выявляется не редко у пациентов с первичным гемохроматозом. В ходе нашего исследования, наличие сахарного диабета подтверждено только у 2 (5,13%), а бронзовой окраски кожи – у 6 (15,38%) пациентов.
Описано, что у пациентов с первичным гемохроматозом выявляется дилатация левого предсердия (ЛП) и ПЖ с низкой или нормальной ФВ ЛЖ [11, 12]. Тяжесть систолической дисфункции миокарда пропорциональна количеству отложений железа в миокарде. Увеличение отложений железа в миокарде приводит к утолщению стенки и к снижению податливости ЛЖ, его дилатации и систолической дисфункции [13].
По данным литературы, клинические проявления гемохроматоза сердца можно разделить на три категории: аритмии, ХСН из-за систолической дисфункции и ХСН из-за диастолической дисфункции [8]. В нашем исследовании наблюдалась ещё четвертая категория, а именно нарушение сердечной проводимости, преимущественно с наличием АВ блокады, БЛНПГ, БПНПГ, тахикардии и брадикардии, что может быть следствием нарушения функционирования синоатриального (СА) и/или АВ-узлов и/или электрических путей вследствие накопления в них железа.
Вследствие изменений миокарда, аритмий и нарушений проводимости пациенты с гемохроматозом могут испытывать такие симптомы, как сердцебиение, общая слабость и/или утомляемость, что встречалось у 30,77% и 23,08% наших пациентов соответственно.
Миокард особенно чувствителен к окислительному стрессу, вызванному железом, из-за высокой концентрации митохондрий и низкого содержания антиоксидантов [8]. Железо после переливания крови или после длительных курсов перорального приема с большей вероятностью накапливается в сердце, чем железо, поступающее с пищей. При накоплении в сердце железо откладывается преимущественно в эпикардиальных миоцитах, позже – во всей толще стенки. Перегрузка сердца железом первоначально приводит к увеличению перинуклеарных отложений железа с последующим накоплением в других структурах клетки. Отложение железа более обширно в желудочках, чем в предсердиях. Часто вовлекается проводящая система сердца [13].
Предсердные аритмии могут быть вызваны отложением железа в предсердиях и дилатацией предсердий из-за повышенного давления наполнения желудочков. Особенности аритмий при гемохроматозе еще предстоит изучить, но вполне вероятно, что они вызывают одышку (присутствовавшую у 10,26% пациентов в нашем исследовании), сердцебиение, перебои в работе сердца (у 30,77% из них) и могут быть одним из механизмов, лежащих в основе инсульта и транзиторных ишемических атак при гемохроматозе.
По данным нашего исследования, частота наджелудочковой тахикардии у пациентов с генетически подтвержденными мутациями в гене HFE составила 10,26%, ФП – 2,56%, это означает, что, ФП не была широко распространена у наших пациентов.
ГЛЖ увеличивает конечно-диастолическое давление в левом желудочке и в ЛП, что приводит к его расширению и деформации. Это является предиктором возникновения и рецидива ФП [14]. У большинства пациентов наблюдалась диастолическая дисфункция без ГЛЖ, что позволяет предположить, что прямое накопление железа в сердце может повышать жесткость миокарда ЛЖ и нарушать его релаксацию даже без наличия гипертрофических изменений. Фиброз миокарда, наблюдаемый при гемохроматозе, предрасполагает к желудочковым аритмиям, хорошо известным как наиболее распространенная причина внезапной сердечной смерти (ВСС). У некоторых пациентов могут возникнуть симптомы предобморочного состояния или обморока, связанные с брадиаритмиями, включая синусовую брадикардию, АВ второй степени Мобитц II или даже АВ блокаду третьей степени. Брадикардия у пациентов с перегрузкой железом может возникнуть из-за внешних или внутренних факторов. Например, повышенное содержание железа может повлиять на активность автономной нервной системы, возможно, за счет нарушения нейронной функции или вмешательства в другие элементы барорецепторных рефлекторных путей, внешних по отношению к сердцу [15]. С другой стороны, внутренняя электрическая активность специализированных кардиостимуляторных миоцитов, расположенных в СА узле, также может быть нарушена железом в результате модуляции ряда мембранных токов, обработки Ca2+ или внутриклеточной сигнализации [12]. Брадиаритмия при гемохроматозе, включая дисфункцию СА и/или АВ-узла, встречается чаще, чем тахиаритмия, которая, по оценкам, составляла 10,26% в нашей когорте. В одном исследовании использовалась модель мышей с хронической перегрузкой железом для изучения влияния железа на функцию СА-узла. Инъекция железа в течение 2 недель снижала частоту сердечных сокращений (ЧСС), не оказывая заметного влияния на суточные колебания сна и бодрствования. Средняя ЧСС за 48 часов постепенно снижалась по мере увеличения периода инъекции железа, при этом ЧСС снижалась (P<0,05) с 60,5±12 ударов/мин на исходном уровне до 52,9±14 ударов/мин после 4 недель хронической перегрузки железом. Результаты показывают, что собственная электрическая активность миоцитов, расположенных в СА узле, также может быть нарушена железом в результате модуляции ряда мембранных токов или внутриклеточной сигнализации. Эти изменения объясняют развитие синусовой брадикардии, замедление электропроводности и повышенную восприимчивость к ФП у мышей, а также у пациентов с перегрузкой железом [16]. В нашей когорте частота синусовой брадикардии составила 28,21%. Факторы риска, связанные с брадиаритмией, включают пожилой возраст, дисфункцию ЛП, низкую ЧСС в состоянии покоя, увеличенную продолжительность PR и QRS, использование терапии бета-блокаторами.
Изменения ЭКГ, типичные для гипертрофии миокарда, в частности глубокие отрицательные зубцы T в прекардиальных отведениях, особенно в сочетании с болью в сердце, часто интерпретируются как ИМ, но, несмотря на высокую частоту сте-нокардитических болей в груди как у мужчин, так и у женщин, было относительно мало записей о процедурах коронарной реваскуляризации или инфаркте миокарда. Гемохроматоз не был предложен в качестве фактора риска преждевременной атеросклеротической ишемической болезни сердца.
Пациенты с ГЛЖ часто сообщали о боли в груди, что позволяет предположить, что такие факторы, как повышенная потребность миокарда в кислороде, заболевание мелких сосудов и эндотелиальная дисфункция, которые вызывают микрососу-дистую стенокардию у пациентов с другими причинами ГЛЖ, также важны для гемохроматоза. Аналогично, мы не можем исключить возможность того, что гемохроматоз усугубляет сердечно-сосудистый риск у пациентов с другими предрасполагающими факторами, такими как гиперлипидемия, АГ и курение.
Все клинические проявления гемохроматоза неспецифичны, поэтому для подтверждения диагноза необходимы лабораторные и молекулярно-генетические исследования [17].
ЗАКЛЮЧЕНИЕ
Пациентам с сердечно-сосудистой патологией неизвестной этиологии, в т.ч. утолщением стенки ЛЖ и/или сердечной недстаточностью, нарушениями ритма и проводимости, псев-доинфарктными изменениями ЭКГ, особенно при наличии синусовой брадикардии, необходим скрининг на гемохроматоз. Пациентам с верифицированным гемохроматозом необходимо тщательное обследование сердечно-сосудистой системы для своевременной диагностики отклонений, профилактики и терапии кардиальных осложнений.


