Химические процессы при микродуговом оксидировании
Автор: Михеев А.Е., Трушкина Т.В., Гирн А.В., Раводина Д.В., Ивасев С.С.
Журнал: Сибирский аэрокосмический журнал @vestnik-sibsau
Рубрика: Технологические процессы и материалы
Статья в выпуске: 2 (48), 2013 года.
Бесплатный доступ
Рассмотрены химические процессы, протекающие при микродуговом оксидировании (МДО) алюминиевого сплава АМг-6 в силикатно-щелочном электролите; показаны возможные химические превращения в результате взаимодействия компонентов, входящих в состав электролитов; приведены результаты исследований по определению элементного состава получаемых покрытий; установлена зависимость содержания таких оксидных элементных форм, как SiO 2 и Al2О 3 химического состава покрытия от технологических режимов. Проведенные исследования показывают, что покрытие на образцах алюминиевого сплава состоит из двух основных оксидных элементных форм: SiO 2 и Al2О 3. При проведении исследования фазового состава покрытия методом рентгеноструктурного анализа было выявлено, что покрытие, сформированное микродуговым оксидированием на сплаве АМг-6, состоит из а и γ-Al 2O 3, причем а фаза Al 2O 3 присутствует только во внутренних слоях покрытия, γ-Al 2O 3 присутствует по всей толщине покрытия, и на внешнем крае покрытия выявлена фаза муллита (3Al 2O 3 • 2SiO 2) и оксид кремния SiO 2.
Микродуговое оксидирование, химические реакции, алюминиевый сплав, элементный анализ
Короткий адрес: https://sciup.org/148177062
IDR: 148177062 | УДК: 541.138.2
Chemical processes at microarc oxidation
The authors consider the chemical processes occurring during microarc oxidation (MAO) of the aluminum alloy AMG-6 silicate-alkaline electrolyte, the possible chemical changes as a result of interaction of the components included in the electrolyte, the results of studies to determine the elemental composition of the coatings, the dependence of the content of such oxide elemental forms of SiO 2 and Al 2O 3 as the chemical composition of the coating process conditions. The studies indicate that the coating of the aluminum alloy samples consists of two basic elements if the oxide forms, such as SiO 2 and Al2O 3. The study of the phase composition of the coating made with X-ray analysis revealed that the coating formed by oxidizing microarc alloy AlMg-6 consists of a and γ-Al 2O 3, with Al 2O 3, and the a phase is present only in the inner layers of the coating, γ-Al 2O 3 is present throughout all the thickness of the coating, and on the outer edge of the coating the mullite phase (3Al 2O 3 • 2SiO 2) and silica SiO 2 was revealed.
Текст научной статьи Химические процессы при микродуговом оксидировании
Микроплазменное оксидирование является сложным многофакторным процессом. Влияние отдельных факторов на свойства и качество покрытий исследуются достаточно широко, особое внимание уделяют анодно-катодному режиму процесса, который обеспечивает получение покрытий с повышенными физикомеханическими характеристиками, такими как адгезия, микротвердость, прочность и износостойкость [1; 2]. Но в данный период по микроплазменным процессам еще нет целостной картины, описывающий весь процесс МДО, в том числе и с точки зрения происходящих химических процессов. Характеристики МДО покрытий в значительной степени зависят от технологических режимов, состава и концентрации электролитов и ряда других факторов. В работе рассмотрены процессы химических превращений в силикатнощелочном растворе электролита, в котором содержащиеся катионы и/или анионы образуют нерастворимые оксиды, входящие в состав покрытия. Обработке подвергались образцы из алюминиевого сплава АМг-6 в электролите, содержащем 4 г/л NaOH и 10 г/л Na2SiO3, при следующих технологических режимах: плотность тока I = 5–40 А/дм2; продолжительность оксидирования – 60 мин; соотношение анодной и катодной составляющих силы тока I k / I a , = 0,6–1,4; температура электролита – 15–40 °С. В процессе химических превращений происходит последовательное формирование покрытия переменного фазового состава, содержащее различные аллотропические модификации оксида алюминия: α-Аl 2 О 3 , δ-Аl 2 О 3 , γ-Аl 2 О 3 и муллита 2SiO2·3Аl2O3. Рассмотрим возможные химические реакции, приводящие к их образованию.
В процессе МДО на поверхности металла возможно растворение алюминия с образованием тетрагид-роксоалюмината:
2Al + 2OH– + 6H 2 O →2[Al(OH) 4 ]– + 3H 2
В электролите происходит диссоциация силиката натрия:
Na 2 SiO 3 + 3H 2 O ↔ 2Na+ + 2OH– + H 4 SiO 4
Na 2 SiO 3 + H 2 O ↔ NaНSiO 3 + NaOН
SiO 3 – + H 2 O ↔ НSiO 3 – + OH–
При взаимодействии силикат-иона с водой образуется поликремнекислота HSiO 3 . Возникшее поверхностное соединение – поликремнекислота – содержит реакционноспособные силанольные группы SiOH, способные к частичной диссоциации в воде по кислотному типу:
SiOН →SiO– + Н+
Образующиеся ионы Н+ переходят в жидкую фазу, но вследствие кулоновского взаимодействия с ионами –SiO– образуют внешнюю обкладку в растворе у поверхности твердой фазы. Ионы ОН– способствуют диссоциации силанольных (SiOH) групп. Возникает ЭДС с внутренней обкладкой (определяющей отрицательный знак Δφ), состоящей из –SiO–. Потенциало-пределяющими ионами будут ионы, влияющие на степень диссоциации SiOH-групп, а именно Н+ и ОН–:
О :
si о™ ; н
О :
I :
-si-o- ; н+
О :
Затем происходит взаимодействие ионов алюминия с одной силанольной группой (образование моно-дентатного комплекса):
SiOН + Al3+ → SiOAl2+ + Н+
Связывание одного иона алюминия с двумя силанольными группами (образование бидентатного комплекса) выражается формулой
2SiOН + Al3+ → (SiO) 2 Al+ + 2Н+
Связывание одного иона алюминия с тремя силанольными группами (образование тридентатного комплекса):
3SiOН + Al3+ → (SiO)3Al+ + 3Н+ а также образование комплекса, в котором с силанольной группой взаимодействует гидролизованный ион металла:
2SiOН + Al3+ +H 2 O→ (SiO) 2 AlOH + 2Н+
В этом растворе возможен гидролиз компонентов электролита с последующим термолизом продуктов гидролиза в зоне разряда:
SiO 3 2– + 2Н+ → Н 2 SiO 3 → SiO 2 + H 2 O
Авторы работы [1] считают, что разлагаясь, при высоких температурах кремниевая кислота дает диоксид кремния SiO 2 в виде α-кристобалита и α-кварца, и воду, а далее возможно образование силиманита на алюминиевом электроде по реакции
Al2O 3 + SiO2 →Al2SiO 5
Если в составе электролита есть силикаты, то образующийся из них в разряде оксид кремния при нагреве с Al 2 O 3 и другими оксидами металлов может дать тугоплавкие и термически стойкие вещества, не взаимодействующие с растворами большинства кислот и щелочей – алюмосиликаты, такие, как ортоклаз K[AlSi 3 O 8 ], альбит Na[AlSi3O8], нефелин Na[AlSiO4] [3].
При МДО выделяют реакции анодного и катодного полупериода [3]. В анодный полупериод будут протекать реакции растворения алюминия, образование кислорода из гидроксид-ионов и оксида алюминия:
2OH– – 4e = O 2 ↑ + 2H 2 O
Al0 – 3e +OH– → Al(OH) 3
Al0 – 1e +2OH– → AlO 2 – +H 2
2Al0 – 6e +6OH– → Al 2 O 3 ↓+3H 2 O
В катодный полупериод будет происходить восстановление воды, ионов водорода и оксидов металлов, входящих в состав покрытия:
2H 2 O +2e = 2OH– + H 2 ↑
2H+ +2e = H 2 ↑
Al 2 O 3 ↓+ 6e +3H+ = 2Al0 + 3OH–
SiO 2 +4e = 4HSiO 2 ↓ + O ↑ + 2H 2 O
В присутствии метасиликата натрия в анодный полупериод становится возможным разряд ионов НSiO3 – продуктов гидролиза метасиликата натрия:
4HSiO 3 – – 4e = 4HSiO 2 ↓ + O ↑ + 2H 2 O
Кроме того, при повышенных температурах в каналах пробоя пленки может протекать химическая реакция алюминия с метасиликатом натрия, приводящая к образованию силикатов типа nSiO 2 и mSiO 2 алюмосиликатов с фазами – 3Al 2 O 3 ·2SiO 2 (муллит), Al2O3·2SiO2 (каолин), Al2O3·SiO2 (силиманит):
[mSiO 2 ∙ n SiO 2 ∙ H 2 O] =
= mSiO 2 ∙ n SiO 2 ∙ H 2 O +1/2O 2 ↑ + 2e
2Al + 3Na 2 O ∙ 3nSiO 2 +6H 2 O =
= 6NaOH + Al 2 O 3 + 3nSiO 2 +3H 2 ↑
На поверхности металла возможно образование неоднородного покрытия, включающего оксид алюминия и поверхностные комплексы, образующиеся в результате взаимодействия с силанольными группами, а также формирование покрытия переменного фазового состава, содержащего различные аллотропические модификации оксида алюминия (α – Аl 2 О 3 , δ-Аl 2 О 3 , γ-Аl 2 О 3) и муллита (2SiO 2 ·3Аl 2 O) 3 .
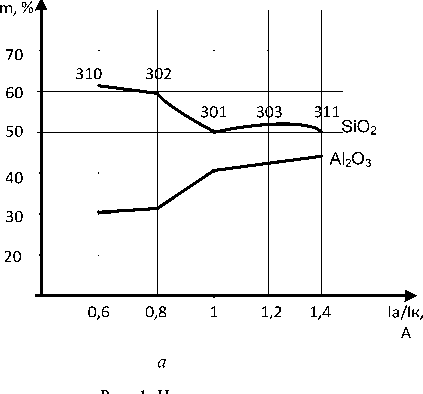
В работе были проведены исследования по выявлению химического состава полученных покрытий на рентгенофлуоресцентном спектрометре ARL Quant’x. По результатам элементного анализа на образцах алюминиевого сплава АМг-6, обработанных МДО в силикатно-щелочном электролите, было выявлено содержание таких оксидных элементных форм, как SiO 2 и Al 2 О 3 (рис. 1), содержание которых зависит от технологических режимов.
В работе [4] установлено, что покрытие, сформированное микродуговым оксидированием на сплаве АМг-6, состоит из α и γ-Al 2 O 3 , причем α фаза Al 2 О 3 присутствует только во внутренних слоях покрытия, γ-Al 2 O 3 присутствует по всей толщине покрытия и на внешних слоях покрытия выявлена фаза муллита (3Al 2 O 3 · 2SiO 2 ) и оксида кремния SiO 2 . Изменение количественного соотношения фазовых составляющих Аl 2 О 3 от плотности тока I S и отношения I к / I а представлены на рис. 2.
. .
m,
A
б
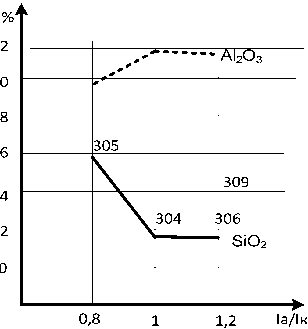
нение химического состава МДО-покрытия в зависимости от Ik/Ia: а – плотность тока 20 А/дм2; б – плотность тока 10 А/дм2
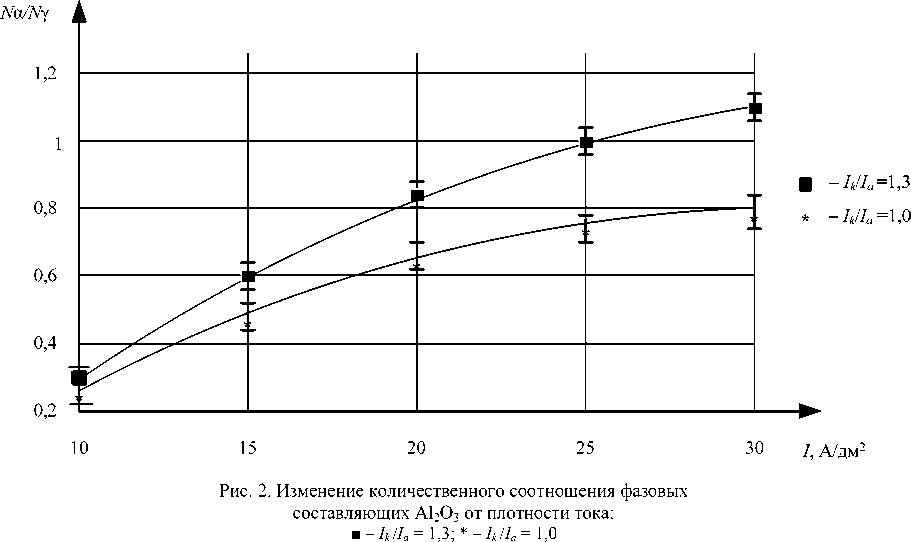
Повышение содержания модификации α-Аl 2 О 3 в покрытии, происходит за счет роста плотности тока и увеличения отношения I к / I а .
В процессе химических превращений происходит последовательное формирование покрытия переменного фазового состава, содержащее различные аллотропические модификации оксида алюминия: α-А12О3, δ-А1 2 О 3 , γ-А1 2 О 3 и муллита 2SiO 2 ·3А1 2 O 3 .
Экспериментально подтверждено, что образование различных аллотропических модификаций, содержание той или иной фазы А1 2 О 3 и муллита зависит от режимов обработки: соотношения анодной и катодной составляющих силы тока и плотности тока.


