Химизм извлечения кремнезема из состава рудоносных минералов
Автор: Токтосунова Батма Бадировна, Айткулов Бексултан Таалайбекович, Токтосунов Темирлан Маратович
Журнал: Академический журнал Западной Сибири @ajws
Рубрика: Природопользование
Статья в выпуске: 2 (63) т.12, 2016 года.
Бесплатный доступ
Цель статьи - изучение химизма извлечения кремнезема из состава рудоносных минералов с помощью гидроксидов и солями щелочных металлов с созданием оптимальных соотношений компонентов рудоносных пород и реагентов которое приводит к уменьшению количества кремнезема с 70% до 30% и количественному увеличению Ti, Mo, Cr, Ni, Pb, Ag в конечном продукте.
Рудоносные минералы, образцы лидита, кремнезём, соотношение компонентов, гидроксид натрия, карбонат натрия, концентрация, пустая порода, обогащение
Короткий адрес: https://sciup.org/140221829
IDR: 140221829 | УДК: 622.284.8
Chemistry of silica extraction and composition of ore-bearing minerals
The study of the chemistry of the extraction of silica from the composition of ore-bearing minerals with the help of hydroxides and salts of alkali metals with the creation of optimal proportions of the components of ore-bearing rocks and reagents which leads to a decrease in the number of silica from 70% to 30% and a quantitative increase of Ti, Mo, Cr, Ni, Pb, Ag in the final product.
Текст научной статьи Химизм извлечения кремнезема из состава рудоносных минералов
Лидитов Беркутского месторождения находятся на южном склоне хр. Тескей Алатоо в междуречье От-тук и Кенсуу, которые являются правыми притоками р. Сарыджаз. Абсолютные высоты над уровнем моря 2900-3500 м. В административном отношении расположены они в пределах Аксуйского района Иссык-Кульской области. Эти месторождения открыты в 1946 г. и разведены детально (1950–1957 гг.), сложены кембро – ордовикско - силурийскими, кремнисто -карбонатно-терригенными отложениями, содержащими отдельные покровные тела преимущественно базальтового состава. Прорваны дайками диабазовых порфиритов Музбулакского интрузивного комплекса позднего палеозоя [1, 2, 3].
Как известно в составе минералов извлекаемый металл находится вместе с пустой породой (в виде песка, глины, известняка) в различных весовых соотношениях [4]. Когда их количественное значение намного превышает от основного компонента, выплавка металла из таких руд экономически не выгодна. Поэтому такие руды предварительно обогащают, отделяют от них часть пустой породы и в результате в составе оставшегося концентрата содержание рудного минерала повышается.
Имеются различные методы обогащения рудных минералов и избавления их от пустой породы.
Целью нашей работы является разработка способов извлечения кремнезема из состава лидита с гидроксидом щелочных металлов и их солями.
Объектом исследования были образцы лидита (116–Л и 115-Л). По результатам спектрального анализа (табл. 1) в исходном образце лидита (116-Л) указано значительное содержание SiO2 и Fe2O3 и отсутствие некоторых металлов (Mn, Co, Sn, Ag).
Экспериментальная часть.
Опыт 1 . Извлечение кремнезёма расплавом гидроксида натрия (NaOH).
Образцы лидита (116-Л) в количестве 5 г, разделенные при помощи магнитки от оксида железа (Fe2O3), нагревали на фарфоровой чашке в теч. 30 мин, с последующим охлаждением до 30оС. В это время в другой фарфоровой чашке расплавляли NaOH и добавляли в охлажденный образец лидитовой пробы. Полученную смесь тщательно перемешивали в течение 5 мин. При этом соотношение лидита и NaOH составляло соответственно 1:2. Охлажденную смесь после тщательного перемеши-вания растворили в воде и фильтровали. Затем не растворимые части в воде (116–Л) отделяли фильтрованием, сушили, прокаливали в муфельной печи и проводили спектральный анализ (табл. 2).
Фильтрат с ожидаемым содержанием Na2SiO3 добавляли 4,21г HCl (d–1,189 г/cм3) из расчета 1,67:1 (Na 2 SiO 3 : HCl) по массе и полученный студенистый осадок кремниевой кислоты отделяли фильтрованием.
Таблица 1
Спектральный анализ исходного образца лидита 116-Л
|
№ проб |
10-2 М 11 |
10-3 Ni |
10-3 Со |
10-1 Ti |
10-2 V |
10-3 Cr |
10-3 Mo |
10-2 W |
10-2 Zr |
10-2 Hf |
10'3 Nb |
10-1 Ta |
10-3 C11 |
10 Pb |
10-4 Ag |
10-2 Sb |
10-3 Bi |
10-2 As |
10-2 Z n |
|
116-л |
- |
0,5 |
- |
0,07 |
20 |
3 |
1,2 |
- |
04 |
- |
- |
9 |
0,5 |
- |
- |
- |
- |
2 |
|
|
№ проб |
10-2 Ci |
10-3 Sn |
10-3 Ge |
10-3 Ga |
10-3 In |
10-3 Yb |
10-3 Y |
10-2 La |
10-1 Ce |
10-1 p |
10-4 Be |
10-2 Sr |
10-2 Ba |
10-3 Li |
10-2 Th |
10-1 I" |
10-3 Pt |
10-3 Au |
10-3 Sc |
|
11 б-Л |
0.5 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|||
|
№ проб 11 б-Л |
SiO2 |
A12O3 |
M gO |
Fe2O |
CaO |
Ma2O |
|||||||||||||
|
70 |
0,3 ■ 0,12 |
3 |
0.3 |
- |
|||||||||||||||
Опыт 2. Извлечение кремнезёма водным раствором гидроксида натрия (NaOH). Также брали разделенного магниткой от оксида железа исходного образца лидита (116–Л) в количестве 5 г, нагревали, охлаждали, как в предыдущем опыте. В другом стакане приготавливали водный раствор гидроксида натрия (18%), затем нагревали и смешивали с образцом лидита при соотношении 1:2 (Л:NaOH). Полученную смесь перемешивали, охлаждали и после чего добавляли воду.
Водонерастворимую часть смеси отделяли фильтрованием, осадок сушили, прокаливали и провели спектральный анализ, результаты которого представлены в табл. 2.
По результатам спектральных исследований наблюдается при щелочном способе извлечении кремнезема уменьшение SiO2, с расплавом гидроксида натрия до 52 %, с его водным раствором на 45 %. В то же время наблюдается обогащение количество некоторых металлов (Ni, Ti, Cr, Zr, Pb), начинают проявляться металлы Mn,Co, Sn, Ag, которые не были обнаружены в исходном образце. (Из литературных источников известно что некоторые металлы сразу не дают о себе знать [5,6]).
Особенно увеличивается количество меди (до 40%) и серебра (до 7%) с водным раствором гидроксида натрия (NaOH). Наблюдается уменьшение количества меди от 9 до 2 % с расплавом гидроксида натрия (NaOH). Также наблюдается уменьшение количества ванадия (V), цинка (Zn) как с раствором,
Таблица 2
так и с расплавом гидроксида натрия (NaOH). По результатам спектрального анализа не наблюдается количественное содержание железа, кроме исходного образца пробы лидита.
Опыт 3. Извлечение кремнезёма с расплавом гидроксида натрия. Отделенного от оксида железа магниткой образцы лидита 115–Л в количестве 5 г нагревали, затем охлаждали как в первом опыте. В другой фарфоровой чашке расплавляли гидроксида натрия и смешивали с охлажденной до 30 оС лидитовой пробой при соотношении компонентов 1:2. Полученную смесь при нагревании тшательно перемешивали, охлаждали, затем добавляли воду. При этом нерастворимую в воде часть отделили от растворимой, сушили, прокаливали и провели спектральный анализ (табл. 2).
Опыт 4. Извлечение кремнезёма со смесью расплавом гидроксида и карбонатом натрия. Полученную смесь гидроксида и карбоната натрия при соотношении 1:1 расплавляли на фарфоровой чашке и добавляли в нагретый, а затем охлажденные до 30 оС образцы лидита, как в первом опыте и тщательно перемешивали при нагревании в течение 5 мин. Соотношение образцов лидита со смесью гидроксида и карбоната натрия составляло 1:2 [2, 3]. Затем после охлаждения к смеси добавляли воду и отделяли растворимую в воде часть от нерастворимой. Последнюю предварительно сушили, затем на муфельном печи прокаливали, после чего проводили спектральный анализ (табл. 2).
Результаты спектрального анализа исходных проб, исходных проб с гидроксидом и со смесью гидроксида и карбонатом натрия
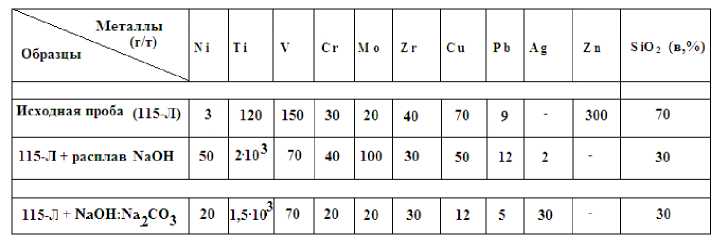
По результатам спектрального анализа исходной пробы образца лидита с расплавленным NaOH наблюдается увеличение количества некоторых металлов (Ni, Ti, Cr, Mo, Pb), в том числе Ag, который не был обнаружен в исходном образце (рис. 1.) В то же время, с расплавом гидроксида натрия наблюдается уменьшение количества ванадия, меди, циркония в нерастворимой части раствора (рис. 2).
При проведении исследования лидитовой пробы со смесями гидроксида и карбоната натрия, содержание кремнезёма резко падает до 30 %, где, в случае с расплавом гидроксида натрия, такого изменения не наблюдалось, его количество было, как и в исходном образце.
Благоприятствует смесь гидроксида и карбоната натрия к увеличению количества серебра до 30 г/т, когда с расплавом гидроксида натрия количество его увеличивалось всего лишь на 2 г/т. В то же время смесь гидроксида и карбоната натрия не благоприятствует увеличению количества тех металлов (Ni, Ti, Mo, Cr, Pb), содержание которых увеличивалось на значительное количество с расплавом гидроксида натрия. Наоборот, приводить к уменьшению их количества в составе нерастворимой части раствора (рис. 1).
Количество металлов, которое уменьшалось с расплавом гидроксида натрия (V, Zr), стабильно держится в этой смеси, за исключением резкого снижения количества меди.
Цинк, по спектральному анализу с расплавом гидроксида натрия и смесями NaOH:Na 2 CO 3 , не обнаруживается в составе твердой части раствора.
Выводы:
-
1. Для уменьшения количества кремнезёма в составе образца лидита можно применять и расплав и раствор гидроксида натрия.
-
2. Для обогащения количества некоторых металлов особенно Cu и Ag и уменьшения количество кремнезёма в составе образца лидита превосходит свойства раствора гидроксида натрия.
-
3. Смесь расплавов гидроксида и карбоната натрия является подходящим реагентом для уменьшения количества кремнезёма в составе образца лидита до 30%, и для увеличения количества серебра до 30 г/т.
-
4. Расплав гидроксида натрия вполне подходит в качестве реагента для обогащения таких металлов как Ti, Mo, Cr, Ni, Pb, Ag в образце лидита и применим для уменьшения количества кремнезёма.
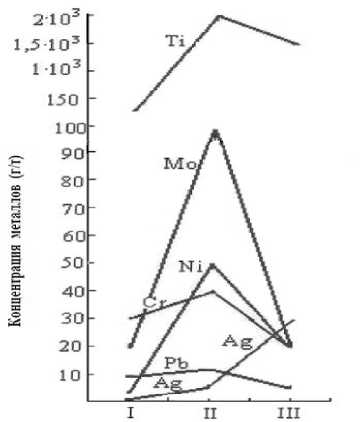
Рис. 1. Изменение концентрации металлов от реагентов (I - исходная проба; II – исходная проба с расплавом NaOH; III – исходная проба с расплавом смеси NaOH: Na 2 СO 3 ).
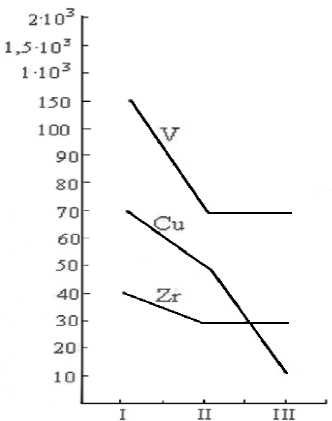
Рис. 2. Влияние реагентов на уменьшение количества металлов (I – исходная проба; II – исходная проба с расплавом NaOH; III – исходная проба с расплавом смеси NaOH: Na 2 СO 3 ).
Список литературы Химизм извлечения кремнезема из состава рудоносных минералов
- Адышев М.М. О стратиграфическом положении ванадиеносной углеродисто-кремнистой формации Тянь-Шаня//Докл. АН СССР. -1964. -0 Том 156, № 3. -С.543-546.
- Джаратов А. Особенности геологического строения, условий формирования и полезные ископаемые нижнепалеозойских отложений верховьев рек Чаткал и Сарыджаз (Срединный Тянь-Шань): Автореф. канд. дисс. -Фрунзе, 1986.
- Джаратов А. Об особенностях распространения потенциально платинометальных, алмазосодержащих рудно-геологических формаций в аспекте геогомографии//Известия КГТУ. -2007. -№ 12. -С. 255-257.
- Калмурзаев К.С., Сартбаев М.К., Джаратов А., Айтбаев Д.В. Металлоносные углеродистые отложения Кыргызстана. -Бишкек, 1992. -С. 23-26.
- Шарло Г. Методы аналитической химии. Количественный анализ неорганических соединений. -М-Л: «Химия», 1965. -811 с.
- Лабораторный практикум по общей химии/Под. ред. А.А. Таперовой. -Высшая школа, 1969. -186 с.


