Хирургическая коррекция коарктации аорты с гипоплазией дистальной дуги у пациентов раннего возраста
Автор: Сойнов Илья Александрович, Синельников Ю.С., Корнилов И.А., Ничай Н.Р., Гасанов Э.Н., Кулябин Ю.Ю., Омельченко А.Ю., Горбатых Ю.Н.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Врожденные пороки сердца
Статья в выпуске: 2 т.20, 2016 года.
Бесплатный доступ
Цель. Оценка отдаленных результатов, причин осложнений при хирургическом лечении коарктации с гипоплазией дистальной части дуги аорты. Материал и методы. В данном проспективном рандомизированном исследовании выполнена оценка результатов хирургического лечения 54 пациентов, которые перенесли оперативное лечение по поводу коарктации аорты. Пациенты были разделены на две группы по методу коррекции порока: реконструкция с использованием модифицированной реверсивной пластики левой подключичной артерии (I группа, 27 человек) и реконструкция с помощью extended анастомоза (II группа, 27 человек). Результаты. Рекоарктация аорты в отдаленном периоде наблюдалась в I группе у одного (3,84%) пациента, во второй группе у двоих (7,7%) пациентов; p = 0,5. Артериальную гипертензию в I группе имели 2 (7,7%) пациента, во II группе 8 (30,8%) пациентов; p = 0,03. Заключение. При современных типах коррекции зона анастомоза имела пропорциональный роет в различных сегментах дуги аорты и не влияла на послеоперационные осложнения. Предиктором артериальной гипертензии в отдаленном периоде после коррекции коарктации аорты у пациентов первого года жизни является фиброэластоз эндокарда и ригидность стенки восходящей аорты. Фактором развития рекоарктации аорты в отдаленном периоде является низкая масса тела пациента до операции. Персистенция артериальной гипертензии зависит от варианта коррекции. Одномоментная реконструкция дистальной части дуги позволяет снизить встречаемость артериальной гипертензии с 30,8 до 7,7%. Несмотря на разнообразие осложнений в отдаленном послеоперационном периоде, качество жизни детей не ухудшалось и находилось на высоком уровне в обеих группах.
Короткий адрес: https://sciup.org/142140869
IDR: 142140869 | DOI: 10.21688-1681-3472-2016-2-66-73
Surgical correction of coarctation of the aorta with distal aortic arch hypoplasia in infants
Aim: The paper focuses on assessment of the late results and causes of complications when repairing coarctation with distal aortic arch hypoplasia. Methods: This prospective randomized study included 54 patients who underwent repair of coarctation of the aorta. All patients were divided in 2 groups depending on the correction type: reconstruction using the modified reverse left subclavian artery flap plasty (Group I, 27 pts) or extended end-to-end anastomosis (Group II, 27 pts). Results: A postoperative follow-up period was 26 (21;31) months. Recoarctation of the aorta during long-term follow-up was found in 1 patient (3.84%) in Group I and in 2 patients (7.7%) in Group II (p=0.5). Two patients in the Group I (7.7%) and 8 patients in the Group II (30.8%) had arterial hypertension (p=0.03). Conclusion: With modern types of surgical correction used, the anastomotic area tended to proportionally grow in different segments of the aortic arch and did not influence the postoperative complications rate. Endocardial fibroelastosis and ascending aortic wall rigidity could be considered as predictors of arterial hypertension in the late period after coarctation repair in infants. Low body weight before surgery is a factor of aortic recoarctation development in the late postoperative period. Arterial hypertension persistence depends on the correction type. One-stage reconstruction of the distal aortic arch allows for reducing the rate of arterial hypertension from 30.8% to 7.7%. Despite a range of complications in the late postoperative period, the infants' quality of life was not affected and was high in both groups.
Текст научной статьи Хирургическая коррекция коарктации аорты с гипоплазией дистальной дуги у пациентов раннего возраста
Коарктация аорты относится к группе распространенных врожденных пороков сердца, среди новорожденных и младенцев данный порок составляет 6–10% случаев [1]. Локальное сужение аорты в 70% случаев сочетается с гипоплазией дистальной части или всей дуги аорты [1, 2]. Обычно обструкция дуги аорты у ново- рожденных требует неотложного хирургического вмешательства. С первых операций по устранению коарктации аорты, выполненных Crafoord и Gross более 70 лет назад [3], результаты лечения были значительно улучшены, однако отдаленные результаты нельзя назвать удовлетворительными. Достаточно данных свидетельствуют
Статья доступна по лицензии Creative Commons Attribution 4.0.
о высокой частоте развития рекоарктации аорты, артериальной гипертензии, аневризм аорты [3–5]. Многие авторы связывают высокую распространенность осложнений с выбранной методикой коррекции и вариантом формирования анастомоза [5, 6]. В настоящее время нет единого подхода к выбору варианта хирургической коррекции коарктации аорты [6–8]. Мы представляем проспективное исследование оценки двух популярных хирургических техник лечения коарктации аорты с гипоплазией дистальной части дуги аорты.
Материал и методы
В представленном проспективном рандомизированном исследовании выполнена оценка результатов хирургического лечения 54 пациентов первого года жизни с коарктацией и гипоплазией дистальной части дуги аорты, которые перенесли оперативное лечение в ННИИПК им. акад. Е.Н. Мешалкина с 2013 по 2014 г. Реконструкция дуги выполнялась двумя методами: с использованием комбинации модифицированной реверсивной пластики лоскутом левой подключичной артерии extended анастомозом (I группа, 27 пациентов) и с помощью extended анастомоза (II группа, 27 пациентов).
Диагноз «гипоплазия дуги аорты» устанавливался в том случае, если отклонение Z было не более –2. Степень гипоплазии аорты и пропорциональность роста анастомоза оценивалась по шкале Z score [9]. Всем пациентам проводили эхокардиографию в послеоперационном периоде.
Эластические свойства аорты оценивались в М-ре-жиме на двух уровнях: 1 – проксимальный отдел восходящей аорты, на 5 мм выше синотубулярного гребня; 2 – нисходящая брюшная аорта, проксимальнее чревного ствола. Курсор устанавливается строго перпендикулярно центральной линии аорты. Производились измерения максимальных и минимальных размеров движения стенки аорты. Параллельно фиксировалось давление на правой верхней конечности. Оценивались два показателя: растяжимость и индекс ригидности стенки Ао [10]. Ремоделирование дуги аорты исследовалось по методу Ou и соавторов [11].
Диагноз рекоарктации ставили, если градиент давления между верхними и нижними конечностями был выше 20 мм рт. ст. Артериальная гипертензия устанавливалась после трехкратного измерения артериального давления на приеме у детского кардиолога и подтверждалась с помощью суточного мониторирования артериального давления. Критерием диагностики артериальной гипертензии по данным суточного мониторирования являлось повышение средних значений систолического и/или диастолического артериального давления выше 95-го пер- центиля распределений этих параметров для соответствующих ростовых показателей [12].
Оценку качества жизни пациентов проводили через 24 мес. после коррекции порока с помощью родительского опросника для детей 2–4 года Pediatric Quality of Life Inventory™ 3.0 Cardiac Module (PedsQL Cardiac Module). Родительская форма отчета оценивала восприятие участниками качества жизни их ребенка [13]. Оперативное лечение выполнялось двумя хирургами.
После катетеризации с целью мониторинга артериального давления правых лучевой и бедренной артерий пациента укладывали на правый бок. Выполнялась заднебоковая торакотомия по 3-му межреберью. Осуществлялась мобилизация нисходящей аорты, дуги аорты до брахиоцефального ствола, а также на протяжении 3–4 см выделялась левая подключичная артерия. Открытый артериальный проток лигировался у легочного конца. Аортальные зажимы накладывались: проксимальный сразу после отхождения брахиоцефального ствола, дистальный на нисходящую аорту на 2–3 см ниже суженного участка аорты.
У 27 пациентов выполнялся extended анастомоз [8], и у 27 пациентов формирование расширенного косого анастомоза под дугу было дополнено реверсивной пластикой дистальной дуги лоскутом левой подключичной артерии [14].
Статистический анализ
Анализ данных хирургического лечения проводился с помощью программы Stata 13 (StataCorp LP). Количественные переменные представлены в виде медианы (25-й; 75-й процентили), если не указаны другие. Качественные переменные представлены в виде чисел (%). Использовались тесты Манна – Уитни, критерии хи-квадрат или Фишера для межгрупповых сравнений. При сравнении трех и более независимых групп по одному количественному признаку применяли методы непараметрической статистики (ранговый анализ вариаций по Краскелу – Уоллису). При выявлении статистически значимых различий в группах проводилось парное сравнение групп с использованием непараметрического теста Манна – Уитни с поправкой Бонферрони для преодоления проблем множественных сравнений. Анализ выживаемости в отношении свободы от возврата артериальной гипертензии и рекоарктации аорты проводился с применением метода Каплана – Майера. Для сравнения двух кривых выживаемости использовался лог-ранк тест. Для выявления предикторных переменных в отношении бинарных исходов применялись простая и множественная логистические регрессии. Регрессия пропорциональных рисков Кокса
Таблица 1 Демографические характеристики
|
Характеристика |
I группа |
II группа |
p |
|
Возраст, дней |
63,6 (9; 96) |
67,55 (21; 94) |
0,85 |
|
Фиброэластоз, n (%) |
4 (14,8) |
7 (25,9) |
0,31 |
|
Вес, кг |
3,95 (3,2; 4,25) |
4,5 (3,2; 5,1) |
0,11 |
|
Площадь поверхности тела, м2 |
0,24 (0,21; 0,26) |
0,25 (0,21; 0,29) |
0,35 |
|
Пол, n (%) |
0,08 |
||
|
мужской |
15 (55,5) |
21 (77,7) |
34 |
|
женский |
12 (44,5) |
6 (22,3) |
20 |
Представлена медиана
(25-й; 75-й процентили) или числовой показатель (%)
использовалась для оценки связи между одной и более непрерывными или категориальными переменными и временем до наступления неблагоприятного события. Уровень значимости для всех методов p<0,05.
Результаты
Демографические характеристики пациентов приведены в табл. 1. Группы были сопоставимы по возрасту, полу, массе и площади поверхности тела, удельному весу фиброэластоза.
Сразу после хирургической коррекции градиент давления (правая лучевая бедренная артерия) отсутствовал. Общее время пережатия аорты составило не более 25 мин.
Во время операции никто из пациентов не умер, 2 случая летальности произошли в ближайший послеоперационный период. Летальность в группе с модифицированной реверсивной пластикой левой подключичной артерии составила 1 (3,7%) случай, причиной смерти явилась поли- органная недостаточность. В группе с extended анастомозом летальность составила также 1 (3,7%) случай, причина смерти – полиорганная недостаточность в сочетании с сепсисом. Достоверного различия по показателю госпитальной летальности между группами не было; р>0,99.
Средний период наблюдения пациентов в отделении реанимации достоверно различался: в I группе 5,4 (3; 7) суток, во II группе 4,6 (2; 5) суток; p = 0,01.
До операции выявлены высокий индекс ригидности и низкий уровень растяжимости аорты, которые достоверно не различались между группами (индекс ригидности p= 0,9; индекс растяжимости p = 0,76). В раннем послеоперационном периоде обнаружено улучшение эластических свойств аорты, однако показатели ригидности и растяжимости восходящей аорты не различались достоверно между группами (индекс ригидности p = 0,38; индекс растяжимости p = 0,4).
При оценке параметров дуги аорты Z score проксимальной дуги аорты в I группе составил –0,8 (–1,2; –0,5), во II группе –0,75 (–1,2; –0,4); p = 0,97. Показатели Z score дистальной дуги аорты достоверно различались между группами: в группе с реверсивной пластикой показатель составил 0,43 (0; 1), в группе extended анастомоза –0,15 (–0,9; 0,5); p = 0,005. Послеоперационные осложнения представлены в табл. 2.
Как видно из табл. 2, самым частым и специфичным осложнением послеоперационного периода явилась парадоксальная гипертензия, которая была значительно выше в группе с extended анастомозом – 66,6 против 37% у пациентов с реверсивной пластикой подключичным лоскутом; p = 0,048. Многофакторный регрессионный анализ выявил, что увеличение возраста пациента на каждые 10 дней повышает риск парадоксальной гипертензии в 1,27 раза (ОШ 1,27; 95% ДИ 1,06–1,4; p = 0,012). Частота прочих осложнений не различалась между группами.
Таблица 2 Ранние послеоперационные осложнения
|
Показатель |
I группа, n (%) |
II группа, n (%) |
p |
|
Сердечная недостаточность |
2 (7,4) |
1 (3,7) |
0,56 |
|
Дыхательная недостаточность |
8 (29,5) |
5 (18,5) |
0,15 |
|
Почечная недостаточность |
2 (7,4) |
2 (7,4) |
>0,99 |
|
Полиорганная недостаточность |
3 (11,1) |
1 (3,7) |
0,3 |
|
Гастроинтестинальная недостаточность |
1 (3,7) |
2 (7,4) |
0,56 |
|
Пневмония |
5 (18,5) |
5 (18,5) |
>0,99 |
|
Хилоторакс |
0 (0) |
1 (3,7) |
0,32 |
|
Сепсис |
0 (0) |
1 (3,7) |
0,32 |
|
Компрессия бронха |
0 (0) |
1 (3,7) |
0,32 |
|
Парадоксальная гипертензия |
10 (37,0) |
18 (66,6) |
0,048 |
Представлена медиана (25-й; 75-й процентили) или числовой показатель (%)
Таблица 3 Внутригрупповая оценка пропорциональности роста анастомоза
I группа (Z score)
|
Показатель |
До операции |
После операции |
12 мес. |
p |
|
Проксимальная дуга |
–1,8 (–2; –1,2) |
–0,8 (–1,2; –0,5) |
–0,39 (–0,9; 0) |
0,0001 |
|
Дистальная дуга |
–2,95 (–3,4; –2,6) |
0,43 (0; 1) |
0,66 (–0,1; 1,2) |
0,0001 |
|
II группа (Z score) |
||||
|
Проксимальная дуга |
–1,75 (–2,1; –1,3) |
–0,75 (–1,2; –0,4) |
–0,31 (–0,8; 0) |
0,0001 |
|
Дистальная дуга |
–2,85 (–3,3; –2,4) |
–0,15 (–0,9; 0,5) |
0,39 (–0,1; 0,9) |
0,0001 |
Представлена медиана (25-й; 75-й процентили) или числовой показатель (%)
Послеоперационный период наблюдения составил 26 (21; 31) мес. Всем пациентам для оценки упруго-эластических свойств и индекса массы миокарда выполняли эхокардиографию. При оценке эхокардиографических параметров индекс массы миокарда в I группе составил 49,3 (44; 59,5), во II группе 62,8 (52; 73); p = 0,006. Обнаружена тенденция к снижению эластических свойств и повышению ригидности в обеих группах как для восходящей, так и нисходящей аорты через год после операции. В I группе растяжимость восходящей аорты значительно выше, p = 0,0018, в то время как ригидность – во II группе; p = 0,017.
В отдаленном периоде Z score проксимальной дуги аорты в I группе составил –0,39 (–0,9; 0), во II группе –0,31 (–0,8; 0); p = 0,7. Z score дистальной дуги аорты также не различались между группами: в группе с реверсивной пластикой показатель составил 0,66 (–0,1; 1,2), в группе extended анастомоза 0,39 (–0,1; 0,9); p = 0,2.
Внутригрупповая оценка пропорциональности роста анастомоза представлена в табл. 3.
При внутригрупповой оценке выявлено, что в обеих группах дуга имела пропорциональный рост с достоверными различиями; p<0,01.
Ремоделирование дуги аорты оценивалось с помощью мультиспиральной компьютерной томографии через 12 мес. после операции. В I группе было 9 (34,6%) случаев ремоделирования дуги, во II группе 12 (46,15%) случаев; p = 0,27. При детальном исследовании ремоделированных дуг аорты готическую дугу имели 4 (15,3%) пациента во II группе, в то время как в I группе случаев готической дуги не отмечено; p = 0,01. Амбразурную дугу имели 9 (34,6%) в I группе и 8 (30,7%) человек во II группе; p = 0,7. Романическую дугу имели 17 (65,4%) в I группе и 14 (53,85%) пациентов во II группе; p = 0,2.
Осложнения в отдаленном периоде были у 15 пациентов (28,8%). Стеноз устья сонной артерии встречался у одного пациента (3,84%) с реверсивной пластикой, p = 0,3, который успешно устранен путем баллонной дилатации устья сонной артерии. Окклюзия левой подключичной артерии также случилась у одного пациента (3,84%) из I груп- пы; p = 0,3. Повторная операция ему не выполнялась, а при оценке функции левой верхней конечности не выявлено отклонений в росте и функции.
Аневризмы аорты зафиксированы в 2 случаях (7,7%). Все случаи приходились на группу пациентов с реверсивной пластикой. При анализе аневризм аорты не выявлено достоверной разницы между группами; p = 0,15.
Рекоарктация аорты в отдаленном периоде наблюдалась у 3 (5,7%) пациентов: в I группе у одного (3,84%), во II группе у двух (7,7%); p = 0,5. В зависимости от степени сужения перешейка аорты выполнялась открытая операция или баллонная ангиопластика (при небольшом сужении перешейка). Согласно однофакторному анализу Кокса, единственный фактор риска рекоарктации аорты – малый вес пациента (ОШ 0,016; 95% ДИ 0,001–0,51; р = 0,047).
Самым частым осложнением отдаленного периода явилась артериальная гипертензия, которую имели 19,2% пациентов. В I группе артериальную гипертензию имели 2 (7,7%) пациента, во II группе 8 (30,8%) пациентов; p = 0,03. Артериальная гипертензия, требующая приема лекарственных препаратов, выявлена у 4 (15,4%) пациентов во II группе, в то время как в I группе такие пациенты отсутствовали; p = 0,02. Остальные пациенты имели скрытую гипертензию или гипертонический ответ: в I группе 2 (7,7%) пациента, во II группе 4 (15,4%) пациента; p = 0,2. Оценка свободы от артериальной гипертензии проводилась по методу Каплана – Майера (рис. 1).
Для выявления предикторов артериальной гипертензии выполнен однофакторный и многофакторный анализ Кокса. Однофакторный и многофакторный анализ Кокса для артериальной гипертензии представлен в табл. 4.
Одним из факторов риска, который влиял на персистенцию артериальной гипертензии, являлся фиброэластоз. Каждый случай фиброэластоза повышал риск артериальной гипертензии в 211,8 раза. Вторым фактором риска являлась ригидность стенки восходящей аорты в период наблюдения 12 мес. Выявлено, что на каждую единицу индекса ригидности стенки восходящей аорты вероятность артериальной гипертензии увеличивалась в 28,5 раза.
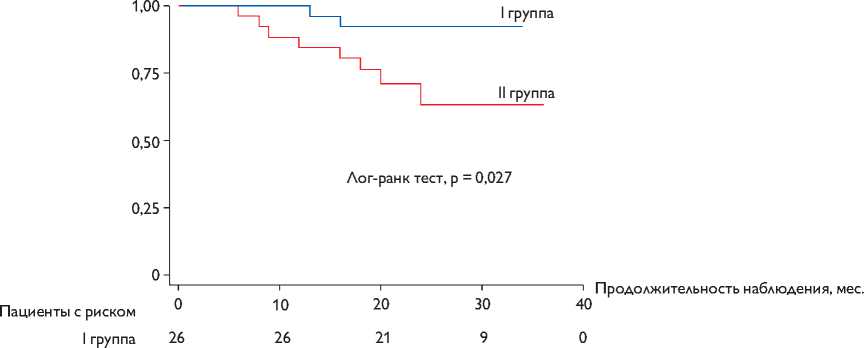
II группа 26 23 15 3 0
Рис. 1. Оценка свободы от артериальной гипертензии по методу Каплана – Майера
Fig. 1. Evaluation of freedom from arterial hypertension as per Kaplan-Meier method
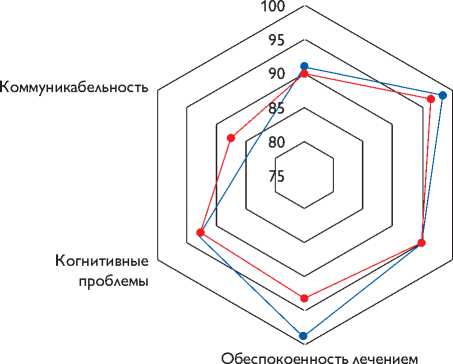
Оценку качества жизни пациентов проводили через 24 мес. после коррекции порока с помощью родительского опросника для детей 2–4 года Pediatric Quality of Life Inventory™ 3.0 Cardiac Module. В ходе анализа опроса родителей выявлено незначительное снижение оценок качества жизни по большинству шкал опросника, что свидетельствовало об исходно хорошем уровне качества жизни детей (рис. 2).
Сердечные проблемы не различались между группами: в I группе 91,2 (85; 97), во II группе 90,1 (83; 97); p = 0,56. Компонент «Лечение» имел статистический прирост, но также не различался между группами: в I группе 99 (98,1; 99,9), во II группе 96,8 (93,7; 99,8); p = 0,06. Восприятие физической внешности в I группе 94,8 (90; 99), во II группе 94,8±5,1 (89; 99); p = 0,99. Достоверно между группами различалась лишь обеспокоенность по поводу лечения: в I группе 98,5 (97,2; 99,8), во II группе 93,2 (86,1; 99,3); p = 0,0004. Показатель «Когнитивные проблемы» в I группе 92,9 (87; 98), во II группе 92,2 (85; 98); p = 0,74. Коммуникабельность в I группе 83,6 (74; 92), во II группе 86,5 (74; 98); p = 0,33.
Обсуждение
Современные возможности диагностики, анестезиологического и медикаментозного обеспечения и внедрение технологий способствовали качественно новому подходу в лечении пациентов с коарктацией аорты и реабилитации пациентов. Однако по-прежнему вызывают обеспокоенность персистенция в послеоперационном
Таблица 4 Однофакторный и многофакторный анализ Кокса для артериальной гипертензии
|
Признак |
Однофакторный анализ |
Многофакторный анализ |
||
|
Отношение рисков (95% доверительный интервал) |
p |
Отношение рисков (95% доверительный интервал) |
p |
|
|
Группа |
4,81 (1,02; 22,7) |
0,047 |
– |
– |
|
Фиброэластоз |
25,4 (4,8; 135) |
0,0001 |
211,8 (4,4; 1013) |
0,007 |
|
Z дистальной дуги аорты 6 мес. |
0,33 (0,13; 0,79) |
0,013 |
– |
– |
|
Ригидность восходящей аорты 1 год |
12,5 (3,8; 40,9) |
0,0001 |
28,5 (2,3; 342) |
0,032 |
|
Растяжимость восходящей аорты 1 год |
0,86 (0,81; 0,92) |
0,0001 |
– |
– |
|
Готическая дуга |
24 (6,2; 92,9) |
0,0001 |
– |
– |
|
Индекс массы миокарда |
1,04 (1,02; 1,07) |
0,0001 |
– |
– |
Проблемы сердечно-сосудистой системы
Лечение
Внешность
Рис. 2. Распределение оценки качества жизни в группах
I группа
II группа
Fig. 2. Distribution of evaluation of quality of life in groups
периоде артериальной гипертензии и случаи рекоарктации аорты. В раннем послеоперационном периоде у 54% пациентов наблюдалась парадоксальная гипертензия. Основным фактором риска парадоксальной гипертензии являлся возраст пациента, поэтому ранняя хирургическая коррекция может снижать частоту парадоксальной гипертензии. Артериальную гипертензию в нашем исследовании после 24-часового мониторинга имели 19,2% пациентов. Высокий процент артериальной гипертензии отмечен во многих исследованиях, в том числе и O’Sullivan, который, как и мы, исследовал детей, оперированных в возрасте до 12 мес. [15]. Мы также установили, что большинство пациентов (11,5%) имели скрытую гипертензию или гипертонический ответ на физическую нагрузку и лишь 7,7% пациентов имеют стойкую гипертензию, требующую приема гипотензивных препаратов. Hager и коллеги [16] в исследовании продемонстрировали противоположные результаты (25% – стойкая гипертензия и 10% – скрытая гипертензия), однако их когорта больных включала как детей раннего возраста, так и взрослых пациентов. Мы считаем, что с ростом ребенка скрытая гипертензия может переходить в стойкую форму. Этому может способствовать ремоделирование дуги аорты или прогрессирующее снижение упруго-эластических свойств стенки аорты [10, 11, 17]. Оценка упруго-эластических свойств стенки восходящей аорты (высокие цифры ригидности стенки) позволяет на ранних этапах предположить артериальную гипертензию.
Персистирующая артериальная гипертензия может также зависеть и от типа анастомоза [4]. В нашем ис- следовании пациенты с extended анастомозом показали более высокую гипертензию в послеоперационном периоде, чем пациенты с реверсивной пластикой: 30,8 против 7,7%. Похожие данные демонстрировали Sciolaro и коллеги [7], которые также выявили, что в группе с extended анастомозом частота гипертонии была значительно выше, 29 против 4%, по сравнению с группой реверсивной пластики. Артериальной гипертензии способствуют структурные особенности микроскопического строения стенки аорты (изменения эластично-коллагенового каркаса), функциональные нарушения (изменение функции барорецепторов) и макроанатомические (геометрические) особенности, обусловленные отличием формы дуги аорты после операции от нормальной нативной формы, иммуновос-палительная реакция [10, 11, 17, 18, 19]. В нашем исследовании мы выявили два основных фактора риска, которые приводили к артериальной гипертензии: ригидность стенки аорты и фиброэластоз эндокарда.
Помимо основных причин непропорциональность роста анастомоза и сужение на уровне анастомоза могут способствовать обструктивной гипертензии [15]. Обструкция дуги на уровне анастомоза может приводить и к рекоарктации, и к аневризмам аорты, поэтому оценка зоны роста анастомоза с помощью параметров Z score в отдаленном периоде способствует ранней диагностики этих заболеваний. В нашем случае в обеих группах рост анастомоза был пропорционален и по данным регрессионного анализа не являлся фактором риска для этих осложнений.
Частота рекоарктации в нашем исследовании составила 5,7%. Cobanoglu A. и соавторы в исследовании полагают, что причиной рекоарктации является остаточная дуктальная ткань [20]. Zehr K. отмечает влияние низкой массы тела (менее 3 кг) на возникновение рекоарктации [21]. Poirier N.C. показал, что причиной рекоарктации у пациентов в 81% случаев явилась некоррегированная гипоплазия дуги [22]. В нашем исследовании единственный фактор риска – низкая масса тела. Еще одной причиной рекоарктации аорты называют тип формирования анастомоза, однако в нашем исследовании частота рекоарктации между группами не различалась: 7,7% extended анастомоз против 3,84% реверсивной пластики.
Находкой в нашем исследовании являются два случая аневризм в дистальной части дуги аорты у пациентов с реверсивной пластикой. Подобные случаи были уже описаны в более чем 7 случаях, однако причина образований аневризм при пластике подключичным лоскутом не ясна. Одни авторы предполагают, что причиной может служить остаточная дуктальная ткань, другие – слабость стенки подключичной артерии. Мы не располагаем аргументированными данными, позволяющими подтвердить или опровергнуть эти гипотезы [23, 24, 25].
Заключение
-
1. При современных типах коррекции зона анастомоза имела пропорциональный рост в различных сегментах дуги аорты и не влияла на послеоперационные осложнения.
-
2. Предикторами артериальной гипертензии в отдаленном периоде после коррекции коарктации аорты у пациентов первого года жизни являются фиброэластоз эндокарда и ригидность стенки восходящей аорты.
-
3. Фактором развития рекоарктации аорты в отдаленном периоде является низкая масса тела пациента до операции.
-
4. Персистенция артериальной гипертензии зависит от варианта коррекции. Одномоментная реконструкция дистальной части дуги позволяет снизить встречаемость артериальной гипертензии с 30,8 до 7,7%.
-
5. Несмотря на разнообразие осложнений в отдаленном послеоперационном периоде качество жизни детей находилось на высоком уровне в обеих группах.
-
6. Группа одифицированной реверсивной пластики левой подключичной артерии имеет более высокие эластические свойства дуги аорты по сравнению с группой extended анастомоза, что позволяет снизить частоту артериальной гипертензии в отдаленном послеоперационном периоде.
Финансирование
Исследование не имело спонсорской поддержки.
Список литературы Хирургическая коррекция коарктации аорты с гипоплазией дистальной дуги у пациентов раннего возраста
- Сойнов И.А., Синельников Ю.С., Горбатых А.В., Ничай Н.Р., Иванцов С.М., Корнилов И.А., Кшановская М.С., Горбатых Ю.Н. Артериальная гипертензия у пациентов после коррекции коарктации и гипоплазии дуги аорты//Патология кровообращения и кардиохирургия. 2015. Т. 19. № 2. С. 102-113.
- Сойнов И.А., Синельников Ю.С., Кливер Е.Э., Корнилов И.А., Ничай Н.Р., Горбатых А.В., Кулябин Ю.Ю., Горбатых Ю.Н. Морфологические особенности брахиоцефальных артерий у пациентов с гипоплазией дуги аорты//Патология кровообращения и кардиохирургия. 2015. Т. 19. № 4. С. 14-18.
- Jenkins N.P., Ward C. Coarctation of the aorta: natural history and outcome after surgical treatment//QJ Med. 1999. Vol. 92. P. 365-371.
- Luijendijk P., Bouma B.J., Vriend J.W., Vliegen H.W., Groenink M., Mulder B.J. Usefulness of exercise-induced hypertension as predictor of chronic hypertension in adults after operative therapy for aortic isthmic coarctation in childhood//Am. J. Cardiol. 2011. Vol. 108. No. 3. P. 435-439. DOI: 10.1016/j. amjcard.2011.03.063.
- Горбатых Ю.Н., Синельников Ю.С., Сойнов И.А., Корнилов И.А., Кшановская М.С., Горбатых А.В., Иванцов С.М., Омельченко А.Ю. Хирургическая коррекция аномалий дуги аорты у младенцев в условиях искусственного кровообращения//Хирургия. Журнал им. Н.И. Пирогова. 2015. № 8. С. 18-21.
- Pandey R., Jackson M., Ajab S., Gladman G., Pozzi M. Subclavian flap repair: review of 399 patients at median follow-up of fourteen years//Ann. Thorac. Surg. 2006. Vol. 81. P. 1420-1428.
- Sciolaro C., Copeland J., Cork R., Barkenbush M., Donnerstein R., Goldberg S. Long-term follow-up comparing subclavian flap angioplasty to resection with modified oblique end-to-end anastomosis//J. Thorac. Cardiovasc. Surg. 1991. Vol. 101. P. 1-13.
- Backer C., Mavroudis C., Zias E.A. Repair of coarctation with resection and extended end-to-end anastomosis//Ann. Thorac. Surg. 1998. Vol. 66. P. 1365-1371.
- Pettersen M.D., Du W., Skeens M.E., Humes R.A. Regression equations for calculation of z scores of cardiac structures in a large cohort of healthy infants, children, and adolescents: an echocardiographic study//J. Am. Soc. Echocardiogr. 2008. Vol. 21. No. 8. P. 922-934 DOI: 10.1016/j.echo.2008.02.006
- Kuhn A., Baumgartner C., Horer J., Schreiber C., Hess J., Vogt M. Impaired elastic properties of the ascending aorta persist within the first three years of neonatal coarctation repair//Pediatr. Cardiol. 2009. Vol. 30. P. 46-51. DOI: 10.1007/s00246-008-9280-6.
- Ou P., Celermajer D., Mousseaux E., Giron A., Aggoun Y., Szezepanski I., Sidi D., Bonnet D. Vascular remodelling after successful repair of coarctation//J. Am. Coll. Cardiol. 2007. Vol. 49. P. 883-890.
- The fourth on the diagnosis and treatment of the high blood pressure in children and adolescents. National High Blood Pressure Education Program Working Group on High Blood Pressure in Children and Adolescents//Pediatrics. 2004. Vol. 114. No. 2. P. 555-576.
- Uzark K., Jones K., Slusher J., Limbers C.A., Burwinkle T.M., Varni J.W. Quality of life in children with heart disease as perceived by children and parents//Pediatrics. 2008. Vol. 121. No. 5. P. 1060-1067 DOI: 10.1542/peds.2006-3778
- Sinelnikov Y.S., Gorbatyh A.V., Ivantsov S.M., Strelnikova M.S., Kornilov I.A., Gorbatyh Y.N. Reverse subclavian flap repair and maintenance of antegrade blood flow within the left subclavian artery in neonates with aortic coarctation and distal arch hypoplasia//Heart Surg. Forum. 2013. Vol. 16. No. 1. P. 52-56 DOI: 10.1532/HSF98.20121044
- O'Sullivan J.J., Derrick G., Darnell R. Prevalence of hypertension in children after early repair of coarctation of the aorta: a cohort study using casual and 24 hour blood pressure measurement//Heart. 2002. Vol. 88. P. 163-166.
- Hager A., Kanz S., Kaemmerer H., Schreiber C., Hess J. Coarctation long term follow up: significance of arterial hypertension in a cohort of 404 patients up to 27 years after surgical resection of isolated coarctationevenin the absence of recordation and prosthetic material//J. Thorac. Cardiovasc. Surg. 2007. Vol. 134. P. 738-745 DOI: 10.1016/j.jtcvs.2007.04.027
- Синельников Ю.С., Кшановская М.С., Прохорова Д.С., Нарциссова Г.П., Горбатых А.В., Иванцов С.М., Сойнов И.А., Корнилов И.А. Хирургическая коррекция коарктации аорты, всегда ли оправданы ожидания?//Сибирский медицинский журнал. 2013. Т. 28. № 4. С. 55-58.
- Kenny D., Polson J., Martin R., Caputo M., Wilson D., Cockcroft J., Paton J., Wolf A. Relationship of aortic pulse wave velocity and baroreceptor reflex sensitivity to blood pressure control in patients with repaired coarctation of the aorta//Am. Heart. J. 2011. Vol. 162. P. 398-404. DOI: 10.1016/j. ahj.2011.03.029.
- Brili S., Antonopoulos A.S., Oikonomou E., Kalampogias A., Papamikroulis G.-A., Chrysochoou C., Mourouzis K., Nihoyanopoulos P., Tousoulis D. Impairment of arterial elastic properties and elevated circulation levels of transforming growth factor-beta in subjects with repaired coarctation of aorta//International Journal of Cardiology. 2016. Vol. 207. P. 282-283 DOI: 10.1016/j.ijcard.2016.01.168
- Cobanoglu A., Teply J.F., Grunkemeier G.L., Sunderland C.O., Starr A. Coarctation of the aorta in patients younger than three months: a critique of the subclavian flap operation//J. Thorac. Cardiovasc. Surg. 1985. Vol. 89. P. 12S-135.
- Zehr K., Gillinov M., Redmond M., Greene P.S., Kan J.S., Gardner T.J., Reitz B.A., Cameron D.E. Repair of coarctation of the aorta in neonates and infants: a thirty year experience//Ann. Thorac. Surg. 1995. Vol. 59. P. 33-41.
- Poirier N.C., Van Arsdell G.S., Brindle M., Thyagarajan G.K., Coles J.G., Black M.D., Freedom R.M., Williams W.G. Surgical treatment of aortic hypoplasia in infants and children with biventricular hearts//Ann. Thorac. Surg. 1999. Vol. 68. P. 229З-2297.
- Fiore A.C., Fischer L.K., Schwartz T., Jureidini S., Balfour I., Carpenter D., Demello D., Virgo K.S., Pennington D.G., Johnson R.G. Comparison of angioplasty and surgery for neonatal aortic coarctation//Ann. Thorac. Surg. 2005. Vol. 80. P. 1659-1665.
- Unnikrishnana M., Theodorea S., Peter A.M. Late thoracic aortic dissecting aneurysm following balloon angioplasty for recoarctation after subclavian flap aortoplasty in childhood-successful surgical repair under circulatory arrest//European Journal of Cardiothoracic Surgery. 2ОО5. Vol. 27. P. 52O-522.
- Theodore S., Varma P.K., Neema P.K., Neelakandhan K.S. Late aneurysm formation with destruction of the left lung after subclavian flap angioplasty for coarctation of aorta//J. Thorac. Cardiovasc. Surg. 2005. Vol. 129. P. 468-469 DOI: 10.1016/j.jtcvs.2004.07.026


