Хирургические методы вторичной профилактики лакунарного инсульта
Автор: Шевченко Ю.Л., Кузнецов А.Н., Виноградов О.И.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.4, 2009 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140187736
IDR: 140187736 | УДК: 616.831-004.8.-0051:
Текст статьи Хирургические методы вторичной профилактики лакунарного инсульта
УДК: 616.831-004.8.-0051: 616-089.193.4
Национальный медико-хирургический центр им. Н.И. Пирогова
SURGICAL METHODS OF SECONDARY PROPHYLAXIS OF LACUNAR STROKE
Shevchenko Yu.L., Kuznetsov A.N., Vinogradov O.I.
Лакунарным называется ишемический церебральный инфаркт, возникающий вследствие окклюзии одной из малых перфорантных артерий, кровоснабжающих глубинные отделы больших полушарий и ствол головного мозга. В исходе лакунарного инфаркта образуется полость округлой формы, заполненная ликвором – лакуна [1, 2, 4, 7, 8].
Согласно «лакунарной гипотезе», сформулированной Fisher C. в 1965 г., лакунарный инфаркт (ЛИ) развивается вследствие микроангиопатии перфорантных артерий, вызванной артериальной гипертензией и церебральным атеросклерозом. Он также ввел термины «липогиалиноз» и «микроатероматоз» для характеристики изменений, происходящих в стенках перфорантных артерий [10].
Возможность эмболического механизма развития ЛИ в настоящее время остается дискутабельной. По мнению Donnan G, верификация лакунарного инсульта у пациента, позволяет сделать точный вывод о патофизиологическом механизме его развития и прогнозе. Автор считает, что патогенез ЛИ заключается в собственно болезни малых сосудов (in situ), следовательно, такие пациенты не требуют поиска удаленного источника церебральной эмболии. Donnan G находит маловероятным, что эмболия из внечерепных отделов сонной артерии, ветвей аорты или сердца может привести к развитию ЛИ, вследствие чего клинические мероприятия можно сосредоточить на профилактике факторов риска острых сосудистых заболеваний и реабилитации [13].
Однако не все исследователи разделяют эту точку зрения. Так, Bakshi R. и соавт. сообщают, что при инфекционном эндокардите (ИЭ) в 50% случаев по данным МРТ головного мозга визуализируются лакунарные очаги [6]. При этом пациенты зачастую не имеют классических «сосудистых» факторов риска, на фоне которых могла бы развиться микроангиопатия перфорантных артерий. Похожие наблюдения продемонстрировали Ю.Л. Шевченко и соавт, которые описали, что при ИЭ в большинстве случаев визуализируются мелкие (до 2 см) ишемические очаги в бассейнах концевых ветвей средних мозговых артерий или лакуны в глубинных отделах полушарий головного мозга [5]. Авторы считают, что такое ишемическое повреждение головного мозга обусловлено небольшими размерами эмболов, представляющих собой фрагменты клапанных вегетаций.
Deborah R. с соавт. в 1992 г. опубликовали данные исследования 108 пациентов с лентикулостриарной локализацией ЛИ. Гипертоническая болезнь была верифицирована у 68% пациентов, сахарный диабет – у 37%, одномоментно обе нозологии присутствовали у 28% больных, одномоментно артериальная гипертензия (АГ) и сахарный диабет (СД) отсутствовали у 23%. Атеросклеротические бляшки, как возможный источник церебральной эмболии, были диагностированы у 23% пациентов, а 18% имели потенциальные кардиальные источники эмболии. Авторы пришли к выводу, что частая встречаемость эмболических источников у пациентов с ЛИ в условиях отсутствия таких факторов риска, как АГ или СД, свидетельствуют о существовании механизмов развития ЛИ, отличных от микроангиопатии [9].
Возможность эмболического механизма развития лакунарного инфаркта головного мозга меняет подходы к его вторичной профилактике. Помимо коррекции «сосудистых» факторов риска и назначении антиагрегантной, антигипертензивной и гиполипидемической терапии необходимо рассмотреть вопрос о хирургическом удалении источника церебральной эмболии.
Существующие в настоящее время рекомендации по вторичной профилактике ишемического инсульта (Европейской организации по инсульту от 2008 г., Американской ассоциации по инсульту от 2007 г. и Всероссийского общества неврологов от 2007 г.) [3, 11, 12] постулируют необходимость выполнения каротидной эндартерэктомии (КЭ) или каротидной чрескожной транслюминальной баллонной ангиопластики и/или стентирования (КАС) в случае наличия у пациента симптомного стеноза внутренней сонной артерии >70%. Решение о хирургической коррекции симптомного стеноза 50–69% принимается в зависимости от наличия дополнительных факторов (пол, возраст и выраженность неврологического дефицита).
Однако, в проведенных в настоящее время проспективных исследованиях, посвященных оценке эффективности и безопасности КЭ у пациентов с симптомным стенозом сонных артерий более 70% (NASCET, ECST и Veterans Affairs Cooperative Study Program) пациенты с ЛИ встречались редко (менее чем в 7% случаев), что не позволило сделать заключение о безопасности энадартерэк-томии сонных артерий у данной категории больных.
В доступной современной литературе отсутствуют критерии верификации эмболического генеза ЛИ, не регламентированы подходы к режиму вторичной профилактики у данных больных и остается неясной безопасность хирургического удаления эмбологенного источника.
Целью настоящего исследования было определить критерии верификации эмболического генеза лакунарного инфаркта головного мозга, предложить подходы к вторичной профилактике у данной категории больных и оценить безопасность хирургического удаления источника церебральной эмболии.
Материал и методы
Нами было обследовано 34 больных ЛИ с верифицированным потенциальным источником церебральной эмболии, подвергшихся оперативному вмешательству с целью его удаления. По виду эмбологенного источника пациенты были разделены на 2 группы. I группа – 20 больных ЛИ с артериальным источником эмболии. II группа – 14 больных ЛИ с кардиогенным источником эмболии. Среди обследованных больных был 21 мужчина и 13 женщин в возрасте от 39 до 79 лет, средний возраст составил 47,2±5,1 года.
Пациентам I группы в 15 случаях была выполнена каротидная эндартерэктомия, в 5 – каротидная чрескожная транслюминальная баллонная ангиопластика со стентированием. У всех больных стеноз сонной артерии >50% был расположен ипсилатерально к аффектированному полушарию.
Во II группе 9 пациентов страдали ревматической болезнью сердца, 5 – инфекционным эндокардитом. Протезирование митрального клапана выполнено 10 пациентам, аортального клапана – 4 пациентам. В случае наличия признаков инфекционного процесса – проводилась санация полостей сердца. Операции выполнялись с использованием искусственного кровообращения, умеренной гипотермии (охлаждение производилось до температуры ядра около 28° С) и фармако-холодовой кардиоплегии.
Диагноз лакунарного инфаркта головного мозга был поставлен на основании клинической картины (наличие «классического» лакунарного синдрома) и данных КТ/МРТ (наличие «лакуны» в глубинных отделах полушария). Давность ЛИ составляла от 2 недель до 14 месяцев.
Всем пациентам выполнялось:
-
1. оценка факторов риска развития инсульта;
-
2. компьютерная томография головного мозга («Som-atom Sensation 4», Siemens, Германия) или магнитнорезонансная томография головного мозга («Giroscan Intera Nova», Philips, Голландия);
-
3. трансторакальная или трансэзофагеальная эхокардиография («Vivid 7», General Electric, США);
-
4. дуплексное сканирование («Vivid 7», General Electric, США) или селективная ангиография («Infinix CS-1», Toshiba, Япония) брахиоцефальных и церебральных артерий;
-
5. транскраниальная допплерография с билатеральной локацией средних мозговых артерий в течение 60 мин и детекцией микроэмболических сигналов («Sonomed-300», Спектромед, Россия);
-
6. лабораторная диагностика биохимических показателей крови («Olympus 640», Olympus, Япония) и свёртывающей системы крови («BCT DADE», Behring, Германия);
-
7. оценка тяжести неврологического дефицита по шкале NIHSS.
Результаты исследования и их обсуждение
В группу больных ЛИ, прооперированных на артериях головного мозга по поводу стенозирующего их поражения, было включено 20 пациентов.
Достоверные различия в частоте встречаемости стеноза сонной артерии между правым и левым каротидными бассейнами отсутствовали, р>0,05. Латерализация стеноза сонной артерии в I группе составила (рис. 1): – ЛВСА – 11 пациентов (55%);
– ПВСА – 9 пациентов (45%).
Для больных ЛИ с симптомным стенозом сонной артерии ипсилатеральной пораженному полушарию, было характерно наличие умеренного стенотического ее поражения. Достоверно чаще встречался симптомный стеноз сонной артерии от 50% до 69% – 16 пациентов (80%), чем стеноз от 70% до 99% – 4 пациента (20%), р<0,05.
В контралатеральных пораженному полушарию сонных артериях у всех 20 пациентов были верифицированы атеросклеротические изменения. В сонной артерии стеноз <50% или утолщение комплекса интима-медиа более 1 мм наблюдался у 12 пациентов (60%), стеноз от 50% до 69% – у 4 пациентов (20%), стеноз от 70% до 99% – у 1 пациента (5%) и окклюзия – у 3 пациентов (15%).
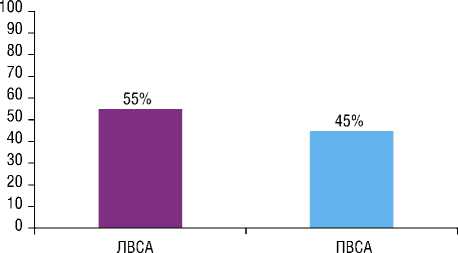
Рис. 1. Частота поражения церебральных сосудистых бассейнов у больных, подвергшихся операции на сонных артериях
Необходимо отметить, что стеноз сонной артерии >50% достоверно чаще встречался ипсилатерально аффектированному полушарию, чем контралатерально, р<0,05. Однако, невозможно было определить генез лакунарного инфаркта у больного с потенциальным источником артерио-артериальной эмболии, оперируя только данными дуплексного сканирования брахиоцефальных артерий. Так, у пациента с грубым атеросклеротическим поражением сонных артерий окклюзия церебральной перфорантной артерии могла произойти как вследствие артерио-артериальной эмболии, так и вследствие микроатероматоза. Таким образом, наличие стеноза сонной артерии более 50% у больного ЛИ не позволяет постулировать эмболический генез инсульта.
Проведен анализ встречаемости микроэмболических сигналов у пациентов I группы. При 60-минутном мониторировании средних мозговых артерий спонтанные МЭС обнаружены у 7 (35%) пациентов. В ипсилатеральной пораженному полушарию СМА спонтанные МЭС выявлены у 6 пациентов (30%), в контралатеральной СМА – у 2 пациентов (10%). У одного пациента с окклюзией контралатеральной пораженному полушарию ВСА спонтанные МЭС зафиксированы в обеих СМА. Так как при транскраниальной допплерографии у этого больного было верифицировано функционирование передней соединительной артерии, занос эмболического материала в контралатеральную СМА происходил из питающей ее ипсилатеральной ВСА. Хотя в ипсилатеральной СМА инцидентность спонтанных МЭС была выше, чем в контралатеральной, уровня статистической значимости различия не достигли, р>0,05.
При пальпации сонных артерий индуцированные МЭС в СМА зафиксированы у 14 (70%) пациентов. В ипсилатеральной пораженному полушарию СМА индуцированные МЭС выявлены у 10 пациентов (50%), в контралатеральной СМА – у 6 пациентов (30%). У 2 пациентов (10%) индуцированные МЭС зафиксированы в обеих СМА.
В связи с тем, что микроэмболические сигналы встречаются и в ипсилатеральной, и в контралатеральной пораженному полушарию СМА, изолированная оценка наличия спонтанных или индуцированных МЭС в церебральном кровотоке также не позволяет определить генез ЛИ.
У всех пациентов с верифицированными МЭС при 60-минутном мониторировании средних мозговых артерий по данным дуплексного сканирования брахиоцефальных артерий обнаружены изъязвленные атеросклеротические бляшки в сонных артериях.
Клинический пример 1.
Больной С., 79 лет. Диагноз: ишемический инсульт в бассейне правой средней мозговой артерии от августа 2004 г. (лакунарный патогенетический подтип), левосторонний гемипарез. Стеноз внутренней сонной артерии справа 80%, стеноз внутренней сонной артерии слева 66%. Фон: гипертоническая болезнь 3 ст., 3 ст., риск 4. Сопутствующий: ИБС: стенокардия напряжения II функ- ционального класса. Пациент поступил 04.10.04 в неврологическое отделение с данными КТ головного мозга от августа 2004 г., по которым в области внутренней капсулы правого полушария визуализировался гиподенсный очаг округлой формы диаметром 17 мм. Клиническая картина была представлена центральным левосторонним гемипарезом до 3 баллов. Нарушения высших мозговых функций отсутствовали. По данным дуплексного сканирования брахиоцефальных артерий был выявлен стеноз внутренней сонной артерии справа 80% (рис. 2), внутренней сонной артерии слева – 66%. В правой ВСА бляшка имела гипоэхогенный характер и неровности контуров. Допплеровская детекция церебральной эмболии зафиксировала 5 спонтанных микроэмболов в ипсилатеральной СМА в течение 60 минут (рис. 3). Так как бляшка обладала высокой эмбологенностью, от пальпации ее было решено воздержаться. 21.10.2004 пациенту была выполнена эверсионная каротидная эндартерэктомия справа (рис. 4). При ревизии обнаружена слоистая рыхлая атеросклеротическая бляшка протяженностью 2 см с переходом из правой ВСА на бифуркацию ОСА. Послеоперационное течение заболевания протекало без особенностей. Пациенту назначена антиагрегантная, антигипертензивная и гиполипидемическая терапия с целью вторичной профилактики ишемического инсульта.
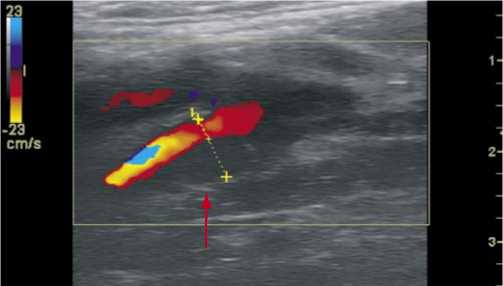
Рис. 2. Дуплексное сканирование брахиоцефальных артерий (стрелкой указана гипоэхогенная атеросклеротическая бляшка с неровностями контуров, стенозирующая просвет внутренней сонной артерии на 80%)
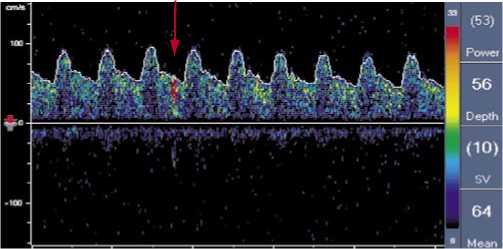
Рис. 3. Транскраниальная допплерография правой средней мозговой артерии (стрелкой указан сигнал от микроэмбола)
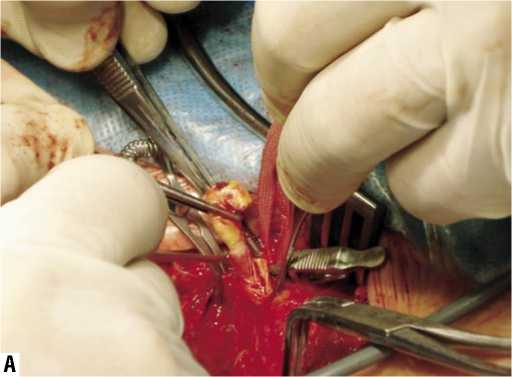
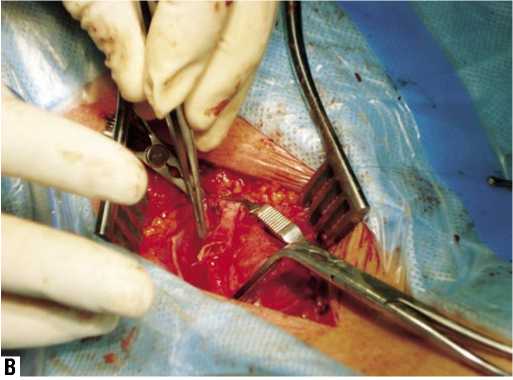
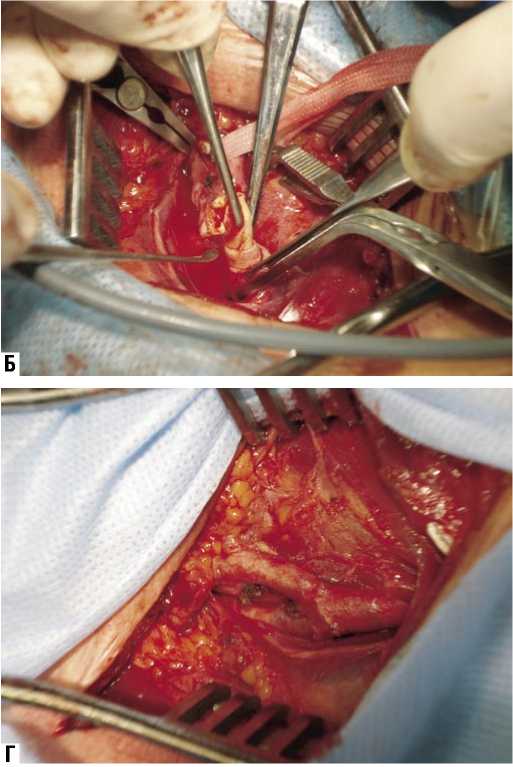
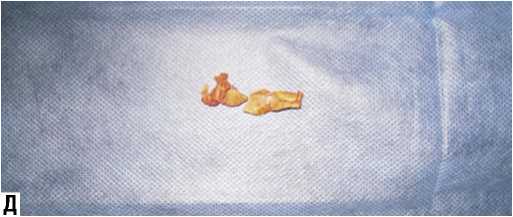
Рис. 4. Этапы эверсионной каротидной эндартерэктомии в правом каротидном бассейне: А – выделение атеросклеротической бляшки; Б – удаление атеросклеротической бляшки; В – наложение сосудистого шва; Г – вид сонной артерии после операции; Д – препарат удаленной атеросклеротической бляшки
Нейровизуализационная картина у больных I группы была представлена крупными лакунарными очагами (более 15 мм) в одном сосудистом бассейне, или сочетанием «лакун» и территориальных корковых инфарктов. Множественный корреляционный анализ обнаружил наличие прямой сильной (r=0,74) значимой (р<0,05) корреляционной связи между «множественным» фокальным поражением вещества головного мозга и наличием стеноза >50% ипсилатеральной сонной артерии.
Можно констатировать, что для определения причины развития ЛИ необходимо проведение тщательного обследования больного. Паттерном развития ЛИ вследствие артерио-артериальной эмболии является: наличие артериального потенциального источника церебральной эмболии; МЭС в ипсилатеральной пораженному полу- шарию СМА; наличие по данным нейровизуализации крупных лакунарных очагов (более 15 мм) в одном сосудистом бассейне, или сочетание «лакун» и территориальных корковых инфарктов.
Клинический пример 2.
Больной Д., 49 лет. Диагноз: Ишемический инсульт в бассейне левой средней мозговой артерии от 16.07.09. Правосторонняя гемигипестезия. Стеноз левой внутренней сонной артерии – 75%. Фон: Гипертоническая болезнь III ст., III ст., риск IV. При поступлении пациент предъявлял жалобы на чувство онемения в правой половине тела. В клинической картине невыраженная правосторонняя гемигипестезия. По данным дуплексного сканирования брахиоцефальных артерий был выявлен стеноз в каротидной бифуркации по передней и задней стенкам с переходом на устье и проксимальный отдел внутренней сонной артерии слева до 70–85% (рис. 5). Атеросклеротическая бляшка имела гетерогенный характер с наличием мягкого подвижного компонента. Селективная субтракционная дигитальная ангиография церебральных артерий подтвердила наличие стеноза ВСА слева до 75%. Билатеральный допплеровский мониторинг средних мозговых артерий с эмболодетекцией в течение 60 минут зарегистрировал 7 спонтанных микроэмболиче-ских сигналов в левой СМА мощностью от 8,2 до 23,1 дБ. При МРТ головного мозга визуализированы лакунарный ишемический очаг в области наружной капсулы слева диаметром 7 мм и территориальный ишемический очаг в левой теменной доле 2,9х2,1х2,5 см (рис. 6). Наличие потенциального очага артериальной эмболии, МЭС в ипсилатеральной очагу СМА и сочетание лакунарного и коркового территориального очагов по данным МРТ головного мозга подтвердило эмболический генез ЛИ у данного пациента. Спустя 2 недели от момента развития
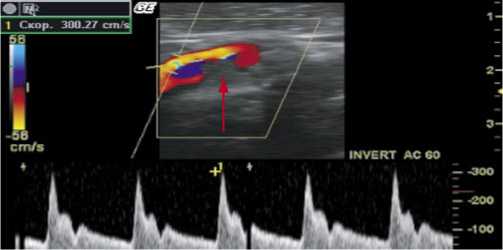
Рис. 5. Дуплексное сканирование брахиоцефальных артерий (стрелкой указана гетерогенная атеросклеротическая бляшка с мягким подвижным компонентом, стенозирующая просвет внутренней сонной артерии слева до 70–85%)
ЛИ пациенту была выполнена транслюминальная баллонная ангиопластика со стентированием левой ВСА (рис. 7). Интраоперационный билатеральный допплеровский мониторинг СМА зафиксировал массивную микроэмболизацию левой СМА (рис. 8), однако в послеоперационном периоде отсутствовало появление «нового» неврологического дефицита.
Принципиально важным является вопрос безопасности оперативных вмешательств на каротидных артериях при грубом атеросклеротическом их поражении у больных ЛИ.
В послеоперационном периоде неврологические осложнения наблюдались у 6 пациентов (30%). Геморрагических и тяжелых ишемических инсультов не было.
После каротидной эндартерэктомии у 5 пациентов (25%) зафиксировано поражение периферических нервов. Страдали подъязычный и возвратный нервы. У одного пациента (5%) диагностировано острое нарушение мозгового кровообращения в бассейне оперированной ВСА. Проявившийся после пробуждения неврологический дефицит регрессировал в течение 2 часов, что позволило диагностировать транзиторную ишемическую атаку. Дуплексное сканирование брахиоцефальных артерий в послеоперационном периоде продемонстрировало отсутствие рестенозирования в месте операции, в связи с чем ТИА была расценена, как проявление интраоперационной эмболизации церебральных артерий.
После каротидной чрескожной транслюминальной баллонной ангиопластики со стентированием появления «новой» неврологической симптоматики не наблюдалось.
Среди соматических осложнений, в 1 случае (5%) развился острый инфаркт миокарда (при выполнении КЭ).
Наблюдаемая нами частота осложнений при операциях на сонных артериях у пациентов с ЛИ не превышает таковые значения, зарегистрированные при проведении
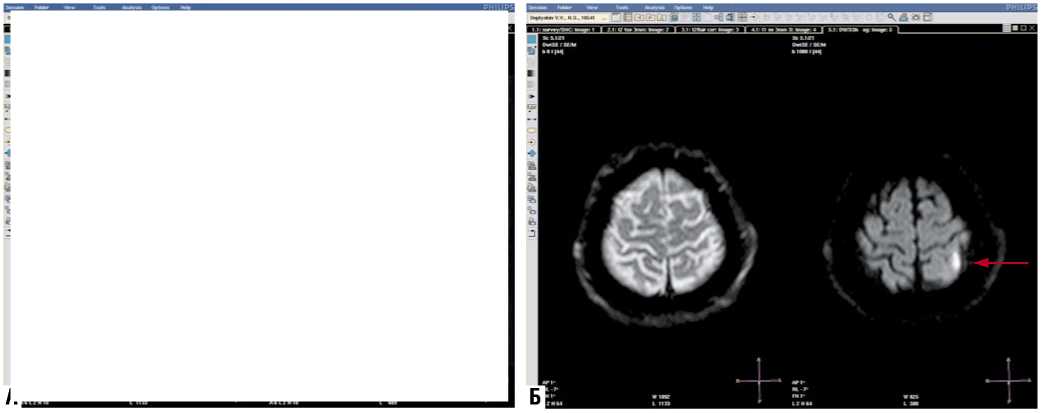
Рис. 6. МРТ головного мозга в диффузионном режиме: А – лакунарный ишемический очаг в области наружной капсулы слева диаметром 7 мм; Б – территориальный ишемический очаг в левой теменной доле 2,9х2,1х2,5 см.
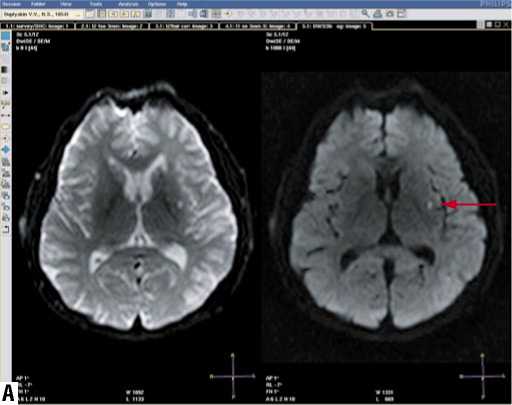
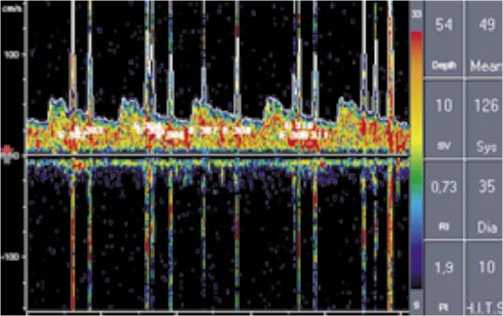
Рис. 8. Интраоперационная транскраниальная допплерография левой СМА (множественные сигналы от микроэмболов)
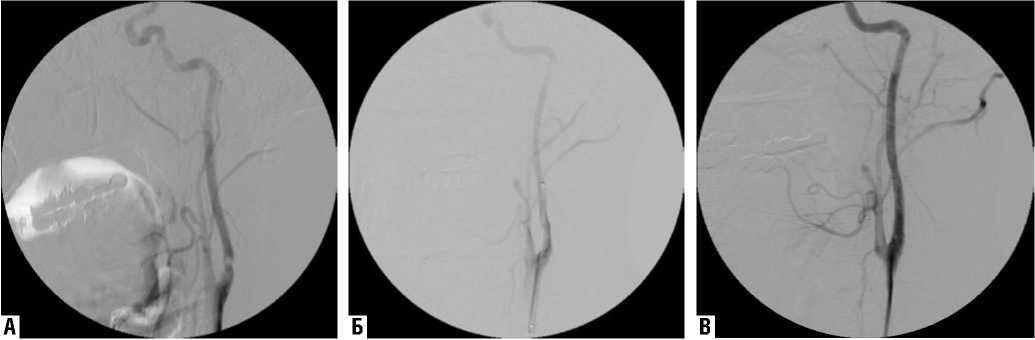
Рис. 7. Транслюминальная баллонная ангиопластика со стентированием левой внутренней сонной артерии: А – до операции; Б – этап раскрытия стента; В – после операции
международных клинических исследованиях (NASCET, ECST и Veterans Affairs Cooperative Study Program), что позволяет сделать вывод об их безопасности у данной категории больных.
В группу больных ЛИ, подвергшихся протезированию клапанов сердца, было включено 14 пациентов.
Обнаружены следующие источники кардиогенной церебральной эмболии с высоким риском развития ишемического инсульта: тромбы в левых камерах сердца – 4 пациента (28,6%), вегетации на клапанах сердца – 5 пациентов (35,7%), искусственные клапаны сердца – 3 пациента (21,4%) и ревматическое поражение клапанов сердца – 12 пациентов (85,7%). Необходимо отметить, что 9 пациентов (64,3%) не получали адекватной анти-тромботической терапии в доинсультном периоде, несмотря на то, что на сегодняшний день эффективность и безопасность проведения такой профилактической терапии доказана многочисленными исследованиями и не вызывает сомнений.
Как правило, пациенты с инфекционным эндокардитом и ревматическим поражением клапанного аппарата сердца являются молодыми людьми, у которых отсутствуют такие «классические» сосудистые факторы риска, как гипертоническая болезнь, сахарный диабет и гиперлипидемия. В проведенном нами исследовании факторы риска развития острых сердечно-сосудистых осложнений отсутствовали у 8 (57,1%) пациентов. Таким образом, у данных больных единственной причиной окклюзии перфорантной церебральной артерии могла быть эмболия из кардиального источника.
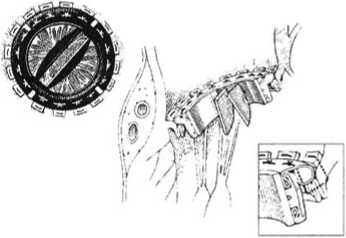
Клинический пример: больная Ю., 41 года. Диагноз: Ревматизм, неактивная фаза. Ревматический стенозирующий митральный порок сердца, тромбоз левого предсердия. Постоянная форма фибрилляции предсердий. Пациентка в апреле 2005 г. перенесла ишемический инсульт в бассейне левой средней мозговой артерии. В неврологическом статусе отмечается правосторонняя пирамидная недостаточность в виде анизорефлексии глубоких рефлексов D>S. На представленных снимках КТ головного мозга от апреля 2005 г. визуализируются гипо-денсные очаги: лакунарный очаг размером 20x15x12 мм и территориальный корковый очаг в теменной доле размером 35x21x27 мм. На ЭКГ - фибрилляция предсердий, нормосистолическая форма. При эхокардиографии: митральный клапан фиброзно изменен, площадь митрального отверстия 1,2 см2, в полости левого предсердия лоцируется массивный, малоподвижный, организованный тромб конусовидной формы, занимающий % предсердия. В связи с наличием гемодинамически значимого порока сердца и высоким риском кардиогенной эмболии (тромб в левом предсердии) пациентке выполнена тромбэктомия, санация камер сердца и протезирование митрального клапана протезом МедИнж-25 в условиях искусственного кровообращения (рис. 9). При ревизии полости левого предсердия выявлен тромб с признаками инфицирования, выстилающий его заднюю стенку, от устьев левых легочных вен до ушка предсердия. Послеоперационный период у пациентки протекал без особенностей.
Транскраниальная допплеровская детекция микро-эмболических сигналов при 60-минутном билатеральном мониторировании средних мозговых артерий позволила в дооперационном периоде обнаружить МЭС у 8 пациентов (57,1%). Эмболическая нагрузка на головной
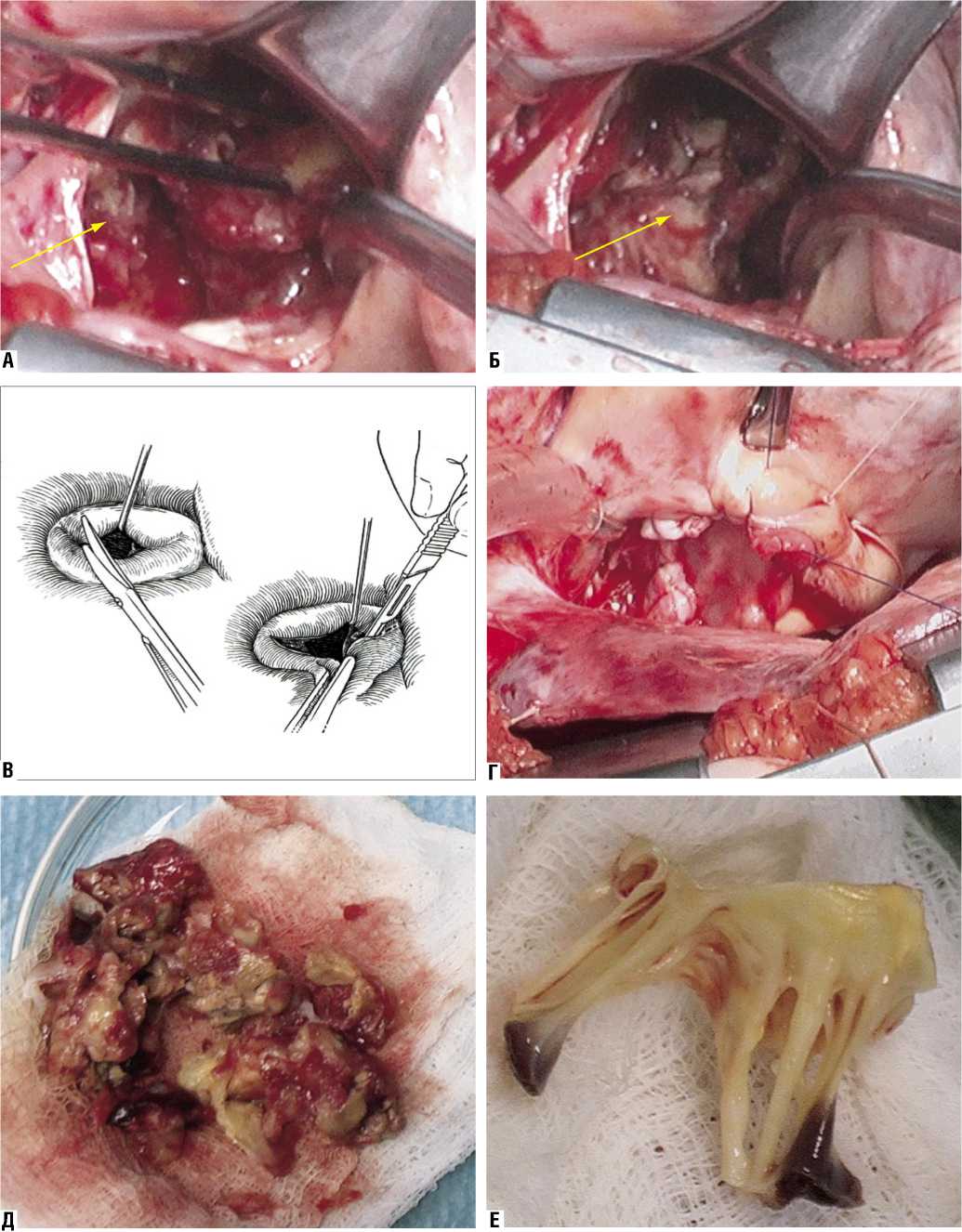
Рис. 9. А, Б – Интраоперационная ревизия полости левого предсердия у больной Ю. (стрелкой отмечен тромб в левом предсердии), В – Схема выполнения 1 этапа операции «открытая митральная комиссуротомия», Г – Закрытие дефекта левого предсердия (доступа в него) заплатой из аутоперикарда, Д – Удаленный тромб из полости левого предсердия, Е – Препарат иссеченной передней створки митрального клапана
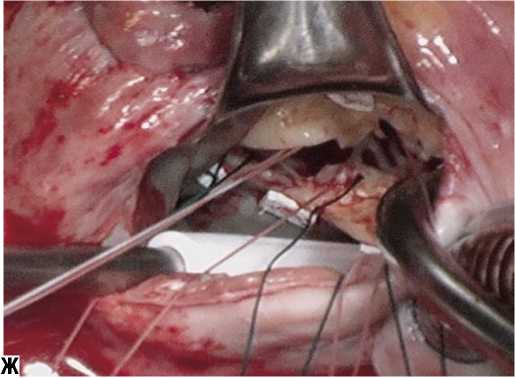
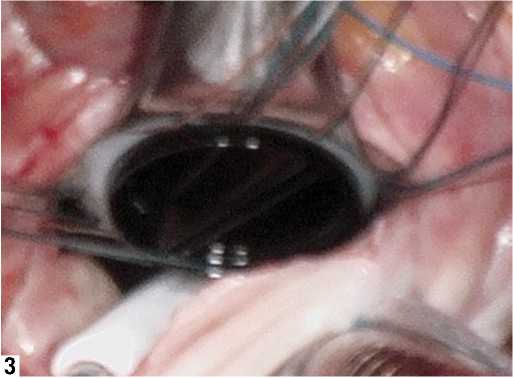
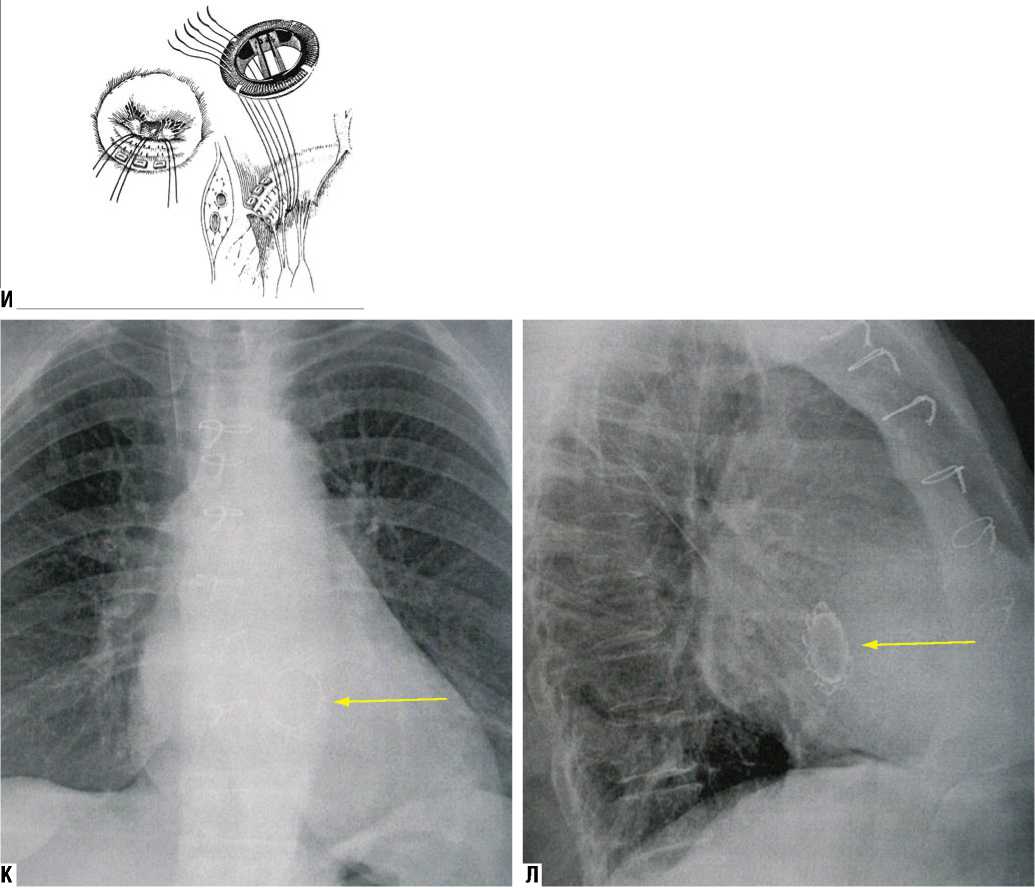
Рис. 9. Ж, З – Этапы протезирования митрального клапана у больной Ю. Ж – наложение швов на фиброзное кольцо МК с сохранением задней створки МК и ее подклапанного аппарата; З – этап имплантации механического двустворчатого протеза МедИнж-25 с оплеткой, прошитой серебряной нитью). И – Методика выполнения плицирующего шва на створках митрального клапана при фиксации искусственного протеза. К, Л – Рентгенограмма больной Ю. после операции (стрелкой отмечен имплантированный протез митрального клапана с манжетой, прошитой серебряной нитью)
мозг составляла от 1 до 59 МЭС за 60 минут в среднем – 22±8,3.
Поражение нескольких церебральных сосудистых бассейнов наблюдалось у 5 больных (35,7%) II группы. Частота поражения церебральных сосудистых бассейнов составила (рис. 10):
– ЛСМА – 11 больных (78,6%);
– ПСМА – 5 больных (35,7%);
– ВББ – 3 больных (21,4%).
Обращает на себя внимание более высокая частота поражения бассейна левой СМА по сравнению с другими церебральными сосудистыми бассейнами, не достигшая, однако, уровня статистически значимых различий, р>0,05. Полученные результаты согласуются с данными других исследователей, которые сообщают, что для кардиогенной эмболии характерно поражение нескольких сосудистых бассейнов, а особенности отхождения брахиоцефальных артерий от дуги аорты делает физиологичным занос эмболического материала в левый каротидный бассейн [5].
При КТ\МРТ головного мозга, нейровизуализа-ционная картина была представлена большим (более 15 мм) лакунарным очагом, несколькими лакунарными очагами в разных сосудистых бассейнах и сочетанием территориальных и лакунарных очагов. Достоверно чаще лакуны располагались латеральнее внутренней капсулы, чем медиальнее от неё, р<0,05.
Такие особенности нейровизуализационной картины у данных больных были обусловлены механизмом кардиогенной церебральной эмболии, для которой характерно поражение нескольких церебральных сосудистых бассейнов. Непосредственно внутри сосудистого бассейна эмболы попадают в корковые ветви мозговых артерий, а также в крупные перфорантные артерии, которые отходят под более тупым углом от ствола СМА, чем мелкие, которые отходят практически под прямым углом.
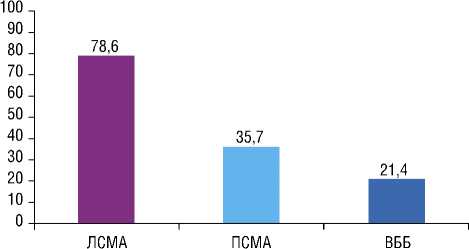
Рис. 10. Частота поражения церебральных сосудистых бассейнов у больных, подвергшихся протезированию клапанов сердца
Крайне важным является вопрос безопасности кардиохирургических вмешательств у больных ЛИ с целью вторичной профилактики ишемических церебральных событий. К сожалению, в доступной современной литературе отсутствуют подобные данные.
Известны следующие осложнения со стороны ЦНС после операций на сердце в условиях искусственного кровообращения: фатальное повреждение мозга, нефатальная энцефалопатия, эпиприпадки, инсульт.
Среди прооперированных больных исследуемой группы зафиксированы следующие осложнения: летальные исходы – отсутствовали (0%); энцефалопатия – 12 пациентов (85,7%), которая клинически проявлялась нарушением поведения и снижением интеллектуально-мнестических функций в послеоперационном периоде; эпиприпадки – отсутствовали (0%); повторный ишемический инсульт – 1 пациент (7,1%).
Частота периоперационных осложнений у больных ЛИ, подвергшихся кардиохирургической агрессии, не превышает среднестатистического уровня при подобных вмешательствах [5], что также позволяет сделать вывод о безопасности их у данной категории больных.
Таким образом, можно констатировать, что эмболия в перфорантные артерии головного мозга является одной из причин развития лакунарного инфаркта. Критериями эмболического генеза ЛИ являются: наличие верифицированного потенциального источника артерио-артери-альной или кардиальной церебральной эмболии; МЭС в ипсилатеральной пораженному полушарию СМА; наличие по данным КТ/МРТ головного мозга большого (более 15 мм) лакунарного очага, нескольких лакунарных очагов в разных сосудистых бассейнах, расположение лакунарного очага латеральнее внутренней капсулы, сочетание территориальных и лакунарных очагов.
Больным ЛИ с симптомным стенозом ВСА, ревматическим поражением клапанов сердца и инфекционным эндокардитом показано хирургическое устранение источника церебральной эмболии. Частота периоперационных осложнений у больных ЛИ, подвергшихся кардиохирургической агрессии, не превышает среднестатистический уровень при подобных вмешательствах. Таким образом, в настоящее время с точки зрения степени радикальности профилактических мероприятий альтернатив хирургическому удалению источника церебральной эмболии нет.
Список литературы Хирургические методы вторичной профилактики лакунарного инсульта
- Верещагин Н.В., Моргунов В.А., Гулевская Т.С. Патология головного мозга при атеросклерозе и артериальной гипертонии. -М.: Медицина. -1997.
- Ворлоу Ч.П., Деннис М.С., Ван Гейн Ж, и др. Инсульт: Практическое руководство для ведения больных. -СПб.: Политехника, 1998. -629 с.
- Гусев Е.И., Коновалова А.Н., А.Б. Гехт. Клинические рекомендации. Неврология и нейрохирургия -М.: ГЭОТАР-Медия, 2007. -368 с.
- Максимова М.Ю. Малые глубинные (лакунарные) инфаркты головного мозга при артериальной гипертонии и атеросклерозе: Автореф. дис. … доктор мед. наук. -М., 2002. -50 с.
- Шевченко Ю.Л., Одинак М.М., Кузнецов А.Н., Ерофеев А.А. Кардиогенный и ангиогенный церебральный эмболический инсульт (физиологические механизмы и клинические проявления).//М.: ГЭОТАР -Медиа, 2006. -272 с.
- Bakshi R., Wright P.D., Kinkel P.R. et al. Cranial magnetic resonance imaging findings in bacterial endocarditis: The neuroimaging spectrum of septic brain embolization demonstrated in twelve patients.//J. Neuroimaging. -1999. -Vol.9. -P. 78-84.
- Bamford J., Warlow C. Evolution and testing jf the lakunar hypothesis//Stroke. -1988. Vol. 19. -№ 9. -P.1074 -1082.
- Boiten J. Lakunar stroke: a prospective clinical and radiological study.//Arch. Gerontol. Geriatr. -1991. -№ 5. -P. 258-264.
- Deborah R. MD; Tuhrim, Stanley MD; Weinberger, Jesse M. MD; Rudolph, Steven H. MD. Mechanisms in Lacunar Infarction//Stroke. -1992. -23(3). Р. 325-327.
- Fisher CM. Lacunes: small, deep cerebral infarcts. Neurology. 1965;15: 774-784.
- Guidelines for Prevention of Stroke in Patients With Stroke and Transient Ischemic Attack, 2006//Stroke. -2006. Vol. 37. -№ 2. -P. 577-617.
- Recommendations for stroke management Update 2003 EUSI//Cerebrovasc Dis. -2003. -Vol.16. -P. 311-337.
- You R., McNeil J.J., O'Malley H.M., Davis S.M., Donnan G.A. Risk factors for lacunar infarction syndromes. Neurology 1995; 45(8):1483-7.


