Хирургическое лечение ятрогенного сложного рецидивного экстрасфинктерного прямокишечного свища. Клинический случай
Автор: Маркарьян Д.Р., Гарманова Т.Н., Казаченко Е.А., Агапов М.А.
Журнал: Хирургическая практика @spractice
Рубрика: Статьи
Статья в выпуске: 1 (45), 2021 года.
Бесплатный доступ
Введение: свищи прямой кишки представляют собой одно из самых распространенных доброкачественные заболеваний аноректальной области и встречаются в среднем 1,69 на 10 000 населения. Заболевание значительно снижает качество жизни и имеет тенденцию к рецидивирующему течению, при котором неоднократные попытки хирургического лечения могут приводить к нарушению работы сфинктерного аппарата анального канала. Основная причина возникновения свищей - парапроктит. Однако встречаются и ятрогенные травматические свищи, возникающие после различных хирургических вмешательств на аноректальной области и прямой кишке.Клинический случай: Пациентка Е. 44 лет обратилась в МНОЦ МГУ в марте 2020 года с жалобами на наличие раны промежности с постоянным гнойным отделяемым. При осмотре: дефект мягких тканей (40х25х25см) по срединной линии промежности, на дне раны - наружное свищевое отверстие. Перианальная область деформирована за счет рубцовых изменений. Внутреннее свищевое отверстие (2х3мм) определяется на 12 часах УЦ. Из анамнеза известно, что в 2016 году пациентка перенесла оперативное вмешательство «устранение ректоцеле, задняя кольпорафия, леваторопластика, пластика передней стенки прямой кишки». В послеоперационном периоде развился синдром обструктивной дефекации, было проведено повторное оперативное лечение - передняя аносфинктеролеваторопластика, геморроидэктомия по Миллиган-Морган. На 9-е сутки случился «разрыв мягких тканей раны промежности» с кровотечением и «локальным повреждением надсфинктерной зоны передней стенки прямой кишки». Выполнено «ушивание дефекта прямой кишки, остановка кровотечения». Рана промежности была оставлена открытой. Через 3 месяца пациентка была снова прооперирована по поводу ректовагинального свища без эффекта. В МНОЦ МГУ была выполнена фистулэктомия с устранением дефекта анального канала перемещенным слизисто-подслизистым лоскутом. Операционная рана заживает вторичным натяжением.Вывод: В современной литературе описывается небольшое число случаев возникновения прямокишечных свищей после аноректальных хирургических вмешательств. При этом данные о дальнейшей тактике ведения и выборе метода хирургического лечения таких пациентов практически отсутствуют. Мы считаем важным представление случаев возникновения ятрогенных прямокишечных свищей, не только с точки зрения разбора причины возникновения свища, но и для описания выбранной методики хирургического лечения и ее эффективности.
Свищ прямой кишки, ятрогенный свищ, аноректальная хирургия, осложнения после аноректальной хирургии, хирургическое лечение прямокишечных свищей
Короткий адрес: https://sciup.org/142230050
IDR: 142230050 | УДК: 616.352-007.253-089.85 | DOI: 10.38181/2223-2427-2021-1-13-19
Surgical treatment of iatrogenic complex recurrent extrasphincter anorectal fistula: a clinical case
Background: Anorectal fistula is a benign disease with an average prevalence of 1.69/10,000 population. The disease significantly reduces the life quality and has a tendency to relapse. Repeated surgical treatment can lead to anal sphincter impairment. Paraproctitis is the main anorectal fistulas cause. However, there are also iatrogenic traumatic fistulas that occur after various anorectal surgical interventions.Clinical case: A 44-year old female patient applied to the MSU University clinic in March 2020 with perineal wound with permanent purulent discharge. During examination perianal soft tissue defect was determined, the external fistula opening (40x25x25cm) was visualized at the wound bottom, the internal fistula opening (2x3mm) was visualized at 12h of the clock dial. The perianal area is deformed due to scarring. In 2016 the patient underwent surgical «rectocele elimination, posterior colporaphy, levatoroplasty, plastic surgery of the anterior rectal wall». Obstructive defecation syndrome developed during postoperative period, and repeated surgical treatment was performed - anterior anosfincterolevatoroplasty, Milligan-Morgan hemorrhoidectomy.On the 9th day, there was a «perianal soft tissue rupture» with bleeding and «local anterior rectal wall damage in the suprasphincter zone». Then «the rectal defect suturing» was performed. The perineal wound was left open. The patient was reoperated in 3 months due to a rectovaginal fistula with no effect. A fistulectomy was performed at the Moscow State University Medical Center with the removal of the anal canal defect by mucosal-submucosal flap. The surgical wound heals by secondary tension.Conclusion: The current studies describe a small number of cases of anorectal fistulas secondary to anorectal surgery. At the same time, there is no data on the further surgical management of such patients. It is important to present the iatrogenic anorectal fistulas cases, not only to analyze the fistula cause, but also to describe the surgical treatment method and its efficacy.
Текст научной статьи Хирургическое лечение ятрогенного сложного рецидивного экстрасфинктерного прямокишечного свища. Клинический случай
Свищ прямой кишки представляет собой патологический ход, открывающийся внутренним свищевым отверстием в просвет прямой кишки и наружным отверстием на коже промежности. Заболевание затрагивает преимущественно людей трудоспособного возраста и приводит к значительному снижению качества жизни [1–3]. Наиболее частыми симптомами являются локальная болезненность, выделения слизисто-гнойного характера из наружного отверстия при наличии активного воспаления. По этиологии выделяют криптогландулярные свищи, возникающие в результате воспаления анальной железы, прямокишеные свищи при болезни Крона, травматические (ятрогенные) свищи, возникающие после других хирургических вмешательств в аноректальной области и свищи, возникшие в результате других заболевания (инфекционные и онкологические заболевания,врож-денные аномалии) [1].
По данным европейских источников распространенность прямокишечных свищей в среднем составляет 1,69 на 10 000 населения и считается редко встречающимся заболеванием.Чаще всего встречаются криптогландулярные свищи и свищи при болезни Крона (0,86 и 0,76 на 10 000 населения соответственно). Ятрогенные свищи прямой кишки встречаются в среднем 0,31 на 10 000 населения Европы [1].
Единичные случаи возникновения ятрогенных травматических свищей прямой кишки чаще всего описываются как последствия хирургических вмешательств по поводу геморроидальной болезни.При этом по данным исследований нет достоверной взаимосвязи возникновения свищей и конкретным видом методики операции. [1, 4].
В данной статье мы представляем клинический случай успешного хирургического лечения ятрогенного свища прямой кишки у пациентки после открытой ге-морроидэктомии и ректопексии.
Описание клинического случая
Пациентка Е., 44-х лет обратилась в МНОЦ МГУ им. М.В.Ломоносова в марте 2020 года в МНОЦ МГУ с жалобами на наличие крупной раны на коже промежности с постоянным гнойным отделяемым, резкое нарушение качества жизни.
При осмотре в проекции промежностного тела по срединной линии имелся дефект мягких тканей размерами 40х25х25см, на дне которого визуализировалось наружное свищевое отверстие с гнойным отделяемым (рис.1).Перианальная область несколько деформирована за счет рубцовых изменений от предыдущих вмешательств. При трансанальном исследовании определялось внутреннее отверстие свищевого хода на 12 часах условного циферблата, размером 2х3 мм.
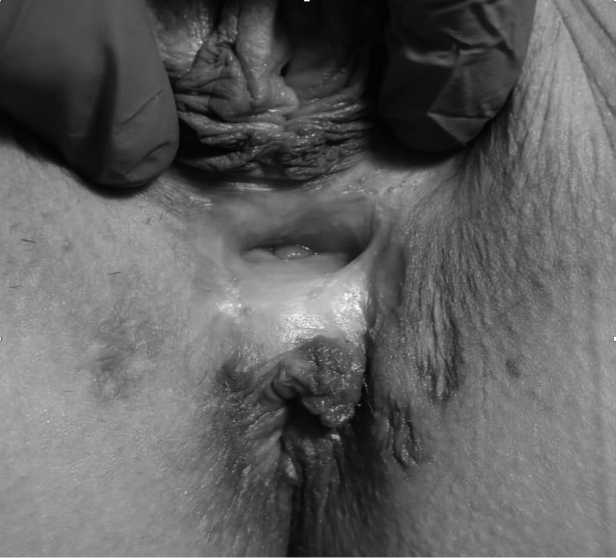
Рис. 1. Внешний вид промежности пациентки при обращении в МНОЦ МГУ им. М.В. Ломоносова
Fig. 1. The appearance of the patient's perineum when contacting the Moscow State University Medical Research Center. M.V. Lomonosov
При осмотре в проекции промежностного тела по срединной линии имелся дефект мягких тканей размерами 40х25х25см, на дне которого визуализировалось наружное свищевое отверстие с гнойным отделяемым (рис.1).Перианальная область несколько деформирована за счет рубцовых изменений от предыдущих вмешательств. При трансанальном исследовании определялось внутреннее отверстие свищевого хода на 12 часах условного циферблата, размером 2х3 мм.
Из анамнеза известно, что в 2016 году пациентка обратилась к проктологу по поводу выпадающих геморроидальных узлов. Других жалоб на тот момент пациентка не отмечала. При осмотре согласно представленной медицинской документации был установлен диагноз: «Тазовый пролапс. Рек-тоцеле 3-й степени. Обострение хронического геморроя».
Пациентка перенесла оперативное вмешательство: «устранение ректоцеле, задняя кольпорафия, леваторо-пластика,пластика передней стенки прямой кишки».
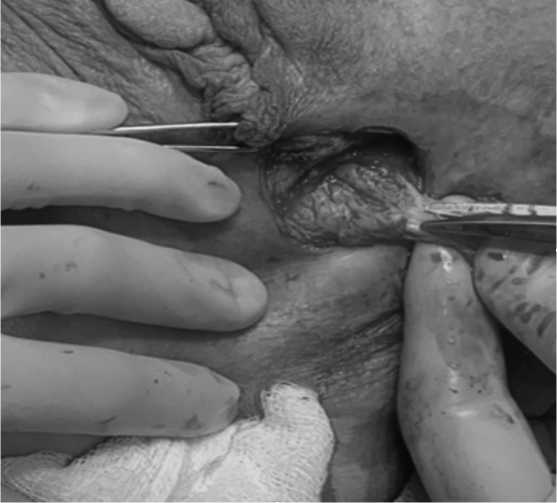
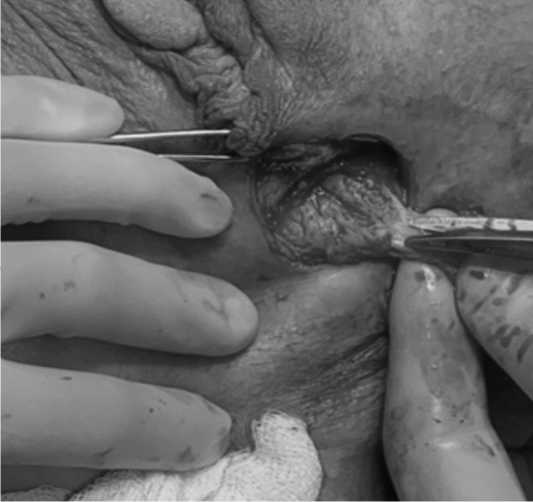
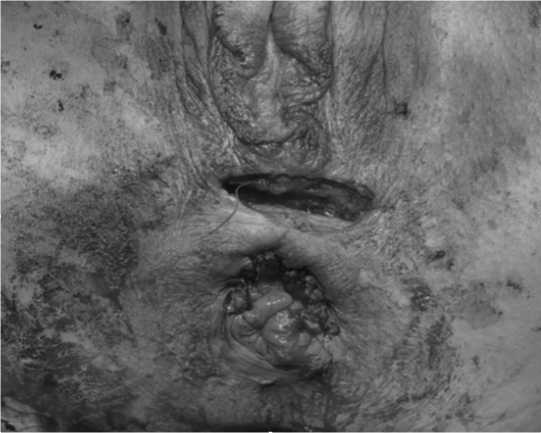
Рис. 2. Этапы оперативного лечения ятрогенного свища прямой кишки
А – «экономное» иссечение свища, Б – мобилизация слизисто-подслизистого лоскута прямой кишки для перемещения в анальный канал, В – внешний вид послеоперационной раны.
Fig. 2. Stages of surgical treatment of an iatrogenic fistula of the rectum
A – «economical» excision of the fistula, B – mobilization of the muco-submucosal flap of the rectum to move into the anal canal, C – the appearance of the postoperative wound.
В послеоперационном периоде, через несколько месяцев после вмешательства у пациентки развился синдром обструктивной дефекации.Пациентке в другом лечебном учреждении было проведено дополнительное обследование и после установления диагноза «переднее ректоцеле 3 ст., рецидив» выполнено повторное оперативное лечение – передняя аносфинктеролеваторопластика, гемор-роидэктомия по Миллиган-Морган.
Ранний послеоперационный период, согласно представленной документации, осложнился на 9-е сутки «краевым разрывом мягких тканей раны промежности» с развитием кровотечения и «локальным повреждением надсфинктерной зоны передней стенки прямой кишки». В экстренном порядке было выполнено «ушивание дефекта прямой кишки, остановка кровотечения» . Рана промежности была оставлена открытой. Пациентка была выписана, однако через несколько дней обнаружила выделения кала из раны промежности.
Через три месяца пациентка была снова прооперирована по поводу ректовагинального свища (документы не представлены) без эффекта.
В МНОЦ МГУ пациентке было проведено хирургическое лечение: фистулэктомия с устранением дефекта анального канала перемещенным слизисто-подслизистым лоскутом (рис. 2). На 25 день после операции пациентка в удовлетворительном состоянии, жалоб не предъявляет, заживление раны полное, на протяжении всего послеоперационного периода осложнений не было.
Обсуждение
Таким образом, у пациентки Е. возникновение свища прямой кишки произошло в результате двух хирургических вмешательств на аноректальной области. При этом со слов пациентки, симптомы, беспокоящие на момент обращения в МНОЦ МГУ им.Ломоносова,появились почти сразу после второй операции в 2017 году (ректо-пексии).
В исследовании Gleditsch et al. были продемонстрированы 19-летние исходы ректопексии различными методиками (лапароскопические и открытые операции с или без использования сетчатых имплантов). За этот период не было выявлено ни одного случая формирования свища прямой кишки без эрозии сетчатого импланта [5]. При лапароскопической ректопексии с использованием сетчатых имплантов редко встречаются случаи эрозии имплантов в стенки органов (прямая кишка, мочевой пузырь, свод и канал влагалища) с образованием свищевых ходов (1,3-2%), также были описаны случаи образования свищевых ходов (чаще ректовагинальных) без эрозии импланта [6–8]. При этом эрозии чаще всего встречались при использовании синтетических сетчатых имплантов (2,4%), нежели чем при использовании биологических имплантов (0,7%) [8]. При небольшом объеме эрозии или формировании неосложненной формы свища прямой кишки потребовалось только ушивание дефектов с заменой или частичной резекцией сетчатого импланта, в случае осложненных форм свищей и эрозии большей части импланта потребовалась лапароскопическая резекция участка кишки с формированием низкого анастомоза. [7, 8].
В современной литературе приводятся различные данные о возникновение прямокишечных свище после хирургического лечения геморроя. Так, в исследованиях Aytac et al. и Kim et al. не было выявлено ни одного случая формирования свищей через 7,7 лет после закрытой ге-морроидэктомии, через 6,3 года после степлерной гемор-роидопексии и через 5 лет после открытой гемор-роидэктомии [9, 10]. Единичные случаи формирования прямокишечного свища после степлерной (срок наблюдения 6-36 месяцев) и открытой геморроидэктомии описываются в исследованиях Bilgin et al., Ripetti et al. [4, 11, 12]. После геморроидэктомии с использованием Ligasure свищи прямой кишки встречались лишь в 1% случаев через 1-2 месяца и в 0,2% более чем через 2 месяца. [13] В исследовании Klang et al. изучались КТ-снимки пациентов после геморроидэктомии в срок менее чем 30 дней с момента операции: из 12 пациентов только у одного был выявлен свищ прямой кишки [14]. Таким образом, формирование свищей прямой кишки после хирургического лечения геморроя встречается только как единичные случаи и достоверно не связано с тем или иным видом вмешательства.
Во всех представленных исследованиях, описывающих случаи возникновения прямокишечных свищей после хирургического лечения геморроидальной бо-лезни,не было описано дальнейшей хода лечения таких пациентов.В доступной литературе отсутствуют рекомендации по выбору метода лечения прямокишечных свищей ятрогенной природу.
Повторные случаи возникновения свищей прямой кишки во многом зависят от вида свища, направления и количества свищевых ходов,наличия внутреннего отверстия, выбранной тактики лечения, предшествующих операций в аноректальной области и от сопутствующих заболеваний и в среднем составляет 15,6% [2, 15, 16]. У пациентки Е. такие факторы риска отсутствуют. Но ввиду того, что в анамнезе имеются несколько операций в аноректальной области (геморроидэктомия и ректо-пексия), не исключено наличие избыточного количества рубцовой ткани и фиброза, затрудняющих идентификацию внутреннего отверстия, свищевого хода и затеков. По этой причине данную пациентку, вероятно, можно отнести к группе повышенного риска рецидива заболевания.
Лечением рецидивных свищей прямой кишки остается до настоящего момента очень сложной задачей [17]. Частота рецидивирования остается высокой, несмотря на большой арсенал различных вмешательств, при этом более хирургически агрессивные методики сопровождаются высокой частой недержания кала в послеоперационном периоде. На сегодняшний день спектр операций, которые могут выполняется у пациентов с рецидивными свищами включает в себя фистулотомию, использование лигатуры и поэтапная фистулотомия, инъекция различных биоматериалов, фистулоэктомию с первичным ушиванием сфинктера и формированием лоскута для пластики внутреннего отверстия,методика LIFT, FILAC, при этом уровень доказательности эффективности каждой методики остается низким [3].
Фистулотомия с первичной сфинктеропластикой (FIPS) демонстрирует хорошие результаты заживления (88-100%) и низкий риск рецидива (0-8%) при лечении простых неосложненных свищей. В то время как при лечении сложных и рецидивных свищей до 34% пациентов отмечают снижение функции удержания [2]. При вовлечении сфинктера или в случае сложных форм свищей эффективность таких методик как LIFT, лоскутной пластики и предоперационное использование дренирующей лигатуры с последующим хирургическим лечением колеблется от 75 до 90% [2, 15–17]. Хирургическая методика с использованием лоскута достаточно высокую эффективность при первичном использовании (72%), при этом в случае повторной операции полное избавление от свища наблюдалось у 57% пациентов [18]. Zimmerman и соавтр. сообщили о том, что эффективность хирургического лечения с использованием лоскута прямой кишки составил лишь 67% при выполнении первичной операции [19]. Эффективность повторной пластики с использованием лоскута ограничена, учитывая, что наличие рубцовой ткани, возможно, компрометирует повторную пластику внутреннего отверстия свища [20, 21].
В случае сложных свищей рекомендуется использовать дренирующую лигатуру либо для купирования инфекционно-воспалительного процесса, либо же как мост к другим минимально инвазивным методам лечения.В литературе представлены различные данные по сравнению дренирующей лигатуры с другими техниками, в большей части исследований указывается на равную эффективность «режущей» лигатуры и фистулотомии и фистулоэктомии [16].
Комбинация нескольких хирургических методик лечения демонстрирует более высокие результаты заживления, чем при использовании только одного метода [22]. В последнее время также разрабатываются новые методики для лечения рецидивных, осложненных форм свищей, такие как фотодинамическая терапия, методика PERFACT, различные биоматериалы для заполнения сви-щей,но на данный момент оценить их реальную эффективность невозможно ввиду отсутствия крупных рандомизированных исследований [2].
Несмотря, на большой объем доступной профессиональной информации, касающейся лечения свищей прямой кишки, алгоритма лечения сложных, рецидивирующих свищей не разработано. Техника и объем операции становятся творческим процессом врача-проктолога.
Выводы
В современной литературе описывается небольшое число случаев возникновения прямокишечных свищей после аноректальных хирургических вмешательств. В большинстве случаев ятрогенные травматические свищи были описаны после хирургического лечения геморроидальной болезни и ректоцеле.При этом данные о дальнейшей тактике ведения таких пациентов практически отсутствует, равно как и не доказано явное превосходства какого-либо одного метода хирургического лечения рецидивных, сложных свищей прямой кишки. Мы считаем важным представление случаев возникновения ятрогенных свищей прямой кишки, не только с точки зрения разбора причины возникновения свища, но и для описания и представления выбранной методики хирургического лечения и ее эффективности.
Список литературы Хирургическое лечение ятрогенного сложного рецидивного экстрасфинктерного прямокишечного свища. Клинический случай
- D. García-Olmo et al., «Prevalence of Anal Fistulas in Europe: Systematic Literature Reviews and Population-Based Database Analysis». Adv. Ther., vol. 36, no. 12, pp. 3503- 3518, 2019, https://doi.org/10.1007/s12325-019-01117-y.
- L. Ji, Y. Zhang, L. Xu, J. Wei, L. Weng, and J. Jiang, «Advances in the Treatment of Anal Fistula: A Mini-Review of Recent Five-Year Clinical Studies». Front. Surg., vol. 7, no. February, pp. 1-9, 2021, https://doi.org/10.3389/fsurg.2020.586891.
- A.P. Visscher, D. Schuur, R. Roos, G.J.H. Van Der Mijnsbrugge, W. J. H. J. Meijerink, and R. J. F. Felt-Bersma, «Long-term follow-up after surgery for simple and complex cryptoglandular fistulas: Fecal incontinence and impact on quality of life». Dis. Colon Rectum, vol. 58, no. 5, pp. 533-539, 2015, https://doi.org/10.1097/DCR.0000000000000352.
- Q. Z. Ruan et al., «A systematic review of the literature assessing the outcomes of stapled haemorrhoidopexy versus open haemorrhoidectomy». Tech. Coloproctol., vol. 25, no. 1, pp. 19-33, 2021, https://doi.org/10.1007/s10151-020-02314-6.
- D. Gleditsch, W. A. Wexels, and A. Nesbakken, «Surgical options and trends in treating rectal prolapse: long-term results in a 19-year follow-up study». Langenbeck’s Arch. Surg., vol. 403, no. 8, pp. 991-998, 2018, https://doi.org/10.1007/s00423-018-1728-4.
- A. H. Badrek-Al Amoudi, G. L. Greenslade, and A. R. Dixon, «How to deal with complications after laparoscopic ventral mesh rectopexy: Lessons learnt from a tertiary referral centre». Color. Dis., vol. 15, no. 6, pp. 707-712, 2013, https://doi.org/10.1111/codi.12164.
- E. C. J. Consten, J. J. Van Iersel, P. M. Verheijen, I. A. M. J. Broeders, A. M. Wolthuis, and A. D’Hoore, «Longterm outcome after laparoscopic ventral mesh rectopexy». Ann. Surg., vol. 262, no. 5, pp. 742-748, 2015, https://doi.org/10.1097/SLA.0000000000001401.
- C. Evans et al., «A multicenter collaboration to assess the safety of laparoscopic ventral rectopexy». Dis. Colon Rectum, vol. 58, no. 8, pp. 799-807, 2015, https://doi.org/10.1097/DCR.0000000000000402.
- E. Aytac, E. Gorgun, H. H. Erem, M. A. Abbas, T. L. Hull, and F. H. Remzi, «Long-term outcomes after circular stapled hemorrhoidopexy versus Ferguson hemorrhoidectomy». Tech. Coloproctol., vol. 19, no. 10, pp. 653-658, 2015, https://doi.org/10.1007/s10151-015-1366-6.
- J. S. Kim et al., «Stapled Hemorrhoidopexy Versus Milligan-Morgan Hemorrhoidectomy in Circumferential Third-Degree Hemorrhoids: Long-Term Results of a Randomized Controlled Trial». J. Gastrointest. Surg., vol. 17, no. 7, pp. 1292-1298, 2013, https://doi.org/10.1007/s11605-013-2220-7.
- Y. Bilgin, S. Hot,̄lhami Soykan Barlas, A. Akan, and Y. Eryavuz, «Short - and long-term results of harmonic scalpel hemorrhoidectomy versus stapler hemorrhoidopexy in treatment of hemorrhoidal disease». Asian J. Surg., vol. 38, no. 4, pp. 214-219, 2015, https://doi.org/10.1016/j.asjsur.2014.09.004.
- V. Ripetti, V. La Vaccara, S. Greco, and A. Arullani, «A randomized trial comparing stapled rectal mucosectomy versus open and semiclosed hemorrhoidectomy». Dis. Colon Rectum, vol. 58, no. 11, pp. 1083-1090, 2015, https://doi.org/10.1097/DCR.0000000000000454.
- M. Rho et al., «Ligasure Hemorrhoidectomy: Updates on Complications After an 18-Year Experience». Rev. Recent Clin. Trials, 2020, https://doi.org/10.2174/1574887115999201006201926.
- E. Klang, T. Sobeh, M. M. Amitai, S. Apter, Y. Barash, and N. Tau, «Post hemorrhoidectomy complications: CT imaging findings». Clin. Imaging, vol. 60, no. 2, pp. 216-221, 2020, https://doi.org/10.1016/j.clinimag.2019.12.015.
- K.D. Hong, S. Kang, S. Kalaskar, and S. D. Wexner, «Ligation of intersphincteric fistula tract (LIFT) to treat anal fistula: Systematic review and meta-analysis». Tech. Coloproctol., vol. 18, no. 8, pp. 685-691, 2014, https://doi.org/10.1007/s10151-014-1183-3.
- Z. Mei et al., «Risk Factors for Recurrence after anal fistula surgery: A meta-analysis». Int. J. Surg., vol. 69, no. June, pp. 153-164, 2019, https://doi.org/10.1016/j.ijsu.2019.08.003.
- S. H. Emile, «Recurrent anal fistulas: When, why, and how to manage?». World J. Clin. Cases, 2020, https://doi.org/10.12998/WJCC.V8.I9.1586.
- A. Jarrar and J. Church, «Advancement flap repair: A good option for complex anorectal fistulas». Dis. Colon Rectum, vol. 54, no. 12, pp. 1537-1541, 2011, https://doi.org/10.1097/DCR.0b013e31822d7ddd.
- D.D.E. Zimmerman, L. E. Mitalas, and W. R. Schouten, «Long-term functional outcome and risk factors for recurrence after surgical treatment for low and high perianal fistulas of cryptoglandular origin». Diseases of the Colon and Rectum, vol. 52, no. 6. 2009, https://doi.org/10.1007/DCR.0b013e3181a51354.
- Lindsey, M. M. Smilgin-Humphreys, C. Cunningham, N. J. M. Mortensen, and B. D. George, «A randomized, controlled trial of fibrin glue vs. conventional treatment for anal fistula». Dis. Colon Rectum, vol. 45, no. 12, pp. 1608-1615, 2002, https://doi.org/10.1007/s10350-004-7247-0.
- I. J. Kodner, A. Mazor, E. I. Shemesh, R. D. Fry, J. W. Fleshman, and E. H. Birnbaum, «Endorectal advancement flap repair of rectovaginal and other complicated anorectal fistulas». Surgery, vol. 114, no. 4, 1993, https://doi.org/10.5555/uri:pii:003960609390255C.
- Q. Wang, Y. He, and J. Shen, «The best surgical strategy for anal fistula based on a network meta-analysis». Oncotarget, vol. 8, no. 58, pp. 99075-99084, 2017, https://doi.org/10.18632/oncotarget.21836.


