Хирургическое лечение пациента с сочетанным поражением коронарного и каротидного бассейнов
Автор: Ридель В.Ю., Михайлов К.М., Сенцова М.Д., Михайлов Н.М.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 1 (49), 2021 года.
Бесплатный доступ
Представлено клиническое наблюдение хирургического лечения пациента с атеросклеротическим сочетанным поражением коронарного и каротидного бассейнов. Было выполнено этапное оперативное вмешательство. Первым этапом была выполнена каротидная эндартерэктомия последовательно с двух сторон, вторым - трехсосудистое аортокоронарное шунтирование. Пациент осмотрен через два года после операции. Данных за рестеноз зоны реконструкции каротидного бассейна нет. Возврата стенокардии не отмечается.
Коронарные артерии, брахиоцефальные артерии, каротидная эндартерэктомия
Короткий адрес: https://sciup.org/143176787
IDR: 143176787 | УДК: 616.127-005.8+ | DOI: 10.20340/vmi-rvz.2021.1.CLIN.1
Surgical treatment of a patient with combined lesion of the coronary and carotid arterial systems
A clinical case of surgical treatment of a patient with atherosclerotic combined lesions of the coronary and carotid areas is presented. A staged surgery was performed. The first stage was carotid endarterectomy sequentially on both sides. The second stage is three-vessel coronary artery bypass grafting. The patient was examined 2 years after the operation. There are no data on restenosis of the reconstruction zone of the carotid system. The return of angina pectoris is not noted.
Текст научной статьи Хирургическое лечение пациента с сочетанным поражением коронарного и каротидного бассейнов
Cite as: Ridel V.Yu., Mikhailov K.M., Sentsova M.D., Mikhailov N.M. Surgical treatment of a patient with combined lesion of the coronary and carotid arterial systems. Bulletin of the Medical Institute Reaviz. Rehabilitation, Doctor and Health. 2021;1(49):21-28. CLIN.1
Актуальность
Несмотря на современные достижения медицины, последнее десятилетие характеризуется неуклонным ростом сердечнососудистых заболеваний. Проблема мультифокального атеросклероза в настоящее время является неразрешенной и актуальной проблемой в мире. Инфаркт миокарда и его осложнения в общей структуре смертности составляют 36 %, инсульт – 15–17 % [1]. Частота сочетанного атеросклероза брахиоцефальных и коронарных артерий у пациентов с ИБС по данным патологоанатомических исследований составляет 47,7 % [2]. В настоящее время вопрос о целесообразности реваскуляризации как коронарного, так и каротидного бассейнов ни у кого не вызывает сомнений [3].
Техника выполнения этапного оперативного вмешательства сопряжена с риском развития осложнений нереваскуляризиро-ванного сосудистого бассейна [4]. Неврологические осложнения после операции аортокоронарного шунтирования (КШ) остаются серьезной клинической проблемой [5]. У 1,2–6 % пациентов в раннем послеоперационном периоде после КШ возникают очаговые неврологические расстройства, приводящие к инвалидизации и значительно ухудшающие клинический и социальный прогноз [6]. При выполнении операций каротидной эндартерэктомии (КЭ) на фоне верифицированного поражения коронарного русла уровень смертности и частота инфаркта миокарда (ИМ) достигают 2 % и 12 % соответственно [7].
Сочетанные открытые операции на сосудах нескольких бассейнов несут повышенный риск: в 8–14 % случаев в раннем послеоперационном периоде возникают инфаркты миокарда, ишемические инсульты, случаи летальных исходов [8, 9]. Неудо- влетворительные результаты как одномоментных, так и этапных хирургических подходов в лечении пациентов с сочетанным атеросклеротическим поражением коронарных и сонных артерий, отсутствие четких международных рекомендаций по ведению данной категории пациентов заставляют искать новые подходы к этапности и вариантам хирургического лечения, использование, в том числе, эндоваскулярных, гибридных технологий [10].
Таким образом, тактика в отношении хирургического лечения пациентов с сочетанным атеросклеротическим поражением коронарных и сонных артерий до настоящего времени окончательно не определена. Как правило, решение вопроса о выборе того или иного метода операций, а также последовательность их выполнения зависят от опыта конкретной клиники или конкретного хирурга. Учитывая вышесказанное, в настоящее время подход в лечении данных пациентов должен быть индивидуальным, основыванным на специфическом уровне риска каждого пациента и опыте хирурга.
Собственное клиническое наблюдение
Пациент П., 79 лет, 14 мая 2015 г. доставлен бригадой скорой помощи из районной больницы в отделение реанимации и интенсивной терапии ГБУЗ «Самарский областной клинический кардиологический диспансер им. В.П. Полякова» с жалобами на интенсивные боли за грудиной, давящего характера с иррадиацией в левую верхнюю конечность, левую лопатку, продолжительностью 2–3 минуты, возникающие при минимальной физической нагрузке, купируемые нитроглицерином (принимает нитроспрей до 10 раз в сутки). Боли сопровождались холодным потом, чувством нехватки воздуха.
Заболел 2 недели назад, когда стали беспокоить боли за грудинной, продолжительностью до 30 минут, купировались нитратами короткого действия в течении 5–7 минут. Находился на лечении в районной больнице с 13.05.2015 г., когда боли приобрели интенсивный, давящий характер. Боли в области сердца беспокоили в течение последних 3 лет. Лечился амбулаторно. Артериальная гипертензия более 10 лет. Сахарный диабет 2-го типа выявлен в 2010 году. Принимает диабетон.
При поступлении общее состояние тяжелое. При аускультации сонных артерий выслушивается систолический шум с обеих сторон. Дыхание везикулярное, хрипов нет. Число дыханий 18 в мин. Тоны сердца глухие, ритм правильный, ЧСС – 72 ударов в мин. АД 140 и 80 мм рт. ст. Печень не увеличена, отеков на конечностях нет.
Тропонин –14,08 нг/мл, глюкоза крови от 6,05 до 8,23 ммоль/л.
На ЭКГ ритм синусовый, отклонение электрической оси влево, QS-II, III, AVF, депрессия ST- в V4-6.
Эхокардиография: фракция выброса по Симпсону – 54 %, левое предсердие 38x42x59 мм, ЛЖ: конечно-диастолический размер – 54 мм, конечно-систолический размер – 40 мм, правый желудочек – 28 мм, акинезия задней стенки базальный и частично медиальный сегменты, гипокинезия апикального сегмента задней стенки, задне-боковой стенки апикального и медиального сегмента; аортальный клапан – средний градиент 11 мм рт. ст., регургитация 1 ст., vena CONTRACTA 2,4 мм из центра смыкания створок; митральный клапан – регургитация 1 ст., малый объем; трехстворчатый клапан – систолический градиент 20 мм рт. ст., систолическое давление в правом желудочке 25 мм рт. ст., регургитация 1 ст.
Коронарография заключение: тип кровоснабжения левый. Выраженный кальциноз стенок артерий. Ствол левой коронарной артерии с неровными контурами. Передняя межжелудочковая ветвь (ПМЖВ) – устьевой стеноз 90 %, осложненные диссекцией стенозы 75 % в проксимальной трети, 50 % в дистальной трети 1-го сегмента. Огибающая артерия (ОА) – окклюзия в проксимальной трети 2-го сегмента, дистальные отделы фрагментарно заполняются через интракоронарные коллатерали. Критический стеноз 99 % в средней трети крупной ВТК. Правая коронарная артерия (ПКА) – гипоплазированая (рис. 1).
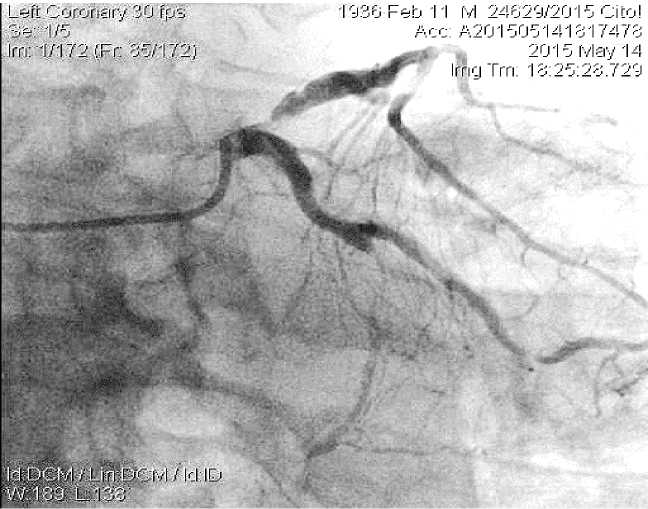
Рис. 1. Коронарография. Стеноз передней межжелудочковой ветви и огибающей артерии
Поставлен клинический диагноз: ИБС. Инфаркт миокарда с зубцом Q задней стенки от 13.05.2015 г. Ранняя постинфарктная стенокардия. Гипертоническая болезнь 3 стадии, риск 4. НI, 2 ф.кл. по NYHA. Сахарный диабет 2-го типа, средней степени тяжести.
Переведен в отделение кардиологии 19.05.2015 г. При подготовке пациента к аортокоронарному шунтированию было выполнено цветное дуплексное картирование брахиоцефальных сосудов (ЦДК БЦС).
ЦДК БЦС, заключение: в области бифуркации обеих общих сонных артерий (ОСА) с переходом на проксимальные отделы внутренних сонных артерий (ВСА) на протяжении 35–38 мм лоцируются гетерогенные атеросклеротические бляшки, суживающие просвет ОСА слева до 62 %, справа – до 50 %; ВСА слева до 70 %, ВСА справа – до 80 % по диаметру.
Был проведен консилиум мультидисци-плинарной бригадой в составе кардиолога, сердечно-сосудистых хирургов, анестезиолога, реаниматолога, невролога. Учитывая высокий риск развития ишемического инсульта при реваскуляризации миокарда, пациенту первым этапом решено выполнить операции на каротидном бассейне с двух сторон.
После стабилизации общего состояния и подбора оптимальной антиангинальной и дезагрегантной терапии 28.05.2015 г. пациент был переведен в отделение сосудистой хирургии ГБУЗ «Самарская городская клиническая больница № 1 им Н.И. Пирогова» (ГКБ № 1) для выполнения операции каротидной эндартерэктомии.
Мультиспиральная компьютернотомографическая ангиография брахиоцефальных артерий от 01.06.2015 г. с в/в болюсным контрастным усилением (Омнипак 350 – 100,0 мл).
Экстракраниально:
Справа: бифуркация правой ОСА на уровне С4 позвонка. В области бифуркации правой ОСА определяется гетерогенная атеросклеротическая бляшка, распространяющаяся на правую ВСА со стенозом правой ВСА до 98 %. Ход правой ВСА плавно извит.
Слева: бифуркация левой ОСА на уровне С4 позвонка. В области бифуркации левой ОСА определяется гетерогенная атеросклеротическая бляшка, распространяющаяся на левую ВСА со стенозом левой ВСА до 95 %. Ход левой ВСА плавно извит.
Позвоночные артерии контрастируются на всем протяжении, диаметром справа 3,5 мм, слева – 5 мм, без участков стеноза и патологических извитостей.
Интракраниально: Виллизиев круг не замкнутого типа: передняя соединительная артерия визуализируется, левая задняя соединительная артерия не визуализируется. Правая задняя мозговая артерия получает питание из правой внутренней сонной артерии, сегмент А1 правой задней мозговой артерии гипоплазирован. Основная артерия имеет прямолинейный ход (рис. 2, 3).
На 2-е сутки после поступления в ГКБ № 1 выполнено оперативное лечение – эверсионная каротидная эндартерэктомия справа. Послеоперационный период протекал без осложнений. Швы сняты на 6 сутки.
Спустя 5 дней после операции выполнена – эверсионная каротидная эндартерэктомия слева.
Послеоперационный период протекал без осложнений. Спустя 6 дней выписан в удовлетворительном состоянии. В течении всего срока госпитализации в условиях сосудистого отделения СГКБ № 1 ангиналь-ные боли не рецидивировали.
Через 24 часа после выписки из ГСКБ №1 госпитализирован в кардиохирургическое отделение СОККД. После предоперационной подготовки выполнено трехсосудистое коронарное шунтирование (ПМЖВ – ВГА, ЗБВ1, ЗБВ2-аутовена). Время пережатия аорты – 32 минуты, время искусственного кровообращения (ИК) – 52 минуты, ишемия – 11 минут.
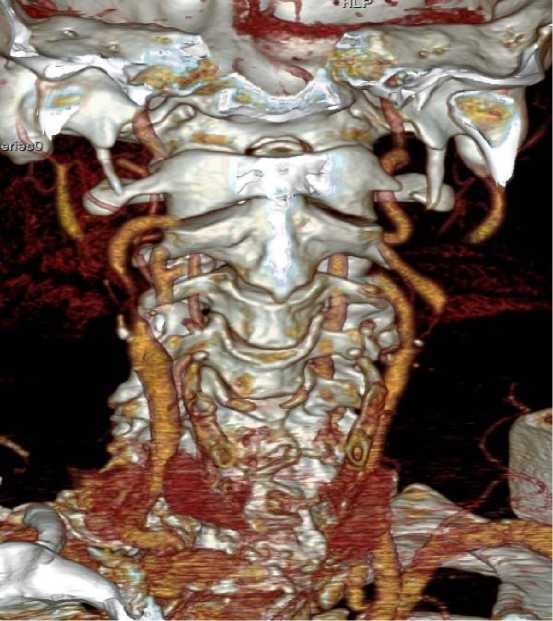
Рис. 2. КТ-ангиография с контрастированием 01.06.2015 г. Субокклюзия ВСА с двух сторон
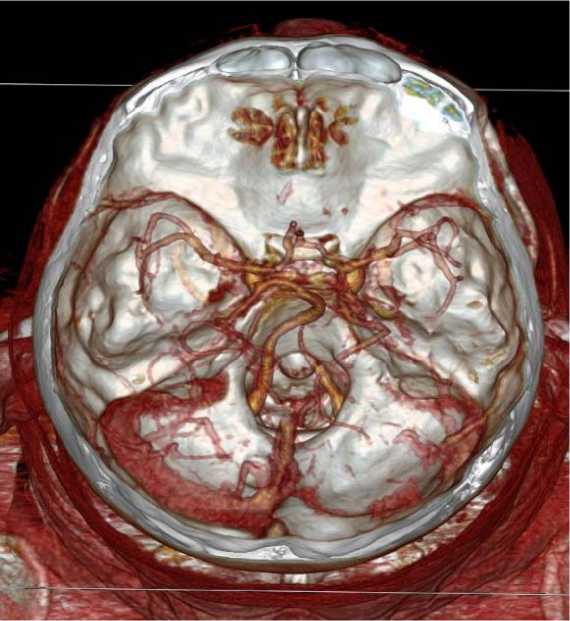
Рис. 3. КТ-ангиография с контрастированием. Задняя трифуркация средне-мозговой артерии справа
Операция проводилась на кровяной антеградной кардиоплегии миокарда при нормотермии (37 °С). Кровотоки: ПМЖВ – 37 мл/мин (2,5), ЗБВ 1 – 58 мл/мин. (2,4), ЗБВ 2 – 23 мл/мин. (1,3). Интраоперационно перелито 869 мл эритроцитарной взвеси для коррекции гемической гипоксии. Диурез составил 400 мл за операцию. Ввиду назначенной пациенту на предоперационном этапе двухкомпонентной антиагрегантной терапии, операцию проводили с использованием системы Cell Saver (Fresenius C.A.T.S. plus). Систему Cell Saver использовали как интраоперационно, так и в послеоперационном периоде (первые 8 часов для реинфузии потерь по дренажам). Операция прошла без особенностей. Грудина зашита продольно-поперечным способом. Пациент переведен в отделение реанимации. Для коррекции системы гемостаза перелито 900 мл свежезамороженной плазмы. Послеоперационные потери по перикардиальным дренажам составили 550 мл, из которых системой Cell Saver отмыто 150 мл эритроцитарной взвеси, которая, в свою очередь, была реинфузирована пациенту. Экстубирован через 5 часов после операции. Неврологический статус без особенностей. Кислотно-щелочной баланс удовлетворительный. Красная кровь без особенностей. Через 16 часов после операции переведен в кардиохирургическое отделение, где проходил послеоперационное лечение и реабилитацию в течении 12 дней. На момент выписки из стационара выполнено ЭХО КГ: левое предсердие 34x36x55 мм, конечнодиастолический размер ЛЖ 51 мм, конечносистолический размер ЛЖ 34 мм, фракция выброса 63 %, нарушения локальной сократимости левого желудочка не выявлено; митральный клапан – регургитация 1 ст., малый объем; аортальный клапан – пиковый градиент 20 мм рт. ст., средний – 10 мм рт. ст., регургитация 1 ст., малый объем; трехстворчатый клапан – регургитация 1 ст.; перикардиальная щель не расширена, в плевральных полостях свободной жидкости нет. Заживление послеоперационных ран пер- вичным натяжением. Выписан в удовлетворительном состоянии под наблюдение кардиолога и невролога по месту жительства.
Проведено наблюдение за пациентом в течение 2 лет. Пациенту 81 год. Жалоб на боли в области сердца не предъявляет. Качество жизни после операции значительно улучшилось. По данным ЦДК БЦС, КТ-ангиографии БЦС – данных за рестеноз зоны реконструкции сонных артерий не выявлено (рис. 4).
Обсуждение
Поражение коронарного русла выявляется у 30–60 % пациентов, перенесших острое нарушение мозгового кровообращения по ишемическому типу [11]. У пациентов с атеросклерозом коронарного русла сочетанное поражение сонных артерий достигает, по некоторым данным, 28 % [12]. Взаимосвязь между атеросклеротическим поражением этих двух бассейнов позволяет объяснить как высокий риск развития инсультов у оперированных по поводу ИБС, так и возникновение инфаркта миокарда у пациентов после каротидной эндартерэктомии.
Техника выполнения этапного оперативного вмешательства сопряжена с риском развития осложнений нереваскуля-ризированного сосудистого бассейна. В случае выполнения первым этапом операции на сонных артериях увеличивается риск осложнений и летальности от инфаркта миокарда. Вмешательство на коронарных артериях первым этапом сочетается с риском развития ишемического инсульта в периоперационном периоде. Операции на брахиоцефальных и коронарных артериях одномоментно сочетаются с риском развития как инсульта, так и инфаркта миокарда.
В тактике реваскуляризации каротидных артерий у данного пациента имелись следующие особенности: в предоперационном периоде проводилась инфузия фосфокреатина («Неотон») в дозе 4 грамма; интраоперационно-управляемая артериальная гипертензия проводилась под мониторингом показателей церебральной оксиметрии и степенью элевации сегмента ST по ЭКГ.
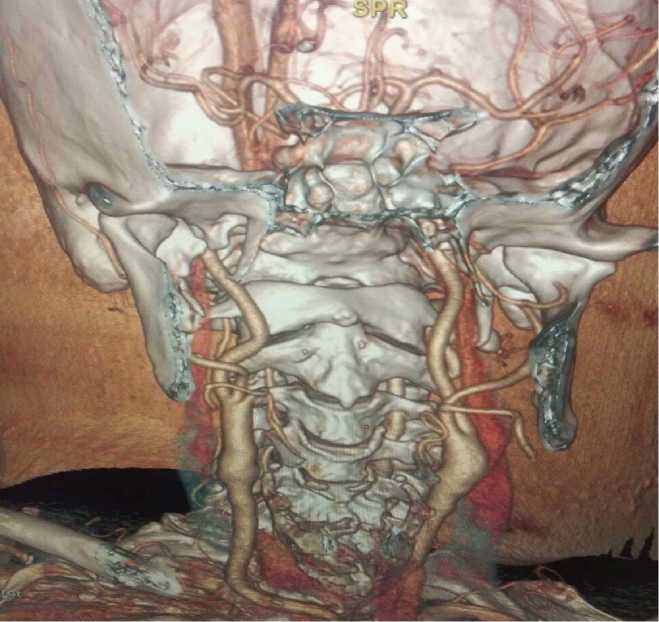
Рис. 4. КТ-ангиография с контрастированием 16.11.2017 г. Эверсионная каротидная эндартерэктомия с двух сторон от 06.2015 г.
«Приемлемые» показатели SpO 2 и степени подъема ST достигнуты при повышении АД на 15–20 мм рт. ст. от исходного уровня; выполнялась блокада каротидного синуса 2 % раствором лидокаина; на этапе формирования анастомоза проводилась инфузия нитратов и нимодипина в дозе 1 мг под контролем ЧСС. В раннем послеоперационном периоде – 24 часовое мониторирование и стабилизация АД, коррекция антигипертензивной терапии.
Несмотря на наличие множества публикаций, посвященных данной проблеме, к настоящему времени нет единого мнения о подходах к хирургическому лечению сочетанных поражений коронарных и брахиоцефальных артерий. Каждый хирургический центр придерживается своей методики, отработанной в течение многих лет. Однако тенденция мирового сообщества сердечно- сосудистых хирургов и анестезиологов сводится к тому, что разделение хирургического лечения данной группы пациентов на этапы является в настоящее время более предпочтительной.
Заключение
В данном клиническом случае пациенту с атеросклеротическим сочетанным поражением коронарного и каротидного бассейнов было выполнено этапное оперативное вмешательство. Первым этапом была выполнена каротидная эндартерэктомия последовательно с двух сторон. Вторым этапом – трехсосудистое аортокоронарное шунтирование. Осложнений во время операций не наблюдалось. Представленное успешное наблюдение демонстрирует один из современных подходов в лечении пациентов с мультифокальным атеросклерозом.
Список литературы Хирургическое лечение пациента с сочетанным поражением коронарного и каротидного бассейнов
- Bokeriya L.A., Bukharin V.A., Rabotnikov V.S. Khirurgicheskoe lechenie bol'nykh ishemicheskoy bolezn'yu serdtsa s porazheniem brakhiotsefal'nykh arteriy. M.: Izdatel' stvo NTSSSKH im Bakuleva RAMN. 1999; 174.
- Karpov R.S., Dudko V.A. Ateroskleroz: patogenez, klinika, funktsional'naya diagnostika, lechenie. Tomsk: STT. 1998; 656.
- Filsoufi F., Rahmanian P.B., Castillo J.G., Bronster D., Adams D.H. Incidence, imaging analysis, and early and late outcomes of stroke after cardiac valve operation. The American journal of cardiology. 2008;101(10): 1472-1478.
- Salasidis G.C., Latter D.A., Steinmetz O.K., Blair J.F., Graham A.M. Carotid artery duplex scanning in preoperative assessment for coronary artery revascularization: the association between peripheral vascular disease, carotid artery stenosis, and stroke. Journal of vascular surgery. 1995;21(1): 154-162. http://doi.org/10.1016/S0741-5214(95)70254-7
- Costa, M.A.C.D., Gauer M.F., Gomes R.Z., Schafranski M.D. Risk factors for perioperative ischemic stroke in cardiac surgery. Brazilian Journal of Cardiovascular Surgery. 2015;30(3):365-372.
- Kolh P.H., Comte L., Tchana-Sato V., Honore C., Kerzmann A., Mauer M., Limet R. Concurrent coronary and carotid artery surgery: factors influencing perioperative outcome and long-term results. European heart journal. 2006;27(1):49-56.
- Trachiotis G.D., Pfister A.J. Management strategy for simultaneous carotid endarterectomy and coronary revascularization. The Annals of thoracic surgery. 1997;4(64):1013-1018.
- Naylor A.R., Cuffe R.L., Rothwell P.M., Bell P.R.F. A systematic review of outcomes following staged and synchronous carotid endarterectomy and coronary artery bypass. European Journal of Vascular and Endo-vascular Surgery. 2003;25(5):380-389. http://doi.org/10.1053/ejvs.2002.1895
- Ricotta J.J., Wall L.P., Blackstone E. The influence of concurrent carotid endarterectomy on coronary bypass: a case-controlled study. Journal of vascular surger. 2005;41(3):397-401.
- Chernyavskiy A.M., Edemskiy A.G., Chernyavskiy M.A. Patologiya krovoobrashcheniya i kardiokhirurgiya. 2013;1:45-50. (in Russ).
- Craven T.E., Ryu J.E., Espeland M.A., Kahl F.R., McKinney W.M., Toole J.F., ... & Crouse 3rd J.R. Evaluation of the associations between carotid artery atherosclerosis and coronary artery stenosis. A case-control study. Circulation. 1990;82(4):1230-1242.
- Hertzer N.R., Young J.R., Beven E.G., Graor R.A., O'Hara P.J., Ruschhaupt W.F., ... & Maljovec L.C. Coronary angiography in 506 patients with extracranial cerebrovascular disease. Archives of internal medicine. 1985; 145(5):849-852.


