Хирургическое лечение переломов позвонков на фоне агрессивных гемангиом. Серия случаев и обзор литературы
Автор: Островский В.В., Лихачев С.В., Папаев А.В., Зарецков В.В., Арсениевич В.Б., Мизюров С.А., Зарецков А.В.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Обзор литературы
Статья в выпуске: 3 (53), 2023 года.
Бесплатный доступ
Обоснование. Гемангиома позвонка (ГП) - это смешанная группа сосудистых образований позвоночника, вызывающих деструкцию костной ткани позвонка. Клинически значимым формам ГП сопутствует болевой синдром или неврологический дефицит, обусловленные прогрессирующим снижением опороспособности пораженного позвонка или его патологическим переломом, который сопровождает клиническое течение 3,6-10,9% всех агрессивных ГП. В доступной литературе нет алгоритма хирургического лечения переломов при ГП. Цель исследования. Определить спектр хирургических методик, применяемых при переломах пораженных гемангиомами позвонков. В литературе за период 1983-2020 гг. обнаружено 15 публикаций, посвященных патологическим переломам на фоне ГП. Среди них: 6 - клинические случаи, 9 - обзоры литературы. Описаны следующие варианты хирургического лечения: 3 - резекция тела позвонка из переднего доступа, замещение дефекта аутокостью; 1 - вертебропластика (кифопластика); 5 - декомпрессия и фиксация металлоконструкцией из переднего доступа; 5 - транспедикулярная фиксация (ТПФ) и открытая вертебропластика; 1 - ТПФ и ламинэктомия. В 80% отмечен полный регресс неврологического дефицита, в 20% - полного регресса неврологического дефицита не произошло ввиду длительных сроков с момента перелома. Представлены 3 клинических случая, иллюстрирующие авторский опыт хирургического лечения пациентов с патологическими переломами на фоне ГП. Выполненные вмешательства: транскутанная транспедикулярная баллонная кифопластика L1; двухэтапное оперативное лечение (транскутанная транспедикулярная фиксация L3-L5 с биопсией новообразования L4 + передний опорный корпородез); вертебропластика С7. Описаны результаты лечения. Наблюдение в послеоперационном периоде 1 год. Болевой синдром купирован полностью. Потери достигнутой стабильности нет.
Гемангиома позвоночника, патологический перелом, вертебропластика, декомпрессивно-стабилизирующая операция
Короткий адрес: https://sciup.org/142239950
IDR: 142239950 | УДК: 611.711.1:617-089.844 | DOI: 10.17238/2226-2016-2023-3-91-100
Surgical management of vertebral fractures caused by aggressive hemangiomas. A series of case reports and a review
Relevance. Vertebral hemangioma (VH) is a combined group of spine vascular formations that destruct bone tissue of vertebrae. The clinically relevant VH forms cause pain syndrome or neurological defi t due to the progressive decrease of support ability in the affected vertebra or its pathologic fracture that occure within the clinical course of 3.6-10.9 percent of all aggressive VH. No algorithm for the surgical management of fractures in VH was found in the available studies. Th objective of this study was to determine the range of surgical techniques used for fractures in hemangioma affected vertebrae. Th ee case reports are presented. The available sources of 1983-2020 contain 15 studies on pathologic fractures associated with VH including 6 case reports and 9 reviews. They describe 3 anterior corpectomies with autograft bone substitutes, 1 vertebroplasty (kyphoplasty), 5 decompressions and anterior fi tion with a hardware, 5 transpedicular fi tions (TPF) and open vertebroplasties, 1 TPF and laminectomy. 80 percent of the outcomes featured the complete regression of neurological defi t. However, in 20 percent of the outcomes the neurological defi t never regressed completely due the long time that passed since the fractures occurred. We present three case reports that demonstrate the unique practice of surgical management for pathologic fractures in VH and involve L1 transcutaneous transpedicular balloon kyphoplasty, two-stage surgical treatment (L3-L5 transcutaneous transpedicular fi tion and L4 neoplasm biopsy+ anterior corporodesis); C7 vertebroplasty. The outcomes featured the complete reversal of pain syndrome in 1 post-op year without any loss in the induced stability.
Текст обзорной статьи Хирургическое лечение переломов позвонков на фоне агрессивных гемангиом. Серия случаев и обзор литературы
Обоснование. Гемангиома позвонка (ГП) — это смешанная патоморфологическая группа сосудистых образований позвоночника, представленная липоангиоматозными включениями, сосудистыми мальформациями и опухолями, вызывающими деструкцию костной ткани позвонка. ГП составляют до 3% всех новообразований позвоночника, а предполагаемая частота встречаемости в общей популяции 1,9-27% [1]. Клинически значимые формы ГП (до 10% от общего числа ГП) сопровождаются болевым синдромом или неврологическим дефицитом [2], обусловленными прогрессирующим снижением опоро-способности пораженного позвонка или его патологическим переломом, который сопровождает клиническое течение 3,610,9% всех агрессивных гемангиом по литературным данным [3]. Болевой синдром и/или неврологический дефицит может быть также обусловлен компрессией структур позвоночного канала экспансивно эпидурально растущей опухолью [4-7].
Большинство известных классификаций ГП разработано для определения показаний к хирургическому лечению. Самая известная разработана J. Laredo с соавт. (1986). Агрессивность гемангиомы авторы оценивают по совокупности показателей: расположение, объём поражения, наличие экстравертебральной экспансии, характер структурных изменений позвонка, низкий сигнал на Т1 и высокий сигнал на Т2 взвешенном изображении (ВИ) на магнитно-резонансной томографии (МРТ), накопления контраста при компьютерной томографии (КТ). Авторы предлагают рассматривать гемангиому как агрессивную при выявлении трех из любых перечисленных признаков [8]. В отечественной литературе доминирует классификация агрессивности
ГП, основанная на суммировании баллов, соответствующих интроскопическим и клиническим признакам, предложенная М.Н. Кравцовым (2010). Во внимание принимается наличие экстравертебрального компонента, компрессионный перелом тела позвонка, наличие костной экспансии, объём поражения, истончение или деструкция, характер структурных изменений тела позвонка, распространение гемангиомы на дугу позвонка, низкая доля жировой ткани (низкий сигнал от гемангиомы на Т1 и высокий — на Т2 ВИ на МРТ, высокий сигнал на Т2 ВИ в режиме подавления сигнала от жира), болевой синдром [3, 9]. Существует и опыт использования при классифицировании ГП классификации, разработанной для работы со злокачественными новообразованиями. Классификация опухолей позвоночника W.F. Enneking с соавт. (1980), экстраполированная на пациентов с ГП, включает в себя три стадии: I – низкая степень; II – высокая степень; III – наличие поражения как с анатомической локализацией в пределах четко очерченных хирургических компартментов (по мнению Enneking, позвонок является онкологическим компартментом – обособленной областью), так и в нечетко определенных фасциальных плоскостях и пространствах. Концепция представляется удобной для ста-дирования поражения костей и мягких тканей позвоночника любого генеза с подразделением по степени биологической агрессивности, анатомической структуре и наличию метастазов. Это позволяет проводить соответствующую оценку и выбрать более оптимальный вариант лечения [10-12].
В ряде классификаций, используемых при ГП, интегрирована регистрация факта такого грозного, хотя и редкого, осложнения
ГП, как патологический перелом в качестве аргумента в пользу хирургической тактики. Доступная литература преимущественно посвящена декомпрессивно-стабилизирующим вмешательствам при эпидуральной экспансии опухоли и относительно сохранной геометрии тела позвонка [13-15]. Единого алгоритма хирургической реконструкции при патологическом переломе, обусловленном ГП, в доступной литературе не обнаружено.
В данной работе представлен опыт хирургического лечения трех пациентов с патологическими переломами на фоне агрессивных ГП с описанием клинических и интроскопических результатов лечения.
Клинический случай №1. Больная Р., 65 лет, при поступлении предъявляла жалобы на боли в поясничном отделе позвоночника, усиливающиеся в положении сидя. После прохождения МРТ и КТ (рис. 1) обследований диагностирован патологический перелом L1 позвонка на фоне агрессивной гемангиомы. На момент осмотра обращает на себя внимание напряжение паравертебральных мышц в области поясничного отдела позвоночника. При пальпации остистых отростков болезненность на уровне L1 позвонка. Амплитуда движений в грудном и поясничном отделах позвоночника снижена на 50% с усилением болевого синдрома при движении и физической нагрузке, интенсивность болевого синдрома по визуально аналоговой шкале (ВАШ) — 6. По итогу осмотра и диагностических обследований поставлен диагноз: Агрессивная гемангиома L1 позвонка. Патологический компрессионный перелом L1 позвонка. Вертеброгенный болевой синдром.
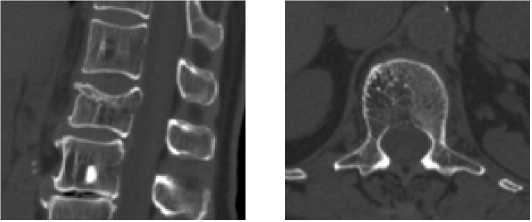
Рисунок 1. Предоперационная КТ пациентки Р., 65 лет
Техника и результаты операции. С контролем электронно-оптического преобразователя (ЭОП) под м/а Sol. Lidocaini 2% 20,0 в положении пациента лежа на животе произведено билатеральное транспедикулярное введение троакаров к передней 1/3 тела L1 позвонка. Сверлами созданы туннели для баллонов. Затем введены гидравлические баллоны системы Balex. Произведена их дилатация. После в троакары введено 10 мл. костного цемента. На введение пластического материала реакции не было. На контрольных рентгенограммах распространение пластического материала правильное. Пациентка активизирована через 2 часа после операции.
В первые сутки после операции выполненное КТ-обследование (рис. 2), продемонстрировавшее отсутствие миграции костного цемента. К выписке из стационара болевой синдром полностью регрессировал (ВАШ – 0).
Наблюдение за пациенткой в течение 1 года не выявило осложнений, рецидива гемангиомы, болевого синдрома.
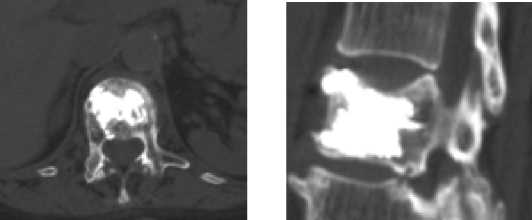
Рисунок 2. Послеоперационная КТ пациентки Р., 65 лет
Клинический случай №2. У больной Б., 27 лет, на 6 месяце беременности без внешних причин возникли интенсивные боли в поясничном отделе позвоночника, усиливающиеся при движениях. В связи с беременностью не обследовалась.
После родоразрешения путём кесарева сечения прошла рентгенологическое (рис. 3a), МРТ (рис. 3б) и КТ (рис. 3в), обследования, по итогу которых диагностирован компрессионный перелом тела L4 позвонка, с нарушением целостности кортикального слоя; структура костной ткани неоднородная, с разряжением и сохранением единичных трабекул, с частичным распространением на задние опорные структуры (предположительно – агрессивная ГП). На момент осмотра: в сознании, ориентирована. Коленные рефлексы средней живости, равномерные. Боль при пальпации в проекции остистого отростка L4 позвонка, её усиление при движении и физической нагрузке с показателем по шкале ВАШ – 7. Выраженное снижение чувствительности в области правого бедра. По итогу осмотра и диагностических обследований поставлен диагноз: Патологический компрессионный перелом тела L4 позвонка. Агрессивная гемангиома L4 позвонка (?). Вертеброгенный болевой синдром.
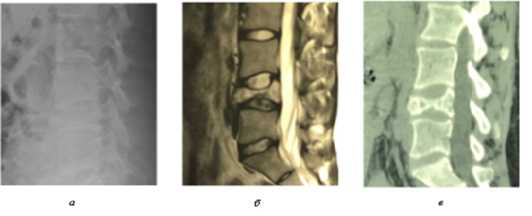
Рисунок 3. Пациентка Б., 27 лет, результаты обследования до оперативного вмешательства: а – рентгенография, б – МРТ, в – КТ.
Техника и результаты двухэтапного хирургического лечения. Первый этап: транскутанная транспедикулярная фиксация L3-L5. Биопсия новообразования L4 позвонка. Под эндотрахеальным наркозом (ЭТН), в положение больной на животе. После обработки и отграничения операционного поля произведены 4 продольных разреза кожи длиной по 3 см, подкожной клетчатки и фасции в проекции дугоотростчатых суставов L3-L4, L4-L5 билатерально. Гемостаз. Через разрезы под ЭОП контролем установлены транспедикулярно 4 троакара до границы передней и средней третей позвонков. Через иглы установлены 4 спицы-направителя, иглы удалены. Поэтапно установлены дилятаторы, метчик, полиаксиальные транспедикулярные винты (4 шт). Винты соединены двумя штангами, фиксация гайками. В проекции правого дугоотростчатого сустава L3-L4 произведен разрез в 1 см, под ЭОП контролем, мечиком сформирован тоннель в ножке дуги L4 позвонка. Через него под ЭОП контролем конхотомом взяты ткани патологически измененного тела L4 позвонка (рис. 4). Окончательная протяжка гаек, ЭОП контроль (рис. 5). Металлоконструкция стабильна.
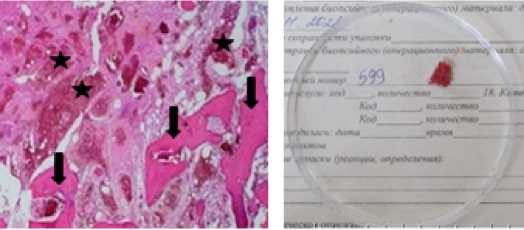
а б
Рисунок 4. а – гистологическое изображение гемангиомы, окраска гематоксилин-эозином. Стрелками обозначены костные трабекулы тела позвонка, звёздами – тонкостенные кровеносные сосуды.
Увеличение: объектив 10, окуляр 40; б – фотография макропрепарата
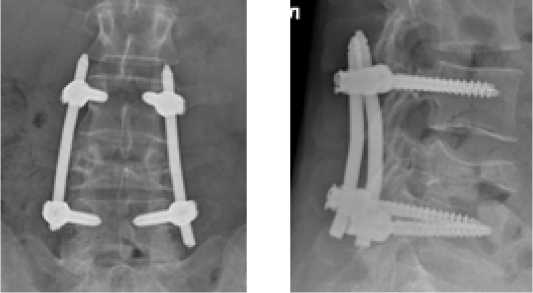
Рисунок 5. Послеоперационный рентген контроль пациентки Б., 27 лет
Послеоперационный период без осложнений, интенсивность болевого синдрома уменьшилась (ВАШ – 3), раны зажили первичным натяжением. Через 3 недели в условиях онкостационара проведен курс лучевой терапии (ЛТ) с модуляцией интенсивности пучка. КТ планирование, объёмная визуализация мишени; суммарная доза (СОД) дистанционной гамма терапии (ДГТ) – 38Гр разовая доза (РОД) – 2,0 Гр. Лучевую терапию перенесла удовлетворительно.
Через 2 месяца после ЛТ выполнен второй этап хирургического лечения: люмботомия слева. Резекция тела L4 позвонка с передним корпородезом MESH и аутокостью.
Положение больной на правом боку. После обработки и отграничения операционного поля произведён косой разрез кожи и подкожной клетчатки на 6 см ниже 12 ребра и параллельно ему, длиной 15 см. Люмботомия слева. Скелетировано тело L4 позвонка со смежными дисками после лигирования сегментарных сосудов. Произведена дискэктомия с L3 по L5, частичная резекция тела L4 позвонка. Тело позвонка составляет собой совокупность крупных каверн и гипертрофированных костных трабекул, практически не кровоточит, материал в объёме 2 см3 отправлен на цитоморфологическое исследование (рис. 6). Сформировано костное ложе для эндопротеза тела позвонка. Произведён передний корпородез MESH, аутокостью. Установлен дренаж в забрюшинное пространство. Рана герметично ушита послойно.
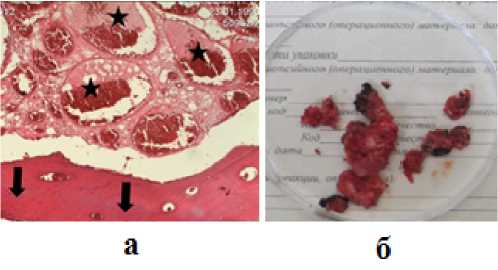
Рисунок 6. а – кавернозная гемангиома. Окраска гематоксилином-эозином. Между костными трабекулами (стрелки) тела позвонка рыхлая фиброзная ткань с тонкостенными кровеносными сосудами кавернозного типа (звезды). Сосуды аневризмально расширены, заполнены кровью и серозной жидкостью. Отмечаются обширные очаги свежих кровоизлияний.
Увеличение: объектив 10, окуляр 40; б – фотография макропрепарата
В первые сутки после операции проведена КТ и рентгенографический контроль (рис. 7), металлоконструкция стабильна. Осуществлена полная резекция пораженной части тела позвонка. К моменту выписки из стационара болевой синдром регрессировал (ВАШ – 0), осевая нагрузка безболезненна, чувствительность и иннервация не нарушена.
Наблюдение за пациенткой в течение 1 года не выявило чувствительных и неврологических осложнений, металлоконструкция стабильна, в сегментах L3-L5 костно-металлический блок.
Клинический случай №3. Больная Н., 47 лет, предъявляет жалобы на остро начавшиеся без видимой причины боли в шейном отделе позвоночника, которые беспокоят её в течение
1 года. Обратилась к неврологу по месту жительства. После консультации специалиста, МРТ и КТ исследований (рис. 8), было сделано заключение: патологический компрессионный перелом С7 позвонка, КТ признаки гемангиомы тела С7 позвонка.
Контуры тела позвонка четкие, ровные, не деформированные. Дуральный мешок деформирован до 2 мм, содержимое его однородно. В прилежащих мягких тканях дополнительных образований не обнаружено.
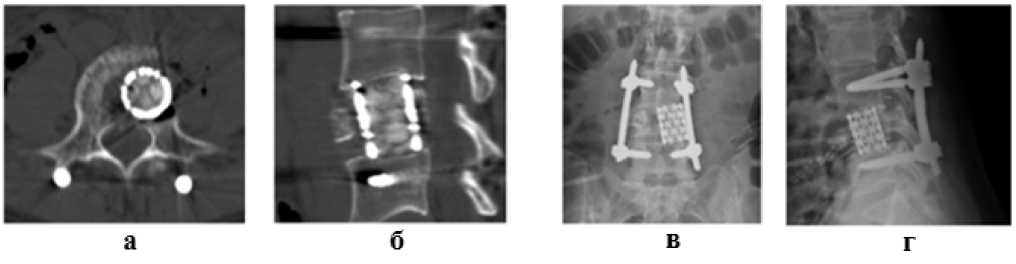
Рисунок 7. Послеоперационный КТ (а, б) и рентгенографический (в, г) контроль пациентки Б., 27 лет
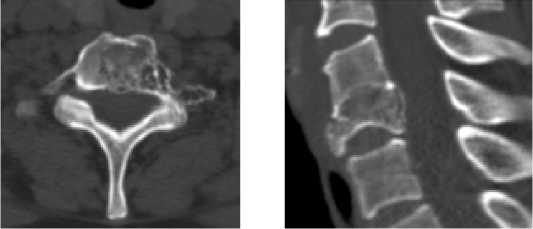
Рисунок 8. Предоперационное КТ обследование пациентки Н., 47 лет
На момент осмотра: в сознании, ориентирована. ЧМН в норме. Рефлексы с рук средней живости равномерные. Коленные рефлексы живые, равномерные. Ахилловы рефлексы живые. Отмечается напряжение паравертебральных мышц в шейном отделе позвоночника. При пальпации остистых отростков болезненность на уровне С7 позвонка. Болезненность при пальпации в области тела С7 позвонка спереди. Объем движений в шейном отделе позвоночника снижен на 50%, которые болезненны, показатель по шкале ВАШ — 6.
Техника и результаты операции. Под ЭТН, в положении больной лежа на спине, с валиком между лопаток. После обработки и отграничения операционного поля – кожный разрез по переднему краю правой грудино-ключично-сосцевидной мышцы на уровне щитовидного хряща, длиной 7 см. Правосторонний доступ по Смиту-Робинсону к вентральной поверхности тела С7 позвонка. Скелетирован участок вентральной поверхности тела позвонка 1х1 см, под ЭОП контролем произведено введение иглы для вертебропластики в центральный отдел тела С7 позвонка. Под ЭОП контролем введено 4 мл костного цемента Synicem. На контрольных рентгенограммах распространение пла- стического материала правильное. Игла удалена, гемостаз, рана ушита послойно.
В первые сутки после операции проведено КТ-обследование (рис. 9), результаты которого свидетельствовали об отсутствии экстравертебральной миграции костного цемента и практи- чески полном заполнении тела позвонка полиметилметакрилатом. К выписке из стационара болевой синдром полностью регрессировал (ВАШ – 0).
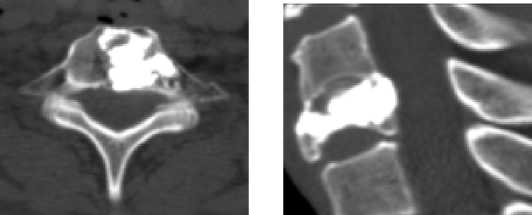
Рисунок 9. Послеоперационный КТ контроль пациентки Н., 47 лет
Наблюдение за пациенткой в течение 1 года нежелательных последствий операции не выявило.
Обзор литературы и обсуждение. Проведён тематический поиск в отечественной и зарубежной литературе в основных медицинских базах данных PubMed, Medline, Elibrary за период 1983-2023 гг. с использованием ключевых слов: compression fracture, aggressive vertebral hemangioma, vertebroplasty. Поиск был дополнен по разделу «similar articles» и списку литературы наиболее подходящих исследований [16, 20]. Диаграмма, отражающая особенности результатов поиска, представлены на рис. 10. Обращает на себя внимание скачкообразный рост публикационной активности, посвященной патологическим переломам на фоне ГП, с 2000 г. по настоящее время.
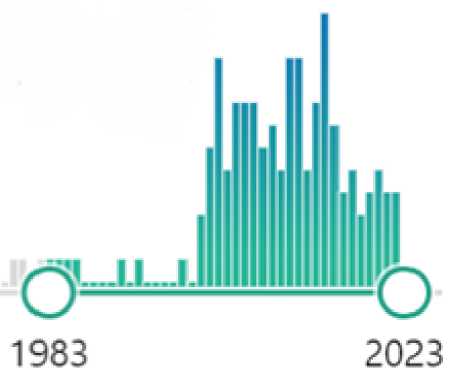
Рисунок 10. Диаграмма результатов поиска
После анализа названий публикаций и изучения их полнотекстовых вариантов были удалены повторяющиеся и неподходящие. Таким образом, в систематический обзор включены 15 публикаций (табл. 1). Во всех отобранных публикациях определяли возраст, пол пациента, локализацию перелома, неврологический статус, тактику лечения и его исход.
Исходя из полученной информации, можно определить варианты хирургического лечения патологических переломов, зависящие от степени поражения позвонка агрессивной ГП: ламинэктомия, резекция тела позвонка из переднего доступа со спондилодезом аутокостью, фиксация винтовой конструкцией из переднего доступа, задний спондилодез, межтеловой корпородез MESH, транспедикулярная фиксация, вертебропластика (кифопластика), комбинированный вариант. В 8 из 15 случаев (3 [29], 4 [19], 5 [20], 8 [23], 9 [24], 12 [26], 14 [32], 15 [28]) пациенты женского пола с диагностированной ГП и вызванным ею патологическим переломом в период беременности. На фоне беременности отмечен быстрый рост ГП с последующим патологическим переломом, сопровождающимся неврологическим дефицитом, что определило показания к экстренному оперативному лечению. Быстрый рост ГП связан с сосудистыми, гемодинамическими и эндокринными изменениями во время беременности: компрессия нижней полой вены (НПВ), вызванная увеличением матки (за счет плода), затрудняет кровоток из паравертебральных вен в НПВ, а увеличение кровотока через позвоночное венозное сплетение приводит к расширению ранее существовавших ГП. Высокий уровень прогестерона и увеличение объема плазмы во время беременности могут еще больше увеличить растяжение венозных каналов, а эндотелиальные пролиферативные эффекты эстрогена являются другими факторами, способствующими патогенезу увеличения гемангиомы [29, 30].
Таблица 1
Публикации, посвященные патологическим переломам тел позвонков на фоне агрессивных гемангиом
По данным литературы, у 3 пациентов выполнена резекция тела позвонка через передний доступ с замещением дефекта аутокостью; 1 пациент – вертеброплатика (кифопластика); 5 – декомпрессия с фиксацией металлоконструкцией из переднего доступа; 5 – транспедикулярная фиксация (ТПФ) и открытая вертебропластика; 1 – ТПФ и ламинэктомия. Доминировали случаи с поражением на уровне переходных отделов позвоночника: грудопоясничного и шейногрудного: Th11 – L2 (6) и C7 (1). Это может свидетельствовать в пользу механической теории роста гемангиом (рост вследствие реканализации тромбов, образовавшихся при переломах трабекул на переферии дефекта кости в биомеханически более нагруженных позвонках). Из всех перечисленных оперативных вмешательств 13 из 15 привели к полному регрессу неврологическиого дефицита, у 2 из 15 пациентов полного регресса неврологического дефицита не произошло ввиду длительно существовавшего до операции неврологического дефицита.
Заключение. ГП, являясь доброкачественными по своей природе новообразованиями, могут становиться агрессивными. На фоне агрессивных ГП существует риск возникновения патологического перелома, особенно у «биомеханически уязвимых» позвонков.
Поврежденный позвонок должен быть исследован с помощью КТ и МРТ для определения характера и объема поражения (в сомнительных случаях рекомендована биопсия).
При патологическом переломе без неврологического дефицита и значительного снижения тела позвонка возможно малоинвазивное лечение в объеме вертебро- или кифопластики [31-34].
Необходимость реконструкции неопороспособного тела позвонка, показания к декомпрессии структур позвоночного канала предполагает металлоспондилосинтез, адекватный морфологии поражения и структуре перелома. Выбор оптимальной тактики хирургического лечения обеспечивает хорошие клинические и рентгенологические результаты. При этом обращает на себя внимание отсутствие в доступной литературе общепринятого алгоритма выбора тактики при патологических переломах на фоне ГП, что подтверждает необходимость продолжения исследования по данной теме.
Список литературы Хирургическое лечение переломов позвонков на фоне агрессивных гемангиом. Серия случаев и обзор литературы
- Zafeiris C.P., Lewkonia P., Jacobs W.B. Atypical vertebral hemangioma: an aggressive form of a benign disease. Case Report and Literature Review. J Musculoskelet Neuronal Interact. 2021;21(2):317-321.
- Goraya G.S., Singhal S., Paul B.S., Paul G. Aggressive Vertebral Hemangioma: The Mystery of Spastic Legs Unveiled by a Purple Shoulder. Cureus. 2022;14(1):e21568. DOI: 10.7759/cureus.21568
- Кравцов М.Н. Агрессивные гемангиомы позвонков оптимизация тактики лечения: автореферат дисс. на соискание учёной степени кан. мед. наук. СПб., 2010. 24 с. [Kravtsov M.N. Aggressive vertebral hemangiomas optimization of treatment tactics: PhD abstract. Saint-Petersburg, 2010. 24 p.]
- Acosta F.L. Jr., Sanai N., Chi J.H., Dowd C.F., Chin C., Tihan T., Chou D., Weinstein P.R., Ames C.P. Comprehensive management of symptomatic and aggressive vertebral hemangiomas. Neurosurg Clin N Am. 2008;19(1):17-29. DOI: 10.1016/j.nec.2007.09.010
- Krueger E.G., Sobel G.L., Weinstein C. Vertebral hemangioma with compression of spinal cord. J Neurosurg. 1961;18:331-338.
- McAllister V.L., Kendall B.E., Bull J.W. Symptomatic vertebral haemangiomas. Brain 1975;98:71-80. DOI: 10.1093/brain/98.1.71
- Nguyen J.P., Djindjian M., Gaston A., Gherardi R., Benhaiem N., Caron J.P., Poirier J. Vertebral hemangiomas presenting with neurologic symptoms. Surg Neurol. 1987;27:391-7. DOI: 10.1016/0090-3019(87)90020-6
- Laredo J.D., Reizine D., Bard M., Merland J.J. Vertebral hemangiomas: radiologic evaluation. Radiology. 1986;161(1):183-9. DOI: 10.1148/radiology.161.1.3763864
- Кравцов М.Н., Мануковский В.А., Манащук В.И., Свистов Д.В. Диагностика и лечение агрессивных гемангиом позвоночника. Клинические рекомендации. М., 2015. С. 35. [Kravtsov M.N., Manukovsky V.A., Manashchuk V.I., Svistov D.V. Diagnostics and treatment of aggressive spinal hemangiomas. Clinical recommendations. Мoscow, 2015. P. 35.]
- Enneking W.F., Spanier S.S., Goodman M.A. A system for the surgical staging of musculoskeletal sarcoma. Clin Orthop Relat Res. 2003;(415):4-18. DOI: 10.1097/01.blo.0000093891.12372.0f
- Jawad M.U, Scully S.P. In Brief: Classifications in Brief: Enneking Classification: Benign and Malignant Tumors of the Musculoskeletal System. Clinical Orthopaedics and Related Research. 2010;468(7):2000-2002. DOI:10.1007/s11999-010-1315-7
- Заборовский Н.С., Пташников Д.А., Михайлов Д.А., Смекаленков О.А., Масевнин С.В. Онкологические принципы в хирургии опухолей позвоночника. Хирургия позвоночника. 2021;18(2):64-72. [Zaborovskii N.S., Ptashnikov D.A., Mikhaylov D.A., Smekalenkov O.A., Masevnin S.V. Oncological principles in spinal tumor surgery. Hir. Pozvonoc. 2021;18(2):64-72. In Russian]. DOI: 10.14531/ss2021.2.64-72
- Кит О.И., Закондырин Д.Е., Росторгуев Э.Е., Юндин С.В. Особенности хирургического лечения синдрома эпидуральной компрессии у пациентов со злокачественными опухолями позвонков. Креативная хирургия и онкология. 2022;12(1):21-27. [Kit O.I., Zakondyrin D.E., Rostorguev E.E., Yundin S.V. Specifics of epidural compression syndrome surgery in patients with spinal malignancy. Creative Surgery and Oncology. 2022;12(1):21-27. In Russian]. DOI: 10.24060/2076- 3093-2022-12-1-21-27
- Patchell R.A., Tibbs P.A., Regine W.F., Payne R., Saris S., Kryscio R.J., Mohiuddin M., Young B. Direct decompressive surgical resection in the treatment of spinal cord compression caused by metastatic cancer: a randomised trial. Lancet. 2005;366(9486):43-648. DOI: 10.1016/S0140-6736(05)66954-1
- Al-Omair A., Masucci L., Masson-Cote L., Campbell M., Atenafu E.G., Parent A., Letourneau D., Yu E., Rampersaud R., Massicotte E., Lewis S., Yee A., Thibault I., Fehlings M.G., Sahgal A. Surgical resection of epidural disease improves local control following postoperative spine stereotactic body radiotherapy. Neuro Oncol. 2013;15(10):1413-1419. DOI: 10.1093/neuonc/not101
- Островский В.В., Бажанов С.П., Арсениевич В.Б., Лихачев С.В., Зарецков В.В., Мизюров С.А., Папаев А.В. Нейроортопедический подход к тактике лечения пациента со шванномой и агрессивной гемангиомой на уровне одного позвоночно-двигательного сегмента: клиническое наблюдение. Хирургия позвоночника. 2022;19(2):67-73. [Ostrovskij V.V., Bazhanov S.P., Arsenievich V.B., Likhachev S.V., Zaretskov V.V., Mizyurov S.A., Papaev A.V. Neuroorthopedic approach to treating a patient with schwannoma and aggressive hemangioma at a single spinal motion segment: a case study. Spine Surgery. 2022;19(2):67-73. In Russian.] DOI: 10.14531/ss2022.2.67-73
- Greenspan A., Klein M.J., Bennett A.J., Lewis M.M., Neuwirth M., Camins M.B. Case report 242. Hemangioma of the T6 vertebra with a compression fracture, extradural block and spinal cord compression. Skeletal Radiol. 1983;10(3):183-188. DOI: 10.1007/BF00357777
- Graham J.J., Yang W.C. Vertebral hemangioma with compression fracture and paraparesis treated with preoperative embolization and vertebral resection. Spine (Phila Pa 1976). 1984;9(1):97-101. DOI: 10.1097/00007632-198401000-00022
- Schwartz T.H., Hibshoosh H., Riedel C.J. Estrogen and progesterone receptor-negative T11 vertebral hemangioma presenting as a postpartum compression fracture: case report and management. Neurosurgery. 2000;46(1):218-221.
- Chi J.H., Manley G.T., Chou D. Pregnancy-related vertebral hemangioma. Case report, review of the literature, and management algorithm. Neurosurg Focus. 2005;19(3):E7. DOI: 10.3171/foc.2005.19.3.8
- Vinay S., Khan S.K., Braybrooke J.R. Lumbar vertebral haemangioma causing pathological fracture, epidural haemorrhage, and cord compression: a case report and review of literature. J Spinal Cord Med. 2011;34(3):335-9. DOI: 10.1179/2045772311Y.0000000004
- Haque M.U., Wilson A.N., Blecher H.D., Reich S.M. Lumbar hemangioma masking a plasma cell tumor--case report and review of the literature. Spine J. 2013;13(8):e11-15. DOI: 10.1016/j.spinee.2013.01.050
- Moles A., Hamel O., Perret C., Bord E., Robert R., Buffenoir K. Symptomatic vertebral hemangiomas during pregnancy. J Neurosurg Spine. 2014;20(5):585-591. DOI: 10.3171/2014.2.SPINE13593
- Staikou C., Stamelos M., Boutas I., Koutoulidis V. Undiagnosed vertebral hemangioma causing a lumbar compression fracture and epidural hematoma in a parturient undergoing vaginal delivery under epidural analgesia: a case report. Can J Anaesth. 2015;62(8):901-906. DOI: 10.1007/s12630-015-0381-4
- Knechtle B., Nikolaidis P.T., Lutz B., Rosemann T., Baerlocher C.B. Pathologic fracture of the thoracic spine in a male master ultra-marathoner due to the combination of a vertebral hemangioma and osteopenia. Medicina (Kaunas). 2017;53(2):131-137. DOI: 10.1016/j.medici.2017.02.003
- Fereydonyan N., Taheri M., Kazemi F. Recurrent symptomatic vertebral hemangioma during two consecutive pregnancies: Case report and review of the literature. Surg Neurol Int. 2017;8:105. DOI: 10.4103/sni.sni_93_17
- Kilic K., Unal E., Toktas Z.O., Aker F.V., Akakın A., Kilic T. Posttraumatic Progressive Vertebral Hemangioma Induced by a Fracture. Case Rep Surg. 2017;2017:8280678. DOI: 10.1155/2017/8280678
- Bourghli A., Abduljawad S.M., BoissiÈre L., Khalifa H., Obeid I. Aggressive Thoracic Hemangioma Leading to Secondary Kyphosis with Paraparesis in the Postpartum Period. A Case Report. Int J Spine Surg. 2020;14(3):418-425. DOI: 10.14444/7055
- Liu C.-L., Yang D.-J. Paraplegia Due to Vertebral Hemangioma during Pregnancy. Spine. 1988;13(1):107-108. DOI:10.1097/00007632-198801000-00025
- Nayak R., Singh H., Khwaja G., Chowdhury D., Gupta M. Pregnancy related symptomatic vertebral hemangioma. Annals of Indian Academy of Neurology. 2014;17(1):120. DOI:10.4103/0972-2327.128577
- Li C., Zhang H.B., Zhang H., Li Q., Zhang J., Wang J., Guo K.J., Wang L.X. Severe pathological fractures caused by vertebral hemangiomas with posterior decompression, bone cement augmentation and internal fixation. Orthop Traumatol Surg Res. 2016;102(4):489-494. DOI: 10.1016/j.otsr.2016.01.024
- Wang G.X., Mu Y.D., Che J.Y., Zhang G.F., Jiang G., Gao C.P. Compressive myelopathy and compression fracture of aggressive vertebral hemangioma after parturition: A case report and review of literature. Medicine (Baltimore). 2019;98(50):e18285. DOI: 10.1097/MD.0000000000018285
- Мизюров С.А., Островский В.В., Зарецков В.В., Арсениевич В.Б., Лихачев С.В., Зарецков А.В., Папаев А.В. Баллонная кифопластика в хирургическом лечении агрессивных гемангиом позвоночника (обзор литературы). Гений ортопедии. 2021;27(6):821-826. [Miziurov S.A., Ostrovskij V.V., Zaretskov V.V., Arsenievich V.B., Likhachev S.V., Zaretskov A.V., Papaev A.V. Balloon kyphoplasty for surgical treatment of aggressive vertebral hemangiomas (literature review). Genij Ortopedii. 2021;27(6):821-826. In Russian]. DOI: 10.18019/1028-4427-2021-27-6-821-826
- Арсениевич В.Б., Лихачев С.В., Зарецков В.В., Островский В.В., Бажанов С.П., Мизюров С.А., Степухович С.В. Открытая вертебропластика при агрессивных гемангиомах шейного отдела позвоночника. Хирургия позвоночника. 2021;18(1):53-60. [Arsenievich V.B., Likhachev S.V., Zaretskov V.V., Ostrovskij V.V., Bazhanov S.P., Mizyurov S.A., Stepukhovich S.V. Open vertebroplasty for cervical spine aggressive hemangioma. Spine Surgery. 2021;18(1):53-60. In Russian.] DOI: 10.14531/ss2021.1.53-60


