Хронобиологические аспекты применения прямой электростимуляции спинного мозга для лечения неврологических осложнений остеохондроза шейного отдела позвоночника
Автор: Чехонацкий А.А., Коршунова Г.А., Овсянников Д.М., Чехонацкий В.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: История медицины, юбилейные даты
Статья в выпуске: 2 т.8, 2012 года.
Бесплатный доступ
Цель: изучить влияние времени проведения сеансов, длительности заболевания, возраста на эффективность применения прямой электростимуляции спинного мозга. Материал. Биоритмологические характеристики для выбора оптимального времени проведения сеансов электростимуляции были изучены у 32 больных шейным остеохондрозом, которым пункционно установили электроды к задним отделам спинного мозга. Результаты. В группе больных, где сеансы проводились утром, тяжесть клинических проявлений по шкале JOA изменялась с 8,4±0,2 до 12,8±0,3 балла, что составило 46,6 %. При проведении сеансов в дневное время тяжесть клинических проявлений снижалась на 25,1 %, а в вечернее время на 22,1 %. В возрасте до 40 лет средний процент снижения неврологической симптоматики после лечения составил 83,6±3,6 %, после 60 лет 74,6±3,2 %. При длительности болезни до четырёх лет наблюдалось снижение тяжести миелопатии, оцениваемой по шкале JOA, в среднем на 73,6±4,8 %, после 10 лет не превышало 63,7±2,1 %. Заключение. Максимальный эффект от прямой электростимуляции спинного мозга наблюдается в утренние часы. Клинический эффект от изолированного применения прямой электростимуляции спинного мозга в комплексе лечения неврологических симптомов остеохондроза шейного отдела позвоночника снижается с увеличением длительности заболевания. Эффект от применения электростимуляции уменьшается с возрастом, а максимальные положительные результаты применения данного метода лечения достигаются в период с первого по четвертый год болезни.
Шейный остеохондроз, электростимуляция
Короткий адрес: https://sciup.org/14917576
IDR: 14917576
Текст научной статьи Хронобиологические аспекты применения прямой электростимуляции спинного мозга для лечения неврологических осложнений остеохондроза шейного отдела позвоночника
Введение. Для лечения неврологических проявлений остеохондроза шейного отдела позвоночника в настоящее время широко применяются как хирургические, так и консервативные методы. Анализ научно-медицинской информации по лечению шейной миелопатии убеждает в том, что выполнением только декомпремирующе-стабилизирующих операций восстановление утраченных функций спинного мозга не достигается. Основной лечебный эффект получают уже в послеоперационном периоде от применения различных медикаментозных средств и физиотерапевтических методов лечения. [1-4]. Особенно широкие возможности в восстановлении функций спинного мозга открывают методы прямой электростимуляции спинного мозга. Электрические стимулы, близкие по параметрам к физиологическим нервным импульсам, усиливают аксональный транспорт, повышают уровень обменных процессов, синаптическую передачу и тем самым способствуют восстановлению проводниковых функций спинного мозга. В научно-медицинской литературе вопросам электростимуляции посвящено большое количество работ [5-7].
В научных исследованиях по хронотерапии указывается на необходимость проведения некоторых лечебных мероприятий в определённое время су-
Адрес: 410012, г. Саратов, ул. Б. Казачья, 112.
Тел.: 8 (8452) 63-04-27, 8-904-706-24-12
ток, месяца, года, то есть приспособления лечебных мероприятий к суточным, месячным и годовым биоритмам [8, 9]. Кроме этого, хорошо известно, что эффект от проводимого лечения чётко коррелирует с длительностью заболевания и возрастом пациента. До настоящего времени зависимость эффективности прямой электростимуляции спинного мозга от данных факторов не анализировалась.
Цель : изучить влияние времени проведения сеансов, длительности заболевания, возраста на эффективность применения прямой электростимуляции спинного мозга.
Методы. Биоритмологические характеристики для выбора оптимального времени проведения сеансов электростимуляции были изучены у 32 больных шейным остеохондрозом. В исследование включались пациенты с длительностью шейного остеохондроза не менее 5 лет. Критерием исключения были чёткие указания на отсутствие травматических повреждений шейного отдела позвоночника, а также наличие у больного острых заболеваний и хронических в стадии обострения: сахарного диабета, бронхиальной астмы, подтверждённых документально ревматических и системных заболеваний соединительной ткани, инфекционных заболеваний.
Количество мужчин и женщин, включённых в исследование, было статистически сопоставимым: 17 (53,1%) и 15 (46,9%) соответственно. Средний возраст больных составил у женщин 48,3±1,5 года, у мужчин — 45,2±1,4 года. Среди больных в обеих группах преобладали лица трудоспособного возраста до 60 лет — 25 человек (78,1 %). Можно отметить, что 78,1% (25 чел.) всех больных составили лица со «стажем» заболевания до 15 лет.
Всем больным проведено оперативное лечение, включающее в себя пункционную установку электродов к задним отделам спинного мозга для проведения электростимуляции.
Электростимуляция проводилась отечественным электростимулятором «Нейроэлект». Параметры электростимуляции следующие: амплитуда составляла 5-25 мА, частота 50-60 ГЦ, длительность 0,2-0,5 мс. Сеансы проводили по 20-30 мин 1-2 раза в день. Курс электростимуляции обычно длился 2-3 недели.
Исследование продолжалось 48 часов. Каждые четыре часа у всех больных регистрировалась температура тела, систолическое и диастолическое давление, частота сердечных сокращений и дыхательных движений в минуту.
Для перечисленных показателей определялись следующие параметры:
-
— среднее значение параметра для каждого исследования с учётом акрофазы и батифазы (время регистрации максимального и минимального значения);
-
— величина суточных колебаний (разница между наибольшим и наименьшем значением показателя в течение суток);
-
— среднесуточный уровень (среднее расчетное значение показателя).
Обработка данных проводилась с помощью пакета анализа Microsoft Office Excel 2007, Statistica 6.0. Производился корреляционный анализ, однофактор- ный дисперсионный анализ, использовали t-критерий Стьюдента. Для анализа таблиц сопряженности непараметрических признаков использовался критерий χ2. Достоверность различий считали статистически значимой при ρ<0,05.
Результаты. По результатам исследования у 26 (81,3%) больных шейным остеохондрозом отмечалось совпадение акрофаз ЧСС, АДс, АДд, температуры тела и ЧДД. Акрофазы большинства показателей приходились на дневные и вечерние часы, батифазы — на ночные и ранние утренние (рис. 1).
Вместе с тем у 6 (18,8%) больных отмечалось «блуждание» акрофаз в течение суток. Важно отметить, что «блуждание» акрофаз и батифаз наблюдалось преимущественно у лиц с локализацией поражения на уровне С4-С5 межпозвонкового диска.
Однако даже наличие информации о суточных биоритмах у конкретного больного требует решения вопроса о том, в какой фазе (акрофаза, батифаза или промежуток между ними) назначение электростимуляции окажется максимально эффективным.
Решение указанной задачи осуществлялось следующим образом. В группе больных из 9 человек сеансы электростимуляции проводились в утренние часы (9-10 часов), у 12 больных в период с 13 до 15 часов и у 11 человек в период с 19 до 20 часов вечера. Результаты лечения оценивались через один и шесть месяцев (табл. 1).
Анализ полученных данных показывает, что наибольшей эффективностью сеансы прямой электростимуляции спинного мозга обладают при их проведении в утренние часы.
В группе больных, где сеансы проводились утром, тяжесть клинических проявлений по шкале JOA из-
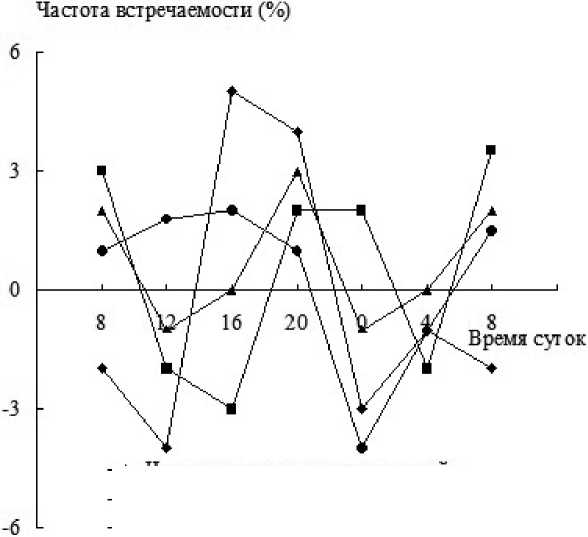
Рис. 1. Динамика исследуемых параметров в течение суток у больных шейным остеохондрозом
—*- Частота дыхательных движении
-•- Систолическое артериальное давление
-*- Частота сердечных сокращений
-■- Температура тела
Таблица 1
Результаты лечения шейной миелопатии при использовании сеансов прямой электростимуляции спинного мозга в различное время суток
|
Время проведения сеансов |
Тяжесть клинических проявлений миелопатии по шкале JOA |
||
|
до лечения |
через 1 месяц |
через 6 месяцев |
|
|
Утреннее время (9-10 часов) |
8,4±0,2 |
12,8±0,3* |
14,6±0,3* |
|
Дневное время (13-15 часов) |
7,9±0,1 |
10,4±0,2* |
11,7±0,1* |
|
Вечернее время (19-20 часов) |
8,2±0,3 |
10,6±0,3* |
10,1±0,2* |
П р и м еч а н и е : * — достоверность различий с исходными значениями (р<0,05).
Таблица 2
Показатели ЭНМГ-обследования до проведения прямой электростимуляции спинного мозга
|
Симптомы |
Показатели n. medianus |
|||||
|
М-ответ мВ (М±m) |
СПИ м/с (М±m) |
Спонтанная активность |
Н-рефлекс m.soleus, % |
F-волна, % блока нейрональных ответов |
||
|
ПФЦ |
ПОВ |
|||||
|
Радикулопатия |
3,2±0,7 |
37,0±2,4* |
+ |
+ |
53 |
40* |
|
Радикуло-миелопатия |
1,2±0,6* |
36,0±1,8* |
++ |
+++ |
25 |
75 |
|
Миелопатия |
2,4±0,3* |
42,3±1,2* |
+++ |
++ |
16* |
90* |
П р м еч а н и е : * — достоверное отличие (р<0,05) от показателей нормы.
менялась с 8,4±0,2 до 12,8±0,3 балла, что составило 46,6%. При проведении сеансов в дневное время тяжесть клинических проявлений снижалась на 25,1 %, а в вечернее время на 22,1%. Важно отметить, что отдалённый клинический эффект сеансов прямой электростимуляции спинного мозга при её проведении в утренние часы оказывался также значительно выше тех случаев, когда сеансы проводились днём или вечером. После прямой электростимуляции в утренние часы выраженность клинической симптоматики по шкале JOA через шесть месяцев с оставила 14,6±0,3 балла, в дневное время 11,7±0,1 балла и в вечерние часы 10,1±0,2 балла (различия с первой группой статистически значимы, р<0,05).
Обсуждение. С учётом полученных данных можно говорить о том, что электростимуляция спинного мозга при её проведении в период акро-фазы различных функциональных систем оказывается эффективнее, чем когда она проводится в другие фазы биологической активности. Наибольшую эффективность проведения сеансов прямой электростимуляции спинного мозга в утренние часы по сравнению с дневными и вечерними часами, наряду с клиническим улучшением, подтверждали результаты электронейромиографических исследований (ЭМНГ). Результаты электронейро-миографического исследования до проведения сеансов прямой электростимуляции спинного мозга представлены в табл. 2.
Согласно полученным данным у больных с изолированным поражением корешков спинномозговых нервов при первоначальном ЭМНГ-обследовании было обнаружено снижение скорости распространения возбуждения (СРВ) по нервным стволам плечевого сплетения (по срединному нерву до 37,0±2,4 м/с, р<0,05) (при норме не ниже 51,0±1,5 м/с), скорость распространения возбуждения по локтевому нерву составила 42,3 ±1,2 м/с.
Амплитуда вызванного мышечного ответа с m. gy-hothenar (М-ответ) снижалась до 3,2±0,7 мВ (р<0,05) (при норме 6,2±0,2 мВ). Блок нейрональных ответов с уровня С7 спинного мозга при исследовании антидромной проводимости составил 60%.
В зоне иннервации корешка С7 практически у каждого больного, в мышцах предплечья и кисти регистрировались, помимо потенциалов двигательных единиц (ПДЕ), сдвиг показателей длительности влево и спонтанная активность в виде потенциалов фасцикуляций (ПФЦ), потенциалов фибрилляций (ПФ) и позитивно острых волн (ПОВ), что свидетельствовало о существенном нарушении иннервации. ЭНМГ-данные подтверждали наличие корешковой патологии (рис. 2).
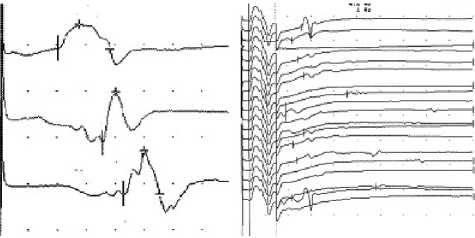
Рис. 2. Показатели М-ответа и F-волны до проведения электростимуляции
У больных со спинномозговыми нарушениями исходные показатели ЭНМГ-исследования свидетельствовали о поражении передних рогов спинного мозга на шейном уровне, разной степени выраженности. Помимо признаков корешковой патологии, выявлены проявления нейронопатии диффузного характера вследствие поражения мотонейронов спинного мозга на уровне компрессии.
Таблица 3
Влияние прямой электростимуляции спинного мозга на показатели электронейромиографического исследования
|
Стадии |
Показатели n. medianus |
|||||
|
М-ответ мВ (М±m) |
СРВ м/с (М±m) |
Потенциалы денервации |
Н-рефлекс m.soleus, % |
F-волна, % блоков |
||
|
ПФЦ |
ПОВ |
|||||
|
До лечения |
1,2±0,6* |
36,0±1,8* |
++ |
+++ |
25 |
75 |
|
После лечения |
3,1±0,4 |
46,2±1,9 |
+ |
- |
47 |
35 |
Примечание: * — достоверное отличие (р<0,05) от показателей нормы.
Таблица 4
Влияние прямой электростимуляции спинного мозга на показатели электронейромиографического исследования с учетом времени проведения сеансов
|
Анализируемые показатели |
Исходно |
Время проведения сеансов |
||
|
Утренние часы |
Дневное время |
Вечерние часы |
||
|
М-ответ, мВ |
1,2±0,6 |
3,6±0,4* |
3,0±0,2 |
2,9±0,4 |
|
СРВ, м/с |
36,0±1,8 |
52,7±1,0* |
41,6±1,2 |
44,6±1,7 |
|
ПФЦ |
++ |
- |
+ |
+ |
|
ПОВ |
+++ |
- |
+ |
+ |
|
Н-рефлекс, % |
25 |
47 |
51 |
49 |
|
F-волна, % блоков |
75 |
23 |
36 |
41 |
П р и м еч а н и е : * — достоверность различий со второй и третьей колонкой (р<0,05).
Кроме этого, выявлялось наличие параметров потенциалов действия двигательных единиц (ПДДЕ) в мышцах плеча, предплечья и кисти, соответствующих III-IV стадии деиннервационно-реиннервацион-ных процессов, потенциалов фасцикулляций выше и ниже уровня поражения спинного мозга, потенциалов спонтанной активности денервационного характера (ПФ, ПОВ).
Увеличение значений резидуальной латенции в 60% случаев свыше 5,6±1,3 мс (при норме не более 2,4±0,8 мс) без существенных изменений проводимости по нервам.
В табл. 3 представлена динамика показателей после прямой электростимуляции спинного мозга у больных шейным остеохондрозом с наличием неврологических проявлений остеохондроза шейного отдела позвоночника.
Анализ результатов исследований показал, что после сеансов электростимуляции при стимуляции n. medianus достоверно увелич и валась величина М-ответа (рис. 3) с m. guhothenar с 1,2±0,6 мВ до 3,1±0,4 мВ (различия статистически значимы, р<0,05).
Показатель скорости распространения возбуждения (СРВ) возрастал с 36,0±1,8 м/с до 46,2±1,9 м/с. Уменьшалась выраженность ПФЦ (потенциалы фас-цикуляций) и ПОВ (позитивно острых волн), наряду с положительной динамикой Н-рефлекса m.soleus и снижением F-волны.
Важно отметить, что наиболее выраженно эти показатели изменялись при проведении сеансов электростимуляции в утренние часы (табл. 4).
Было изучено влияние возраста больных и длительности заболевания на результаты лечения шейной миелопатии с использованием прямой электростимуляции спинного мозга. Постав- ленная задача решалась следующим образом. У всех больных перед началом лечения и через три месяца после его окончания по шкале JOA определялась выраженность клинической симптоматики. За исходный уровень, равный 100%, принималась тяжесть заболевания до применения прямой электростимуляции. Затем по формуле x x
у = —---1 х 100x1
определялось изменение тяжести. В формуле х1 — тяжесть до лечения, х2 — тяжесть через три месяца. После изучения данных исследования выявлено, что с увеличением возраста больных эффективность прямой электростимуляции спинного мозга при лечении миелопатии снижается.
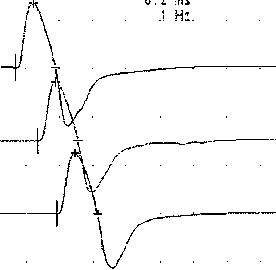
Рис. 3. Показатели М-ответа после проведения электростимуляции
Если в возрасте до 40 лет средний процент снижения неврологической симптоматики после лечения составил 83,6±3,6%, то после 60 лет 74,6±3,2%.
Аналогичная взаимосвязь обнаруживалась и с длительностью заболевания. Если при длительности болезни до четырёх лет наблюдалось снижение тяжести миелопатии, оцениваемой по шкале JOA, в среднем на 73,6±4,8%, то после 10 лет не превышало 63,7±2,1%.
Особо следует отметить, что при лечении шейной миелопатии прямой электростимуляцией результаты оказывались несколько ниже, чем в период болезни с двух до четырех лет.
Заключение. Оценивая хронобиологические аспекты применения электростимуляции, можно сделать следующее заключение: по результатам электронейромиографического исследования максимальный эффект от прямой электростимуляции спинного мозга наблюдается в утренние часы. Полученные данные подтверждаются четырьмя исследуемыми величинами: величина М-ответа, СРВ, ПФЦ и ПОВ. Их показатели при использовании электростимуляции в утреннее время достоверно выше, чем при применении данного метода лечения в вечернее и дневное время.
Результаты исследования показали, что клинический эффект от изолированного применения прямой электростимуляции спинного мозга в комплексе лечения неврологических симптомов остеохондроза шейного отдела позвоночника снижается с увеличением длительности заболевания. Эффект от применения электростимуляции уменьшается с возрастом, а максимальные положительные результаты применения данного метода лечения достигаются в период с первого по четвертый год болезни.
Список литературы Хронобиологические аспекты применения прямой электростимуляции спинного мозга для лечения неврологических осложнений остеохондроза шейного отдела позвоночника
- Pomerantz S. R., Hirsch J. A. Intradiscal therapies for discogenic pain//Semin. Musculoskelet. Radiol. 2006. Vol. 10, № 2. P. 125 -135
- Singh K., Ledet E., Carl A. Intradiscal therapy: a review of current treatment modalities//Spine. 2005. Vol. 30 (17 Suppl). S. 20 -26
- Van Dijk H., Jannink M. J., Hermens H. J. Effect of augmented feedback on motor function of the affected upper extremity in rehabilitation patients: a systematic review of randomized controlled trials//J. Rehabil. Med. 2005. Vol. 37, №4. P. 202 -211
- Wong W. Intradiscal electrothermal therapy (IDET)//JBR-BTR. 2003. Vol. 86, № 5. P. 297 -299
- Лившиц Л. Я., Гордеев М. Ю., Колесниченко И. Ю. Элек-тронейростимуляция и эндолимфатическая фармакотерапия в лечении хронической боли и грубых неврологических расстройств при поясничном остеохондрозе//Матер. 8-го Все-рос. съезда неврологов. Казань, 2001. С. 159
- Лившиц А. В. Хирургия спинного мозга. М.: Медицина, 1990. 350 с.
- Лившиц Л. Я., Меламуд Э. Е. Электростимуляция спинного мозга в лечении тяжких болевых синдромов туловища и конечностей нейрогенного происхождения//Матер. Рос. науч.-практ. конф., посвящ. 50-летию клиники нейрохирургии. Саратов, 1998. С. 19 -22
- Влияние медико-биологических факторов на распространенность неврологических проявлений остеохондроза позвоночника у коренных жителей юга Горного Алтая/И. Р. Шмидт, В. С. Саяпин, В. Ч. Ван [и др.]//Бюллетень экспериментальной биологии и медицины: ежемес. междунар. науч.-теор. журн./РАМН. 2003. Т. 135, № 5. С. 585 -589
- Кузнецов В. Ф. Вертеброневрология: клиника, диагностика, лечение заболеваний позвоночника. М.: Книжный дом, 2004. 640 с.


