Иммобилизация активатора плазминогена в пористую матрицу оксида алюминия для создания новых тромболитических препаратов
Автор: Виноградов Василий Валентинович, Дуданов Иван Петрович
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Медицинские науки
Статья в выпуске: 4 (149), 2015 года.
Бесплатный доступ
Основным препятствием при разработке новых тромболитических систем на основе ферментов является их низкая стабильность и короткий период полувыведения (не превышающий, как правило, 2-6 мин.), который требует введения их в больших дозах для достижения необходимого эффекта и, как следствие, неизбежно приводит к значительным геморрагическим осложнениям. В данной работе мы представляем новый подход к решению этой проблемы путем разработки нового семейства парентеральных композитов для тромболизиса. Иммобилизация активатора плазминогена в пористую матрицу на основе оксида алюминия значительно увеличивает стабильность тромболитического фермента, усиливает его термическую стабильность и маскирует от иммунной системы организма.
Оксид алюминия, золь-гель синтез, тромболизис, активатор плазминогена
Короткий адрес: https://sciup.org/14750899
IDR: 14750899 | УДК: 544.7
Immobilisation of plasminogen activator within porous alumina matrix for creation of new thrombolytic materials
A major obstacle in the development of new enzyme-based thrombolytic systems is their low stability and extremely short period of half-life (usually, less than 2-6 min of the circulation half-life), which requires their administration in large doses to obtain therapeutic effects, and, therefore, inevitably leads to a significant incidence of hemorrhagic complications. Here, we point out to a potential solution of this problem by developing a new family of injectable composites for thrombolysis: plasminogen activator entrapped within alumina. In that case alumina is a pertinent drug carrier developed to prolong activity in vivo, to reduce the total administered dose of the drug necessary for the treatment, and to decrease its side effects.
Текст научной статьи Иммобилизация активатора плазминогена в пористую матрицу оксида алюминия для создания новых тромболитических препаратов
Тромбоз является симптомом перекрывания русла кровяного потока вследствие образования тромба в кровеносном сосуде. Тромболитическая терапия, которая используется для растворения сгустков крови, в основном имеет дело с введением соответствующих ферментов, таких как стрептокиназа, урокиназа и активатор плазминогена тканевого типа (ТАП) [15]. Тем не менее эти тромболитические препараты неизбежно ведут к риску геморрагических осложнений из-за их неспецифической активации [5], что существенно ограничивает их реальное применение в терапии [8]. Высокая стоимость и быстрая потеря активности тромболитических ферментов стимулируют разработку новых видов систем, где фермент будет иммобилизирован в биологически инертную матрицу, обеспечивающую высокую стабильность, подход субстрата и сохранение активности.
Ранее нами были разработаны методики золь-гель синтеза высокочистых нанокристаллических оксидов при помощи ультразвука [11], [14], предложена новая концепция для создания парентеральных золь-гель материалов на основе оксида алюминия [11]. В работе [13] были использованы три различных терапевтических фермента для изучения их стабильности в иммобилизованном состоянии. Результаты показывают, что введение ферментов в матрицу приводит к сдвигу температуры денатурации на 30–50 °C. Кроме того, было
установлено, что матрица оксида алюминия защищает не только от тепловой денатурации, но в определенном диапазоне температур существенно повышает активность ферментов с ростом температуры, тогда как свободные ферменты при этих температурах полностью теряют свою активность.
В данной работе мы показали, что тканевый активатор плазминогена может быть успешно иммобилизирован в матрицу из оксида алюминия с сохранением тромболитической активности и повышением термической стабильности. Несмотря на то что поведение большинства ферментов уже исследовалось в золь-гель матрицах [1], [2], [12], активность тромболитических ферментов в иммобилизованном состоянии до сих пор не была исследована. Это обусловлено тем, что при проведении химической реакции реагирующему веществу необходимо пройти через сеть микропор (характерную для большинства золь-гель матриц) для достижения каталитического центра. В том случае когда один из реагентов – профермент (плазминоген), практически невозможно достичь прямой диффузии внутри пор размером менее 3 нм. Поэтому необходимо обеспечить доставку высокомолекулярной молекулы к каталитическому реакционному центру через поры большего диаметра. В данной работе получены композиты с бимодальной пористой структурой и изучены механизмы действия и активации иммобилизованных тромболитических ферментов in vitro .
МАТЕРИАЛЫ И МЕТОДЫ. ХИМИЧЕСКИЕ ПРЕПАРАТЫ
Изопропоксид алюминия, плазминоген из бычьей плазмы крови (ПГ, кат. № P9156), фибриноген из бычьей плазмы крови (ФГ, кат. № F8630), тромбин из бычьей плазмы крови (ТБ, кат. № T7513), тканевый активатор плазминогена (ТАП, кат. № T5451) были получены от компании Sigma-Aldrich. Глициновый буфер (рН = 7,4) был получен из растворов глицина (0,05 М; Sigma-Aldrich) при добавлении определенного объема 1,0 М NaOH.
Золь-гель синтез оксида алюминия. Золь оксида алюминия получен по методике, изложенной в работе [11]: 2,2 г Al (C 3 H 7 O) 3 добавили к 50 мл деионизированной воды при 90 °C. При этом образуется белый студенистый осадок. Перед обработкой ультразвуком осадок выдерживали при 90 °C и интенсивном перемешивании в течение 15 мин. для формирования наночастиц бемита и испарения изопропанола, образующегося в процессе гидролиза. Конечную суспензию подвергали ультразвуковой обработке в течение 2 ч. Спустя 2 ч. образовывался вязкий золь. Полученный золь охлаждали до комнатной температуры. Высушенная матрица имела площадь поверхности 153 м 2/г, объем пор 0,097 см 3/г и средний размер пор ~2,5 нм.
Процедура иммобилизации ТАП в оксид алюминия. Для иммобилизации ТАП смесь, состоящую из 50 мкл буферного раствора гли-цин–NaOH (рН 7,4) и 150 мкл свежеприготовленного золя оксида алюминия, помещали в кювету, а затем добавляли 20 мкл ТАП (500 U/мл). Через десять минут золь помещали в вакуумный эксикатор при комнатной температуре на 24 ч. Для удаления адсорбированных белков ТАП@оксид алюминия был промыт внутри конечной поли-стирольной кюветы раствором глицина объемом 1,0 мл (рН 7,4). Полная иммобилизация фермента подтверждалась отсутствием активности промывочного раствора.
Ферментативная активность. После промывки 1,0 мл раствора глицина (рН 7,4) биоактивный гибрид оставляли на инкубацию при 37 °C в течение 30 мин. Затем промывочный раствор был заменен смесью 1,0 мл раствора бычьего фибриногена с концентрацией 5 мг/мл и 0,5 мл раствора бычьего плазминогена (1,2 U/мл) с последующим добавлением 0,5 мл раствора тромбина (50 U/мл) в глициновом буфере (рН 7,4). После образования сгустка ферментативную активность измеряли спектроскопически путем поглощения при длине волны 340 нм и температуре 37 °C. Соответствующая кривая образования и лизиса сгустка (КОЛС) показана на рис. 1. Растущая часть кривой соответствует образованию фибринового сгустка, а нисходящая – его лизису. Промывочный раствор также тестировали на ферментативную активность пу- тем помещения 500 мкл раствора в кювету при последующем введении тромбообразующего раствора. Чтобы скомпенсировать реакционную способность иммобилизованных ферментов, концентрация свободных ферментов была снижена в 10 раз. Кинетические кривые были интерпретированы в соответствии с указаниями работы [10], при этом в качестве стандарта принималась активность свободного ТАП.
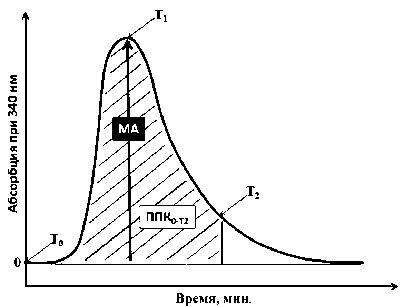
Рис. 1. Кривая образования и лизиса сгустка. Измерения включают максимальную амплитуду (MA), время до максимальной абсорбции (Т 1), завершение первого этапа снижения оптической плотности (Т 2 ) и площадь под кривой (ППК), из которой можно рассчитать индекс коагуляции (ИК) и фибринолитический коэффициент (ФК)
Кривая образуется во время анализа, начиная при нулевых значениях показателя поглощения (см. рис. 1) с последующим постепенным повышением оптической плотности до точки MA (достигается при T 1 ). Первая стадия снижения оптической плотности заканчивается при Т 2 , в точке, в которой наклон снижения оптической плотности меняется на 10 мОП/мин и завершается при возвращении оптической плотности к нулевой отметке. Параметры MA, T1 и T2 получаются непосредственно из данных по оптической плотности. Используя ППК на протяжении начального периода анализа до T 2 , можно рассчитать ИК, который связывает ППК образца и стандарта (активность свободного ТАП взята в качестве стандарта), а именно:
ИК =
( ППК 0 - T ) образец
( ППК 0 - T 2 )
стандарт
Х 100.
Также были измерены ФК. Они могут быть вычислены по соотношению времени завершения первого этапа снижения оптической плотности (T2) и времени до достижения максимального поглощения (T1) для соответствующего образца по сравнению со стандартом (с поправкой на различие в максимальном поглощении) следующим образом:
ФК =
T / T
2 1 образец
T / T
2 1 стандарт
MA стандарт
MA образец
Х 100.
В данной работе анализ КОЛС иммобилизованного ТАП анализировали по MA, T 1 , T 2 , ИК и ФК с использованием указанных выше расчетов.
Стабильность композитного материала в модельной системе крови. Для проверки стабильности синтезированного композита в реальной системе крови был использован концентрированный раствор Рингера. В растворе Рингера соотношение концентраций солей аналогично крови. Для этого пластиковые кюветы с композитом обрабатывались раствором Рингера и выдерживались при перемешивании в течение 30 дней. Активность иммобилизованного ТАП после испытания была сопоставлена с исходной активностью. Наблюдаемое снижение активности составило лишь 2,5 %.
Методика определения свойств. Удельная площадь поверхности, объем пор и распределение пор по размерам определяли методом адсорбции-десорбции азота при 77 К (Quantachrome Nova 1200, серия E). Площади поверхности были рассчитаны с использованием уравнения БЭТ. Методом BJH были рассчитаны объемы пор и распределение пор по размерам. Распределение микропор по размерам рассчитывалось с использованием метода Дубинина – Астахова (ДА). Перед анализом образец дегазировали в течение 24 ч. при комнатной температуре. Кристаллическая фаза и кристалличность образцов были исследованы методом рентгеновской дифракции (Bruker D8 Advance) с использованием излучения Cu-Kα с длиной волны λ = 1,54 Å, образцы сканировали по 2θ в диапазоне 4–75° со скоростью 0,5 градуса в минуту. Спектральный анализ ферментативной активности проводили с использованием спектрофотометра PG Instruments T80. При использовании сканирующей электронной микроскопии (СЭМ, электронный микроскоп Magellan 400L сверхвысокого разрешения) конечную суспензию захваченного фермента наносили на кремниевую подложку и полностью высушивали в вакууме. Образцы для просвечивающей электронной микроскопии (ПЭМ) были получены путем диспергирования небольшой пробы в этаноле с образованием гомогенной суспензии. Затем каплю суспензии наносили на медную сетку, покрытую углеродом, для анализа ПЭМ (FEI Tecnai G2 F20 при рабочем напряжении 200 кВ).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Следует отметить, что разработанная методика получения нанокристаллического золя AlOOH в водном растворе при ультразвуковом облучении подразумевает использование почти нейтральных значений рН, которые являются комфортными для биомолекул и соответствуют диапазону, где может быть достигнута полная иммобилизация.
Среди шести кристаллических фаз оксида алюминия биосовместимой формой, применяемой в качестве адъюванта, является бемит/ псевдобемит. Чтобы идентифицировать кристаллическую фазу, мы использовали метод рентгеновской дифракции. Положение максимумов на рентгенограмме как для индивидуальной матрицы, так и для композита с ТАП соответствует типичной структуре бемита. Анализ размера кристаллитов, проведенный с использованием уравнения Шерера, указывает на присутствие в полученных материалах кристаллитов со средним размером 3–4 нм.
Анализ удельной поверхности и пористости (методом адсорбции азота, с помощью уравнений БЭТ и BJH) был проведен в предположении типичной микро- и мезопористости образца (рис. 2). Для композита были получены следующие характеристики: площадь поверхности 175 м 2/г, объем пор 0,116 см 3/г, размер пор <4 нм с максимумом при 2,2 нм (по методу ДА). Следует предположить, что высвобождение фермента из матрицы оксида алюминия сильно зависит от размера белка и среднего размера пор матрицы. С этой целью опыт по высвобождению ТАП из матрицы оксида алюминия проводили в течение 30 дней в концентрированном растворе Рингера. Снижение активности было незначительным (рис. 3). Это связано с полной иммобилизацией фермента в матрицу на основе оксида алюминия удерживанием его в сетке микро- и мезопор.
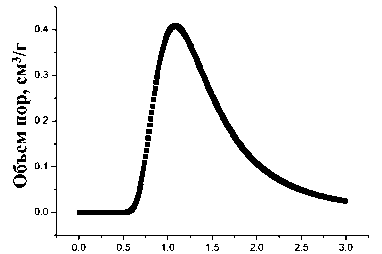
Радиус пор, нм
Рис. 2. Распределение пор композита по размерам, рассчитанное с использованием метода Дубинина – Астахова
Данные анализа КОЛС по методике [10]
|
T 1 , мин. |
T 2 , мин. |
MA, ОП |
ФК, % |
ИК, % |
|
|
Свободный ТАП (стандарт) |
1,6 |
2,4 |
0,44 |
100 |
100 |
|
Промывочный раствор |
3 |
0 |
0,47 |
0 |
0 |
|
Иммобилизованный ТАП |
7,5 |
15,9 |
0,54 |
115 |
882 |
|
Иммобилизованный ТАП после раствора Рингера |
7,6 |
16,9 |
0,55 |
119 |
883 |
Перед испытаниями были поставлены три вопроса: способен ли иммобилизованный фермент растворить тромб? Каковы параметры лизиса по сравнению со свободным ферментом? Каков механизм тромболизиса при использовании гетерогенной системы?
Во-первых, на рис. 3 показано, что тромболизис с иммобилизованным ферментом возможен. Данные фибринолитической активности представлены в таблице. Из рис. 3 видно, что время тромбообразования после добавления тромбина составляет около 2 мин. Если тромболизис со свободным ферментом начинается сразу после образования сгустка при достижении максимального поглощения, то промывочный раствор (см. рис. 3) показывает лишь незначительную активность, сравнимую с неферментативным поведением.
Добавление фермента в матрицу приводит к ингибированию фибринолизиса (см. рис. 3). Наблюдается 4,7-кратное (T 1 ) увеличение времени сохранения максимального поглощения. Эта величина характеризует процесс накопления активного плазмина, поскольку лизис сгустка начинается только после того, как концентрация активного фермента достигла определенного значения [6]. Индекс коагуляции также превышает нормальное значение в 8,8 раза. Таким образом, уменьшение скорости активации плазминогена обусловлено диффузией плазминогена через пористую структуру матрицы для достижения каталитических реакционных центров, способных к формированию активаторного комплекса, который постепенно образуется в ходе реакции. Это также подтверждается значительным повышением ФК (на 15 % больше, чем свободный ТАП), что объясняется как уменьшением скорости образования комплекса ТАП – плазминоген, так и снижением количества активированного плазмина. Возможно, в этот период процесс формирования активированного плазминогена начинает ограничиваться количеством функционально активного ТАП и диффузией плазминогена к каталитическим центрам. Необходимо отметить, что в ходе испытания композита в концентрированном растворе Рингера активность практически не изменялась. После 30 дней испытаний активность иммобилизованного ТАП снизилась по сравнению с начальным состоянием лишь на 2,5 %.
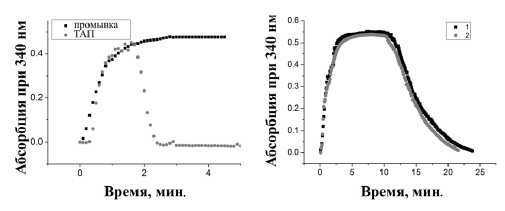
Рис. 3. КОЛС свободного ТАП и промывочного раствора по сравнению с иммобилизованным ТАП (1 – после, 2 – до опыта в растворе Рингера)
Принимая во внимание то, что размер пор для композита составляет около 2 нм и эта величина обеспечивает необходимые условия для захвата фермента внутрь пористой матрицы бемита, можно предположить, что обеспечивать доставку крупных молекул плазминогена к активным центрам фермента будет крайне сложно. Тем не менее наблюдаемая активность иммобилизованного фермента указывает на наличие пор бимодального типа. Чтобы убедиться в этом, образец был исследован методами СЭМ и ПЭМ (рис. 4).
По результатам микроскопии видно, что образец состоит из бемитовых стержней размером около 2 × 12 нм, которые довольно плотно упакованы. В самом деле размер пор в материале не превышает 2–4 нм (рис. 4б), что хорошо согласуется с результатами физической адсорбции азота (см. рис. 2). В то же время отчетливо наблюдается присутствие пор гораздо большего размера (> 20 нм, см. рис. 4а), которые могут обеспечить свободное перемещение больших молекул плазминогена. Таким образом, структура синтезированного композита напоминает муравейник, где каналы большего диаметра постепенно переходят в поры меньшего размера. Так как высвобождение фермента из матрицы практически не наблюдается, разумно предположить, что основная его часть контактирует с внешней средой через поры меньшего диаметра.
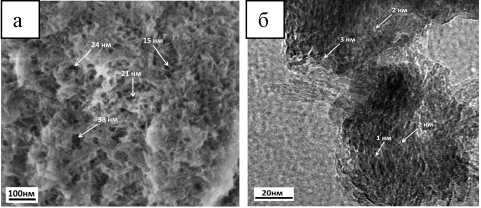
Рис. 4. Изображения СЭМ (a) и ПЭМ (б) для композита. Показано наличие бимодальной мезопористой структуры
ДАЛЬНЕЙШЕЕ ОБСУЖДЕНИЕ И ВЫВОДЫ
В качестве заключения мы хотели бы предложить механизм тромболизиса с использованием иммобилизированного тканевого активатора плазминогена (рис. 5).
Плазмин является основной фибринолитической протеазой (см. рис. 5). Плазминоген (ПГ), циркулирующий в плазме зимоген, может быть преобразован в плазмин с помощью ТАП [4], [6]. Фибрин, главный субстрат плазмина, регулирует собственную деградацию путем связывания на своей поверхности ПГ и ТАП, локализуя и усиливая таким образом образование плазмина. В то время как ТАП является слабым активатором ПГ в отсутствие фибрина, его каталитическая эффективность в активации ПГ усиливается по крайней мере на два порядка в присутствии фибрина [9]. Сродство между ТАП и ПГ является низким в отсутствие фибрина, но значительно увеличи-
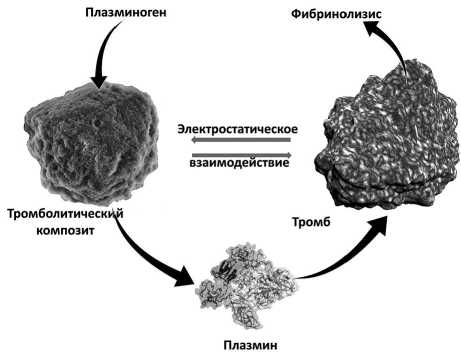
Рис. 5. Схема работы фибринолитической системы с иммобилизированным тканевым активатором плазминогена вается в его присутствии. В нашем случае роль фибрина в улучшении сродства между ТАП и ПГ берет на себя матрица оксида алюминия, которая соединяет их в одной поре. Необходимое электростатическое взаимодействие между отрицательно заряженным фибрином и оксидом алюминия (дзета-потенциал для синтезированного оксида алюминия составляет 32 мВ) является движущей силой для соединения двух компонентов. Чтобы обеспечить образование плазмина, плазмино- ген должен проникнуть в бемитовую матрицу, содержащую активный ТАП, чего можно легко достичь при наличии пор большего диаметра (около 20 нм). При входе в такой канал плазминоген начинает гидролизоваться функциональными группами ТАП, расположенными в порах меньшего диаметра (менее 4 нм).
Поскольку свободный ТАП может легко ингибироваться [3], еще одной функцией матрицы оксида алюминия является защита ТАП от нежелательного разложения и ингибирования. Золь-гель матрицы, как известно, являются идеальными кандидатами для осуществления функции защиты от температуры, химических веществ, растворителей и т. д. [7], [11].
После своего образования плазмин расщепляет фибрин, давая растворимые продукты разложения и карбоксильные концевые остатки лизина. Вследствие диффузионных ограничений образованный плазмин может быть подвержен действию ингибиторов только после выделения из матрицы, что приводит к значительному увеличению времени полураспада плазмина.
Авторы благодарны Центру нанотехнологий в Еврейском университете (г. Иерусалим, Израиль) за помощь в проведении экспериментов сканирующей и просвечивающей электронной микроскопии.
IMMOBILISATION OF PLASMINOGEN ACTIVATOR WITHIN POROUS ALUMINA MATRIX FOR CREATION OF NEW THROMBOLYTIC MATERIALS
Список литературы Иммобилизация активатора плазминогена в пористую матрицу оксида алюминия для создания новых тромболитических препаратов
- Avnir D., Braun S., Lev O., Ottolenghi M. Enzymes and Other Proteins Entrapped in Sol-Gel Materials. Chem. Mater. 1994. № 6. Р 1605-1614.
- Avnir D., Coradin T., Lev O., Livage J. Recent bio-applications of sol-gel materials. J. Mater. Chem. 2006. № 16. Р 1013-1030.
- Bangert K., Johnsen A. H., Christensen U., Thorsen S. Different N-terminal forms of a2-plasmin inhibitor in human plasma. Biochem. 1993. № 291. Р. 623-625.
- Bennett W., Paoni N., Key t B., B ot stein D., Jones A. J. S., Presta L., Wurm F. M., Zoller M. J. High resolution analysis of functional determinants on human tissue-type plasminogen activator. J. Biol. Chem. 1991. № 266. P. 5191-5201.
- B i F., Zhang J., Su Y., Tang Y. C., and Liu J. N. Chemical conjugation of urokinase to magnetic nanoparticles for targeted thrombolysis. Biomaterials. 2009. № 30. P. 5125-5130.
- Cesarman-Maus G., Hajjar K. A. Molecular mechanisms of fibrinolysis. British Journal of Haematology. 2005. № 129. Р 307-321.
- Frenkel-Mullerad H., Avnir D. Sol-gel materials as efficient enzyme protectors: preserving the activity of phosphatases under extreme ph conditions. J. Am. Chem. Soc. 2005. № 127. Р 8077-8081.
- Hacke W., Kaste M., Fieschi C., Kummer R. V., Davalos A., Meier D., Larrue V., Bluhmki E., Davis S., and Donnan G. Randomised double-blind placebo-controlled trial of thrombolytic therapy with intravenous alteplase in acute ischaemic stroke. Second European-Australasian Acute Stroke Study Investigators. Lancet. 1998. № 352. Р 1245-1251.
- L ij nen H. R., Collen D. Strategies for the improvement of thrombolytic agents. Thromb Haemostas. 1991. № 66. P. 88-110.
- Goldenberg N. A., Hathaway W. E., Jacobson L., Manco-Johnson M. J. A new global assay of coagulation and fibrinolysis. Thrombosis Research. 2005. № 116. Р 345-356.
- Rutenberg A., Vinogradov V., Avnir D. Synthesis and enhanced thermal stability of albumins@alumina: towards injectable sol-gel materials. Chem. Commun. 2013. № 49. Р. 5636-5638.
- Van der Worp H. B., Gijn J. van. Acute ischemic stroke. New Eng. J. Med. 2007. № 357. Р 572-579.
- Vinogradov V., Avnir D. Exceptional thermal stability of therapeutical enzymes entrapped in alumina sol-gel matrices. J. Mater. Chem. B. 2014. № 2. Р 2868-2873.
- Vinogradov A. V., Ermakova A. V., Butman M. F., Hey-Hawkins E., Vinogradov V. V. A facile sol-gel synthesis of impurity-free nanocrystalline titania. Phys. Chem. Chem. Phys. 2014. № 16. 10614-10619.
- Wang M., Zhang J., Yuan Z., Yang W., Wu Q., Gu H. Targeted thrombolysis by using of magnetic mesoporous silica nanoparticles. J. Biomed. Nanotechnol. 2012. № 8. P. 624-632.


