Иммобилизация клеток нитрилгидролизующих бактерий Rhodococcus erythropolis 4-1 и Alcaligenes faecalis 2 с использованием термотропных и ионотропных гелей
Автор: Мочалова Елена Михайловна, Максимова Юлия Геннадьевна
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 1, 2020 года.
Бесплатный доступ
Клетки амидазосодержащих бактерий штаммов Rhodococcus erythropolis 4-1 и Alcaligenes faecalis 2 были иммобилизованы с использованием таких носителей, как альгинат бария, агароза, хитозан и к-каррагинан. Цель работы заключалась в изучении влияния методов иммобилизации бактериальных клеток на операционную стабильность биокатализатора. Определено, что наилучшим материалом носителя для стабильной работы биокатализатора является агароза. Наибольшее количество акриловой кислоты было получено при многоцикловой трансформации акриламида иммобилизованными клетками A. faecalis 2.
Амидазная активность, агароза, альгинат бария, хитозан, биокатализатор, биотрансформация, иммобилизация, нитрилгидролизующие бактерии
Короткий адрес: https://sciup.org/147229632
IDR: 147229632 | УДК: 579.24 | DOI: 10.17072/1994-9952-2020-1-26-32
Immobilization of cells of nitrile-hydrolyzing bacteria Rhodococcus erythropolis 4-1 and Alcaligenes faecalis 2 using thermotropic and ionotropic gels
Cells of amidase containing bacteria of Rhodococcus erythropolis 4-1 and Alcaligenes faecalis 2 were immobilized using carriers such as barium alginate, agarose, chitosan and к-carrageenan. The aim of the work was to study the effect of bacterial cell immobilization methods on the operational stability of a biocatalyst. It has been determined that the best carrier for the stable operation of the biocatalyst was agarose. The highest amount of acrylic acid was obtained during multi-cycle transformation of acrylamide by immobilized A. faecalis 2 cells.
Текст научной статьи Иммобилизация клеток нитрилгидролизующих бактерий Rhodococcus erythropolis 4-1 и Alcaligenes faecalis 2 с использованием термотропных и ионотропных гелей
Использование нитрилгидролизующих бактерий и их ферментов является одним из приоритетных направлений биотехнологии для получения разнообразных амидов и карбоновых кислот из соответствующих нитрилов [Sharma et al., 2009]. К примерам такого производственного ферментативного синтеза можно отнести: биокаталитическое получение акриламида, никотинамида, акрилата аммония, акриловой кислоты [Tepe, 2016]. Биотрансформация нитрилов основана на использовании селекционированных штаммов бактерий, обладающих высокой активностью таких ферментов, как нитрилгидратазы, амидазы и нитрилазы [Полтавская и др., 2004, Дебабов, Яненко, 2011, Махсумханов и др., 2015, Kamal et al., 2011]. Биокаталитический метод получения коммер- чески значимых органических соединений, в отличие от традиционного химического, обладает мягкими условиями проведения процесса, экологической безопасностью и имеет исключительно высокую избирательность действия.
Амидазы широко распространены среди бактерий, грибов, растений и животных. Интерес исследователей к этим ферментам связан с их энан-тиоселективными свойствами, а также перспективой использования в биокатализе [Дебабов, Янен-ко, 2011, Павлова, Неустроева, Максимов, 2011]. Продукция амидаз обнаружена как у представителей бактерий родов Arthrobacter , Agrobacterium , Alcaligenes , Acinetobacter , Brevibacterium , Bacillus , Burkholderia , Delftia , Enterobacter , Enterococcus ,
Escherichia , Helicobacter , Microbacterium , Morax-ella , Nocardia , Klebsiella , Pseudomonas , Rhodococ-cus , так и среди грибов родов Aspergillus , Candida , Kluyvera , Kluyveromyces [Silva et al., 2009; Duda-Chodak et al., 2016].
Для повышения эффективности процессов биотрансформации используют методы иммобилизации каталитически активных клеток бактерий. Это позволяет стабилизировать их ферментативную активность, повысить устойчивость к токсичным субстратам, продлить использование биокатализатора по сравнению с суспендированной биомассой и увеличить выход конечного продукта. Иммоби-лизационные технологии часто обладают стабильностью и селективностью; также возможно повторное использование биокатализаторов [Eş et al., 2015], что, в свою очередь, снижает стоимость процесса. Поэтому большинство отраслей промышленности, применяющих методы зеленой химии, используют иммобилизованные клетки в производстве химических веществ [Sjahrir et al., 2016].
Помимо получения разнообразных соединений в результате ферментативного синтеза, иммобилизованные бактериальные клетки, обладающие высокой амидазной активностью, могут быть использованы в качестве биоселектирующего элемента биосенсора. Использование жизнеспособных целых клеток имеет свои преимущества, так как живые клетки являются самоподдерживающейся системой; они метаболизируют всевозможные химические соединения, в результате чего образуются различные конечные продукты, такие как аммиак, диоксид углерода, кислоты и т.д., которые можно контролировать с помощью различных преобразователей сигнала [Сазыкина и др., 2015], при этом не требуется дорогостоящее и трудозатратное выделение ферментов.
Благодаря селективности, надежности, возможности повторного использования и легкой интеграции иммобилизованных клеток в портативные устройства, биодатчики являются отличным аналитическим инструментом [Fleming, 2004].
Процесс иммобилизации включает в себя несколько этапов: от выбора материала носителя до метода с подходящими биокатализаторами.
Основные методы клеточной иммобилизации подразделяются на адсорбцию, ковалентную сшивку с носителями, включение в структуру гелей и инкапсуляцию [Michelini, Roda, 2012]. Каждый из вышеперечисленных способов имеет свои преимущества и недостатки и может быть оптимизирован для конкретных биотехнологических целей.
Целью настоящей работы явилось изучение влияния методов иммобилизации клеток бактерий R. erythropolis 4-1 и A. faecalis 2, обладающих амидазной активностью, и используемых носите- лей, на операционную стабильность иммобилизованного биокатализатора.
Материалы и методы исследования
Бактериальные штаммы, условия культивирования и подготовка биомассы
Штаммы бактерий R. erythropolis 4-1 и A. faecalis 2, выделенные из почвенных образцов и активного ила биологических очистных сооружений г. Перми соответственно [Демаков и др., 2015], культивировали на минимальной солевой среде следующего состава (г/л): КН 2 РО 4 – 1.0; K 2 HPO 4 ×3H 2 O – 3.7; NaCl – 0.5; MgSO 4 ×7H 2 O – 0.5; FeSO 4 ×7H 2 O – 0.005; CoCl 2 ×6H 2 O – 0.01, рН 7.2 ± 0.2. В качестве источника углерода для родококков использовали глюкозу в концентрации 0.1%, а источником азота служил ацетонитрил в концентрации 0.05%. Для штамма A. faecalis 2 единственным источником углерода и азота был 0.1 М ацетамид.
Культивирование проводили в конических колбах объемом 1000 мл в 400 мл минеральной среды в течение 7 дней на шейкере со скоростью вращения 120 об/мин при температуре 30°С.
Биомассу концентрировали центрифугированием в течение 20 мин при 4500 g на центрифуге 5804 R («Eppendorf», Германия), отмывали однократно от среды культивирования калийфосфатным буфером (рН 7.2 ± 0.2), центрифугировали повторно, разводили в свежем буфере и использовали для иммобилизации.
Иммобилизация клеток в структуре агарозного геля
Раствор агарозы в концентрации 4% нагревали до температуры кипения. После охлаждения до 40°C смешивали 30 мл агарозы с 10 мл бактериальной суспензии и 10 мл смеси помещали в чашку Петри. После застывания гель измельчали механически, размер гранул составлял 1–2 мм2.
Иммобилизация клеток в структуре геля альгината бария
Альгинат натрия растворяли в кипящей воде в концентрации 2% и автоклавировали при 121°C в течение 15 мин. После охлаждения до 40°C к 20 мл альгината натрия добавляли 10 мл бактериальной суспензии. Полученную смесь объемом 3 мл продавливали через шприц для подкожных инъекций в 10 мл холодного 0.1 М раствора BaCl 2 . Гранулы диаметром 2 мм ресуспендировали в свежем BaCl 2 в течение 24 ч. при температуре 4–6°C. После гранулы отмывали дистиллированной водой.
Иммобилизация клеток в структуре геля к-каррагинана
Растворенный в горячей воде κ-каррагинан в концентрации 2% автоклавировали при 121°C в течение 15 мин. После охлаждения до 40°C к 50 мл κ-каррагинана добавляли 25 мл бактериальной суспензии. Полученную смесь сразу продавливали через шприц объемом 5 мл в 20 мл охлажденного до 4–6°C 0.1 М раствора KCl. Образовавшиеся гранулы оставляли для затвердения в растворе KCl в течение 20 мин. Затем гранулы отмывали дистиллированной водой.
Иммобилизация клеток на неактивированном и активированном хитозане
Раствор хитозана средней вязкости (2%) в 2%-ной уксусной кислоте нагревали до полного растворения и оставляли на несколько суток при комнатной температуре для удаления пузырьков воздуха из раствора. Затем накапывали раствор через шприц объемом 5 мл для подкожных инъекций в 20 мл 1 М раствора KOH. Гранулы оставляли на 1 ч. в щелочном растворе для затвердения, затем отмывали большим количеством 0.1 М фосфатного буфера (рН 7.2 ± 0.2) до нейтральной реакции промывных вод (pH 6.5–7.0). Полученные гранулы использовали для адсорбции и ковалентной сшивки клеток. Для активации гранул добавляли 10 мл 0.1%-ного раствора глутарового альдегида и оставляли на 15 мин при комнатной температуре, после чего отмывали 20–30 мл дистиллированной воды. Гранулы хитозана смешивали с 10 мл бактериальной суспензии, перемешивали в течение 40 мин на шейкере со скоростью вращения 120 об/мин при 30°С, отфильтровывали несвязавшиеся клетки через бумажный фильтр (марки “белая лента”) и промывали иммобилизованный биокатализатор 20 мл дистиллированной воды.
Массу связавшихся с хитозаном клеток определяли по разности оптической плотности растворов до и после контакта с носителем и вычисляли по формуле: A = m×V×(D исх – D фильтр ) / D исх , где А – масса связанных клеток, мг; m – концентрация клеток в суспензии до иммобилизации, мг/мл; V – объем суспензии, из которого иммобилизовали клетки, мл; D исх – оптическая плотность клеточной суспензии до иммобилизации, при длине волны 540 нм; D фильтр – оптическая плотность клеточной суспензии после иммобилизации.
Операционная стабильность иммобилизованного биокатализатора
Операционную стабильность биокатализаторов на основе иммобилизованных клеток R. erythropolis 4-1 и A. faecalis 2 оценивали по количеству акриловой кислоты при последовательном проведении полной конверсии 100 мМ раствора акриламида, вносимого в каждом цикле в реакционную среду. Время полного цикла составляло 24 ч. Реакцию проводили в 10–20 мл калийфосфатного буфера, рН 7.2 ± 0.2, при 30°С, останавливали, добавляя в 1 мл пробы 50 мкл концентрированной HCl, центрифугировали 10 мин. при 13 000 об/мин и определяли концентрацию образовавшейся акриловой кислоты методом ВЭЖХ на хроматографе LC-10 («Shimadzu», Япония) с колонкой Synergi 4u Hydro–RP 80A (250 × 4.6 мм). В качестве подвижной фазы использовали 25 мМ NaH2PO4, со скоростью потока 0.75 мл/мин при 25°C, детекцию проводили при длине волны 200 нм [Максимова и др., 2015]. После проведения реакционного цикла биокатализаторы отфильтровывали через бумажный фильтр (марки “белая лента”), отмывали калий-фосфатным буфером (рН 7.2 ± 0.2) и использовали в следующем цикле.
Статистическая обработка результатов выполнена с помощью пакета программ Microsoft Excel 2013. Результаты представлены как среднее значение не менее чем трех независимых экспериментов ± стандартная ошибка среднего (M±m, n=3).
Результаты и их обсуждение
Нами была проведена иммобилизация клеток бактерий штаммов R. erythropolis 4-1 и A. faecalis 2 с использованием таких органических носителей, как агароза, альгинат бария, хитозан и κ-каррагинан. Гели агарозы и κ-каррагинана относятся к термотропным, это означает, что золь-гель переход этих полимеров происходит при изменении температуры, альгината и хитозана – к ионотропным: смена агрегатного состояния происходит при замене катиона в соли или изменении рН среды. На бактериальные клетки может оказывать неблагоприятное влияние повышенная температура, которая требуется для приготовления смеси геля с клетками, или определенные ионы могут быть токсичными для клеток. Полученные гели с включенными клетками могут обладать различной механической прочностью. Поэтому было необходимо протестировать полученный иммобилизованный биокатализатор в процессе долговременного использования.
Биокатализаторы, приготовленные на основе клеток R. erythropolis 4-1 и A. faecalis 2, включенных в структуру κ-каррагинана, оказались менее стабильными по сравнению с другими. После проведения 1‒3 циклов трансформации субстрата гранулы подверглись растворению в реакционной среде. Можно предположить, что это связано с физико-химическими характеристиками носителя и химической природой реакционной среды.
Определено количество образующейся акриловой кислоты при проведении последовательных циклов трансформации субстрата биокатализаторами на основе иммобилизованных клеток R. erythropolis 4-1 и A. faecalis 2. Показано, что количество акриловой кислоты при трансформации акриламида биокатализаторами на основе иммобилизованных клеток R. erythropolis 4-1 после 1 цикла снижается и остается примерно на одном уровне на протяжении всех циклов (рис. 1‒4). При этом использование агарозы в качестве носителя оказалось наилучшим по сравнению с другими типами матриц, так как не наблюдается потеря клеток в реакционной среде в результате повторного использования.
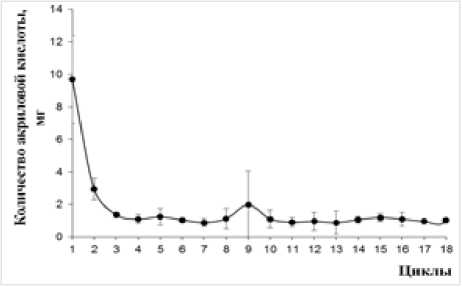
Рис. 1 . Операционная стабильность биокатализатора на основе клеток R. erythropolis 4-1, иммобилизованных в структуре геля альгината бария
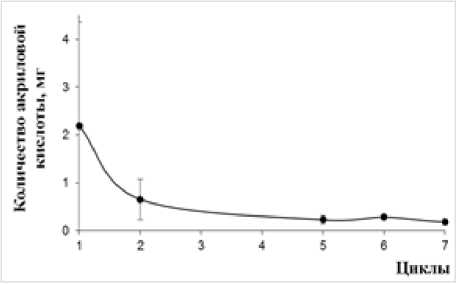
Рис. 2 . Операционная стабильность биокатализатора на основе клеток R. erythropolis 4-1, иммобилизованных на активированном хитозане
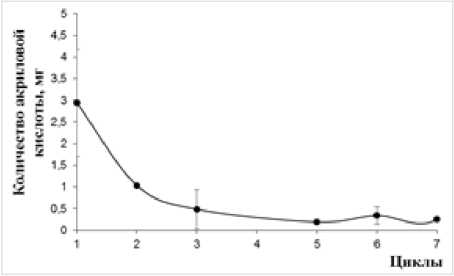
Рис. 3 . Операционная стабильность биокатализатора на основе клеток R. erythropolis 4-1, иммобилизованных на неактивированном хитозане
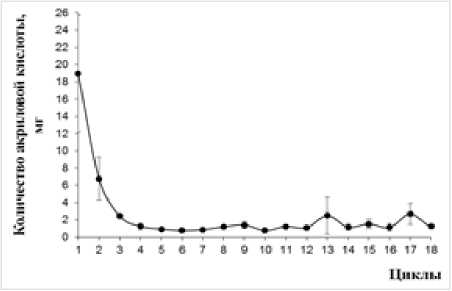
Рис. 4 . Операционная стабильность биокатализатора на основе клеток R. erythropolis 4-1, иммобилизованных в структуре геля агарозы
Биокатализаторы на основе клеток A. faecalis 2, иммобилизованных в структуру геля альгината бария и агарозы, оказались наиболее стабильными по сравнению с клетками, иммобилизованными на активированном и неактивированном хитозане. Показано, что наибольшее количество акриловой кислоты наблюдается при трансформации акриламида биокатализатором на основе альгината бария и составляет 70–100 мг (рис. 5) в отличие от биокатализатора, иммобилизованного в структуре агарозного геля (55–75 мг) (рис. 6). Однако гранулы альгината со временем теряли механическую прочность и разрушались при проведении последовательных циклов трансформации акриламида, чего не наблюдалось при использовании агарозного геля.
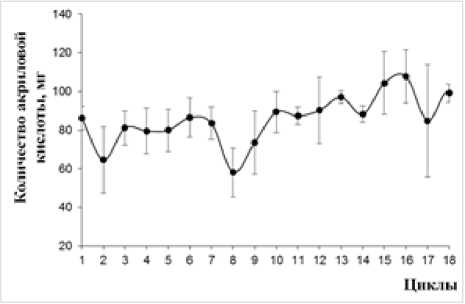
Рис. 5 . Операционная стабильность биокатализатора на основе клеток A. faecalis 2, иммобилизованных в структуре геля альгината бария
Снижение количества образующейся кислоты наблюдали также при трансформации акриламида биокатализатором на основе клеток A. faecalis 2, иммобилизованных на хитозане (рис. 7, 8), что может быть связано с десорбцией клеток и их вымыванием из реакционной среды в результате многократного использования.
Сравнение полученных иммобилизованных биокатализаторов по нескольким параметрам, а именно по общему количеству образованной кис- лоты, сохранению амидазной активности при долговременном использовании и механической прочности гранул, позволяет сделать выбор в пользу клеток A. faecalis 2, включенных в структуру геля агарозы.
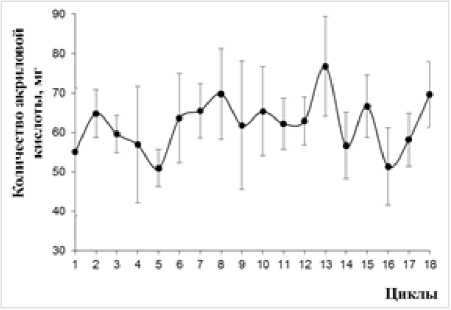
Рис. 6 . Операционная стабильность биокатализатора на основе клеток A. faecalis 2, иммобилизованных в структуре геля агарозы
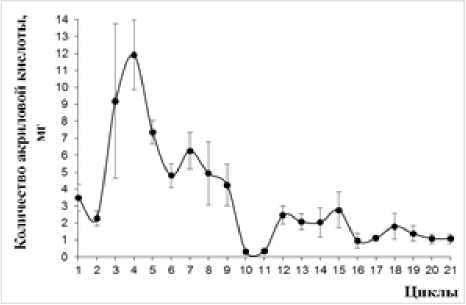
Рис. 7 . Операционная стабильность биокатализатора на основе клеток A. faecalis 2, иммобилизованных на активированном хитозане
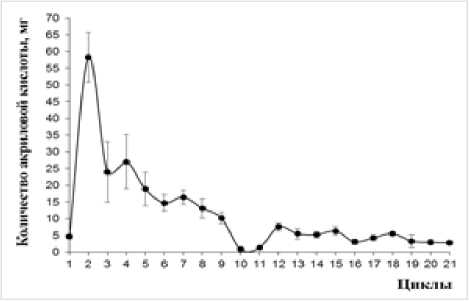
Рис. 8 . Операционная стабильность биокатализатора на основе клеток A. faecalis 2, иммобилизованных на неактивированном
хитозане
Ранее нами было показано, что включение клеток Pseudomanas fluorescens C2, содержащих нит-рилазу, в структуру геля агарозы позволяет получить стабильный биокатализатор, активность ко-
торого при трансформации акрилонитрила в акриловую кислоту не снижается в течение 30 циклов [Максимов, Максимова, Демаков, 2009]. Известны другие примеры успешного использования амидазосодержащих клеток, иммобилизованных в структуре гелей, для долговременной многоцикловой конверсии субстрата. Так, клетки Delftia tsuruha-tensis CCTCC M 205114 в альгинате кальция в течение 8 последовательных циклов сохраняли 83,1% активности при энантиоселективном гидролизе (R)-2, 2-диметилциклопропан карбоксамида [Wang et al., 2010], а при иммобилизации клеток Rhodococcus rhodochrous NHB-2 в агаре и полиакриламиде их амидазная активность увеличивалась в течение 5 циклов и оставалась затем неизменной в течение 10 циклов [Chand et al., 2004]. Следовательно, несмотря на определенные недостатки такого метода иммобилизации клеток, как включение в структуру гелей (лимитирование процессов диффузии, механическая неустойчивость гранул, снижение ферментативной активности), этот метод может быть успешным для некоторых биокатали-тических процессов и иммобилизации клеток в биоселектирующем элементе биосенсора.
Заключение
Таким образом, наибольшее количество акриловой кислоты в настоящем исследовании было получено при использовании иммобилизованных клеток A. faecalis 2. Включение бактериальных клеток в структуру агарозы позволяет получить достаточно стабильный биокатализатор, амидазная активность которого не снижается на протяжении 18 циклов, а также обеспечивает высокую долговечность захваченных клеток при повторном использовании.
Следовательно, иммобилизованные в структуре агарозного геля клетки A. faecalis 2, обладающие амидазной активностью, могут иметь перспективу использования как в биокаталитических процессах, так и для биодетекции акриламида в составе биоселектирующего элемента биосенсора.
Работа выполнена в рамках государственного задания по теме «Поиск и селекция биотехнологически перспективных микроорганизмов и создание иммунохимических диагностических систем», регистрационный номер НИОКТР АААА-А19-119112290010-7.
Список литературы Иммобилизация клеток нитрилгидролизующих бактерий Rhodococcus erythropolis 4-1 и Alcaligenes faecalis 2 с использованием термотропных и ионотропных гелей
- Дебабов В.Г., Яненко А.С. Биокаталитический гидролиз нитрилов // Обзорный журнал по химии. 2011. Т. 1, № 4. С. 376-394.
- Демаков В.А. и др. Бактерии активного ила биологических очистных сооружений, трансформирующие цианопиридины и амиды пиридинкар-боновых кислот // Микробиология. 2015. Т. 84, № 3. С. 369-378.
- Максимова Ю.Г. и др. Трансформация амидов ад-гезированными клетками родококков, обладающими амидазной активностью // Прикладная биохимия и микробиология. 2015. Т. 51, № 1. С. 53-58.
- Максимов А.Ю., Максимова Ю.Г., Демаков В.А. Гидролиз акрилонитрила клетками нитрилути-лизирующих бактерий Rhodococcus ruber gt1 и Pseudomonas fluorescens C2, иммобилизованными в структуре геля агарозы // Вестник Пермского ун-та. 2009. Вып. 10(36) Биология. С. 115-118.
- Махсумханов А.А. и др. Скрининг коллекционных штаммов бактерий по нитрилгидратазной активности // Биотехнология: состояние и перспективы развития. 2015. С. 375-377.
- Павлова Ю.А., Неустроева А.Н., Максимов А.Ю. Сравнительный анализ последовательностей генов амидаз почвенных актинобактерий рода Rhodococcus // Известия Самарского научного центра Российской академии наук. 2011. Т. 13, № 5(3). С. 272-276.
- Полтавская С.В. и др. Разработка и внедрение биокаталитического способа получения акриловой кислоты. I. Выделение штамма Alcaligenes denitrificans, трансформирующего акрилонит-рил в акрилат аммония. Оптимизация среды культивирования // Биотехнология. 2004. № 1. С. 62-70.
- Сазыкина М.А., Мирина Е.А., Сазыкин И.С. Использование биосенсоров для детекции антропогенного загрязнения природных вод // Вода: Химия и Экология. 2015. № 10. С. 64-74.
- Chand D. et al. Treatment of simulated wastewater containing toxic amides by immobilized Rhodococcus rhodochrous NHB-2 using a highly compact 5-stage plug flow reactor // World J. Microbiol. Biotechnol. 2004. Vol. 20. P. 679-686.
- Duda-Chodak A. et al. A review of the interactions between acrylamide, microorganisms and food components // Food Funct. 2016. Vol. 7(3). P. 1282-1295.
- E§ I., Vieira J.D.G., Amaral A.C. Principles, techniques, and applications of biocatalyst immobilization for industrial application // Appl. Microbiol. Biotechnol. 2015. Vol. 99(5). P. 2065-2082.
- Fleming D.L. Evaluating bacterial cell immobilization matrices for use in a biosensor. 2004.
- Kamal A. et al. Bioconversion of acrylonitrile to acrylic acid from Rhodococcus ruber AKSH-84 // J. Microbiol. Biotechnol. 2011. Vol. 21(1). P. 37-42.
- Michelini E., Roda A. Staying alive: new perspectives on cell immobilization for biosensing purposes // Anal. Bioanal. Chem. 2012. Vol. 402(5). P. 1785-1797.
- Sharma M., Sharma N.N., Bhalla T.C. Amidases: versatile enzymes in nature // Reviews in Environmental Science and Bio/Technology. 2009. Vol. 8. P. 343-366.
- Sjahrir F. et al. Biotransformation of acrylonitrile using immobilized cells of Rhodococcus UKMP-5M as biocatalyst // Indian Journal of Fundamental and Applied Life Sciences. 2016. Vol. 6(1). P. 58-67.
- Silva N. et al. Biosensor for acrylamide based on an ion-selective electrode using whole cells of Pseudomonas aeruginosa containing amidase activity // Biocatalysis and Biotransformation. 2009. Vol. 27(2). P. 143-151.
- Tepe Y. Acrylamide in surface and drinking water // Acrylamide in Food. 2016. P. 275-293.
- Wang Y.S. et al. Enantioselective hydrolysis of (R)-2,2-dimethylcyclopropane carboxamide by immobilized cells of an R-amidase-producing bacterium, Delftia tsuruhatensis CCTCC M 205114, on an alginate capsule carrier // J. Ind. Microbiol. Bi-otechnol. 2010. Vol. 37. P. 503-510.


