Иммобилизирующий интерстициальный фиброз сердца
Автор: Шевченко Ю.Л.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Редакционные статьи
Статья в выпуске: 2 т.17, 2022 года.
Бесплатный доступ
В основе сердечной недостаточности, как правило, лежит повреждение кардиомиоцитов. При этом наиболее частой причиной дисфункции миокарда в целом является ИБС, различные воспалительные процессы мышцы, чрезмерные ее физические перегрузки, в том числе при приобретенных и врожденных пороках сердца и прочее. Однако нередко встречаются больные с хронической сердечной недостаточностью, у которых перечисленные причины отсутствуют и не подтверждаются ни инструментальными, ни лабораторными исследованиями. Лечение таких больных, как правило, не эффективно. Многолетняя клиническая практика, многочисленные научно-экспериментальные исследования, позволили предположить, что причиной подобной дисфункции миокарда является иммобилизирующии интерстициальныи фиброз сердца. Заключение. Иммобилизирующий интерстициальный фиброз сердца можно считать самостоятельной патологией и одной из главных причин развития хронической сердечной недостаточности. В основе его лежит процесс изменения соединительнотканного каркаса миокарда, приводящий в итоге к угнетению его работы.
Сердечная недостаточность, иммобилизация, соединительная ткань, интерстициальный фиброз
Короткий адрес: https://sciup.org/140295058
IDR: 140295058 | DOI: 10.25881/20728255_2022_17_2_4
The immobilizing interstitial fibrosis of the heart
Despite the fact that the cause of heart failure is more often cardiomyocyte dysfunction caused by coronary heart disease, inflammatory processes of various etiologies, excessive physical overload, including congenital and acquired heart defects, etc., there is such a group of patients whose etiology remains unclear and there are no obvious signs of myocardial damage according to instrumental and laboratory studies. At the same time, the peculiarity of attempts to treat such patients is the ineffectiveness of heart failure therapy. Long-term clinical practice, numerous scientific and experimental studies have suggested that the cause of such myocardial dysfunction is the immobilizing interstitial fibrosis of the heart. Conclusion. The immobilizing interstitial fibrosis of the heart can be considered an independent pathology and one of the main causes of the development of chronic heart failure. It is based on the process of changing the connective tissue framework of the myocardium, resulting in the suppression of its work.
Текст научной статьи Иммобилизирующий интерстициальный фиброз сердца
Вместе с тем врачу трудно представить недостаточность сердечной деятельности без повреждения собственно миокарда, его анатомо-физиологической структурной единицы — кардиомиоцита. Тем не менее, этот факт существует, но остается вне поля зрения клиницистов и исследователей.
Многолетняя клиническая практика, многочисленные научно-экспериментальные исследования, особенно, макро- и микроморфологические, всесторонний анализ и сопоставление различных выявляемых фактов, позволили предположить, что причиной дисфункции миокарда, когда не определяется иная этиология, объясняющая сердечную недостаточность, с большей вероятностью может быть механический фактор, находящийся за пределами миокардиальных пучков здоровых кардиомиоцитов, но структурно тесно связанный с ними. Таким фактором является межуточная соединительная ткань с измененными физическими свойствами: чрезмерным ее уплотнением, что препятствует нормальному функционированию кардиомиоцитов, т.е. происходит их иммобилизация. Таким образом, речь идет об иммобилизирующем интерстициальном фиброзе сердца как самостоятельной причине сердечной недостаточности.

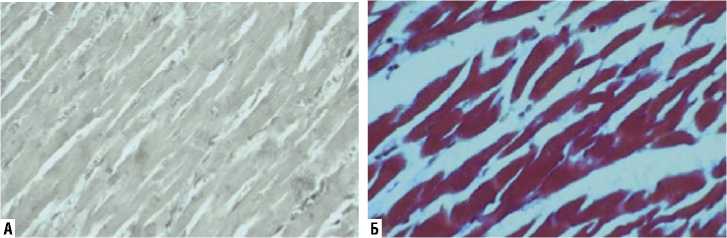
Рис. 1. Нормальный миокард. Кардиомиоциты окружены тонкими прослойками соединительной ткани, А — окраска по Ван-Гизону, увеличение х 400; Б — окраска по Массон, увеличение х 400).
Морфология и физиология интерстициальной соединительной ткани сердца
Кардиомиоциты и их пучки окружены эндомизием и перимизием, основу которых представляют волокнистая соединительная ткань (коллагеновые волокна I, III, VI и XII типов) и межклеточное вещество, содержащее гликопротеины, гликозаминогликаны, протеогликаны, факторы роста и протеазы, которые могут быть активированы после повреждения для репарации [1; 2].
В соединительной ткани миокарда выявляются эндотелиальные, иммунные клетки (макрофаги, тучные и дендритные), клетки стенок сосудов (гладкомышечные и перициты) [3–7]. Кардиальные фибробласты образуют одну из самых больших клеточных популяций в сердце, продуцируют внеклеточный матрикс и регулируют обмен коллагена (Рис. 1) [8; 9].
Благодаря такому рациональному устройству соединительной ткани обеспечивается структурная и функциональная целостность миокарда: формируется каркас и становится возможным беспрепятственное скольжение клеток и их пучков относительно друг друга. Интрамио-кардиальные фасции обеспечивают спиральную «закрутку» сердца при систоле, что увеличивает силу и способствует энергетически экономному и эффективному его сокращению. В здоровом сердце в межклеточном веществе поддерживается баланс между синтезом и деградацией белков, осуществляются механизмы реорганизации этой структуры [10; 11]. Нарушение баланса приводит к неблагоприятным последствиям. Вначале направленный на защиту и восстановление структуры сердца синтез соединительной ткани постепенно приобретает патологический характер: изменяется архитектоника ткани, электрическая проводимость, снижается сократимость миокарда, прогрессирует сердечная недостаточность, это приводит к нарушению межклеточного взаимодействия, к возникновению злокачественных аритмий и внезапной сердечной смерти [7; 12; 13].
В литературе есть сведения о трех различных формах фиброзного поражения сердца по данным гистологических исследований:
«Заместительный» — фиброз, который возникает при инфаркте миокарда, выполняет репаративную функцию. Гибель значительного количества кардиомиоцитов стимули- рует воспаление и последующую активацию фибробластов, что приводит к образованию рубца, который поддерживает структурную целостность стенки сердца, а в случае трансмурального инфаркта — предотвращает катастрофические механические осложнения в виде разрыва [14–17].
«Интерстициальный фиброз» сопровождается расширением эндомизиального и перимизиального пространств, вызванным суммарным накоплением белков внеклеточного матрикса при воспалительных процессах в миокарде и связан с системным склерозом [16].
«Периваскулярный фиброз» может быть результатом длительной активации фиброгенных стимулов и представлять собой первичные повреждающие процессы при гипертонической болезни сердца. Может отражать конверсию фибробластов или фиброгенную активацию эндотелиальных и пристеночных клеток сосудов (Рис. 2) [18–20].
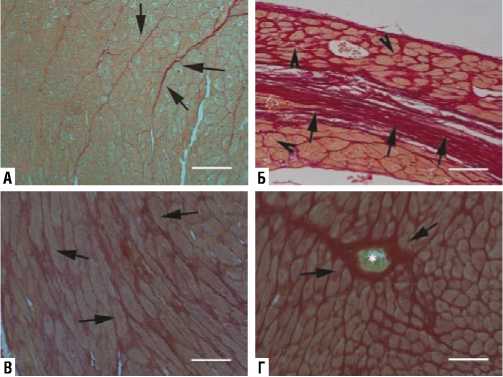
Рис. 2. Гистологические типы сердечного фиброза. На изображениях показаны срезы сердец взрослых мышей, окрашенные пикросириусом красным для маркировки коллагеновых волокон. A — миокард в норме. Каждый кардиомиоцит окружен тонкой сетью эндомизи-ального коллагена, более толстые перимизиальные коллагеновые волокна (указано стрелками) охватывают пучки кардиомиоцитов. Б — заместительный фиброз. Инфаркт миокарда, кардиомиоциты замещаются рубцом. В — интерстициальный фиброз (указано стрелками) на модели перегрузки давлением левого желудочка, вызванной сужением поперечной аорты (7 дней). Г — периваскулярный фиброз (указано стрелками) визуализируется в перегруженном давлением миокарде с большим количеством коллагена, окружающего сосуд (*). Масштабная линейка = 80 мкм [16].
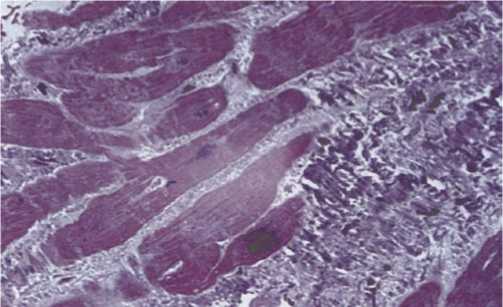
Рис. 3. Вторичная кардиомиопатия при декомпенсированном аортальном пороке. Выраженный кардиосклероз и гипертрофия кардиомиоцитов (окраска гематоксилин и эозин, увеличение х 400) [22].

Перегрузка камер сердца давлением и объемом, сахарный диабет, нарушение липидного обмена при ожирении и многие другие причины влияют на изменения в регуляции синтеза коллагеновых волокон, прогрессирующим интерстициальным и периваскулярным фиброзом, что становится типичным проявлением различных кардиомиопатий (Рис. 3) [21].
Анатомия и физиология иммобилизирующего интерстициального фиброза сердца
Проведенные многочисленные экспериментальные и клинические исследования позволили сделать вывод, что встречается изолированное нарушение структуры эндомизия и перимизия, с тенденцией к уплотнению и постепенному механическому сдавлению кардиомиоцитов — иммобилизации. Причем этот медленный процесс достигает такой степени огрубления, что образу- ется каркас вокруг пучков и отдельных кардиомиоцитов, препятствующий сначала полноценной диастоле, а в дальнейшем и систоле. В этой связи и предложен термин: «иммобилизирующий интерстициальный фиброз сердца». Отличительной особенностью этой отдельной нозологической формы является тотальное, диффузное поражение соединительной ткани (отсутствие локальных зон поражения, характерных для других известных форм фиброза).
Аналогией этого процесса может служить загипсованная для сращения отломков конечность, когда длительная иммобилизация приводит к атрофии мышц и формированию контрактуры. Но более близкой моделью иммобилизации является констриктивный перикардит, при котором через воспаление происходит постепенное уплотнение эпикарда и перикарда с формированием грубого соединительнотканного «каркаса», вплоть до сдавливающего сердце «панциря» («панцирного сердца») (Рис. 4).
Этот принцип правомерно может быть перенесен на клеточный уровень, т.е. на отдельные кардиомиоциты и их пучки: в основе нарушения функции сократительного аппарата при иммобилизирующем интерстициальном фиброзе сердца лежит механическая причина — сдавление клеток и их ассоциаций извне — уплотнение паракардиомиоцитарного каркаса. Следует отметить, что в этой ситуации нарушается очень важный элемент в механике сокращения сердца в целом. Грубый фиброз специфической конструкции интрамиокардиальных фасций препятствует в систолической фазе эффекту спиральной «закрутки», что значительно повышает нагрузку на миокард и изменяет конфигурацию внутрисердечной гемодинамики (Рис. 5, 6).
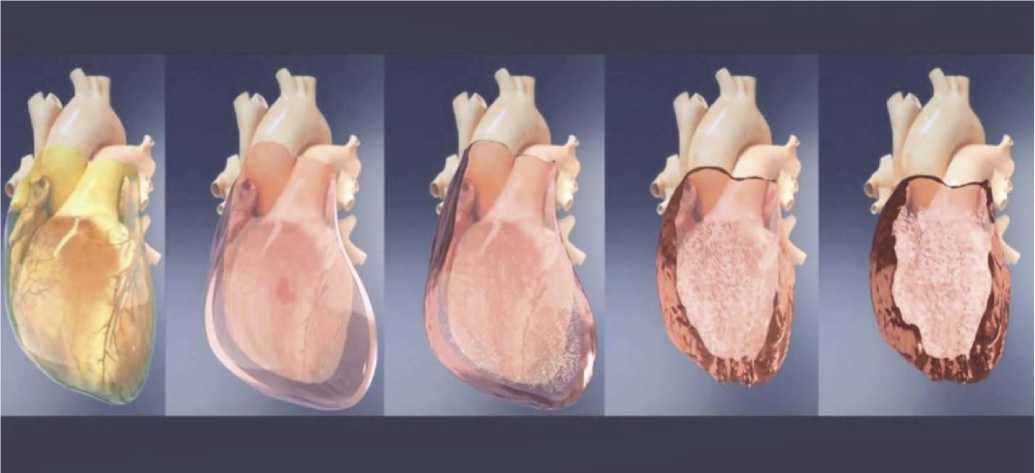
Рис. 4. Процесс формирования «панцирного сердца» при констриктивном перикардите.
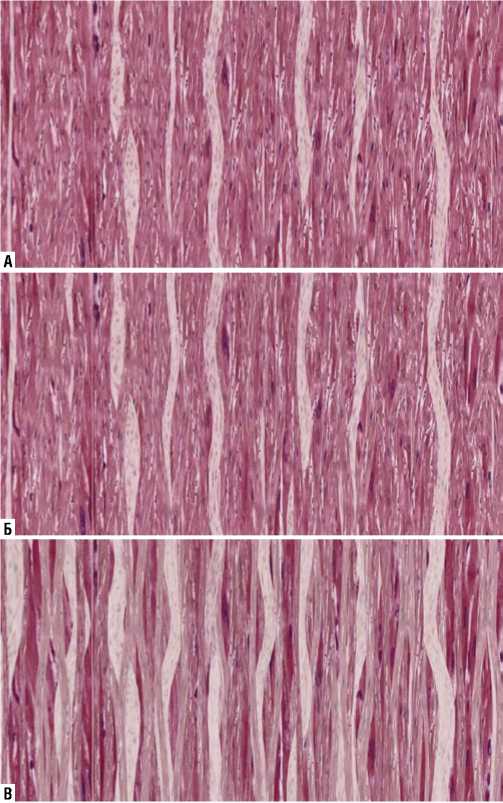
Рис. 5. А–В. Изображение иммобилизации пучков кардиомиоцитов соединительной тканью в разные сроки развития фиброза.
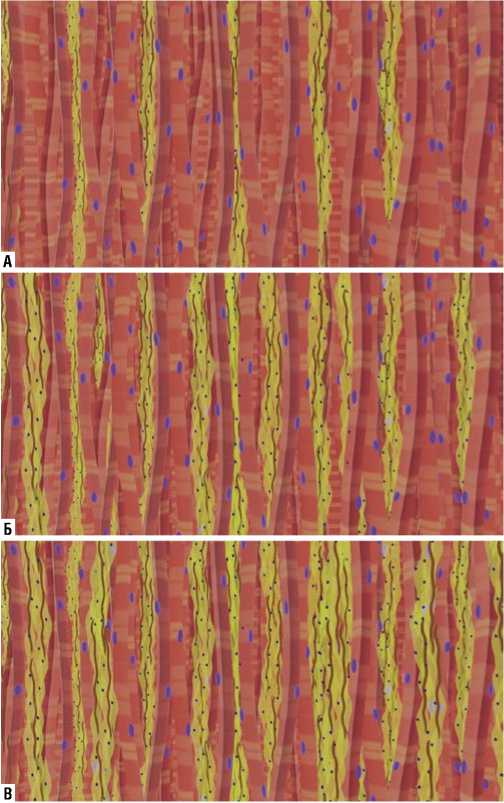
Рис. 6. А–В. Схематическое изображение увеличения количества и плотности соединительной ткани с постепенной иммобилизацией пучков кардиомиоцитов.
В силу различных причин (вирусные заболевания, токсические или лучевые воздействия, а также различной природы аутоиммунные процессы в организме и др.) изменяется молекулярный фенотип соединительной ткани сердца с повышением экспрессии фиброгенных медиаторов, усиливается синтез коллагеновых волокон и нарушается их соотношение, происходит ремоделирование внеклеточного матрикса с формированием сетевидных каркасных структур, окружающих отдельные здоровые кардиомиоциты. Высокая реактивность соединительной ткани способствует ее порой выраженному отеку. При этом в процесс может вовлекаться лимфатическая система сердца с нарушением лимфодренажа и последующим склерозированием мелких лимфатических сосудов, образуя с измененными эндомизием и перимизием общий межуточный соединительнотканный конгломерат.
Так как вначале кардиомиоциты остаются интактными, сократительная способность сердца не изменяется. Но с постепенным уплотнением соединительной ткани она препятствует полноценному расслаблению клеток, в связи с этим начинает страдать диастолическая функция сердца. Миогенная сердечная ауторегуляция (закон Франка-Старлинга) в этих условиях перестает функционировать. Не происходит приспособление работы желудочков сердца к увеличению нагрузки объемом, не уравнивается производительность левого и правого желудочков сердца, не обеспечивается оптимальное количество циркулирующей крови и поддержание необходимого артериального давления. Позже с еще более выраженным уплотнением соединительной ткани происходит «сковывание» кардиомиоцитов до такой степени, что ухудшается систолическая функция правого и левого желудочков. Сердечная недостаточность приводит к развитию общей недостаточности кровообращения (Рис. 7).
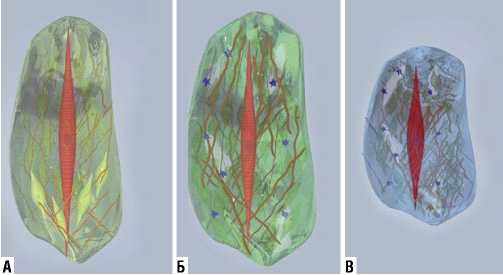
Рис. 7. Схематическое изображение иммобилизации на примере отдельных кардиомиоцитов. А — нормальная структура соединительной ткани (коллагеновый волокна, межклеточное вещество, встречаются единичные фибробласты), полноценная систола и диастола кардиомиоцита; Б — изменение объема и плотности соединительной ткани (увеличение количества фибробластов, коллагена I и III типа; появление металлопротеиназ; лимфостаза за счет склерозирования лимфатических сосудов), ограничивается диастолическая функция, систола не страдает; В — значительное уплотнение соединительной ткани (преобладание «грубых» коллагеновых волокон I типа, формирование иммобилизирующего «каркаса»), ограничиваются и диастолическая, и систолическая функция кардиомиоцитов.
Морфологические основы иммобилизирующего интерстициального фиброза сердца
Накоплен и проанализирован обширный материал прижизненных биопсий сердца и секционных исследований людей разных возрастов, в том числе новорожденных, умерших в разные сроки. Выявлена группа пациентов с интерстициальным иммобилизирующим фиброзом и выраженным уплотнением эндомизия и перимизия не ишемического генеза. Установлено, что в основе этих процессов лежит нарушение белкового обмена, изменение соотношения коллагеновых волокон различных типов. Основной морфологический субстрат фиброза миокарда — стимуляция синтеза коллагенов I и III типов, кроме того, увеличение происходит не пропорционально: коллагена I типа значительно больше (это является ключевым в оценке «жесткости» соединительной ткани). Структурирован он в виде сеток и пересекающихся пучков, образующих замкнутые пространства вокруг отдельных кардиомиоцитов. Такой каркас также включает более многочисленные пучки волокон коллагена III типа, расположенные хаотично без четко различимых пространственных структур. Обращает на себя внимание морфологическое сходство со структурой келоидного рубца, образующегося иногда после ожогов, заживления послеоперационных ран и т.д. (Рис. 8).
Иммуногистохимическим методом выявлена повышенная экспрессия биологических молекул — ма-триксных металлопротеиназ (ММР-2 и ММР-9), которые выделяются иммунными клетками и фибробластами интерстициальной ткани сердца и участвуют в перестройке эндомизия и перимизия сердца. Их выделение — это первый этап разрушения нормальной соединительной ткани.
Происходит снижение экспрессии кардиомиоцитами коннексина-4З, являющегося структурной основой щелевых контактов, и его перераспределение в клетке («латерализация») у пациентов с выраженным фиброзом миокарда на фоне увеличения матриксных металлопротеиназ. Это влияет на проводимость и проницаемость для ионов Na+, уменьшается объем импульсов, проходящих через щелевой контакт (Рис. 9).
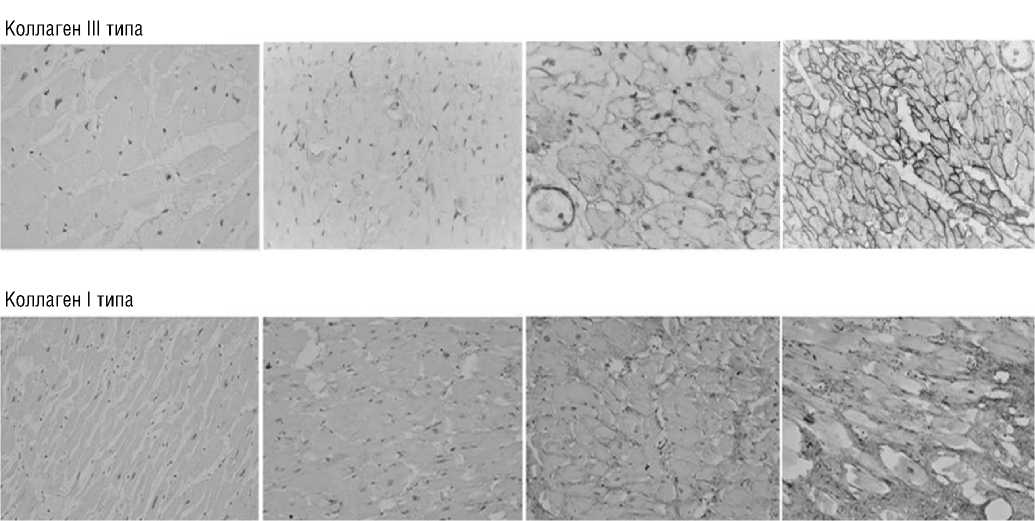
Коллаген III типа
Коллаген I типа
Рис. 8. Иммобилизирующий интерстициальный фиброз сердца, гистологические исследования. Постепенное изменение (слева направо) структуры и количества коллагена I и III типов (окраска по Вейгерту, увеличение х 400).

Экспрессия ММР2 Экспрессия ММР9
(ИГХ х 200) (ИГХ х200)
Экспрессия ММР9 (ИГХ х400)
Экспрессия коннексин 43 Экспрессия коннексин 43
(ИГХ х200)
(ИГХ х400)
Рис. 9. Иммобилизирующий интерстициальный фиброз сердца, гистологические исследования. Экспрессия биологических молекул матриксных металлопротеиназ и коннексина-43 в миокарде (иммуногистохимический метод, увеличение х 200 и х 400).
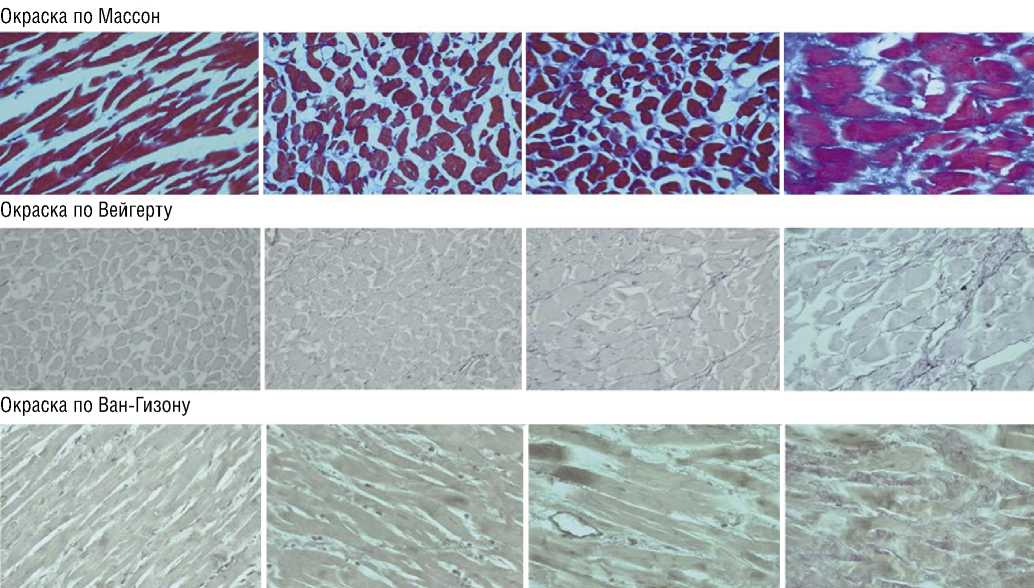
Рис. 10. Иммобилизирующий интерстициальный фиброз сердца, гистологические исследования. Постепенное «огрубление» (слева направо) интерстициальной соединительной ткани миокарда (окраска по Массон, Вейгерту, Ван-Гизону, увеличение х 400).
У пациентов при иммобилизирующем интерстициальном фиброзе происходит изменение структуры индивидуального «оплетения» пучков и отдельных кардиомиоцитов соединительной тканью, увеличивается толщина и плотность «перемычек». При таком изменении межуточной соединительной ткани сердца, ее всё большем уплотнении, страдает и лимфатическая система, склерозирование которой приводит к нарушению лим-фодренажа (Рис. 10).
Клинические признаки иммобилизирующего интерстициального фиброза сердца
Прежде всего, клиническим проявлением иммобилизирующего интерстициального фиброза является необъяснимая сердечная недостаточность. Малоэффективна, а потом и совсем неэффективна общепринятая кардиотоническая терапия. В результате иммобилизации пучков кардиомиоцитов нарушается диастолическая функция миокарда, затем происходит постепенное сни- жение фракции выброса левого желудочка, появляются признаки застоя по малому, а позже и по большому кругу кровообращения. Медленно прогрессирующая сердечная недостаточность, в итоге, переходит в усугубляющуюся недостаточность общего кровообращения со всеми её клиническими проявлениями: развивается легочная гипертензия, цирроз Пика и полиорганная недостаточность. Правда, до такого состояния пациенты, как правило, не доживают. Обращает на себя внимание наличие в анамнезе: ревматических атак, туберкулеза, перенесенных вирусных инфекций (в том числе SARS-CoV-2), наличие или раннее перенесенных очаговых инфекций (синусит, остеомиелит, пародонтит, нефрит, цистит, пиелонефрит, плеврит и прочее), заболеваний соединительной ткани, лучевой терапии при медиастинальной форме лимфогранулематоза, заболеваний щитовидной железы, сахарного диабета 2 типа, нарушения ритма сердца и проводимости. Необъяснимая сердечная недостаточность в климактерическом периоде, особенно у мужчин, также может свидетельствовать об
иммобилизирующем интерстициальном фиброзе сердца. Важным эхокардиографическим критерием является отсутствие локального нарушения сократимости миокарда, на фоне снижения глобальной систолической функции сердца в более поздние периоды.
Конечно, прямым диагностическим критерием является морфологическое исследование биоптатов сердца, с тотальным, диффузным поражением соединительной ткани. Однако это исследование не всегда выполнимо и поэтому в диагностике следует учитывать весь комплекс перечисленных признаков. В перспективе не исключается определение наличия металлопротеиназ в крови и выявление других лабораторных маркеров, а также определение плотности межуточной соединительной ткани сердца.
Возможные принципы лечения
Предполагаем, что положительный эффект возможно достичь применением глюкокортикостероидов, но, по-видимому, в относительно ранние сроки развития болезни. Вероятно, перспективным направлением лечения иммобилизирующего интерстициального фиброза сердца будет использование ингибиторов металлопротеиназ. Не исключается использование ультразвуковой ударно-волновой терапии, направленной на уменьшение плотности соединительной ткани за счет разрыва ее волокон. Вполне возможно, что эффективным может быть и применение цитостатических препаратов. Однако все это требует дальнейших исследований.
Заключение
Итак, иммобилизирующий интерстициальный фиброз сердца можно считать самостоятельной патологией и одной из главных причин развития хронической сердечной недостаточности. В основе иммобилизирующего интерстициального фиброза сердца лежит процесс изменения соединительнотканного каркаса миокарда, приводящий в итоге к угнетению его работы. Расшифровка молекулярных и структурных основ «перестройки» соединительной ткани сердца и собственно миокарда при фиброзе является ключом к пониманию патогенетических основ развития некурабельной сердечной недостаточности, не связанной с ишемическими изменениями сердца.
В основу предупреждения и лечения иммобилизирующего интерстициального фиброза сердца, по-видимому, должен быть положен принцип борьбы с причинами аутоиммунных процессов в организме и подавления реактивности соединительной ткани сердца.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Иммобилизирующий интерстициальный фиброз сердца
- Ricard-Blum S. The collagen family. Cold Spring Harb Perspect Biol. 2011; 3(1): a004978. doi: 10.1101/cshperspect.a004978.
- Halper J. Basic Components of Connective Tissues and Extracellular Matrix: Fibronectin, Fibrinogen, Laminin, Elastin, Fibrillins, Fibulins, Matrilins, Tenascins and Thrombospondins. Adv Exp Med Biol. 2021; 1348: 105-126. doi: 10.1007/978-3-030-80614-9_4.
- Pinto AR, Ilinykh A, Ivey MJ, et al. Revisiting cardiac cellular composition. Circ Res. 2016; 118: 400-409.
- Gersch C, Dewald O, Zoerlein M, et al. Mast cells and macrophages in normal C57/BL/6 mice. Histochem Cell Biol. 2002; 118: 41-49.
- Bajpai G, Schneider C, Wong N, et al. The human heart contains distinct macrophage subsets with divergent origins and functions. Nat Med. 2018; 24: 1234-1245.
- Epelman S, Lavine KJ, Beaudin AE, et al. Embryonic and adult-derived resident cardiac macrophages are maintained through distinct mechanisms at steady state and during inflammation. Immunity. 2014; 40: 91-104.
- Lee JS, Jeong SJ, Kim S, et al. Conventional dendritic cells impair recovery after myocardial infarction. J Immunol. 2018; 201: 1784-1798.
- Camelliti P, Borg TK, Kohl P. Structural and functional characterisation of cardiac fibroblasts. Cardiovasc Res. 2005; 65: 40-51.
- Tallquist MD. Cardiac fibroblast diversity. Annu Rev Physiol. 2020; 82: 63-78.
- Liu X, Wu H, Byrne M, et al. Type III collagen is crucial for collagen I fibrillogenesis and for normal cardiovascular development. Proc Natl Acad Sci U S A. 1997; 94(5): 1852-1856. doi: 10.1073/pnas.94.5.1852.
- Kuivaniemi H, Tromp G. Type III collagen (COL3A1): Gene and protein structure, tissue distribution, and associated diseases. Gene. 2019; 707: 151-171. doi: 10.1016/j.gene.2019.05.003.
- Jugdutt BI. Ventricular remodeling after infarction and the extracellular collagen matrix: when is enough enough? Circulation. 2003; 108: 1395-1403.
- Huang S, Chen B, Su Y, et al. Distinct roles of myofibroblast-specific Smad2 and Smad3 signaling in repair and remodeling of the infarcted heart. J Mol Cell Cardiol. 2019; 132: 84-97.
- Suthahar N, Meijers WC, Silljé HHW, de Boer RA. From Inflammation to Fibrosis-Molecular and Cellular Mechanisms of Myocardial Tissue Remodelling and Perspectives on Differential Treatment Opportunities. Curr Heart Fail Rep. 2017; 14(4): 235-250. doi:10.1007/s11897-017-0343-y.
- Krenning G, Zeisberg EM, Kalluri R. The origin of fibroblasts and mechanism of cardiac fibrosis. J Cell Physiol. 2010; 225: 631-7. doi:10.1002/jcp.22322.
- Frangogiannis NG. Cardiac fibrosis. Cardiovasc Res. 2021; 117(6): 1450-1488. doi:10.1093/cvr/cvaa324].
- Gao XM, White DA, Dart AM, Du XJ. Post-infarct cardiac rupture: recent insights on pathogenesis and therapeutic interventions. Pharmacol Ther. 2012; 134: 156-179.
- Dai Z, Aoki T, Fukumoto Y, Shimokawa H. Coronary perivascular fibrosis is associated with impairment of coronary blood flow in patients with non-ischemic heart failure. J Cardiol. 2012; 60: 416-421.
- Kalkman E, Bilgin Y, Haren P, et al. Determinants of coronary reserve in rats subjected to coronary artery ligation or aortic banding. Cardiovasc Res. 1996; 32: 1088-1095.
- Kramann R, Schneider RK, DiRocco DP, et al. Perivascular Gli1+ progenitors are key contributors to injury-induced organ fibrosis. Cell Stem Cell. 2015; 16: 51-66.
- Wu L, Ong S, Talor MV, et al. Cardiac fibroblasts mediate IL-17A-driven inflammatory dilated cardiomyopathy. J Exp Med. 2014; 211: 1449-1464. doi: 10.1084/jem.20132126.
- Дземешкевич С.Л., Стивенсон Л.У. Дисфункция миокарда и сердечная хирургия: классификация, диагностика, хирургическое лечение. — М.: ГЭОТАР-Медиа, 2009.


