Иммобилизирующий интерстициальный фиброз сердца. Часть 2
Автор: Шевченко Ю.Л., Ульбашев Д.С.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Редакционные статьи
Статья в выпуске: 3 т.17, 2022 года.
Бесплатный доступ
Важной патофизиологической основой сердечной недостаточности является фиброз. Он определяется при кардиомиопатиях различного генеза. По результатам многочисленных экспериментальных и клинических исследований выявлена возможность изолированного нарушения структуры эндомизия и перимизия, с тенденцией к уплотнению и постепенному механическому сдавлению кардиомиоцитов - иммобилизации. Причем этот процесс постепенно достигает такой степени огрубления, что образовавшийся каркас вокруг отдельных кардиомиоцитов и их пучков, препятствует сначала полноценной диастоле, а в дальнейшем и систоле. Эта особая форма названа «иммобилизирующим интерстициальным фиброзом сердца». Заключение. Иммобилизирующий интерстициальный фиброз сердца является одной из главных самостоятельных причин сердечной недостаточности, не связанной с атеросклеротическим поражением коронарных артерий. В далеко зашедших стадиях такой фиброз может приводить к ИБС в результате экстраваскулярного сдавления артериол. Изолированное нарушение структуры эндомизия и перимизия, проявляющееся избыточной выработкой коллагена I и III типов, увеличивает жесткость миокарда и изменяет кардиодинамику. Антифиброзные стратегии, направленные на предотвращение неблагоприятного ремоделирования сердца, становятся многообещающим подходом в профилактике и лечении сердечной недостаточности и требуют дальнейших углубленных клинических исследований.
Фиброз, сердечная недостаточность, соединительная ткань
Короткий адрес: https://sciup.org/140296411
IDR: 140296411 | DOI: 10.25881/20728255_2022_17_3_4
The immobilizing interstitial fibrosis of the heart. Part 2
The fibrosis is an important pathophysiological basis of heart failure. It is determined in cardiomyopathies of various genesis. According to the results of numerous experimental and clinical studies, the possibility of an isolated violation of the structure of the endomysium and perimysium, with a tendency to compaction and gradual mechanical compression of cardiomyocytes - immobilization, has been revealed. Moreover, this process gradually reaches such a degree of coarsening that the formed framework around individual cardiomyocytes and their bundles prevents first a full-fledged diastole, and later systole. This particular form is called "the immobilizing interstitial fibrosis of the heart”. Conclusion. The immobilizing interstitial fibrosis of the heart is one of the main independent causes of heart failure not associated with atherosclerotic lesions of the coronary arteries. In advanced stages, such fibrosis can lead to coronary artery disease as a result of extravascular compression of arterioles. An isolated violation of the structure of the endomysium and perimysium, manifested by excessive collagen production of types I and III, increases myocardial stiffness and changes cardiodynamics. Antifibrosis strategies aimed at preventing unfavorable remodeling of the heart are becoming a promising approach in the prevention and treatment of heart failure and require further in-depth clinical studies.
Текст научной статьи Иммобилизирующий интерстициальный фиброз сердца. Часть 2
Внеклеточный соединительно-тканный матрикс образует структурную основу сердца. Он состоит из комплекса коллагеновых и эластических волокон, протеогликанов и клеточных элементов [1] . Благодаря такой структуре создаются условия для незамедлительной передачи импульсов, генерируемых синусными кардиомиоцитами в организованное систолическое сокращение сердца. Кроме того, эндомизий и перимизий в норме способствуют пассивной жесткости в диастолу и предотвращают тем самым перенапряжение, обеспечивают скольжение пучков кардиомиоцитов относительно друг друга при их сокращении и адекватную деформацию тканей во время заполнения камер сердца кровью. Компоненты интерстиция также служат модуляторами роста, дифференцировки тканей и ангиогенеза [2] .
Важной патофизиологической основой нарушения работы сердца с развитием хронической сердечной недостаточности является его фиброз, который характери- зуется увеличением количества и изменением физических свойств коллагеновых волокон и других компонентов в интерстиции и периваскулярных областях миокарда [3]. Наиболее распространенными типами коллагена в сердце являются — I и III, которые в норме обеспечивают прочность на растяжение миокарда в диастолу и структурную его поддержку [4].
Фиброз определяется при гипертрофической, дилатационной и ишемической кардиомиопатиях. Были предложены разные его типы, включая репаративный и реактивный, относящиеся к формированию рубца как результату повреждения тканей и гибели клеток при ишемии, старении или реактивности фибробластов при гипертонии [5; 6] . Особая форма фиброза сердца, названная « иммобилизирующим интерстициальным фиброзом », признана самостоятельной причиной сердечной недостаточности.
Проведенные многочисленные экспериментальные и клинические исследования свидетельствуют о реальной

возможности изолированного нарушения структуры эндомизия и перимизия, с тенденцией к уплотнению и постепенному механическому сдавлению кардиомиоцитов — иммобилизации. Причем этот процесс постепенно достигает такой степени огрубления, что образовавшийся каркас вокруг отдельных кардиомиоцитов и их пучков, препятствует сначала полноценной диастоле, а в дальнейшем и систоле [7] .
Первичный иммобилизирующий интерстициальный фиброз сердца
Многое в развитии интерстициального иммобилизирующего фиброза проясняют проведенные исследования. Накоплены и проанализированы многочисленные результаты прижизненных биопсий сердца и секционных исследований людей разных возрастов, в том числе новорожденных, умерших в разные сроки. Из них отдельно выбрана группа с интерстициальным иммобилизирующим фиброзом — выраженным уплотнением эндомизия и перимизия неишемического генеза. Установлено, что в основе лежит нарушение белкового обмена и изменение соотношения коллагеновых волокон различных типов. Основной морфологический субстрат фиброза миокарда — стимуляция синтеза коллагенов I и III типов, кроме того, увеличение происходит не пропорционально: коллагена I типа значительно больше (это является ключевым в оценке «жесткости» соединительной ткани).
Структура коллагена I типа представлена в виде хаотичного пересечения пучков и сеток, образующих замкнутые пространства вокруг отдельных кардиомиоцитов. Такой каркас также включает более многочисленные пучки волокон коллагена III типа, располагающиеся неупорядоченно без четко различимых пространственных структур. Обращает на себя внимание морфологическое сходство со структурой келоидного рубца, образующегося иногда после ожогов, заживления послеоперационных ран и т.д.
У пациентов при иммобилизирующем интерстициальном фиброзе происходит изменение структуры индивидуального «оплетения» пучков и отдельных кардиомиоцитов соединительной тканью, увеличивается толщина и плотность «перемычек» (Рис. 1).
Так как вначале кардиомиоциты остаются интактными, сократительная способность сердца не изменяется. Но с постепенным уплотнением интерстициальная ткань препятствует полноценному расслаблению клеток, в связи с этим начинает страдать диастолическая функция сердца. Свободное скольжение пучков кардиомиоцитов между собой сменяется их жестким связыванием и опле-тением плотной соединительнотканной оболочкой. Позже с еще более выраженным уплотнением соединительной ткани происходит «сковывание» кардиомиоцитов до такой степени, что ухудшается систолическая функция правого и левого желудочков. Сердечная недостаточность приводит к развитию общей недостаточности кровообращения.
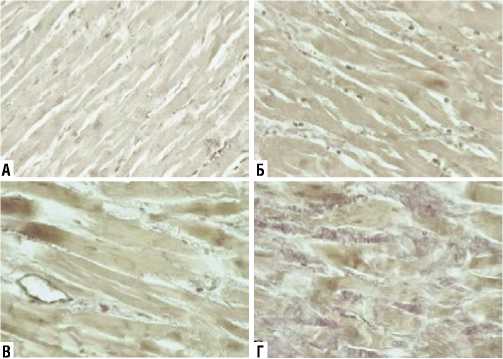
Рис. 1. Иммобилизирующий интерстициальный фиброз сердца . Постепенное «огрубление» (А–Г) интерстициальной соединительной ткани миокарда (окраска Ван-Гизону, увеличение х400).
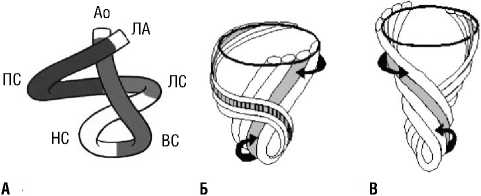
Рис. 2. А — Пространственное расположение миокарда желудочков в виде спирали, состоящей из 2-х витков. Ао — аорта, ЛА — легочная артерия, ПС - правый сегмент, ЛС — левый сегмент, НС — нисходящий сегмент, ВС — восходящий сегмент. В центре имеется сгиб (под углом около 180 градусов), который разделяет базальный и верхушечный циклы. Базальный цикл (ПС — свободная стенка ПЖ от корня ЛА до МЖП; ЛС — свободная стенка ЛЖ от МЖП до центрального сгиба) имеет направление от корня ЛА к центральному сгибу, а верхушечный цикл направлен от сгиба до корня аорты. Переход нисходящего сегмента в восходящий происходит под углом около 90 градусов. Схема последовательности вращения сегментов верхушечного цикла в норме . Б — сокращение нисходящего сегмента полосы: укорочение длинной оси желудочков, циклический сдвиг, изменение размера и формы АВ отверстий. В — сокращение восходящего сегмента: резкое удлинение продольной оси желудочка раскручивание основания, увеличение размера и изменения формы АВ отверстий. В результате, создается мощная сила всасывания предсердной крови [8; 9]. При иммобилизирующем интерстициальном фиброзе эти процессы нарушаются.
Следует отметить, что в этой ситуации нарушается механика сокращений сердца в целом. Грубый фиброз изменяет специфическую конструкцию интрамиокарди-альных фасций и препятствует нормальному функциональному движению сердца — спиральной «закрутке», которая имеет большое значение в экономии энергии внешней работы сердца и обеспечивает ламинарный поток крови. При иммобилизирующем интерстициальном фиброзе сердца повышается нагрузка на миокард и изменяется конфигурация внутрисердечной гемодинамики (Рис. 2).

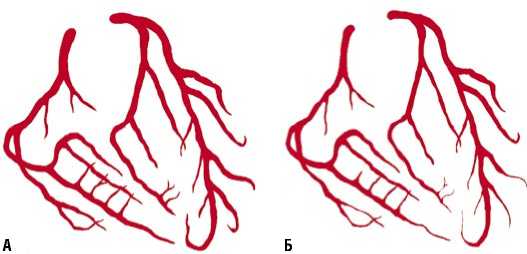
Рис. 3. Схема последовательного развития периваскулярного стенозирующего фиброза: А — коронарное русло в норме, Б — начальные процессы периваскулярной иммобилизации, страдает периферическое русло, В — далеко зашедший интерстициальный фиброз с формированием признака «мышиных хвостов».
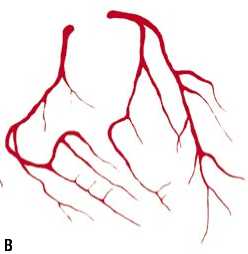
А
В
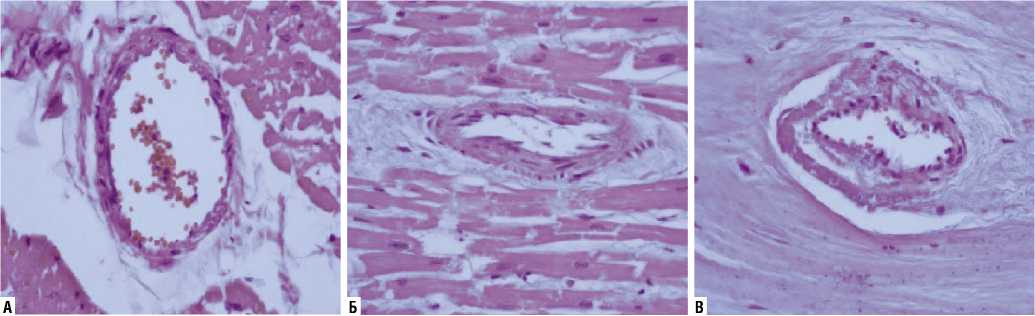
Рис. 4. Развитие периваскулярной иммобилизации артериол: А — норма, Б –выраженный фиброз, В — крайне тяжелая степень интерстициального фиброза со значительным сдавлением коронарных артериол (окраска гематоксилином и эозином, увеличение х400).
При выраженном фиброзном изменении межуточной ткани сердца, ее всё большем уплотнении, страдает и лимфатическая система, склерозирование которой приводит к нарушению лимфодренажа. Особо важным моментом в усугублении фиброза является сдавление периферических отделов венечных артерий, причем процесс начинается с артериол, у которых мышечный слой слабо выражен. В это время могут появляться клинические, инструментальные признаки коронарной недостаточности, не отвечающей на соответствующую терапию. Развивается ангиопатия в результате сдавления артерии извне — соединительная ткань как муфта окутывает их. Проявляется весьма специфичный ангиографический симптом — «мышиных хвостов». Этот известный признак чаще связывали с аномалиями развития коронарных артерий — их гипоплазией. В итоге страдают периферические артериолы, увеличивается склонность основных коронарных артерий к спазмированию в результате нарушения нервной регуляции. На вскрытии лишь гистологическое исследование покажет изменения соединительной ткани и периваскулярную иммобилизацию. На этой стадии первичный интерстициальный фиброз сердца , в результате экстравазальной констрикции артериол, может быть причиной острого инфаркта миокарда (Рис. 3–5).
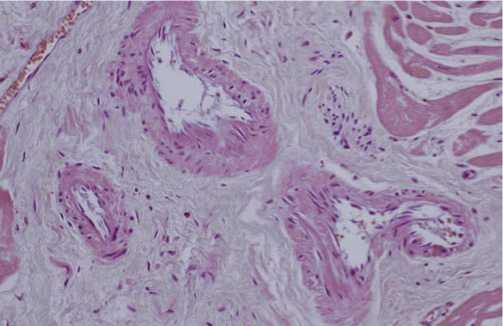
Рис. 5. Стадия коронарной ангиопатии: крайне тяжелая степень фиброза с вовлечением и констрикцией периферического коронарного русла — сдавление группы артериол (окраска гематоксилином и эозином, увеличение х400).
Вторичный (индуцированный) иммобилизирующий интерстициальный фиброз
В определенных условиях рубцовый очаг после инфаркта миокарда может индуцировать формирование иммобилизирующего интерстициального фиброза . В этом случае в перифокальной соединительнотканной

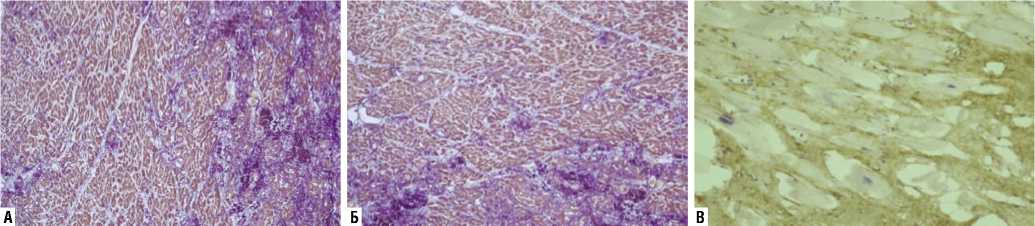
Рис. 6. На гистологических препаратах с окраской по Массону, увеличением х40 (А, Б) и при имммуногистохимическом исследовании с увеличением х400 (В) — хорошо видна граница между очагом ишемического рубца и индуцированным иммобилизирующим интерстициальным фиброзом сердца.
зоне начинают вырабатываться специфические медиаторы, и запускается, подобно цепной реакции, процесс «ползучего» развития плотной соединительной ткани между здоровыми кардиомиоцитами — диффузного межуточного фиброза с дальнейшей усугубляющейся их иммобилизацией. Сердечную недостаточность в этом случае следует расценивать как совокупность двух ее причин: с одной стороны — ишемической болезни сердца, а с другой — индуцированного иммобилизирующего интерстициального фиброза неишемизированных зон сердца (Рис. 6).
Клинические признаки иммобилизирующего интерстициального фиброза сердца
Обращает на себя внимание наличие в анамнезе: ревматических атак, туберкулеза, вирусных инфекций (в том числе SARS-CoV-2), паразитарных заболеваний, наличие или раннее перенесенных очаговых инфекций (синусит, остеомиелит, пародонтит, нефрит, цистит, пиелонефрит, плеврит и прочее), заболеваний соединительной ткани, лучевой терапии при медиастинальной форме лимфогранулематоза, заболеваний щитовидной железы, сахарного диабета 2 типа, нарушения ритма сердца и проводимости. Необъяснимая сердечная недостаточность в климактерическом периоде, особенно у мужчин, также может свидетельствовать об иммобилизирующем интерстициальном фиброзе сердца .
Медленно прогрессирующая сердечная недостаточность, в итоге, переходит в усугубляющуюся недостаточность общего кровообращения со всеми её клиническими проявлениями.
Условно можно выделить следующие стадии развития иммобилизирующего интерстициального фиброза : I — латентная стадия, период бессимптомного течения (ранние изменения соединительной ткани);
II — стадия первичных минимальных проявлений (умеренная степень фиброза с увеличением коллагена I и III типа);
-
III — стадия диастолической дисфункции (выраженная степень фиброза со значимым преобладанием коллагена I типа);
-
IV — стадия систолической и диастолической дисфункции (тяжелая степень фиброза);
V — стадия коронарной ангиопатии (крайне тяжелая степень фиброза с вовлечением периферического коронарного русла).
Особо следует отметить, что если после операции аортокоронарного шунтирования или эндоваскулярных вмешательств на коронарных артериях не наступает улучшения сердечной деятельности (не увеличивается или уменьшается фракция выброса левого желудочка), усугубляется степень сердечной недостаточности, то это может свидетельствовать об исходном индуцированном постинфарктном иммобилизирующем интерстициальном фиброзе сердца в тяжелой стадии.
Важным эхокардиографическим и сцинтиграфическим критерием является отсутствие изолированного локального нарушения сократимости миокарда, на фоне снижения глобальной систолической функции сердца в более поздние периоды, в этом заключается отличие от фиброза ишемического генеза. Однако следует учитывать, что в крайне тяжелой степени фиброза, когда есть перивазальная иммобилизация артериол, — на стадии коронарной ангиопатии могут появляться зоны гипоперфузии и гипокинезии (Рис. 7–12).
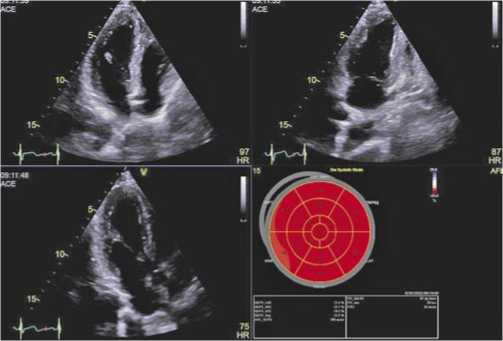
Рис. 7. Эхокардиография. Нормальная сократительная способность миокарда (отсутствие зон гипокинеза), общая ФВ ЛЖ сохранена — 64%.
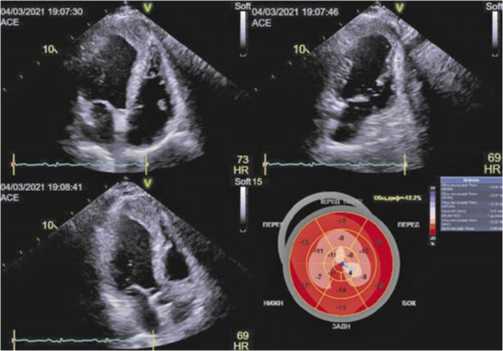
Рис. 8. Эхокардиография. ИБС, верхушечная постинфарктная аневризма с тромбом . Зона локального акинеза (область постинфарктного кардиосклероза) в области верхушки, общая ФВ ЛЖ — 50%.
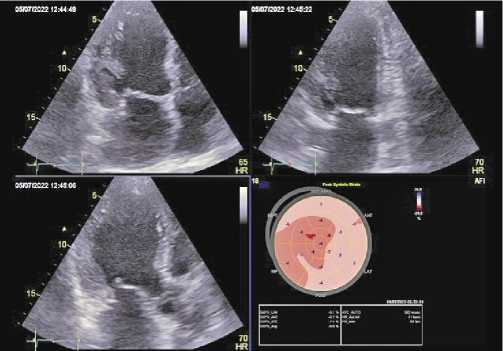
Рис. 9. Эхокардиография. Иммобилизирующий интерстициальный фиброз сердца . Диффузное снижение сократительной способности по всему миокарду ЛЖ. Сократительная способность ЛЖ снижена, общая ФВ ЛЖ — 41%.
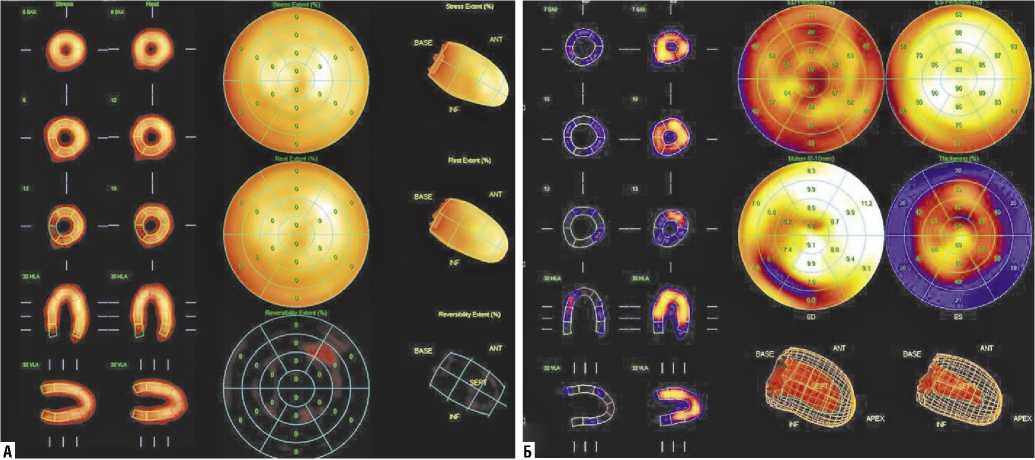
Рис. 10. Сцинтиграфия миокарда с 99mТс-технетрилом (А — перфузия миокарда ЛЖ, Б — функция миокарда ЛЖ). Пациент А., 56 л. Нормальная миокардиальная перфузия при нагрузке и в покое (отсутствие дефектов перфузии) в сочетании с нормальной сократительной способностью миокарда ЛЖ (отсутствие зон гипокинеза), общая ФВ ЛЖ — 67%.
Конечно, прямым диагностическим критерием тотального, диффузного поражения соединительной ткани сердца являются данные морфологического исследования биоптатов. Однако это не всегда выполнимо и поэтому в диагностике следует учитывать весь комплекс перечисленных признаков. В перспективе не исключается определение наличия маркеров фиброза (металлопротеиназ и др.) в крови и выявление других лабораторных маркеров, а также определение плотности межуточной соединительной ткани сердца (эластометрия).
Возможные принципы лечения
Предполагаем, что положительный эффект можно достичь применением глюкокортикостероидов, но, по-видимому, в относительно ранние сроки развития болезни. Вероятно, перспективным направлением лечения иммобилизирующего интерстициального фиброза сердца будет использование ингибиторов металлопротеиназ. Не исключается использование ультразвуковой ударноволновой терапии, направленной на уменьшение плотности соединительной ткани за счет разрыва ее волокон. Вполне возможно, что эффективным может быть и при-
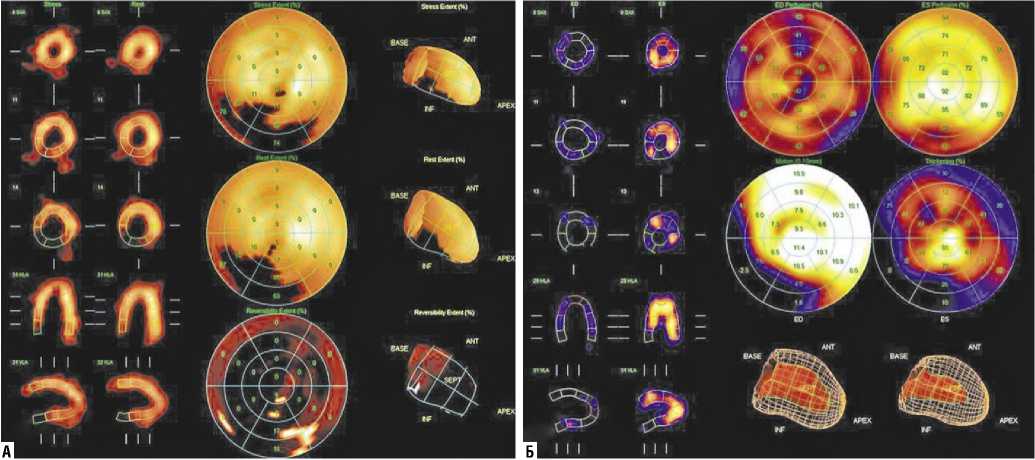
Рис. 11. Сцинтиграфия миокарда с 99mТс-технетрилом (А — перфузия миокарда ЛЖ, Б — функция миокарда ЛЖ). Пациент А., 72 л. ИБС, постинфарктный кардиосклероз . Зона локальной гипоперфузии (область постинфарктного кардиосклероза) в области задней стенки ЛЖ и задней МЖП совпадает с зоной локального гипокинеза. Сократительная способность ЛЖ сохранена, общая ФВ ЛЖ — 58%.
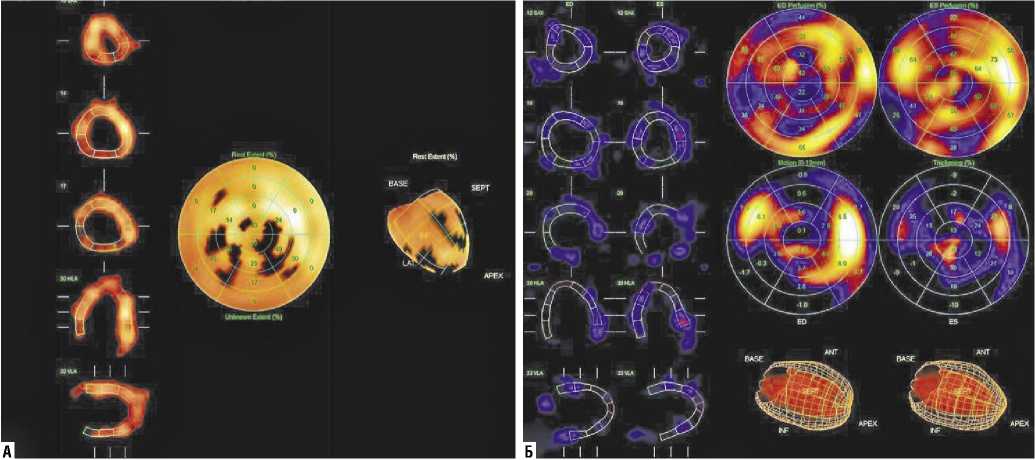
Рис. 12. Сцинтиграфия миокарда с 99mТс-технетрилом (А — перфузия миокарда ЛЖ, Б — функция миокарда ЛЖ). Пациент А., 49 л., Иммобилизирующий интерстициальный фиброз сердца . Диффузное снижение перфузии в сочетании с диффузным снижением регионального систолического утолщения по всему миокарду ЛЖ без четкой дифференциации зон локальной гипоперфузии и локального гипокинеза. ЛЖ значительно увеличен в размерах, полость его расширена. Сократительная способность ЛЖ резко снижена, общая ФВ ЛЖ — 37%.
менение цитостатических препаратов. При прогрессировании фиброза на стадиях появления ангиопатии, когда терапия становится совсем неэффективной, по-видимому, будет рассмотрен вопрос о проведении трансплантации сердца, конечно же, при отсутствии необратимых морфофункциональных изменений в других органах.
Особо стоит отметить, что у больных, перенесших острый инфаркт миокарда, с одной стороны, необходимо как можно раньше в программу лечения включить меры предупреждения развития индуцированного иммобилизирующего интерстициального фиброза здоровой части миокарда, с другой стороны, такой терапией можно замедлить формирование полноценного рубца в зоне инфаркта и таким образом повысить риск разрыва стенки сердца. Поэтому следует учитывать сроки формирования надежного рубца и проявлять разумную сдержанность
в расширении физической активности после острого инфаркта миокарда. Однако все это требует дальнейших исследований.
Заключение
Иммобилизирующий интерстициальный фиброз сердца является одной из главных самостоятельных причин сердечной недостаточности, не связанной с атеросклеротическим поражением коронарных артерий. В далеко зашедших стадиях такой фиброз может приводить к ИБС в результате экстраваскулярного сдавления артериол. Изолированное нарушение структуры эндомизия и перимизия, проявляющееся избыточной выработкой коллагена I и III типов, увеличивает жесткость миокарда и изменяет кардиодинамику. Происходит постепенное механическое сдавление кардиомиоцитов.
Антифиброзные стратегии, направленные на предотвращение неблагоприятного ремоделирования сердца, становятся многообещающим подходом в профилактике и лечении сердечной недостаточности и требуют дальнейших углубленных клинических исследований.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).


