Иммуногистохимическая характеристика акцидентальной инволюции тимуса после спленэктомии
Автор: Москвичев Евгений Васильевич, Меркулова Л.М., Стручко Г.Ю., Михайлова М.Н., Кострова О.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.7, 2012 года.
Бесплатный доступ
Исследована морфология и иммуногистохимический фенотип тимуса крысы с акцидентальной инволюцией после спленэктомии. Показано, что удаление селезенки сопровождается достоверными изменениями в морфологии тимуса и его иммуногистохимическом фенотипе по сравнению с животными из групп контроля. Через пять месяцев после спленэктомии в тимусе на фоне морфологических признаков атрофии паренхимы достоверно изменяется соотношение тимоцитов к компонентам тимопоэтического микроокружения, увеличивается число дендритных клеток и клеток APUD серии в мозговом веществе железы, а также возрастает экспрессия белков апоптоза в структурах коркового вещества.
Спленэктомия, тимус, акцидентальная инволюция тимуса, дендритные клетки, клетки apud серии
Короткий адрес: https://sciup.org/140188066
IDR: 140188066 | УДК: 612.438:616.411-089.87-008.9-092.18
Immunohistochemical characterization of accidental involution of the thymus after splenectomy
The morphology and immunohistochemical phenotype of the accidental thymic involution of the rat after splenectomy was study. It is established that splenectomy is accompanied by significant changes in the morphology and immunohistochemical phenotype of the thymus compared to control groups of animals within a month after the operation. Five months after splenectomy in the thymus against a background of morphological atrophy of the parenchyma significantly change in the ratio of thymocytes to the components of the thymocite microenvironment, the number of dendritic cells and APUD series in the medulla, as well as increased expression of apoptosis proteins in the structures of the cortex.
Текст научной статьи Иммуногистохимическая характеристика акцидентальной инволюции тимуса после спленэктомии
Тимус – центральный орган иммунной защиты, который подвержен возрастным изменениям и является исключительно чувствительным к стрессорному воздействию. Известно, что хронический стресс вызывает инволюцию тимопоэтического компонента железы с последующей структурной перестройкой органа и его атрофией, при этом изменения в железе схожи с возрастной инволюцией, но протекают значительно быстрее [5]. Хирургический стресс также оказывает кратковременное, но обратимое негативное влияние на тимус [1].
Удаление крупного периферического органа иммуногенеза – селезенки приводит к перестройке цепи взаимодействия иммунокомпетентных органов и снижению защитных сил. Это сопровождается нарушением многих звеньев иммунитета, а в некоторых случаях – развитием тяжелой постспленэктомической инфекции или синдрома OPSI (overwhelming post-splenectomy infection) [10]. Ранее было показано, что спленэктомия вызывает акцидентальную инволюцию тимуса, признаки которой сохраняются даже через 120 суток после операции. Было установлено, что спленэктомия сопровождается стойким увеличением уровня кортизола в крови, а так же увеличением уровня биогенных аминов в структурах тимуса [2]. Было высказано предположение, что механизм акци-дентальной инволюции может быть опосредован через клетки APUD серии и дендритные клетки (ДК) тимопо-этического микроокружения, но это предположение не было достоверно подтверждено.
Цель исследования – установление морфологических характеристик, иммуногистохимического фенотипа и особенностей цитоархитектоники клеток тимопоэтиче-ского микроокружения вилочковой железы при акциден-тальной инволюции после спленэктомии.
Материалы и методы исследования
Работа выполнена на 42 белых нелинейных крысах-самцах массой 180–220 г в возрасте 5 месяцев. Уход и содержание животных проводили в соответствии с «Правилами проведения работ с использованием экспериментальных животных». Крысы были разделены на три группы. Животным первой группы (22 крысы) под общей анестезией выполняли спленэктомию с соблюдением правил асептики и антисептики. Животным второй группы – ложнооперированные (10 крыс) – выполняли лапаротомию без удаления селезенки. Третью группу составили интактные животные (10 крыс) соответствующего возраста. Контролем служили интактные и ложнооперированные крысы. Выведение всех групп животных из эксперимента проводилось через 60 и 150 суток после операции путем декапитации. Объектом исследования служил тимус. В работе использованы следующие методы:
-
1. Иммуногистохимический метод с использованием пяти коммерческих моноклональных (МКАТ) и поликлональных (ПКАТ) антител фирм Santa Cruze (США) и Novocastra (Великобритания) [4]:
-
а) МКАТ к цитокератинам эпителиальных клеток;
-
б) ПКАТ к белку S-100 (маркер клеток нейроэктодермального происхождения и дендритных клеток),
-
в) МКАТ к синаптофизину (маркер нейроэндокринных клеток);
-
г) МКАТ к белку-регулятору апоптоза р53;
-
е) МКАТ к антиапоптотическому белку bcl-2.
-
2. Окраска гематоксилином и эозином для оценки общегистологической картины и проведения морфометрических измерений.
-
3. Компьютерная морфометрия с использованием лицензионных программ Leica application suite 3.6.0 (Германия) и Микроанализ (Россия).
-
4. Статистическая обработка с использованием лицензионного пакета программ MS Office 2003, достоверность определялась t-критерием Стьюдента.
Материал для исследования иммуногистохимическими методами фиксировали 10% нейтральным за-буференным формалином в течение 24 час., заливали в парафин, готовили срезы толщиной 4 мкм. Срезы наносили на высокоадгезивные стекла и высушивали при температуре 37° С в течение 18 часов. Демаскировка и иммуногистохимическая окраска проводилась на автостейнере Leica Bond Max (Германия). Контролем иммуногистохимической реакции служила неиммунизированная кроличья сыворотка. Результат реакции оценивали с применением микроскопа Leica DM4000B (Германия) путем подсчета позитивно окрашенных клеток на 100 клеток в десяти полях зрения, выражая результаты в процентах и единицах в поле зрения.
Результаты собственного исследования и обсуждение
Иммуногистохимическое окрашивание препаратов тимуса интактных крыс 6 месяцев антителами к цитоке-ратинам выявляет развитую сеть эпителиальных клеток коркового и мозгового вещества. Эпителиальные клетки занимают 8,3% площади коркового и 21,9% мозгового вещества дольки. Окраска антителами к белкам S-100 и синаптофизину выявляет многочисленные клетки нейроэктодермального и нейроэндокринного происхождения, которые локализуются в мозговом веществе и на границе коркового и мозгового вещества. Количество клеток, дающих положительную реакцию с белком S-100, достигает 18,4 в поле зрения, с синаптофизином – 12,8. При обработке срезов тимуса антителами к белкам-регуляторам апоптоза p-53 и bcl-2 выявляются немногочисленные клетки, дающие положительную реакцию, которые локализуются в корковом и мозговом веществе. Их количество составляет 6,2 и 2,5 клетки в поле зрения, соответственно.
В тимусе интактных крыс 10 месяцев начинают выявляться признаки возрастной инволюции, которые выражаются в снижении массы железы, уменьшении площади дольки и мозгового вещества, а так же толщины коркового слоя. Следует отметить, что морфология тимуса при окраске гематоксилином-эозином у интактных крыс на всех сроках эксперимента меняется незначительно, тогда как количе- ственные показатели иммуногистохимических реакций подвержены существенным изменениям. Нами установлено, что в тимусе интактных крыс 10 месяцев достоверно возрастает число кортикальных эпителиоцитов, которые занимают 15,7% площади. В мозговом же веществе отмечено достоверное уменьшение числа этих клеток до 16,9% (рис. 1). При окраске препаратов тимуса интактных крыс 10 месяцев антителами к белкам S-100 и синаптофизину отмечается существенное увеличение числа клеток, дающих положительную реакцию. Количество клеток, позитивных к S-100, возрастает до 34,3, а позитивных к синаптофизину увеличивается до 22,5 в поле зрения. Обработка препаратов тимуса антителами к белкам-регуляторам апоптоза bcl-2 и p-53 выявляет достоверное увеличение числа клеток, экспрессирующих эти маркеры до 3,9 и 26,8 в поле зрения, соответственно, при этом клетки, экспрессирующие p-53, располагаются преимущественно периваскулярно (рис. 2).
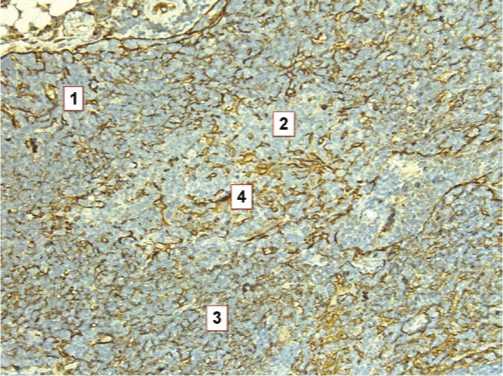
Рис. 1. Тимус интактной крысы 10 месяцев. 1 – корковое вещество, 2 – мозговое вещество, 3 – рыхлая сеть эпителиальных клеток в корковом веществе, 4 – эпителиальные клетки мозгового вещества. Иммуногистохимическая реакция к цитокератинам, ув. 100
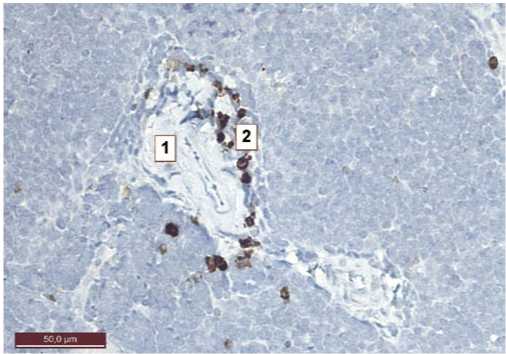
Рис. 2. Тимус интактной крысы 10 месяцев. Периваскулярные скопления клеток, экспрессирующих p-53 в корковом веществе. 1 – кровеносный сосуд мышечного типа. 2 – клетки, экспрессирующие p-53. Иммуногистохимическая реакция к p-53, ув. 400

Изменения в тимусе ложнооперированных крыс на всех сроках достоверно не отличались от изменений у интактных животных. Таким образом, возрастная инволюция сопровождается изменением соотношения эпителиальных клеток к тимической паренхиме с уменьшением их количества в мозговом веществе, а так же повышением экспрессии белков-регуляторов апоптоза и числа клеток нейроэктодермального и нейроэндокринного происхождения в структурах тимуса.
Через месяц после удаления селезенки отмечается уменьшение средней массы тимуса, а также площади мозгового и толщины коркового вещества по сравнению с интактными крысами. Окраска препаратов тимуса спле-нэктомированных крыс 6 месяцев антителами к цитоке-ратинам выявляет достоверное уменьшение количества эпителиальных клеток в мозговом веществе по сравнению с интактными и ложнооперированными крысами. Обработка срезов антителами к синаптофизину выявляет достоверное увеличение клеток, экспрессирующих этот антиген, до 19,6 клеток в поле зрения, тогда как число клеток, экспрессирующих S-100, меняется не достоверно. При исследовании белков-регуляторов апоптоза установлено, что экспрессия bcl-2 достоверно не меняется, тогда как количество клеток, экспрессирующих p-53, достоверно повышается до 8,6 клеток в поле зрения.
Через пять месяцев после спленэктомии дольки тимуса уменьшены в размерах, в них с трудом прослеживается граница между корковым и мозговым веществом. Междольковые септы расширены и заполнены жировой тканью, на периферии железы определяются дольки, подверженные атрофии и состоящие из скоплений эпителиальных клеток без лимфоцитов. Окраска препаратов тимуса антителами к цитокератинам выявляет густую сеть эпителиальных клеток в сохраненных дольках, которая занимает 20,3% площади коркового и 22% площади мозгового вещества (рис. 3). При обработке препаратов тимуса антителами к белкам S-100 и синаптофизину выявляются многочисленные клетки нейроэктодермального и нейроэндокринного происхождения, количество которых достоверно выше, чем у интактных и ложнооперированных животных. Окраска антителами к белку-регулятору апоптоза p-53 демонстрирует достоверное повышение экспрессии этого антигена в корковом веществе тимуса по сравнению с интактными и ложнооперированными крысами (рис. 4). Существенные изменения отмечаются в экспрессии bcl-2. Установлено, что количество клеток, экспрессирующих этот антиген выше, чем у интактных и ложнооперированных крыс в 2,3 раза, при этом клетки, дающие положительную реакцию с этим антигеном, располагаются, преимущественно, в мозговом веществе.
Таким образом, инволюция тимуса после спленэктомии сопровождается достоверным увеличением числа эпителиальных клеток коркового и мозгового вещества. Мы полагаем, что подобное увеличение количества эпителиальных клеток, вероятно, является относительным
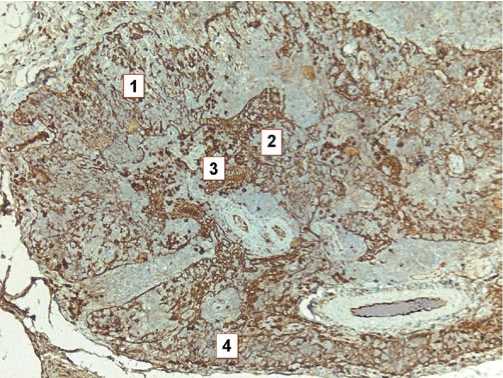
Рис. 3. Тимус спленэктомированной крысы 10 месяцев. Увеличение числа эпителиальных клеток в дольке. 1 – корковое вещество, 2 – мозговое вещество, 3 – компактные скопления эпителиальных клеток в мозговом веществе, 4 – густая сеть эпителиальных клеток коркового вещества. Иммуногистохимическая реакция к цитокератинам, ув. 100
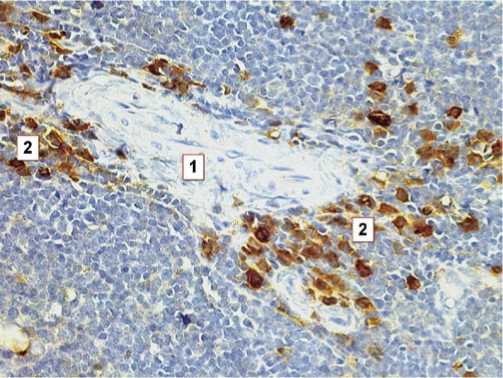
Рис. 4. Тимус спленэктомированной крысы 10 месяцев. Увеличение клеток, экспрессирующих p-53 в корковом веществе. 1 – кровеносный сосуд мышечного типа. 2 – клетки, экспрессирующие p-53. Иммуногистохимическая реакция к p-53, ув. 400
и обусловлено уменьшением количества тимоцитов. Показано, что спленэктомия сопровождается длительным повышением уровня кортизола [2], который нарушает поступление в железу костномозговых предшественников тимопоэза и усиливает апоптоз [6, 9]. Нами установлено, что спленэктомия приводит к увеличению числа клеток тимопоэтического окружения, экспрессирующих белки S-100 и синаптофизин. Известно, что в тимусе позитивную реакцию с маркером нейроэктодермальной дифференцировки S-100 дают медуллярные ДК и некоторые популяции эпителиальных клеток, входящие в состав периваскулярных пространств медуллярной зоны (PVS), а с синаптофизином – нейроэндокринные клетки медуллярной зоны, которые причисляют к клеткам АПУД

серии [3, 7]. Нейромедиаторы, выделяемые нейроэндокринными клетками, регулируют деятельность клеток микроокружения тимоцитов и секрецию ими гормонов и интерлейкинов, которые, в свою очередь, необходимы для созревания и дифференцировки Т-лимфоцитов. Кроме того, нейромедиаторы и белки, выделяемые ДК и клетками APUD серии, регулируют пролиферацию и апоптоз тимоцитов [8]. Мы считаем, что увеличение числа этих клеток может быть обусловлено как изменением соотношения тимоцитов к компонентам микроокружения вследствие инволюции, так и реакцией этих структур на повышенный уровень кортизола. Нами установлено, что инволюция тимуса после спленэктомии сопровождается достоверным увеличением числа клеток, экспрессирующих белок-регулятор апоптоза p-53, а так же клеток, экспрессирующих его антагонист – антиапоптотический белок bcl-2. При этом экспрессия p-53 отмечается, преимущественно, в корковом веществе вокруг сосудов и на границе с мозговым веществом, тогда как клетки, экспрессирующие bcl-2, локализованы в мозговом веществе тимуса (рис. 4). Мы считаем, что подобная экспрессия белков, вероятно, указывает на высокую интенсивность апоптоза в железе, преимущественно, за счет клеток коркового вещества.
Таким образом, инволюция тимуса после спленэктомии имеет существенные иммунофенотипические и морфологические отличия от возрастной инволюции у интактных крыс и сопровождается изменением соотношения лимфоцитов к компонентам микроокружения, увеличением числа дендритных и нейроэндокринных клеток, а так же усилением апоптоза в структурах коркового вещества.
Работа выполнена в рамках гос. контракта № 02.740.11.0708.
ФЦП «Научные и научно-педагогические кадры инновационной России» на 2009–2013 гг.
Список литературы Иммуногистохимическая характеристика акцидентальной инволюции тимуса после спленэктомии
- Бабаева А.Г. Реактивные изменения в тимусе и селезенке как ответ на хирургическое вмешательство/А.Г. Бабаева, Е.И. Гиммельфарб, И.И. Калинина//Архив патологии -1995. -Т. 2. -№ 57. -С. 58-61.
- Стручко Г.Ю. Морфофункциональное исследование тимуса и иммунобиохимических показателей крови после спленэктомии и иммунокоррекции: автореф. дис.. докт. мед. наук./Г.Ю. Стручко -Саранск. -2003. -23 с.
- Bai M. Immunohistochemical expression patterns of neural and neuroendocrine markers, the neural growth factor receptors and the beta-tubulin II and IV isotypes in human thymus/M. Bai, A. Papoudou-Bai, G. Karatzias, M. Doukas, A. Goussia, K. Stefanaki, D. Rontogianni, Y. Dalavanga, N. Agnanti, P. Kanavaros//Anticancer Research -2008. -Vol. 28, № 1(A). -Р. 295-303.
- Dabbs D.J. Diagnostics immunohistochemistry/D.J. Dabbs//Edinburg: Churchill Livingstone. -2002. -673 p.
- Gruver A.L. Cytokines, leptin, and stress-induced thymic atrophy/A.L. Gruver, L. Amanda, Gruver and Gregory D. Sempowski//Journal of Leukocyte Biology -2008. -Vol. 84, № 4. -Р. 915-923.
- Herold M.J. Glucocorticoids in T cell apoptosis and function/M.J. Herold, K.G. McPherson, H.M. Reichardt//Cell Mol Life Science -2006. -Vol. 63, № 1. -Р. 60-72.
- Raica M. Structural heterogeneity and immunohistochemical profile of Hassall corpuscles in normal human thymus./M. Raica, S. Encica, A. Motoc, A. Cimpean, T. Scridon, M. Barsan//Annals of Anatomy -2006. -Vol. 188, № 4. -Р. 345-352.
- Savino W. Hematopoiesis./W. Savino, S. Smaniotto, M. Dardenne//Advances in Experimental Medicine and Biology -2005. -№ 567. -Р. 167-185.
- Smith L.K. Glucocorticoid-induced apoptosis of healthy and malignant lymphocytes/L.K. Smith, J.A. Cidlowski//Prog Brain Research -2010. -№ 182. -Р. 1-30.
- Takehiro O. Overwhelming postsplenectomy infection syndrome in adults -A clinically preventable disease/O. Takehiro, H. Kazuhiro//World Journal of Gastroenterolgy -2008. -Vol. 14, № 2. -Р. 176-179.


