Иммуногистохимические показатели серозных карцином яичников и возможный механизм развития резистентности к препаратам платины
Автор: Жукова Г.В., Ульянова Е.П., Меньшенина А.П., Моисеенко Т.И., Златник Е.Ю., Непомнящая Е.М., Сагакянц А.Б., Вереникина Т.И.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 4 т.23, 2024 года.
Бесплатный доступ
Цель исследования - определение информативности иммуногистохимических показателей серозных карцином яичников и их статистических связей после неоадъювантного лечения для оценки развития резистентности опухолей к платиносодержащим режимам адъювантной полихимиотерапии (АПХТ). Материал и методы. Проводили иммуногистохимическое исследование опухолевой ткани у больных серозным раком яичников высокой степени злокачественности IIIC-IV стадии в возрасте 49-72 лет, чувствительных (n=59) и резистентных (n=22) к платиносодержащим режимам адъювантной полихимиотерапии, у которых был отмечен положительный эффект на неоадъювантную терапию. В ткани опухолей яичников, полученной на этапе хирургического вмешательства после неоадъювантной полихимиотерапии, изучали иммуногисто-химические показатели пролиферативной активности (Ki67), экспрессии белка эксцизионной репарации ДНК ERCC1 и белков семейства АВС-транспортеров - Pgp и BCRP, а также статистические связи между этими показателями (коэффициент ранговой корреляции Спирмена).
Серозная карцинома яичников высокой степени злокачественности, платиноре- зистентность, пролиферация, транспортные белки, статистическая связь, биологическая обратная связь
Короткий адрес: https://sciup.org/140307088
IDR: 140307088 | УДК: 618.11-006.66-08:615.28:57.053 | DOI: 10.21294/1814-4861-2024-23-4-45-53
Immunohistochemical parameters of serous ovarian carcinomas and possible mechanism of development of resistance to platinum-based drugs
The aim of the study was to evaluate a prognostic significance of immunohistochemical parameters in serous ovarian carcinomas and their statistical relationships after neoadjuvant treatment to assess the development of tumor resistance to platinum-containing adjuvant polychemotherapy regimens. Material and Methods. An immunohistochemical study of tumor tissue was carried out in patients with high-grade serous ovarian cancer (stage IIIC-IV). The age of the patients ranged from 49-72 years. There were 59 patients who were sensitive and 22 patients who were resistant to platinum-containing adjuvant polychemotherapy. In the tissue of ovarian tumors obtained during surgery after noadjuvant polychemotherapy, we studied immunohistochemical indicators of proliferative activity (Ki67), expression of the DNA excision repair protein ERCC1 and proteins of the ABC transporter family - Pgp and BCRP, as well as statistical relationships between these indicators (Spearman’s rank correlation coefficient).
Текст научной статьи Иммуногистохимические показатели серозных карцином яичников и возможный механизм развития резистентности к препаратам платины
В настоящее время развитие резистентности к препаратам платины, формирующейся у 75–90 % больных раком яичников (РЯ), является острой проблемой клинической онкологии, резко снижающей шансы пациенток с распространенным РЯ на получение эффективной помощи и определяющей высокую летальность [1, 2]. При этом обнадеживающие результаты первых курсов лекарственного лечения не гарантируют сохранение платиночув-ствительности опухолей на дальнейших этапах терапии. Решение данной проблемы связано с выявлением механизмов развития платинорезистент-ности и поиском эффективных прогностических маркеров. На современном этапе еще не удалось выявить ни одного молекулярно-генетического, иммуногистохимического (ИГХ) или биохимического показателя, позволяющего прогнозировать развитие устойчивости к платиносодержащим режимам химиотерапии [3–5], подобно тому, как это имеет место в отношении выживаемости пациентов с опухолями некоторых других локализаций [6–8].
Известно о связи мутаций в генах BRCA 1/2 c чувствительностью к препаратам платины при РЯ и раке молочной железы (РМЖ) [9]. Однако чувствительностью к указанным факторам могут обладать и пациентки, у которых такие мутации отсутствуют. Ранее в качестве маркеров динамики чувствительности РЯ к препаратам платины рассматривались показатели активности белка ERRCI [6, 7], однако дальнейшие исследования не подтвердили их прогностическую значимость [8, 9]. Распространенность случаев отсутствия сверхэкспрессии эффлюксных белков при платинорезистентном РЯ и выраженного лечебного эффекта при ингибировании их активности [10, 11] свидетельствует о малой изученности кон- кретных форм участия белков-транспортеров в развитии лекарственной резистентности. Остается открытым вопрос о соотношении эффлюкса противоопухолевых химиопрепаратов и транспорта эндогенных проопухолевых факторов, о динамике пролиферативных и транспортных процессов [12]. Не исследована роль не связанных с изменением генов регуляторных нарушений, развивающихся на различных структурно-функциональных уровнях организма, которые могут проявляться не только в виде резких сдвигов тех или иных показателей, но и в изменении динамики их соотношений и корреляционных связей на фоне терапии [13, 14]. Все вышесказанное обусловливает целесообразность проведения комплексного исследования, направленного на уточнение информативности ИГХ характеристик карцином яичников и их статистических связей для прогноза динамики чувствительности опухолей к лекарственной терапии с использованием препаратов платины.
Целью исследования явилось определение информативности иммуногистохимических показателей серозных карцином яичников и их статистических связей после неоадъювантного лечения для оценки развития резистентности опухолей к платиносодержащим режимам адъювантной полихимиотерапии (АПХТ).
Материал и методы
Ретроспективно изучены ИГХ показатели в ткани опухолей яичников у больных РЯ IIIC–IV стадии постменопаузального возраста (49–72 года), у которых был отмечен положительный эффект на неоадъювантную полихимиотерапию (НАПХТ), позволивший перейти к этапу хирургического лечения в объеме оптимальной циторедукции и последующей АПХТ. По данным гистологического исследования у всех пациенток наблюдалась серозная карцинома высокой степени злокачественности (high grade). Больным проводилось 3 курса НАПХТ карбоплатином и паклитакселом. Схема АПХТ также включала карбоплатин и паклитаксел, количество курсов варьировало от 4 до 6. Всем пациенткам проводились стандартные клиниколабораторные исследования в соответствии с клиническими рекомендациями [15], включая определение концентрации сывороточных маркеров СА-125 и Не-4. Всем больным исследован мутационный статус генов BRCA 1/2 с помощью метода HRM-PCR (High Resolution Melt Polymerase chain reaction) и секвенирования по Сэнгеру.
Больные были распределены на 2 группы в зависимости от сроков развития рецидива заболевания, по которому определялась чувствительность опухоли к платиносодержащим режимам АПХТ [15]. В группу больных с опухолями, сохранившими чувствительность к АПХТ (платиночувствительные опухоли), вошло 59 женщин, у которых рецидив РЯ развился в сроки, превышавшие 6 мес с момента окончания последнего курса АПХТ. Группу больных с опухолями, резистентными к платиносодержащим режимам АПХТ (платинорезистентные опухоли), составили 22 пациентки, у которых прогрессирование отмечено на фоне проведения АПХТ или в течение 6 мес после ее завершения. Четвертая стадия РЯ выявлена у 17 (29 %) больных с платиночувствительными опухолями и у 7 (32 %) пациенток с платинорезистентными карциномами. Больные исследованных групп не имели значимых различий по распространенности процесса, возрасту, характеру и выраженности сопутствующих заболеваний.
В последние годы для оценки ответа распространенного РЯ на химиотерапию часто используется система CRS (Chemotherapy Response Score), предусматривающая оценку изменений в ткани большого сальника на фоне НАПХТ. Имеются противоречивые данные об информативности показателей CRS в отношении прогноза платиноре-зистентности, а также отмечается недостаточная стандартизация методических подходов при их определении [16]. В силу этого мы сочли целесообразным использовать традиционные критерии лечебного патоморфоза и сосредоточиться на изменениях в опухолях яичников как при оценке лечебного патоморфоза НАПХТ, так и при выявлении связи резистентности с особенностями экспрессии ИГХ показателей. В результате при гистологическом исследовании опухолевой ткани в обеих группах после НАПХТ отмечены четко выраженное нарушение структуры опухоли и уменьшение ее площади на 30 % и более, а также другие признаки, указывающие на лечебный патоморфоз II или III степени по Г.А. Лавниковой [17].
В ткани серозных карцином яичников, полученных после проведения НАПХТ, с помощью ИГХ методов проводили сравнительное изучение пролиферативной активности (Ki67), а также экспрессии белка эксцизионной репарации ДНК ERCC1 и двух белков семейства АВС-транспортеров – Pgp и BCRP. Для этого использовали поликлональные кроличьи антитела к Pgp (или MDR1, 1:600) и ERCC1 (1:300) фирмы Affinity Biosciences, поликлональные кроличьи антитела к Ki67 (1:200, Diagnostic BioSystem), моноклональные мышиные антитела к BCRP (клон JF0994, 1:300, Hangzhou HuaAn Biotechnology Co.Ltd.). Срезы докрашивали гематоксилином Карацци, для заключения использовали витрогель. Оценка результатов ИГХ реакции проводилась с применением светового микроскопа «AxioLab.A1» (Германия) при ×10, ×20 и ×40.
Для определения экспрессии Ki67 подсчитывали процентное содержание окрашенных в результате ИГХ реакции опухолевых клеток, приходящихся на 100 опухолевых клеток. В соответствии с традиционным способом оценки значения 0–20 % расценивали как низкие, 21–50 % – как умеренные
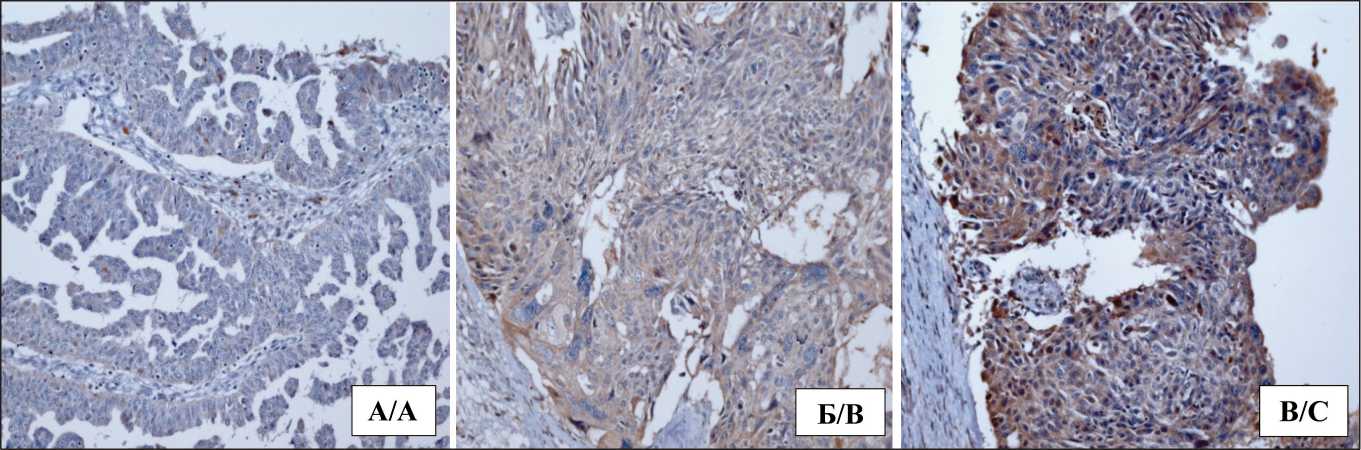
Рис. 1. Микрофото. Различная выраженность экспрессии белка ERRC-I в серозных карциномах яичников, ×200. А – отсутствие экспрессии; Б – низкая экспрессия, 1+; В – высокая экспрессия, 2+. Примечание: микрофото выполнены авторами
Fig. 1. Microphoto. Different expression of ERRC-I protein in serous ovarian carcinomas, ×200. A – lack of expression; B – low expression, 1+; C – high expression, 2+. Note: created by the authors
и 51–100 % – как высокие. Аналогичным образом, но с применением более подробной градации, оценивали экспрессию маркеров Pgp, BCRP и ERCC1: 1 (0–10 %), 2 (11–50 %), 3 (50–74 %), 4 (>75 %). При этом выраженность экспрессии ИГХ параметров в клетке определяли также полуколичественно по интенсивности окрашивания: 1+ – низкая, 2+ – умеренная, 3+ – высокая. Экспрессия считалась положительной при оценке не менее 2 по каждой из двух указанных шкал. На рис. 1 представлены микрофотографии ткани серозных карцином яичников у больных с различной выраженностью экспрессии ИГХ маркеров на примере белка эксцизионной репарации ДНК ERCC1.
Межгрупповые сравнения показателей проводили с помощью непараметрического критерия Манна–Уитни (U-критерий) и критерия согласия Пирсона χ2. В силу важности выявления критических величин, имеющих прогностическое значение, при анализе вариационных рядов обращали внимание на минимальные и максимальные значения рассматриваемых показателей (xmin – xmax) [18]. Статистические связи между исследованными показателями оценивали с помощью рангового коэффициента корреляции Спирмена (с оценкой его статистической значимости) и общепринятой градации выраженности («тесноты») связи на «слабую», «умеренную», «заметную» и «высокую», определяемой абсолютным значением коэффициента (шкала Чеддока). Использовали пакет программ «Statistica 13.3» (StatSoft Inc., США).
Исследования проведены с соблюдением «Этических принципов проведения научных медицинских исследований с участием человека» и в соответствии с «Правилами клинической практики в Российской Федерации».
Результаты и обсуждение
Медиана продолжительности безрецидивного периода у больных с платиночувствительными опухолями составила 19 мес, у больных с платинорезистентными опухолями – 5,2 мес (р=0,00001 Log-Ranktest). Также в исследуемых группах более чем в 2 раза различались показатели 3-летней общей выживаемости: у больных с чувствительностью к АПХТ – 51 %, у больных с резистентным течением – 23 % (p<0,05). Межгрупповые различия в выраженности токсических осложнений АПХТ не отмечены.
При молекулярно-генетическом исследовании у больных с платинорезистентным течением заболевания случаев мутаций в генах BRCA 1/2 не выявлено. У пациенток с опухолями, сохранившими чувствительность к АПХТ с карбоплатином, не наблюдались герминальные мутации в гене BRCА2 . В гене BRCA1 мутации выявлены у 8 из 59 таких больных (13 %). Эти мутации относились к 4 патогенным типам – 5382insC, 300T>G (C61G), 2080delA и c.1960A>T. При этом наиболее часто (n=4) встречалась минорная для российской популяции мутация 300T>G(C61G). В одном случае наблюдалась мутация Asp 1344del с неопределенным клиническим значением. Таким образом, в ходе исследования не отмечено связи между развитием платинорезистентности серозных карцином яичников на этапе АПХТ и наличием герминальных мутаций в генах BRCA 1/2 больных РЯ.
При изучении ИГХ показателей состояния ткани серозных карцином яичников после НАПХТ в целом выявлены признаки более высокого уровня пролиферации (Ki67), а также более высокой активности белков ERCC1, Pgp и BCRP у больных при развития резистентности к препаратам платины на этапе АПХТ (табл. 1, 2). В то же время у больных с платиночувствительными карциномами также отмечены случаи выраженной экспрессии исследуемых факторов, а у пациенток с платинорезистентными карциномами нередко встречались случаи сниженной экспрессии того или иного фактора. В наибольшей степени это
Таблица 1/Table 1
Характеристики пролиферативной активности после НАПХТ в серозных карциномах яичников, продемонстрировавших в дальнейшем различную чувствительность к платиносодержащим режимам АПХТ
Characteristics of proliferative activity in serous ovarian carcinomas after NAPCT, which further demonstrated different sensitivity to platinum-containing APCT regimens
|
Группа (опухоли)/ Groups (tumors) |
Частота встречаемости умеренных и высоких значений Кi67/ Frequency of moderate and high Кi67 values |
Значения Ki67 Ме [xmin–xmax]/ Кi67values Me [xmin–xmax] |
|
Платиночувствительные/ Platinum sensitive |
42 % |
17 [1–60] % |
|
Платинорезистентные/ |
77 %* |
38,5 [10–60] % |
|
Platinum resistiant |
р=0,006 |
p=0,305 |
Список литературы Иммуногистохимические показатели серозных карцином яичников и возможный механизм развития резистентности к препаратам платины
- Molekulyarno-geneticheskie podtipy raka yaichnikov: perspektivy dal'neishikh issledovanii. Voprosy onkologii. 2019; 65(1): 56-62.
- Motohara T., Yoshida G.J., Katabuchi H. The hallmarks of ovarian cancer stem cells and niches: Exploring their harmonious interplay in therapy resistance. Semin Cancer Biol. 2021; 77: 182-93. https://doi.org/10.1016/j.semcancer.2021.03.038.
- Kolesnikov E.N., Maksimov A.Yu., Kit O.I., Kutilin D.S. Zavisimost' obshchei i bezretsidivnoi vyzhivaemosti bol'nykh ot molekulyarno-geneticheskogo podtipa ploskokletochnogo raka pishchevoda. Voprosy onkologii. 2019; 65(5): 691-700. https://doi.org/10.37469/0507-3758-2019-65-5-691-700.
- Yu L., Jiang R., Chen W., Liu Ya., Wang, G., Xin Gong X., Wang Yo. Novel prognostic indicator combining inflammatory indicators and tumor markers for gastric cancer. World J Surg Onc. 2023; 21(1). https://doi.org/10.1186/s12957-023-02926-w.
- Golubeva V.A., Nepomuceno T.C., Monteiro A.N.A. Germline Missense Variants in BRCA1: New Trends and Challenges for Clinical Annotation. Cancers (Basel). 2019; 11(4): 522. https://doi.org/10.3390/cancers11040522.
- Steffensen K.D., Smoter M., Waldstrøm M., Grala B., Bodnar L., Stec R., Szczylik C., Jakobsen A. Resistance to first line platinum paclitaxel chemotherapy in serous epithelial ovarian cancer: The prediction value of ERCC1 and Tau expression. Int J Oncol. 2014; 44(5): 1736-44. https://doi.org/10.3892/ijo.2014.2311.
- Bogush T.A., Popova A.S., Dudko E.A., Bogush E.A., Tyulyandina A.S., Tyulyandin S.A., Davydov M.I. ERCC1 kak marker rezistentnosti raka yaichnikov k preparatam platiny. Antibiotiki i khimioterapiya. 2015; 60(3-4): 42-50.
- Bogush T.A., Stenina M.B., Bogush E.A., Zarkua V.T., Kalyuzhnyi S.A., Mamichev I.A., Tyulyandina A.S., Tyulyandin S.A. Kolichestvennye pokazateli ekspressii ERCC1 v tkani seroznogo raka yaichnikov i effektivnost' I linii khimioterapii s vklyucheniem preparatov platiny. Antibiotiki i khimioterapiya. 2018; 63(1-2): 24-31.
- Bao Y., Yang B., Zhao J., Shen S., Gao J. Role of common ERCC1 polymorphisms in cisplatin-resistant epithelial ovarian cancer patients: A study in Chinese cohort. Int J Immunogenet. 2020; 47(5): 443-53. https://doi.org/10.1111/iji.12484.
- Lu D., Shi H.C., Wang Z.X., Gu X.W., Zeng Y.J. Multidrug resistance-associated biomarkers PGP, GST-pi, Topo-II and LRP as prognostic factors in primary ovarian carcinoma. Br J Biomed Sci. 2011; 68(2): 69-74. https://doi.org/10.1080/09674845.2011.11730326.
- Xiao H., Zheng Yo., Ma L., Tian L., Sun Q. Clinically-Relevant ABC Transporter for Anti-Cancer Drug Resistance. Front Pharmacol. 2021; 12. https://doi.org/10.3389/fphar.2021.648407.
- Muriithi W., Macharia L.W., Heming C.P., Echevarria J.L., Nyachieo A., Filho P.N., Neto V.M. ABC transporters and the hallmarks of cancer: roles in cancer aggressiveness beyond multidrug resistance. Cancer Biol Med. 2020; 17(2): 253-69. https://doi.org/10.20892/j.issn.2095-3941.2019.0284.
- Glass L. Synchronization and rhythmic processes in physiology. Nature. 2001; 410(6825): 277-84 https://doi.org/10.1038/35065745.
- Mikhailov N.Yu., Garkavi L.Kh., Mashchenko N.M., Zhukova G.V. Issledovanie svyazi parametrov leikotsitarnoi formuly krovi s chastotnymi kharakteristikami signala pul'sovoi volny. Biofizika. 2012; 57(1): 99-104. https://doi.org/10.1134/S0006350912010150.
- Tyulyandina A.S., Kolomiets L.A., Morkhov K.Yu., Nechushkina V.M., Pokataev I.A., Rumyantsev A.A., Tyulyandin S.A., Urmancheeva A.F., Khokhlova S.V. Prakticheskie rekomendatsii po lekarstvennomu lecheniyu raka yaichnikov, pervichnogo raka bryushiny i raka matochnykh trub. Zlokachestvennye opukholi. 2022; 12(3s2-1): 198-211. https://doi.org/10.18027/2224-5057-2022-12-3s2-198-211.
- Rodolakis I., Pergialiotis V., Liontos M., Haidopoulos D., Loutradis D., Rodolakis A., Bamias A., Thomakos N. Chemotherapy Response Score in Ovarian Cancer Patients: An Overview of Its Clinical Utility. J Clin Med. 2023; 12(6): 2155. https://doi.org/10.3390/jcm12062155.
- Lushnikov E.F., Abrosimov A.Yu., Dvinskikh N.Yu. Patomorfoz opukholei cheloveka. M., 2021. 224 s.
- Guo C., Lu M., Chen J. An evaluation of time series summary statistics as features for clinical prediction tasks. BMC Med Inform Decis Mak. 2020; 48. https://doi.org/10.1186/s12911-020-1063-x


