Иммуногистохимическое исследование mTOR+-фибробластов в динамике развития и старения кожи человека
Автор: Голубцова Н.Н., Прокопьева Т.Н.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 4 т.32, 2024 года.
Бесплатный доступ
Путь мишени рапамицина у млекопитающих (mTOR) является важным клеточным сигнальным путем, участвующим в ряде важных физиологических функций, включая рост клеток, пролиферацию, метаболизм, синтез белка и аутофагию в ответ на различные внешние стимулы. Сигнальный путь mTOR существенно влияет на процессы старения в организме, регулируя клеточные функции и адаптацию к стрессовым условиям, но его значение для развития и физиологического старения кожи человека остается недостаточно изученным и открывает перспективы для дальнейших исследований. Цель исследования - изучение динамики изменений доли mTOR+-фибробластов в дерме человека в процессе развития и старения кожи и определение возможной роли mTOR в регуляции численности и пролиферативной активности фибробластов в процессе ее возрастных изменений. В качестве материала для исследования использованы 114 препаратов кожи случаев аутопсий различного возраста. Образцы кожи представляли собой аутоптаты нижней части передней поверхности шеи, полученные у плодов, начиная с 20 недели беременности, и людей, от рождения до 85 лет. MTOR+-, PCNA+- и виментин+-фибробласты изучали на фиксированных формалином срезах иммуногистохимическим методом. Полученные результаты позволяют заключить, что в коже плодов достоверно больше mTOR+-фибробластов, по сравнению с кожей людей от рождения до 85 лет. Доля фибробластов экспрессирующих mTOR в дерме человека статистически достоверно уменьшается с 20-недельного возраста до 60 лет с 95% до 78%, что доказывает значение фактора возраста в содержании mTOR+-фибробластов в дерме человека. В постнатальный период наблюдается постепенное уменьшение доли mTOR+-фибробластов. Отрицательная динамика возрастных изменений доли mTOR+-фибробластов в дерме начиная с фетального периода развития до 60 лет однонаправлена с возрастной динамикой общего числа и пролиферативной активности фибробластов. Таким образом, получены доказательства возрастной специфики участия mTOR в регуляции пролиферации фибробластов в дерме кожи человека.
Кожа, фибробласты, виментин, старение
Короткий адрес: https://sciup.org/143184757
IDR: 143184757 | DOI: 10.20340/mv-mn.2024.32(4).915
Immunohistochemical study of mTOR⁺ fibroblasts in the human skin development and aging dynamics
The mammalian target of rapamycin (mTOR) pathway is an important cellular signaling pathway involved in a number of important physiological functions, including cell growth, proliferation, metabolism, protein synthesis and autophagy in response to various external stimuli. The mTOR signaling pathway significantly affects the aging process in the body, regulating cellular functions and adaptation to stressful conditions, but its significance for the development and physiological aging of human skin remains poorly understood and opens up prospects for further research. The aim of the study was to study the dynamics of changes in the proportion of mTOR+-fibroblasts in the human dermis during skin development and aging and to determine the possible role of mTOR in regulating the number and proliferative activity of fibroblasts during its age-related changes. The study material included 114 skin preparations from autopsy cases of different ages. The skin samples were autopsies of the lower part of the anterior neck surface obtained from fetuses starting from the 20th week of pregnancy and from humans from birth to 85 years of age. MTOR+-, PCNA+- and vimentin+-fibroblasts were studied on formalin-fixed sections using the immunohistochemical method. The results obtained allow us to conclude that the skin of fetuses contains significantly more mTOR+-fibroblasts than the skin of humans from birth to 85 years of age. The proportion of fibroblasts expressing mTOR in the human dermis statistically significantly decreases from the age of 20 weeks to 60 years from 95% to 78%, which proves the importance of the age factor in the content of mTOR+-fibroblasts in the human dermis. In the postnatal period, a gradual decrease in the proportion of mTOR+-fibroblasts is observed. The negative dynamics of age-related changes in the proportion of mTOR+-fibroblasts in the dermis from the fetal period to 60 years of age is in the same direction as the age-related dynamics of the total number and proliferative activity of fibroblasts. Thus, evidence has been obtained for the age-specificity of mTOR participation in the regulation of fibroblast proliferation in the dermis of human skin.
Текст научной статьи Иммуногистохимическое исследование mTOR+-фибробластов в динамике развития и старения кожи человека
Голубцова Н.Н., Прокопьева Т.Н. Иммуногистохимическое исследование MTOR+-фибробластов в динамике развития и старения кожи человека. Морфологические ведомости. 2024;32(4):915. (4).915
Golubtsova NN, Prokop'eva TN. Immunohistochemical study of MTOR+-fibroblasts in the human skin development and aging dynamics. Morfolo-gicheskie Vedomosti – Morphological newsletter. 2024;32(4):915. (4).915
Введение. Мишень рапамицина млекопитающих (далее mTOR, от англ. «mammalian target of rapamycin») принадлежит к семейству киназ, связанных с фосфатидилинозитол-3-киназой. Входными сигналами для этой серинтреониновой протеинкиназы служат факторы роста, уровень питательных веществ, энергетический статус клетки и стрессовые условия окружающей среды [1-2]. Являясь центральным регулятором клеточного гомеостаза, сигнальный путь mTOR позволяет клеткам адаптироваться к изменениям окружающей среды, влияя на метаболизм клеток и их пролиферацию. При этом активация mTOR ведет к синтезу белков, липидов, нуклеотидов и к росту клеток, тогда как ингибирование mTOR может приводить к аутофагии и снижению синтеза этих компонентов [3]. Однако, молекулярные механизмы посредством которых реализуются эти процессы с участием mTOR пока малоизуче-ны.
Регулирующие влияния mTOR осуществляются через два белковых комплекса: mTORC1 и mTORC2, которые отличаются структурой и внутриклеточной функцией [4]. mTORC1 (от англ. «mammalian target of rapamycin complex 1») представляет собой клеточный комплекс, состоящий из нескольких ключевых компонентов. Основным белком комплекса является mTOR [5-6]. К этому белку присоединяется Raptor (от англ. «regulatory-associated protein of mTOR»), который помогает mTOR распознавать и фосфорилировать специфические субстраты и таким образом участвовать в активации комплекса [5-6]. Также в состав mTORC1 входит белок mLST8 (от англ. «mammalian lethal with sec13 protein 8»), который стабилизирует комплекс и поддерживает его активное состояние. Следующим компонентом комплекса является PRAS40 (от англ. «proline-rich akt substrate of 40 kDa»), который регулирует активность mTORC1 и может действовать как ингибитор. Еще один компонент -Deptor (от англ. «DEP domain-containing mTOR-interacting protein»), выступает в качестве отрицательного регулятора mTOR и способен подавлять его активность.
mTORC1 характеризуется полифункциональностью в отношении клеточных процессов. Одна из его активностей направлена на регуляцию синтеза белка. mTORC1 также регулирует метаболизм аминокислот и уровень энергии в клетке, активируясь при наличии питательных веществ и отвечая на уровень клеточной энергии, что позволяет клетке адаптироваться к изменениям в ее окружении. Важной функцией mTORC1 является подавление аутофагии, что позволяет клеткам сохранять компоненты, предотвращая разрушение клеточных структур [7-8].
Второй белковый комплекс, названный mTORC2 (от англ. «mammalian target of rapamycin complex 2») состоит из mTOR, который является центральным элементом комплекса и действует как серин-треониновая киназа. Вторым важным компонентом является Rictor (от англ. «rapamycin-insensitive companion of mTOR), который связывается с mTOR и способствует формированию активной структуры комплекса, обеспечивает регуляцию активности mTORC2 и его взаимодействие с другими молекулами. Еще одним структурным элементом комплекса является mLST8, его активность стабилизирует и поддерживает активность комплекса mTORC2. SIN1 (от англ. «SAPK-interacting protein1»), выступает в роли адаптерного белка и взаимодействует с mTOR и Rictor, способствуя их функциональной активности [4-5]. Также в состав mTORC2 входит Protor (от англ. «protein target of rapamycin») – это адаптерный белок, помогающий в стабилизации структуры mTORC2 и участвующий в передаче сигналов в различные клеточные пути.
Комплекс mTORC2 активно влияет на организацию актинового цитоскелета, что важно для клеточной подвижности, морфологии и способности клеток к миграции. Эта регуляция осуществляется через активацию молекул, которые модифицируют структуру и динамику актиновых филаментов. Другой важной функцией mTORC2 является активизация протеинкиназы В (Akt). Активация Akt способствует клеточной выживаемости, росту и метаболическим процессам, регулируя такие ключевые аспекты, как клеточная пролиферация и апоптоз. Кроме того, mTORC2 активирует и другие молекулы, включая серин-треонин протеин-киназу 1 и протеинкиназу C. По данным некоторых авторов, эти молекулы участвуют в различных клеточных сигнальных путях, которые не вовлечены в mTORC1, предоставляя mTORC2 уникальную способность управлять различными аспектами клеточных функций [9]. Комплекс mTORC2 менее чувствителен к рапами-цину, но его активность также может быть косвенно подавлена длительным применением этого препарата [10].
На основании исследований последних лет, mTOR не только регулирует важные онтогенетические процессы, но и оказывает значительное влияние на пролиферацию клеток в различных патологических состояниях, таких как опухолевые заболевания и старение. Ингибирование активности mТОR индуцирует продление жизни у дрожжей, червей, мух и мышей [11-12]. Согласно результатам ранее проведенных нами исследований, процесс старения кожи человека во многом обусловлен уменьшением численности фибробластов в дерме, которое отчасти связано со снижением их пролиферативной активности [13]. Учитывая данные мировой литературы, мы выдвинули гипотезу о возможном участии mTOR в регуляции антенатального развития и постнатальных возрастных изменений в коже человека. Следует отметить, что к настоящему времени данные по локализации и содержанию mTOR в коже человека в возрастном аспекте отсутствуют.
Цель исследования: изучение динамики изменений доли mTOR+ фибробластов в дерме человека в процессе развития и старения кожи и определение возможной роли mTOR в регуляции численности и пролиферативной активности фибробластов в дерме человека в процессе возрастных изменений.
Материалы и методы исследования. Исследование проводили в широком возрастном диапазоне, начиная с 20 недель пренатального развития и закан- чивая 85 годами постнатального. Проведение исследования одобрено локальным этическим комитетом Чувашского государственного университета имени И.Н. Ульянова (протокол № 4 от 15.11.2021). Материалом исследования были 114 аутопсий кожи человека (верхний угол стандартного разреза кожи при патологоанатомическом исследовании). Формалин-фиксированные образцы кожи проходили гистологическую проводку и заливку в парафин по стандартному протоколу. Далее из них изготавливали поперечные срезы в направлении эпидермис-дерма толщиной 5 мкм с помощью ротационного микротома Thermo Scientific.
Все гистологические срезы кожи окрашивали гематоксилином-эозином и применяли иммуногистохимический метод окрашивания с целью выявления кожных структур с экспрессией mTOR, PCNA и виментина. Поликлональные кроличьи антитела к mTOR (NBP1-02454, Novus Biologicals Inc., США) в разведении 1:50, кроличьи поликлональные антитела против PCNA (AHP1419, AbD Serotec, Великобритания) в разведении 1:100, кроличьи поликлональные антитела к виментину (GTX100619, GeneTex, США) в разведении 1:50 применяли в качестве первичных антител [14]. Кроличью полимерную визуализирующую систему, конъюгированную с пероксидазой (GTX83399, GeneTex, США) использовали в качестве вторичных антител. Активность пероксидазы выявляли с помощью перекиси водорода и диаминобензидина (Sigma Chemical Co., США). Структуры, имеющие иммунопозитивную реакцию, имели коричневый цвет. Нормальную кроличью сыворотку в концентрации 1% использовали для контроля специфичности окрашивания Количественный и качественный морфологический анализ окрашенных препаратов проводили с помощью микроскопа Nikon Eclipse 200 и камеры DS-Ri2. Каждый срез фотографировали при 400-кратном увеличении микроскопа как минимум в 3-х случайно выбранных полях зрения. Далее с помощью программы NIS-Elements Br («Nikon», Япония) в каждом из 342 случаев определяли площадь анализируемых участков срезов, подсчитывали в них об- щее число положительно окрашенных на виментин фибробластов и вычисляли число виментин+-фибробластов на 1 мм2 ткани дермы. Подсчитывая численность фибробластов дермы на 1 мм2 ткани дермы негативных и позитивных к mTOR и PCNA, вычисляли долю фибробластов с положительным окрашиванием к этим маркерам.
Все образы разделили на пять групп по возрасту (табл. 1). В настоящем исследовании мы не учитывали половую принадлежность используемых образцов при формировании групп, предварительный анализ с учетом биологического пола показал отсутствие значимого (p<0,05) влияния данного фактора на изменение доли mTOR+-, PCNA+- и виментин+-фибробластов в дерме кожи человека.
Таблица 1 Распределение исследованных групп по возрасту
|
Наименование |
Возраст |
Число образцов, шт. |
|
Группа 1 |
20 – 40 недель |
17 |
|
Группа 2 |
0 - 20 лет |
23 |
|
Группа 3 |
21 - 40 лет |
26 |
|
Группа 4 |
41 - 60 лет |
23 |
|
Группа 5 |
61 - 85 лет |
25 |
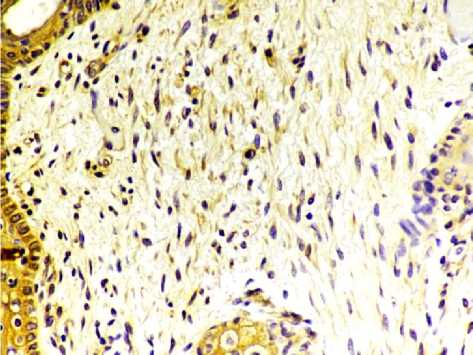
Рис. 1. Микрофото гистологического препарата кожи плода 27 недель разыития. mTOR+-фибробласты. Окр.: см. в тексте. Ув.: х400.
По каждой группе данных рассчитывали средние доли (P) и ошибки долей (p m ), среднюю арифметическую (M) и стандартную ошибку (m). Достоверность влияния возраста или пола на исследуемые параметры кожи оценивали с помощью однофакторного дисперсионного анализа для соответствующих величин. Достоверность отличий между содержанием mTOR+-фибробластов на мм2 в разных возрастных группах оценивали по t-критерию Стюдента. Достоверными считали отличия при р<0,05.
Результаты и обсуждение. Полученные результаты позволяют заключить, что положительную экспрессию mTOR имели кератиноциты, фибробласты, эпителиоциты концевых отделов желез кожи и эндотелиоциты кровеносных сосудов во все изученные возрастные периоды (рис. 1-3).
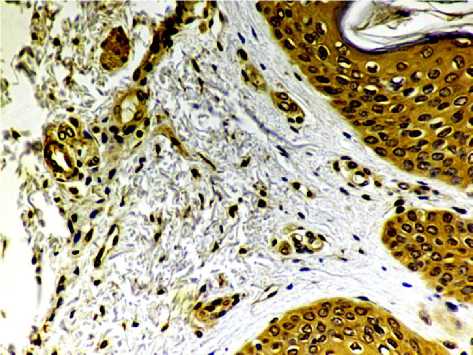
Рис. 2. Микрофото гистологического препарата кожи мужчины 17 лет. mTOR+-фибробласты. Окр.: см. в тексте. Ув.: х400.
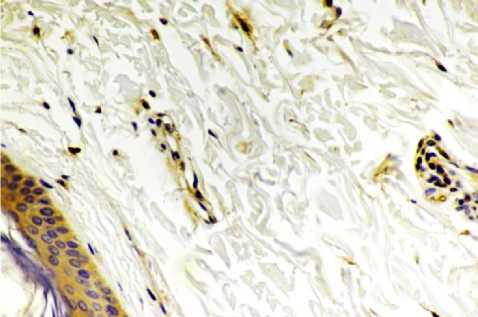
Рис. 3. Микрофото гистологического препарата кожи женщины 55 лет. mTOR+-фибробласты. Окр.: см. в тексте. Ув.: х400
Количественная оценка показала, что 95,1±0,78% фибробластов дермы в 1-й группе плодов 20-40 недель развития были mTOR+ (рис. 4). Таким образом, в антенатальный период, соответствующий гистогенезу кожи человека, преобладающее число фибробластов дермы экспрессируют mTOR. Полученные результаты свидетельствует о значительной роли данного белка в процессе пренатального онтогенеза и согласуются с ключевой ролью mTOR в выживании клеток [2, 8]. Доля фибробластов дермы экспрессирующих mTOR во 2-й возрастной группе, объединяющей аутопсии кожи от рождения до 20 лет, составила 86,4±1,42% (рис. 4). Изменения в численности фибробластов, имеющих положительное окрашивание к mTOR между 1-й и 2-й группами имели статистическую достоверность (p<0,05).
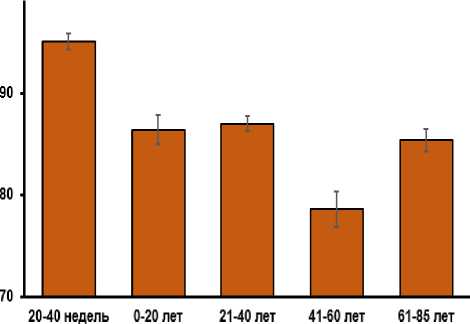
беременности
Рис. 4. Диаграмма долей mTOR+-фибробластов по отношению к общему числу фибробластов в дерме плодов человека и людей разного возраста
В возрастном интервале от 21 до 40 лет (3-я группа) доля фибробластов с положительной окраской к mTOR не имела отличий по сравнению с предыдущим возрастным периодом от 0 до 20 лет (2-я группа) и составила 86,9±0,72% (p>0,05, рис. 4). Доля фибробластов c положительным окрашиванием к mTOR в дерме кожи людей 4-й группы от 41 до 60 лет уменьшилась и составила 78,6±1,75% (рис. 4). Данное значение было статистически достоверным по отношению к 3-й группе 2140 лет (p<0,05). Таким образом, сразу после рождения и до 60 лет мы наблюдали негативную динамику в содержании mTOR+ фибробластов по отношению к общему числу фибробластов в дерме кожи человека. После достижения 60-летнего возраста и до 85 лет содержание mTOR+-фибробластов в дерме человека достоверно увеличилось до 85,4±1,09% (рис. 4), что статистически достоверно превышает параметры характерные для 4-й группы (p<0,05). Результаты дисперсионного анализа подтвердили достоверное влияние возраста на изменение доли mTOR+-фибробластов в дерме человека.
Мы провели подсчет количества клеток с характерным морфологическим строением фибробластов на 1 мм2 дермы имеющих положительное окрашивание к виментину - маркеру промежуточных филаментов соединительнотканных клеток. Количественная оценка доказала постепенное и неуклонное снижение содержания дермальных фибробластов с увеличением возраста. В постнатальном онтогенезе можно выделить два периода: первый, сразу после рождения и до 40 лет, когда происходит наиболее существенное снижение численности фибробластов в дерме и количество клеток фибробластического ряда уменьшается в 3,4 раза по сравнению с фетальным периодом. Второй, начинается после 41 года и продолжается до 85 лет, когда общее число фибробластов в дерме уменьшается незначительно [13]. Достоверное влияние возраста на численность фибробластов в дерме подтверждено дисперсионным анализом.
Некоторыми авторами были получены доказательства уменьшения количества пролиферирующих фибробластов с возрастом [13]. Нами также была подсчитана доля пролиферирующих фибробластов, экспрессирующих PCNA, по отношению к общему числу фибробластов дермы. В возрасте до 40 лет мы наблюдали наибольшее снижение PCNA+-фибробластов в дерме. После 41 года доля фибробластов с экспрессией ядерного антигена пролиферирующих клеток изменялась на уровне тенденции. Влияние возраста на изменение количества имму-нопозитивных к PCNA фибробластов в дерме было статистически значимо по данным дисперсионного анализа (p<0,001).
Подводя итог, можно сделать заключение о том, что доля mTOR+-фибробластов в дерме человека уменьшается с 20 недель беременности до 60 лет. Также мы наблюдали то, что с внутриутробного периода до 85 лет прогрессивно уменьшается общее число фибробластов и доля фибробластов иммунопозитивных к PCNA. Таким образом, динамика изменений содержания mTOR+- фибробластов в период с 20 недель развития до 85 лет частично согласуется с изменениями общего содержания фибробластов и доли PCNA + -фибробластов. В связи с этим можно предположить, что механизм потенциального участия mTOR в регуляции пролиферативной активности дермальных фибробластов зависит от возраста.
Ключевая роль mTOR в клеточном старении связывает старение клеток и организма с возрастными изменениями [15]. Усиленная передача сигналов PI3K/Akt индуцирует клеточное старение через p53-зависимый путь, переводя его в состояние покоя [1, 11]. В этих, склонных к покою, клетках р53 ингибирует путь mTOR, который участвует в программе возрастных изменений [16]. mTOR активирует S6K (ген старения) и подавляет функцию 4E-BP (ген долголетия).
Известно, что mTOR обладает способностью как стимулировать, так и тормозить пролиферацию фибробластов разных локализаций при патологии, включая фибробласты дермы [5], причем экспрессия mTOR, PI3K/Akt в фибробластах при патологических процессах значительно выше, чем в нормальной ткани кожи [17]. В антенатальный период онтогенеза mTOR контролирует накопление биомассы и метаболизм, модулируя ключевые клеточные процессы, включая синтез белка и аутофагию [8]. Вероятно, сразу после рождения включаются механизмы, которые не позволяют далее сохранять повышенный уровень mTOR для поддерживания пролиферации фибробластов. В результате уровень mTOR снижается и продолжает снижаться пролиферативная активность и общее число фибробластов в дерме.
Эффекты mTOR по ингибированию пролиферации фибробластов могут опосредовать ламинин а5 [9], PCNA, TGF-в1 [19]. Сигнальный путь mTOR может опосредовать аутофагию и апоптоз [11]. На примере старения дермы было показано, что активация аутофагии способствует ингибированию фотостарения посредством ингибирования сигнализации PI3K/AKT/mTORC1 [18-19]. Напротив, подавление аутофагии или усиление регуляции mTOR способствует фотостарению [18-20]. Следовательно, можно предположить, что снижение пролиферативной активности фибробластов дермы, наблюдаемое с внутриутробного периода, приводит к компенсаторному снижению содержания mTOR, в том числе в результате уменьшения общей функциональной активности фибробластов. Возможно, mTOR не может реализовать свои эффекты по стимулированию пролиферации с возрастом из-за нарушения в работе вспомогательных белков RAPTOR и RICTOR [1, 14] или есть влияние других регуляторных систем. Однако точные механизмы возрастных изменений доли mTOR позитивных фибробластов и значение mTOR для возрастной регуляции пролиферации клеток дермы остаются неизвестными и требуют дальнейшего изучения.
Заключение. Доля фибробластов экспрессирующих mTOR в дерме человека статистически достоверно уменьшается с 20 недель пренатального развития до 60 лет с 95% до 78%, что доказывает значение возрастного критерия для содержания mTOR-позитивных фибробластов в дерме человека. В постнатальный период наблюдается постепенное уменьшение доли mTOR+-фибробластов. Отрицательная динамика возрастных изменений доли mTOR+-фибробластов в дерме от внутриутробного фетального периода до 60 лет однонаправлена с возрастной динамикой общего числа и пролиферативной активности фибробластов. Таким образом, получены доказательства возрастной специфики участия mTOR в регуляции пролиферации фибробластов в дерме кожи человека.


