Иммунологические и морфологические аспекты диагностики инфекции Helicobacter pylori и вирусов семейства Herpesviridae
Автор: Дудаева Н.Г., Гречушников В.Б., Бугаева И.О., Тарасова Г.Н., Головачева Т.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Глазные болезни
Статья в выпуске: 2 т.6, 2010 года.
Бесплатный доступ
Обследованы 100 пациентов с воспалительными заболеваниями желудочно-кишечного тракта (ЖКТ). Методом полимеразной цепной реакции (ПЦР) определяли микробную составляющую воспалительного процесса: исследовали мононуклеарные клетки (МНК) периферической крови на наличие этиологического микробного фактора. Обнаружено микстинфицирование слизистой оболочки ЖКТ H.pylori и Herpesviridae при заболеваниях гастро-дуоденальной зоны и наличие фрагментов генома этих микроорганизмов в МНК периферической крови, что может иметь существенное значение в патогенезе заболеваний ЖКТ и является основанием для дальнейшего изучения
Мононуклеарные клетки периферической крови, патология жкт
Короткий адрес: https://sciup.org/14917078
IDR: 14917078
Immunological and morphological aspects of diagnostics of Helicobacter pylori infection and Herpesviridae viruses
100 patients with inflammatory diseases of gastrointestinal tract were examined. Microbial component of inflammation process was detected by means of polymerase chain reaction (PCR). By means of PCR etiological microbial factor of mononuclear cells in peripheral blood (MCPB) was investigated. Mixtinfication of mucosa membrane of gastrointestinal tract with H. pylori and Herpesviridae in pathology of gastroduodenal area and presence of fragments of microorganisms DNA in PBMC were revealed. This phenomenon may be important in pathogenesis of pathology of gastrointestinal tract and forms the basis for its further investigation
Текст научной статьи Иммунологические и морфологические аспекты диагностики инфекции Helicobacter pylori и вирусов семейства Herpesviridae
Согласно рекомендациям Американской коллегии гастроэнтерологов (2005) и Европейской группы по изучению H.pylori («Маастрихт-3», 2005г.) диагноз инфекции H.p. должен устанавли в аться преимущественно неинвазивными методами диагностики [1].
Несмотря на значительные достижения в диагностике и лечении Н.р.-ассоциированных заболеваний сохраняются проблемы верификации бактерии. Нередко выявление Н.р.-инфекции проводится лишь одним из лабораторных методов. Наиболее популярными являются иммуноферментный анализ (ИФА) и полимеразная цепная реакция (ПЦР). Однако они не являются абсолютными, дающими максимально объективные результаты.
Достоверная и своевременная диагностика H.p. позволяет избежать необоснованного назначения антибактериальных препаратов, а также адекватно контролировать проводимую антихеликобактерную терапию. Несмотря на большое количество методов определения H.p-инфекции постоянно идет поиск и модификация неинвазивных или малоинвазивных способов диагностики этой инфекции [2, 3].
ткани, ассоциированной со слизистой (MALT), в сочетании с H.p. и в неповрежденной СО [7]. Есть данные о том, что варицелла зостер вирус (ВЗВ) может быть причиной развития необъясненной патологии органов пищеварения, в том числе и гастритов [8].
Не так давно идентифицированы новые вирусы группы герпеса: вирус герпеса 6 типа (ВГЧ-6), – 7 типа (ВГЧ-7) и 8 типа (ВГЧ-8). Роль этих вирусов в патологии человека обсуждается. Однако уже известно, что они играют определенную роль в усилении пролиферативных процессов. Эти вирусы так же обнаруживаются в СО ЖКТ как при патологии, так и в неизмененной ткани [9].
Интересными представляются данные о «вне-желудочных проявлениях», обусловленных инфекцией H.p. Опубликованы результаты клинических и экспериментальных работ, в которых показано присутствие фрагментов генома H.p. в атеросклеротических бляшках кровеносных сосудов [10]. В этой связи представляет определенный интерес изучение вопроса о присутствии фрагментов ДНК H.p. в моно-нуклеарных клетках (МНК).
В связи с вышеизложенным, целью нашего исследования явилось изучение вирусов группы герпеса в СО гастродуоденальной области, а также определение фрагментов ДНК H.p. в МНК периферической крови у пациентов с верифицированной инфекцией H.p.
Присутствие микроорганизма в СОЖ определяли в биопсийном материале методом полимеразной цепной реакции (ПЦР) с использованием коммерческих наборов «Хеликопол», НПФ «Литех» (Россия) на наличие участков генома H.р.. (ure С, cag A-, vac A-генов). В клеточных суспензиях методом ПЦР определяли фрагменты генома (ure C, vac m1, ice a1, bab a1), кодирующие факторы патогенности микроорганизма (использование тест-систем производства НПФ «Литех»). Ферментативную активность Н.р. в биоптате определяли с помощью уреазного теста «H.pylori Quick Test» (Финляндия).
Для определения иммуноглобулинов в периферической крови, специфических к Н.pylori, использовали ИФА тест-системы Euroimmune ( I g A , IgG) , Германия, и «Хелико-Бест антитела» (суммарные антитела к Cag A белку). Кроме того, методом ПЦР исследовали МНК периферической крови на носительство ДНК Н.рylori с использованием указанных наборов для ПЦР. МНК периферической крови, выделяли на градиенте плотности фиколл-урографин (с=1,077) и разделяли на субпопуляции CD4, CD8, CD25 методом иммуномагнитной сепарации, реактивами фирмы «Dynal» (Норвегия).
Для обнаружения вирусов – ВЗВ, ЭБВ, ЦМВ, вирусов герпеса человека 6,-7,-8 типов (ВГЧ-6,-7,-8) использовали готовые наборы фирм-производителей: «Амплисенс», «Биоком», «Литех», «ДНК-технология» (Москва); «Вектор-Бест» (Новосибирск). Амплификацию проводили на амплификаторах «Терцик» («ДНК-технология», Москва).
Статистический анализ результатов исследования проводили с использованием общепринятых методов. Достоверность различий определяли с использованием критерия Краскелла-Уоллеса. Коэффициент корреляции определяли по методу ранговой корреляции Спирмена.
Результаты. При определении специфических антител к H.p. было получено, что группа больных с деструктивными поражениями СОЖ достоверно отличалась от группы с поверхностными изменениями СОЖ по суммарным антителам к Cag A белку (средний индекс позитивности по группам составил 9,4 и 7,5 соответственно, р<0,05). По IgA и IgG отмечалось достоверное различие в зависимости от вида повреждения СОЖ (р< 0,01).
Определение ДНК Н.p в МНК периферической крови дало положительные результаты в 1 группе больных в 20% случаев и во 2 группе – в 49,5 %. При этом, частота определения генов cag A была выше при поверхностном воспалении, а ген vac Аs 1 и vac As2 чаще определялся в группе с деструктивными изменениями (рис. 1).
В МНК периферической крови, полученных от пациентов с различной степенью деструкции (эрозивные и язвенные изменения) СО гастро – дуоденальной зоны, фрагменты генома ure C, ice a1 и bab a1 в общей популяции МНК были обнаружены у всех пациентов. В субпопуляции CD4 фраг м енты ice a1 обнаружены у 42,9%, bab a1 – у 57,1%. В клетк а х с фенотипом CD8 обнаружили фрагмент ice a1 у 42,9%, причем одновременное нахождение этого гена в CD4 и CD8 клет к ах было только в 28,6% случаев. В суспензии клеток с фенотипом CD25 обнаруживали только фрагмент bab a1 у 47,6% пациентов. Одновременное присутствие фрагментов ice a1 и bab a1 в CD4, CD8 и CD25 наблюдалось у 60% пациентов (рис. 2).
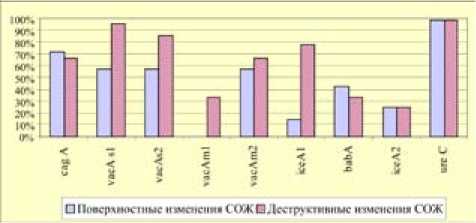
Рис. 1 . Частота встречаемости генов патогенности H.p. в МНК периферической крови
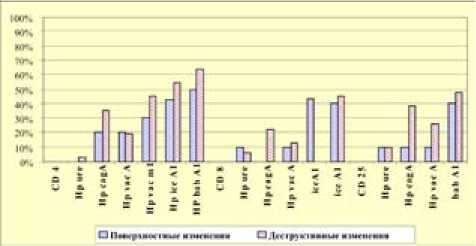
Рис. 2. Частота встречаемости фрагментов генома H.p. в субпопуляциях МНК периферической крови

Результаты ПЦР в биоптатах и Quick Test полностью совпадали. Во всех случаях обнаружения H.p. в СО присутствовал фрагмент генома, кодирующий С-субъединицу уреазы (ure C) .
При деструктивных воспалительных процессах (2 группа) наиболее часто определяли наличие более агрессивных штаммов Н.р ( cagA+vacA+). При этом частота обнаружения агрессивных штаммов инфекции имела четкую положительную корреляцию со степенью повреждения СО (r = 0,8). У пациентов с деструкцией СО H.p. был обнаружен у 95% пациентов, из них в 80% случаев определяли ульцероген-ный (cagA+vacA+) штамм. В группе с поверхностным гастритом (1 группа) инфицирование СО H.pylori было обнаружено у 64 % пациентов, однако из них у 35,7 % обнаружили cagA- vacA- штамм Н.р., а cagA-vacA+ и cagA+vacA+ в 13,8 % и 14,5 % соответственно (рис. 3).
Положительные результаты ИФА при отрицательных данных на Н.р., при исследовании биоптата методом ПЦР и Quick Test, были получены у 5 па ц иентов из первой группы (11%) и у 6 – из второй (17,6%), что можно было объяснить следовыми реакциями на ранее перенесенную Н.р. инфекцию.
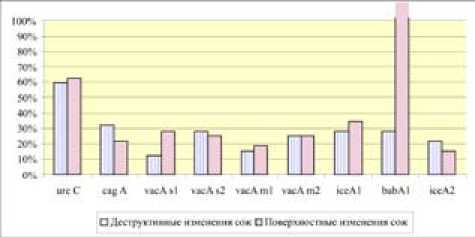
Рис. 4. Частота встречаемости генов патогенности H.p. в биоптате СОЖ
0Н!»1« В1ИЧ' > О АВ П(ЧЧ* В11ГЧ ? BlU'M QILMK
Рис. 5. Частота обнаружения вирусов Herpesviridae в СОЖ
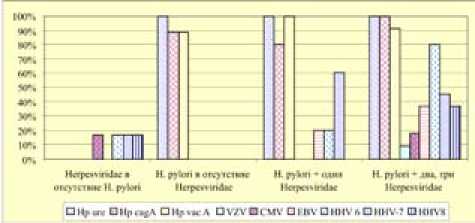
Рис. 6. Частота обнаружения микроорганизмов при различных типах инфицирования СОЖ
Изучение генов патогенности H.p. в биоптатах показало различную частоту их встречаемости при поверхностных и деструктивных изменениях СОЖ (рис. 4).
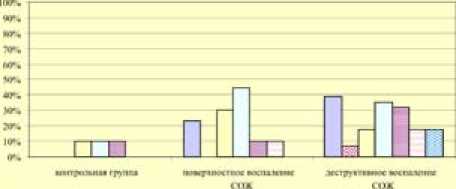
При исследовании биопсийного материала, полученного при гастроскопии, методом ПЦР ВПГ-1 и ВПГ-2 ни у одного пациента обнаружено не было. Вероятно, это объясняется небольшим объемом выборки. Частота обнаружения других представителей вирусов герпеса была следующая. У пациентов при отсутствии жалоб со стороны ЖКТ и без изменений СО по данным эндоскопии и гистологических изменений (контрольная группа) были обнаружены только ВЭБ – 10% случаев, а также вирусы герпеса человека 6 типа (ВГЧ-6) и 7 типа (ВГЧ-7) в 10% случаев каждый. При поверхностном воспалении ВЭБ обнаруживали в 30% случаев, ВГЧ-6 в 44,4% случаев, а вирусы герпеса человека 7 и 8 типов (ВГЧ-7, -8) в 10% случаев соответственно. При деструктивных изменениях СО частота встречаемости составила: ВЗВ – 7,1%, ВЭБ – 17,6%, ЦМВ – 14,3%, ВГЧ-6 – 35,3%. ВГЧ-7 – 32,4%, ВГЧ-8 – 17,5% (рис. 5).
При изучении типа инфицирования СО вирусами герпеса и H.p. были выявлены различные сочетания бактериально-вирусной контаминации и частоты встречаемости микроорганизмов: моноинфицирова- ние H.p., моноинфицирование вирусами герпеса и микст-инфицирование H.p. и одним или несколькими представителям Herpesviridae (рис. 6).
Обсуждение. Данные исследования подтверждают, что ведущий вклад в развитие хронических воспалительных заболеваний гастродуоденальной области, безусловно, вносит H. p и, в первую очередь, ее патогенные штаммы. Частота их выявления, а так же уровни специфических антител прямо связаны с характером и глубиной поражения СО.
Имеет место несовпадение результатов серологической диагностики хеликобактериоза методом ИФА и исследований биопсийного материала этих же пациентов методами ПЦР и быстрым уреазным тестом (Quick Test). Вероятно, это явление связано со следовыми реакциями на ранее перенесенную Н.р.-инфекцию.
Несомненно, что вирусы герпеса не только принимают участие в патологическом процессе, но и развивают его по провоспалительному типу. Неэффективность традиционных схем эрадикации H.p. в большинстве случаев и достаточно частые рецидивы заболевания могут быть, обусловлены присутствием вирусов в очаге воспаления, которые направляют и развивают воспалительный процесс «по замкнутому кругу», создавая условия, благоприятные для длительной персистенции H.р. и других патогенных микроорганизмов.
Наличие в МНК фрагментов генома H.p., в частности генов, кодирующих экспрессию цитотоксических и адгезивных белков микроорганизма, в настоящее время объяснить достаточно сложно. Тем не менее, этот факт, вероятно, свидетельствует о вовлечении в инфекционный процесс при хеликобактериозе организма в целом, а не ограничивается только поражением СО ЖКТ.
Поскольку известна роль вирусов, в частности вирусов группы герпеса, в патологии ЖКТ и их совместной персистенции с H.p. на СО логично предположение, что вирусы могут являться вектором доставки генетического материала H.p. в мигрирующие иммунокомпетентные клетки. С другой стороны, H.p. может локализоваться на поверхности клеток посредством молекул адгезии ICAM-1, относящегося к суперсемейству иммуноглобулинов и служащего лигандом для в2-интегринов (LFA-1, Mac-1). Известно, что последние экспрессируются на лейкоцитах, эндотелии сосудов, фибробластах, эпителии [9].
Заключение.
-
1. Данные исследования подтвержда ю т, что ведущий вклад в развитие хронических воспалительных заболеваний гастродуоденальной области, безусловно, вносит H. p. и, в первую очередь, ее пато г енные штаммы. Частота их выявления, а так же уровни специфических антител прямо связаны с характером и глубиной поражения СО.
-
2. Несовпадение результатов серологической диагностики хеликобактериоза методом ИФА, ПЦР и быстрым уреазным тестом (Quick Test) связано
-
3. Нефагоцитирующие клетки (CD4+, CD8+) могут являться носителями участков генома H.p. При этом часть из них является активированными клетками, экспрессирющими рецептор к интерлейкину-2 (CD25+). Аналогичные д анные получены в суспензиях клеток, выделенных из биопсийного материала.
-
4. H.р. и герпесвирусная инфекция приводят к прогрессирующей деструкции СО гастродуоденальной области, создавая условия, благоприятные для длительной персистенции H.р. и других патогенных микроорганизмов.
-
5. Вирусы группы герпеса, вероятно, принимают непосредственное участие в патогенезе развития гастритов и язвенной болезни ЖКТ. Чем глубже степень повреждения СО, тем чаще и в более разнообразном сочетании определяются представители Herpesviri-dae и патогенные штаммы H. р.
со следовыми реакциями на ранее перенесенную Н.рylori инфекцию. Обнаружение фрагментов генома H.p. в МНК возможно отражает системную реакцию организма на H.p.
Список литературы Иммунологические и морфологические аспекты диагностики инфекции Helicobacter pylori и вирусов семейства Herpesviridae
- Исаков В.А. Маастрихт-3 -2005: Флорентийская мозаика противоречий и компромиссов//Экспер. и клин. гастро-энтерол. 2006. № 1. С. 78-83.
- Баранская Е.К., Ивашкин В.Т., Лапшин А.В. и др. Диагностическое значение лазерного 13 С-уреазного дыхательного теста при различных Helicobacterpylori ассоциированных заболеваниях//Клин. мед. 2006. № 8. С. 47.
- Губергриц Н.Б., Синяченко О.В., Белоконь Т.М. и др. Новые неинвазивные тесты для диагностики инфекции Helicobacterpylori//Сучасна гастроентерологя. 2004. № 2. С. 24-32
- Tsamakidis К., Panotopoulou Е., DimitroulopoulosD. etal. Herpessimplexvirustype 1 inpepticulcerdisease: aninverseassociationwithHelicobacterpylori//WorldJGastroenterol. 2005. №11 (42). Р. 6644-6649.
- Yokose N., Tanabe Y.E. An et al. Acute gastric mucosal lesions associated with cytomegalovirus infection in a non-immu-nocompromised host//Intern Med. 1995. № 34 (9). Р.883-5.
- Leimola-Virtanen R., Happonen P., Syrjnen S. Cytomegalovirus (CMV) and Helicobacter pylori (HP) found in oral mucosal ulcers//J.Oral Pathol. Med. 1995. №1. Р. 14-17.
- Luo B., Wang Y., Wang X.F. et al. Correlation of Epstein-Barr virus and its encoded proteins with Helicobacter pylori and expression of c-met and c-myc in gastric carcinoma//World J Gastroenterol. 2006. № 12. Р. 1842-8.
- Stratman E. Visceral zoster as the presenting feature of disseminated herpes zoster//J Am Acad Dermatol. 2002. № 46 (5). Р. 771-4.
- Halme L., Arola J., H^kerstedt К., Lautenschlager I. Human herpesvirus 6 infection of the gastroduodenal mucosa//Clin Infect Dis. 2008. №46 (3). Р. 434-9.
- Kowalski M. Helicobacter pylori (H. pylori) infection in coronary artery disease: influence of H. pylori eradication on coronary artery lumen after percutaneous transluminal coronary angioplasty. The detection of H. pylori specific DNA in human coronary atherosclerotic plaque//J. Physiol. Pharmacol. 2001.№ 52 (1). Р. 3-31.


