Иммунологические показатели ротовой жидкости больных эрозивно-язвенной формой красного плоского лишая в полости рта на фоне комбинированного метода лечения
Автор: Македонова Ю.А., Фирсова И.В., Поройская А.В., Марымова Е.Б.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Стоматология
Статья в выпуске: 1 (57), 2018 года.
Бесплатный доступ
При лечении красного плоского лишая в полости рта отмечается резистентность к проводимой терапии, увеличение доли тяжёлых форм, приводящих к малигнизации процесса, вовлечение в патологический процесс не только кожи, но и слизистых оболочек рта, желудочно-кишечного и мочеполового трактов. Среди причин болезни большую роль отводят иммунным нарушениям. Воспалительный процесс в полости рта представляет собой очень тонко регулируемый баланс между про- и противовоспалительными медиаторами, которые обеспечивают нейтрализацию вредоносных эффектов раздражения и минимизацию повреждения собственных тканей. В данной работе проведено динамическое изучение цитокинового профиля на фоне комбинированного метода лечения (аппликации Тизоля с L-аргинином в сочетании с инъекциями тромбоцитарной аутоплазмой) у больных эрозивно-язвенной формой красного плоского лишая в полости рта. Доказано, что под действием предложенного метода лечения увеличивается способность слизистой оболочки полости рта к иммунологической защите.
Цитокины, красный плоский лишай, полость рта, лечение
Короткий адрес: https://sciup.org/142216657
IDR: 142216657 | УДК: 616.314-089.27
Immunological indicators of the oral liquid of patients with erosive ulcerous form of red flat lichen in the oral cavity on the background of the combined method of treatment
In the treatment of red flat lichen in the oral cavity, resistance to therapy is observed, an increase in the proportion of severe forms leading to malignization of the process, involvement in the pathological process of not only the skin, but also the mucous membranes of the mouth, gastrointestinal and genito-urinary tracts. Among the causes of the disease, a large role is assigned to immune disorders. The inflammatory process in the oral cavity represents a very finely regulated balance between pro- and anti-inflammatory mediators, which ensure neutralization of harmful irritation effects and minimization of damage to own tissues. In this work, a dynamic study of the cytokine profile was performed against the background of a combined treatment (Tisol application with L - arginine in combination with platelet autoplasmic injections) in patients with erosive ulcerous form of red flat lichen in the oral cavity. It is proved that under the action of the proposed method of treatment, the ability of the oral mucosa to immunological defense increases.
Текст научной статьи Иммунологические показатели ротовой жидкости больных эрозивно-язвенной формой красного плоского лишая в полости рта на фоне комбинированного метода лечения
Существенная роль в этиопатогенезе красного плоского лишая слизистой оболочки полости рта отведена эпителиоцитам: после активации они продуцируют провоспалительные цитокины в значительно большем количестве, чем моно-нуклеарные клетки, инфильтрирующие поражен- ные ткани [11]. При развитии аутоиммунных заболеваний, иммунодефицитных состояний, в том числе и таких как КПЛ СОПР, наблюдается изменение уровня цитокинов в крови и биологических жидкостях (в ротовой жидкости), нередко коррелирующее с тяжестью процесса [5].
Диагностическое значение определения цитокинов значительно возрастает при их исследовании непосредственно в очаге воспалительного процесса [4]. С этой целью используется определение цитокинов непосредственно через жидкости в полостях, т. е. в смешанной слюне полости рта [7]. Содержание цитокинов в ротовой жидкости не коррелирует с их уровнем в крови, что ещё раз доказывает автономность местного иммунитета полости рта. Они регулируют межклеточные и межсистемные взаимодействия, определяют выживаемость клеток, стимуляцию или подавление их роста, дифференциацию, функциональную активность и апоптоз, а также обеспечивают согласованность действия иммунной, эндокринной и нервной систем в нормальных условиях и в ответ на патологические воздействия [3].
Провоспалительные цитокины обеспечивают мобилизацию воспалительного ответа (интерлейкины-1, -2, -6, -8, ФНОα, интерферон γ), а противовоспалительные – ограничивают развитие воспаления (интерлейкины-4, -10, TGFβ). Регуляторы клеточного и гуморального иммунитета – (естественного или специфического) обладают собственными эффекторными функциями (противовирусными, цитотоксическими) [2].
Соотношение между противовоспалительными и провоспалительными цитокинами – важный момент в регуляции возникновения и развития воспалительного процесса. От этого баланса зависит и течение болезни, и исход ее. Именно цитокины стимулируют выработку факторов свертываемости крови в клетках эндотелия сосудов, продукцию хондролитических ферментов, способствуют образованию рубцовой ткани [1].
Интерлейкин ИЛ-1, является лимфоцитак-тивирующим фактором, эндогенным пирогеном, эндогенным медиатором лейкоцитов. Существует в 2 изоформах: ИЛ-1α и ИЛ-1β. ИЛ-1 производится в основном макрофага-ми/моноцитами, а так же фибробластами, эдотелиальными, дендритными клетками, естественными клетками – киллерами, В-клетками. ИЛ-1 вызывает ряд системных эффектов, таких как жар и синтез острофазных белков, простагландинов, стимулирует гипералгезию. Местно ИЛ-1 активирует Т- клетки и стимулируют их к производству ИЛ-2 и простагландинов [6].
ИЛ-1 и фактор некроза опухолей (ФНО) также активируют эндотелиальные клетки и индуцируют экспрессию адгезивных молекул на их мембране, тем самым помогая к привлечению клеток воспаления к месту воспаления.
Биологическое действие ИЛ-1β проявляется в активизации лимфоцитов и макрофагов, усилении клеточной адгезии и в развитии острой фазы воспаления. Интерлейкин ИЛ-1β вместе с другими провоспалительными цитокинами участвует в деградации внеклеточного матрикса, способствует разрушению тканей слизистой и развитию самоподдерживающегося воспалительного процесса [10].
Цитокины II типа – противовоспалительные. Они регулируют активность провоспали-тельных цитокинов. Цитокины в большей степени участвуют в гуморальном иммунитете, т. е. в продукции антител, иммуноглобулина Е и активации эозинофилов, кроме того они имеют важную функцию ингибирования большинства провоспалительных функций, вызванных другими цитокинами и играют важную роль в гемостазе. Таким образом, Th2 – цитокины регулируют иммунный ответ. Эта функция в основном осуществляется за счет ИЛ-4, ИЛ-10, ИЛ-13 [9].
Интерлейкин ИЛ-4 является фактором стимуляции В-клеток. Источником продукции ИЛ-4 являются тучные клетки, Т-клетки. Причем в основном синтез ИЛ-4 связывают с клетками субпопуляции Тh (Т-хелперов) типа Тh2. Клетками-мишенями для ИЛ-4 являются Т-, В-клетки, моноциты, эндотелиальные клетки, фибробласты.
Таким образом, можно рассматривать слизистую оболочку полости рта в качестве «иммунокомпетентного органа», и через содержание в смешанной слюне показателей иммунной защиты, таких как иммуноглобулины, интерлейкины, оценивать состояние слизистой оболочки, её иммунное здоровье, которое имеет свою генетическую детерминированность у каждого человека.
ЦЕЛЬ РАБОТЫ
С целью оценки местного иммунологического статуса больных эрозивно-язвенной формой красного плоского лишая на фоне лечения было проведено иммунологическое исследование нестимулированной смешанной слюны.
МЕТОДИКА ИССЛЕДОВАНИЯ
В качестве материала для исследования была взята ротовая жидкость больных (30 человек) КПЛ слизистой полости рта. Забор не-стимулированной смешанной слюны был проведен у больных по общепринятой стандартной методике. Образцы слюны больных собирали в первой половине дня. Пациентам перед забором слюны рекомендовалось воздержаться от приема пищи, курения, а непосредственно перед процедурой – прополоскать рот. Образцы слюны были собраны в 1,5 мл микропробирки «Эппендорф» и немедленно заморожены при температуре –20 °С до использования. Проводилось определение иммунологических показателей (уровень sIgA, IgM, IgG), цитокинов с провоспалительным (IL TNFα, ИЛ-1β, ИЛ-8, IFNα) и противовоспалительным действием (IL-4) с помощью метода твердофазного иммуно-ферментного анализа (ИФА) с использованием стандартных наборов в соответствии с инструкциями производителя.
На момент первичного обследования до начала лечения у 120 пациентов отмечались следующие значения показателей местного иммунитета ротовой жидкости. Уровень про-воспалительных цитокинов составил: интерлей-кин-1β (IL-1β) – (41,24 ± 1,87) пг/мл, интерлейкин – 8 (IL-8) – (51,3 ± 1,21) пг/мл, фактор некроза опухоли альфа (Tumor necrosis factor – TNFα) – (3,95 ± 0,37) пг/мл, интерферон гамма (IFNγ) – (6,33 ± 0,54) пг/мл. Концентрация противовоспалительного цитокина интерлейкина – 4 (IL-4) составила (10,1 ± 1,3) пг/мл. Уровень иммуноглобулина А (sIgA) составил (0,43 ± 0,01) МЕ/мл, иммуноглобулина G (IgG) – (0,022 ± 0,001) МЕ/мл, иммуноглобулина М (IgМ) – (0,15 ± 0,01) МЕ/мл. Приведенные данные свидетельствуют о том, что у больных наблюдается выраженный воспалительный процесс в полости рта, о чем свидетельствует повышенная концентрация про-воспалительных цитокинов.
Пациентам применяли комбинированный метод, заключающийся в аппликационном применении лекарственной композиции тизоля с L-аргинином в сочетании с инъекциями тромбоцитарной аутоплазмы (PRP-терапия). Контроль эффективности лечения больных с КПЛ осуществляли на основе определения локального цитокинового профиля и иммуноглобулинов в ближайшие сроки наблюдения (на 3-й, 7-й, 14-й, 21-й день).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Так, на 3 день уровень провоспалительных цитокинов заметно снизился, но уменьшение показателей цитокинового профиля было статистически недостоверно по отношению к первоначальным данным. IL-1β составил (35,6 ± 1,1) пг/мл, IL-8 – (46,3 ± 1,04) пг/мл, TNFa – (3,1 ± 0,33) пг/мл, IFNy – (5,52 ± 0,23) пг/мл (р > 0,05). Концентрация IL-4 равнялась (11,5 ± 2,1), что на 13,8 % выше относительно начала лечения (р > 0,05).
Концентрация sIgA незначительно увеличилась и составила (0,43 ± 0,03) МЕ/мл, IgG – (0,021 ± 0,001) МЕ/мл и IgM – (0,17 ± 0,01) МЕ/мл.
Уже через неделю после начала лечения наблюдалась тенденция к снижению уровня про-и противовоспалительных цитокинов. Причем данная разница была статистически достоверной как к первоначальным данным (р < 0,05), так и относительно 3-го дня лечения (р < 0,01). Уровень IL-1 β уменьшился в 1,4 раза относительно первого дня лечения (р < 0,05) и в 1,2 раза по отношению к 3-дневному показателю (р < 0,01) и составил (29,6 ± 0,34) пг/мл. Концентрация IL-8 также достоверно уменьшилась относительно ранних сроков наблюдения и составила (33,1 ± 0,71) пг/мл. TNFa уменьшился на 54,9 % по отношению к первоначальному значению [(2,55 ± 0,22) пг/мл и (3,95 ± 0,37) пг/мл, при р < 0,05], относительно 3-го дня данный показатель уменьшился на 21,5 %, но данная разница была статистически недостоверной (р > 0,05). Интерферон гамма достоверно уменьшился относительно 1-го дня (на 34,7 %) и 3-го дня (на 17,4 %) и составил (4,7 ± 0,12) пг/мл (при р < 0,05 и р < 0,01 соответственно). Противовоспалительный цитокин IL-4 достоверно не изменил своего показателя и равнялся (10,5 ± 0,3) пг/мл, то есть практически вернулся к своим первоначальным данным, что характеризует отсутствие прироста данного значения.
Отсутствие повышения концентраций характерно и для иммуноглобулинов, которые оставались на прежнем уровне: sIgA – (0,42 ± 0,08) МЕ/мл, IgG – (0,020 ± 0,001) МЕ/мл и IgM – (0,17 ± 0,01) Ме/мл. Эти данные свидетельствуют о том, что в полости рта происходит постепенное стихание воспалительных процессов на фоне запуска компенсаторных возможностей организма. Таким образом, уже через семь дней после начала лечения регистрировалась инициация процесса восстановления баланса цитоки-нового профиля, что подтверждало уменьшение выраженности воспалительных явлений в полости рта. Подобная динамика уровня цитокинов связана с осуществлением местной противовоспалительной, противоотечной и обезболивающей медикаментозной терапии, на фоне регенерирующей, стимулирующей местный иммунитет PRP-терапии, что привело к существенному снижению антигенной нагрузки на иммунную систему обследованных лиц.
Через две недели после начала обследования описанные выше тенденции сохранялись. К данному периоду наблюдений диагностировалось достоверное снижение концентрации IL-1β [(10,4 ± 0,11) пг/мл], данное значение было достоверно меньше относительно всех сроков наблюдения (р < 0,05 и р < 0,01). Уровень IL-8 составил (21,8 ± 0,97) пг/мл, что было достоверно ниже относительно 1-го, 3-го и 7-го дня (р < 0,05 и р < 0,01). Фактор некроза опухоли также достоверно уменьшился по срокам наблюдения и равнялся (1,13 ± 0,22) пг/мл (при р < 0,05 и р < 0,01). Аналогичная тенденция наблюдалась и при определении концентрации интерферона гамма, который достоверно уменьшился относительно всех сроков наблюдения и составил (3,8 ± 0,24) пг/мл. IL-4 также достоверно снижался – (6,9 ± 0,1) пг/мл (р < 0,05 и p < 0,01), вероятно за счет действия L-аргинина, способствующего увеличению концентрации NO-синтазы, которая, помимо того что обеспечивает синтез NO, также контролирует биосинтез интерлейкина-4, относящегося к ингибиторам воспалительной реакции на фоне применения инъекций тромбоцитарной аутоплазмы. Достоверно увеличилась концентрация sIgA относительно всех сроков наблюдения и составила (0,52 ± 0,01) МЕ/мл, что характеризует ускорение механизма адаптивного ответа и противостоит развитию хронизации воспалительного процесса в полости рта. Отсутствие повышения концентрации IgG и IgM [(0,020 ± 0,001) МЕ/мл и (0,16 ± 0,01) МЕ/мл] также свидетельствует о развитии воспалительного процесса. Таким образом, к 14-му дню лечения начинал постепенно проявляться эффект потенцирования иммунного ответа, возникающий на фоне применения комбинированного метода лечения. Вероятно, что сочетание лекарственной композиции тизоля с L-аргинином и инъекций тром- боцитарной аутоплазмы потенцируют действие друг друга, проявляющийся в усилении местного терапевтического эффекта на фоне направленной регенерации соединительной ткани в полости рта.
На 21-й день наблюдений уровень про- и противовоспалительных цитокинов продолжил снижаться. К этому моменту концентрации цитокинов были статистически достоверно ниже, чем аналогичные показатели, выявленные на момент первичного обследования (p < 0,05) и относительно 3-го и 7-го дней лечения (р < 0,01). Относительно предыдущих данных (14 дней) достоверной разницы по некоторым показателям получено не было (р > 0,05). IL-1β – (10,2 ± 0,33) пг/мл, IL-8 – (22,3 ± 0,12), TNFa – (1,11 ± 0,11) пг/мл и IFNy – (3,0 ± 0,13) пг/мл, IL-4 – (6,3 ± 0,2) пг/мл, sIgA – (0,58 ± 0,04) МЕ/мл, IgG – (0,019 ± 0,001) МЕ/мл и IgM – (0,10 ± 0,01) МЕ/мл.
Так, уровень провоспалительных цитокинов достоверно снижался на всех сроках наблюдения и по отношению к первоначальным значениям (см. рис.).
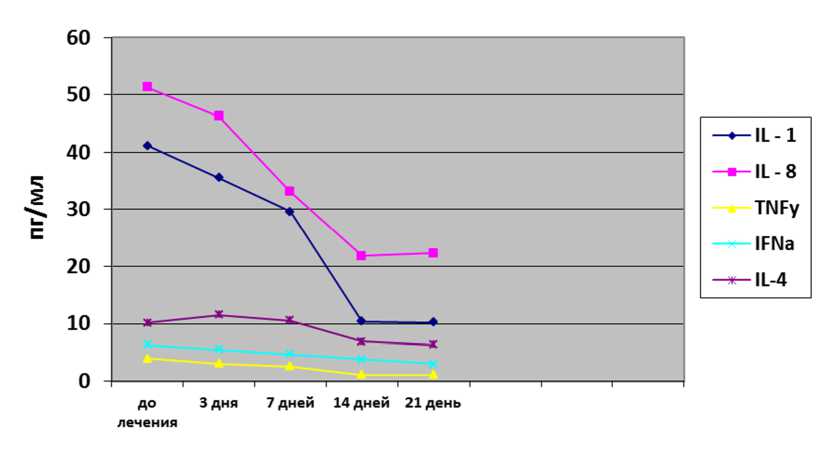
Рис. Динамика цитокинового профиля на фоне комбинированного метода лечения КПЛ
Провоспалительные цитокины продуцируются и действуют на иммунокомпетентные клетки, инициируя воспалительный ответ. Снижение их концентрации является отражением активности и уменьшением тяжести воспалительного ответа. Противовоспалительный цитокин IL-4, регулирующий специфические иммунные реакции и ограничивающий развитие воспаления, также достоверно снижался на всех этапах наблюдения относительно 1-го и 7-го дня. Таким образом, показанный механизм действия L-аргинина в составе аквакомплекса титана глицеросольвата (тизоль) на воспалительный процесс оказывает хороший терапевтиче- ский эффект, что подтверждается проведенным исследованием. Тизоль способствует точной доставке L-аргинина в неизменном виде в очаг воспаления. Далее под действием NО-синтазы происходит синтез NO из L-аргинина. Промежуточным первичным продуктом при превращении L-аргинина является N-гидрокси-L-аргинин. Далее N-гидрокси-L-аргинин под воздействием супероксиданиона продолжает метаболизироваться, генерируя при этом оксид азота. При этом основным индуктором индуцибельной NО-синтазы (iNOS) является IFNγ, а активатором – тетрагидроптерин, который, в свою очередь, активируется TNFα. Оптимальное условие индук- ции iNOS – сочетанное действие IFNγ и TNFα. В то же время увеличение концентрации L- аргинина в тканях способствует увеличению концентрации NO-синтазы, которая, помимо того что обеспечивает синтез NO, также контролирует биосинтез интерлейкинов IL-4, IL-11, IL-13, относящиеся к ингибиторам воспалительной реакции. Отмечено, что применение инъекций тромбоцитарной аутоплазмы улучшает оксигенацию тканей, которая в свою очередь, повышает фагоцитарную, бактерицидную способность иммунных клеток организма. Полученные иммунологические данные подтверждают клиническую эффективность комбинированного метода лечения эрозивно-язвенной формы КПЛ.
ЗАКЛЮЧЕНИЕ
Изменение концентрации про- и противовоспалительных цитокинов является следствием ингибирования воспаления, что очень важно для предотвращения обширного разрушения ткани, в противном случае воспалительный процесс продолжается, становится хроническим, приводя к значительному разрушению ткани. В полости рта происходит нормализация иммунного ответа, активация системы клеточного комплемента.
Таким образом, очевидно, что под действием комбинированного метода лечения эрозивно-язвенной формы КПЛ увеличивается способность слизистой оболочки полости рта к иммунологической защите.
Список литературы Иммунологические показатели ротовой жидкости больных эрозивно-язвенной формой красного плоского лишая в полости рта на фоне комбинированного метода лечения
- Модификация цитокинового профиля у больных красным плоским лишаем Реаферон-ЕС-Липинтом/А. Р. Антонов //Фундаментальные исследования. -2006. -№ 9. -С. 95-97.
- Оскольский, Г. И. Состояние местного цитокинового статуса и его патогенетическое значение при красном плоском лишаем слизистой оболочки полости рта/Г. И. Оскольский, Е. Б. Загородняя//Дальнев. мед. журн. -2010. -№ 4. -С. 32-34.
- Перспективы исследования смешанной слюны у детей при хронических заболеваниях/В. А. Филонов //Дальневосточный медицинский журнал. -2014. -№ 1. -С. 113-116.
- Петрова Т. Г. Дисбаланс цитокинов в ротовой жидкости при воспалительных заболеваниях пародонта у пациентов с лимфомами//Сибирский консилиум. -2007. -Т. 62, № 7. -С. -63-69.
- Разработка и клиническое применение нового ранозаживляющего средства для лечения заболеваний слизистой оболочки полости рта у детей и подростков/А. А. Григорьян //Современные проблемы науки и образования. -2013. -№ 2. -С. 41.
- Ротовая полость и её секреты как система антибактериальной и антирадикальной защиты организма/П. Г. Сторожук //Аллергология и иммунология. -2009. -Т. 10, № 3. -С. 350-357.
- Смирнова, Ю. А. Скрининговые методы диагностики онкологических заболеваний слизистой оболочки рта/Ю. А. Смирнова, Т. Н. Позднякова//Актуальные проблемы стоматологии: матер. всерос. науч.-практич. конф. -М, 2011. -С. 120-125.
- A comparative study of apoptosis in reticular and erosive oral lichen planus/J. M. Brant //Braz Dent J. -2012. -Vol. 23, № 5. -Р. 564-569.
- Carrozzo, M. Tumor necrosis factor-alpha and, interferon-gamma polymorphisms contribute to susceptibility to oral lichen planus/M. Carrozzo, M. Uboldi de Capei, E. Dametto//J. Invest. Dermatol. -2004. -Vol. 122, № 1. -P. 87-94.
- Davies, L. C. Oral mucosal progenitor cells are potently immunosuppressive in a dose-independent manner/L. C. Davies, H. Lonnies, M. Locke//Stem. Cells. Dev. -2012. -№ 21. -P. 1478-1487.
- HTR RNA component as a marker of cellular proliferation in oral lichen planus/C. О. Flatharta //Asian Pacific Journal Of Cancer Prevention: APJCP . -2006. -Vоl. 9, № 2. -Р. 287-290.


