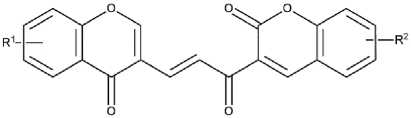
In silico прогноз фармакологической активности, острой токсичности и биодоступности производных (Е)-3-(3-(4-оксо-4Я-хромен-3-ил)акрилоил)-2Я-хромен-2-она
Автор: Шатохин С.С., Оганесян Э.Т.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 3 (71), 2021 года.
Бесплатный доступ
На основе имеющихся литературных данных сформирован ряд виртуальных структур производных (Е)-3-(3-(4-оксо-4Н-хромен-3-ил)акрилоил)-2Н-хромен-2-она, для которых с помощью онлайн-сервисов произведена in silico оценка вероятного спектра фармакологической активности, острой токсичности и биодоступности. Показано, что анализируемые соединения могут проявлять широкий спектр биологической активности, являются малотоксичными и характеризуются высокой биодоступностью при пероральном применении, что подтверждает целесообразность их синтеза и дальнейшего изучения.
Хромон, биодоступность, биологическая активность, острая токсичность
Короткий адрес: https://sciup.org/142230910
IDR: 142230910 | УДК: 615.015.11:615.015.42
In silico prediction of pharmacological activity, acute toxicity and bioavailability of (E)-3-(3-(4-oxo-4H-chromen-3-yl)acryloyl)-2H-chromen-2-one derivatives
Based on the available literature data a number of virtual structures of (E)-3-(3-(4-oxo-4H-chromen-3-yl)acryloyl)-2H-chromen-2-one derivatives have been formed, and the probable spectrum of pharmacological activity, acute toxicity, and bioavailability have been assessed in sili cousing online services. It have been shown that the analyzed compounds can exhibit a wide spectrum of pharmacological activity, are low-toxic and characterized by high oral bioavailability. It confirms the expediency of their synthesis and further study.
Текст научной статьи In silico прогноз фармакологической активности, острой токсичности и биодоступности производных (Е)-3-(3-(4-оксо-4Я-хромен-3-ил)акрилоил)-2Я-хромен-2-она
В настоящее время в медицинской химии активно применяются методы компьютерного прогнозирования биологической активности, острой токсичности и биодоступности соединений до этапа их синтеза. Данный подход позволяет значительно экономить время и ресурсы исследователей в поиске потенциальных биологически активных молекул.
На сегодняшний день однозначно установлена взаимосвязь между уровнем свободных радикалов в организме и развитием ряда патологий [7]. С этой точки зрения поиск новых соединений, проявляющих выраженные анти-радикальные свойства, является актуальной задачей для современной науки.
Известно, что одними из наиболее активных антиоксидантов являются флавоноиды – природные соединения, к числу которых относят и халконы – молекулы, в которых два ароматических цикла соединены α, β-ненасыщенным пропеноновым фрагментом, образующим цепь сопряжения, способствующую передаче элек- тронных эффектов заместителей в этих ядрах и влияющую на биологические свойства молекул. С этой точки зрения прогноз фармакологической активности, острой токсичности и биодоступности предполагаемых для синтеза структур является актуальной задачей.
ЦЕЛЬ РАБОТЫ
Прогноз фармакологической активности, острой токсичности и биодоступности производных ( E )-3-(3-(4-оксо-4 H -хромен-3-ил)акрилоил)-2 H -хромен-2-она, а также расчет их основных молекулярных дескрипторов, позволяющих оценить перспективность синтеза и первичного фармакологического скрининга соединений данного класса.
МЕТОДЫ ИССЛЕДОВАНИЯ
На основе имеющихся данных о взаимосвязи структура-активность в ряду производных халконабыли предложены структуры соединений, целесообразность синтеза которых оценена insilico. С помощью онлайн-сервиса Way 2 Drug PASS Online [9] был сформирован и проанализирован перечень наиболее вероятных видов биологической активности. На основании данных, полученных с использованием онлайн-сервисов Way 2 Drug Gusar [6], admet SAR [3], pk CSM [8] и Pro Tox [5], на модели организма крыс оценено значение LD50 при пероральном применении, а также осуществлено отнесение изучаемых соединений к определенному классу токсичности в соответствии с классификацией OECD [1]. Использование онлайн-платформы Swiss ADME [4] позволило оценить предполагаемую биодоступность виртуальных соединений согласно эмпирическим правилам Липинского и Вебера [2].
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Для оценки перспективности синтезановых производных ( E )-3-(3-(4-оксо-4 H -хромен-3-ил)ак-рилоил)-2 H -хромен-2-она в качестве биологически активных соединений проведено in silico прогнозирование спектра вероятных видов их фармакологических свойств с использованием он-лайн-сервиса PASS Online [9]. Результат прогноза представляет собой перечень вероятных видов биологической активности с указанием вероятности их наличия (Р а ) и отсутствия (P i ) в долях единицы [9]. Из полученного массива данных нами выбраны наиболее перспективные виды активности (P a > P i ), представленные в табл. 1.
Таблица 1
Прогноз фармакологической активности соединений 1-15
|
Вид активности |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
Ингибитор гисти-динкиназы |
0,680 |
0,492 |
0,507 |
0,708 |
0,604 |
0,472 |
0,472 |
0,649 |
0,492 |
0,404 |
0,309 |
0,550 |
0,663 |
0,509 |
0,694 |
|
Гепатопротектор-ная |
0,611 |
0,408 |
0,375 |
0,473 |
0,583 |
0,418 |
0,366 |
0,461 |
0,408 |
0,397 |
0,240 |
0,325 |
0,654 |
0,421 |
0,555 |
|
Ингибитор MAO B |
0,738 |
0,644 |
0,773 |
0,751 |
0,793 |
0,622 |
0,780 |
0,779 |
0,644 |
0,472 |
0,495 |
0,621 |
0,666 |
0,657 |
0,668 |
|
Ингибитор липоксигеназы |
0,276 |
0,168 |
0,218 |
0,227 |
0,247 |
0,155 |
0,218 |
0,218 |
0,168 |
0,164 |
0,144 |
0,149 |
0,268 |
0,227 |
0,232 |
|
Антиоксидантная |
0,372 |
0,259 |
0,326 |
0,278 |
0,330 |
0,265 |
0,327 |
0,274 |
0,259 |
0,259 |
0,255 |
0,215 |
0,395 |
0,377 |
0,310 |
|
Ловушка свободных радикалов |
0,426 |
0,271 |
0,397 |
0,286 |
0,418 |
0,280 |
0,398 |
0,293 |
0,271 |
0,268 |
0,245 |
0,202 |
0,574 |
0,567 |
0,455 |
|
Хемопротективная |
0,409 |
0,235 |
0,288 |
0,247 |
0,374 |
0,239 |
0,290 |
0,246 |
0,235 |
0,236 |
0,207 |
0,185 |
0,384 |
0,301 |
0,255 |
|
Вазодилатирующая |
0,601 |
0,499 |
0,454 |
0,456 |
0,566 |
0,506 |
0,432 |
0,433 |
0,499 |
0,473 |
0,359 |
0,389 |
0,670 |
0,510 |
0,540 |
|
Вазопротекторная |
0,548 |
0,357 |
0,268 |
0,449 |
0,605 |
0,351 |
0,279 |
0,499 |
0,357 |
0,350 |
- |
0,290 |
0,384 |
- |
0,313 |
|
Противоаллергическая |
0,575 |
0,345 |
0,372 |
0,544 |
0,529 |
0,354 |
0,373 |
0,518 |
0,345 |
0,359 |
0,211 |
0,352 |
0,527 |
0,382 |
0,512 |
|
Противовоспалительная |
0,492 |
0,319 |
0,430 |
0,466 |
0,487 |
0,320 |
0,434 |
0,473 |
0,319 |
0,311 |
0,288 |
0,322 |
0,602 |
0,549 |
0,579 |
|
Противоопухолевая |
0,429 |
0,421 |
0,399 |
0,276 |
0,384 |
0,428 |
0,391 |
0,270 |
0,421 |
0,466 |
0,442 |
0,316 |
0,537 |
0,531 |
0,410 |
|
Ингибитор липидпероксидазы |
0,330 |
0,256 |
0,258 |
0,187 |
0,362 |
0,258 |
0,252 |
0,216 |
0,256 |
0,255 |
- |
- |
0,245 |
0,436 |
0,357 |
|
Кардиопротектор-ная |
0,257 |
0,206 |
- |
0,256 |
0,266 |
0,217 |
- |
0,649 |
0,206 |
- |
- |
0,218 |
0,217 |
- |
0,224 |
Как видно из табл. 1, все изучаемые соединения могут являться ингибиторами гистидинки-назы (0,309 < Ра< 0,708) и, следовательно, могут проявлять антибактериальную и противогрибковую активность. Производные 1-15 могут оказывать противоаллергическое (0,211 < Ра < 0,575), вазодилатирующее (0,359 < Ра < 0,670) и гепа- топротекторное (0,240 < Ра < 0,654) действие, а также проявлять антиоксидантную активность (0,215 < Ра< 0,395) и выступать в качестве ловушки свободных радикалов (0,202 < Ра < 0,574), что подтверждает перспективность изучения их анти-радикальных свойств. Прогноз возможного токсического действия соединений 1-15 на орга- низм произведен с помощью четырех онлайн-сервисов [3, 5, 6, 8], позволяющих спрогнозировать величину LD50 виртуальных структур при пероральном введении в организм крыс, а также отнести их к одному из классов токсичности. Полученные данные представлены в табл. 2.
Из данных прогноза видно, что анализируемые соединения относятся к 4-му классу токсичности (835,435 < LD50 < 1855,46), соединение 8 по среднему значению LD50 может быть классифицировано как практически нетоксичное (5 класс). Таким образом, все анализируемые структуры являются малотоксичными. Прогнозирование био-доступности соединений 1-15 проводили in silico с использованием онлайн сервиса Swiss ADME [4]. Согласно «правилу пяти» Липинского [2], наибольшей биологической доступностью при пероральном введении характеризуются молекулы с молекулярной массой до 500 а. е. м., содержащие не более 5 доноров и 10 акцепторов водородной связи, а также имеющие коэффициент распределения в системе октанол-вода (LogP), не превышающий 5. Правило Вебера предъявляет требования к площади полярной поверхности молекулы (не более 140 Å2) и числу вращающихся связей (не более 10) [2]. Полученные данные для анализируемых соединений представлены в табл. 3.
Таблица 2
Прогнозируемая острая токсичность при пероральном введении соединений 1-15 (LD 50 , мг/кг)
|
Соединение |
LD 50 , мг/кг |
Класс токсичности |
||||
|
Gusar |
admetSAR |
pkCSM |
ProTox |
Среднее значение |
||
|
1 |
458,4 |
744.76 |
846,34 |
5000 |
1762,375 |
4 |
|
2 |
819,6 |
759.09 |
1072.48 |
2500 |
1287,793 |
4 |
|
3 |
394,2 |
999,97 |
1138,57 |
809 |
835,435 |
4 |
|
4 |
790,9 |
739,34 |
891,60 |
5000 |
1855,46 |
4 |
|
5 |
500,3 |
908,75 |
899,79 |
5000 |
1827,21 |
4 |
|
6 |
581,9 |
801,35 |
1073,48 |
2500 |
1239,183 |
4 |
|
7 |
693,7 |
1083,95 |
1198,12 |
809 |
946,1925 |
4 |
|
8 |
1289,0 |
789,51 |
1021,25 |
5000 |
2024,94 |
5 |
|
9 |
768,1 |
984,98 |
1074,93 |
2500 |
1332,003 |
4 |
|
10 |
1169,0 |
1049,58 |
1284,46 |
2500 |
1500,76 |
4 |
|
11 |
1780,0 |
1334,97 |
1360,28 |
2500 |
1743,813 |
4 |
|
12 |
992,1 |
1140,88 |
1189,91 |
2500 |
1455,723 |
4 |
|
13 |
366,6 |
907.53 |
1147.91 |
2500 |
1230,51 |
4 |
|
14 |
1063,0 |
1208.98 |
1423.93 |
2905 |
1650,228 |
4 |
|
15 |
82,09 |
842.59 |
1235.27 |
2905 |
1266,238 |
4 |
Таблица 3
|
Соединение |
MW1 |
HBD2 |
HBA3 |
TPSA4, Å2 |
MLOGP5 |
RB6 |
|
1 |
344,32 |
0 |
5 |
77,49 |
1,82 |
3 |
|
2 |
403,34 |
0 |
7 |
123,31 |
1,06 |
4 |
|
3 |
437,24 |
0 |
5 |
77,49 |
2,63 |
3 |
|
4 |
378,76 |
0 |
5 |
77,49 |
2,31 |
3 |
|
5 |
358,34 |
0 |
5 |
77,49 |
2,04 |
3 |
|
6 |
417,37 |
0 |
7 |
123,31 |
1,27 |
4 |
|
7 |
451,27 |
0 |
5 |
77,49 |
2,84 |
3 |
|
8 |
392,79 |
0 |
5 |
77,49 |
2,52 |
3 |
|
9 |
403,34 |
0 |
7 |
123,31 |
1,06 |
4 |
|
10 |
462,37 |
0 |
9 |
169,13 |
0,39 |
5 |
|
11 |
496,26 |
0 |
7 |
123,31 |
1,86 |
4 |
|
12 |
437,79 |
0 |
7 |
123,31 |
1,54 |
4 |
|
13 |
461,38 |
0 |
9 |
149,61 |
0,95 |
6 |
|
14 |
495,28 |
0 |
7 |
103,79 |
2,44 |
5 |
|
15 |
436,80 |
0 |
7 |
103,79 |
2,13 |
5 |
Прогноз биологической доступности соединений 1-15
Согласно данным, представленным в табл. 3, можно сделать вывод об удовлетворении соединений 1-15 всем критериям, предъявляемым правилом Липинского. Однако соединения 10 и 13 , для которых значение площади полярной поверхности превышает 140 Å2, не удовлетворяют требованиям правила Вебера. Следовательно, полученные гетероциклические аналоги халкона могут характеризоваться высоким значением биологической доступности при пероральном введении.
ЗАКЛЮЧЕНИЕ
С использованием современных онлайн-сервисов выполнен in silico прогноз вероятного спектра фармакологической активности, острой токсичности и биодоступности виртуальных производных ( E )-3-(3-(4-оксо-4 H -хромен-3-ил) акри-лоил)-2 H -хромен-2-она. Показано, что соединения могут проявлять широкий спектр фармакологической активности, являются малотоксичными и характеризуются высокой биодоступностью при пероральном применении.
Таким образом, установлена целесообразность синтеза и первичного фармакологического скрининга всех анализируемых соединений.
Список литературы In silico прогноз фармакологической активности, острой токсичности и биодоступности производных (Е)-3-(3-(4-оксо-4Я-хромен-3-ил)акрилоил)-2Я-хромен-2-она
- ГОСТ 32644-2014. Методы испытания по воздействию химической продукции на организм человека. Острая пероральная токсичность - метод определения класса острой токсичности. -Москва: Стандартинформ, 2015. - 11 с. - Текст: непосредственный.
- BDDCS, the Rule of 5 and drugability / L. Z. Benet, C. M. Hosey, O. Ursu, T. I. Oprea. - Text (visual): unmediated // Adv. Drug Deliv. Rev. - 2016. Vol. 101. - P. 89 - 98.
- Admet SAR: A comprehensive source and free tool for assessment of chemical ADMET properties / F. Cheng, W. Li, Y. Zhou, [et al.]. - Text (visual): unmediated // J. Chem. Inf. Model. - 2012. -Vol. 52. - P. 3099 - 3105.
- Daina, A. SwissADME: a free web tool to evaluate pharmacokinetics, drug-likeness and medicinal chemistry friendliness of small molecules / A. Daina, O. Michielin, V. Zoete. - Text (visual): unmediated // Sci. Rep. - 2017. - Vol. 7. - P. 42717.
- ProTox: A web server for the in silico prediction of rodent oral toxicity / M. N. Drwal, P. Banerjee, M. Dunkel, [et al.]. - Text (visual): unmediated // Nucleic Acids Res. - 2014. - Vol. 42. - P. 3 - 8.
- Lagunin, A. QSAR modelling of rat acute toxicity on the basis of PASS prediction / A. Lagunin, A. Zakharov, D. Filimonov, V. Poroikov. - Text (visual): unmediated // Mol. Inform. - 2011. - Vol. 30. - P. 241 - 250.
- Olennikov, D. N. A novel HPLC-Assisted method for investigation of the Fe2+-chelating activity of flavonoids and plant extracts / D. N. Olennikov, N. I. Kashchenko, N. K. Chirikova. - Text (visual): unmediated // Molecules. - 2014. - Vol. 19, Iss. 11. -P. 18296 - 18316.
- Pires, D. E. V. pkCSM: Predicting small-molecule pharmacokinetic and toxicity properties using graph-based signatures / D. E. V. Pires, T. L. Blundell, D. B. Ascher. - Text (visual): unmediated // J. Med. Chem. - 2015. - Vol. 58. - P. 4066 - 4072.
- Computer-aided prediction of biological activity spectra for organic compounds: the possibilities and limitations / V. V. Poroikov, D. A. Filimonov, T. A. Gloriozova, [et al.]. - Text (visual): unmediated // Russ. Chem. Bull. - 2019. - Vol. 68, Iss. 12. - P. 2143 - 2154.


