Индивидуальный подход в лечении пациентов с раком гортани и гортаноглотки III-IV стадии в Алтайском крае
Автор: Фролова А.А., Петриков А.С., Гликенфрейд Г.М., Вихлянов И.В., Глотов С.С., Шаробарова Т.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Опыт работы онкологических учреждений
Статья в выпуске: 5 т.23, 2024 года.
Бесплатный доступ
Среди опухолей головы и шеи рак гортани и гортаноглотки занимает лидирующие позиции и является социально значимой патологией. В настоящее время при наличии разнообразия химиопрепаратов, вариантов оперативного лечения, режимов лучевой терапии и их комбинаций лечение данной патологии является актуальной проблемой, а вопросы о последовательности комбинированного лечения остаются открытыми. Цель исследования - оценить эффективность персонифицированного лечения, одногодичную безрецидивную выживаемость у пациентов с раком гортани и гортаноглотки поздних стадий, включая развитие осложнений в послеоперационном периоде (ВТЭО, кровотечения) в течение года. Материал и методы. С июля 2022 г. по октябрь 2023 г. в отделении опухолей головы и шеи КГБУЗ«Алтайский краевой онкологический диспансер», г. Барнаул пролечено 100 больных раком гортани и гортаноглотки III-IV стадии, из них 95 (95 %) мужчин, 5 (5 %) женщин. Пациентам с местнораспространенным раком гортани (I группа, n=50) выполнялась ларингэктомия с последующей лучевой терапией на ложе и зону лимфооттока до 54 Гр. Пациентам с раком гортаноглотки (II группа, n=50) проведено 3 курса химиотерапии с последующей лучевой терапией в дозе 70-74 Гр.
Рак гортани, рак гортаноглотки, комбинированное лечение, ларингэктомия, химиолучевая терапия, выживаемость, профилактика втэо, нмг, кровотечение
Короткий адрес: https://sciup.org/140307909
IDR: 140307909 | УДК: 616.22+616.321]-006.6-08(571.15) | DOI: 10.21294/1814-4861-2024-23-5-103-111
Individual approach to the treatment of patients with stage III-IV laryngeal and laryngopharyngeal cancer in the Altai territory
Laryngeal and laryngopharyngeal cancer is the most common malignancy within the head and neck. Although there are many treatments for laryngeal and laryngopharyngeal cancer, the treatment still faces great challenging. The aim of the study was to evaluate the effectiveness of personalized treatment and one-year recurrence-free survival in patients with stage III-IV laryngeal and laryngopharyngeal, including postoperative complications (VTE, bleeding) within a year. Material and Methods. From July 2022 to October 2023, 100 patients with stage III-IV laryngeal and laryngopharyngeal cancer were treated in the Department of Head and Neck Tumors at the Altai Regional Oncology Center (AROC), Barnaul. There were 95 men (95 %) and 5 women (5 %). Patients were divided into two groups. Group I patients (n=50) with locally advanced laryngeal cancer underwent laryngectomy followed by radiation therapy with a total dose of 54 Gy delivered to the bed of the removed tumor and lymph node drainage region. Group II patients (n=50) received 3 courses of chemotherapy followed by radiation therapy at a dose of 70-74 Gy.
Текст научной статьи Индивидуальный подход в лечении пациентов с раком гортани и гортаноглотки III-IV стадии в Алтайском крае
Рак гортани и гортаноглотки занимает лидирующие позиции среди опухолей ЛОР-органов в России [1]. Более чем в 95 % случаев опухоли данной локализации представлены плоскоклеточным раком [1–3]. В России за 2021 г. заболеваемость раком гортани составила 5,53 на 100 тыс. мужского населения и 0,36 на 100 тыс. женского населения. В 2021 г. при раке гортаноглотки показатель заболеваемости составил 1,96 и 0,18 на 100 тыс. населения в год соответственно. Заболеваемость у мужчин существенно выше, чем у женщин. В 2022 г. в Алтайском крае с раком гортани выявлено 122 мужчины (5,66 на 100 тыс. населения) и 5 женщин (0,23 на 100 тыс. населения), с раком гортаноглотки – 53 мужчины (2,46 на 100 тыс. населения) и 7 женщин (0,32 на 100 тыс. населения). Следует отметить, что показатель заболеваемости раком гортани в Алтайском крае не отличается от среднестатистических данных по России, тогда как частота встречаемости рака гортаноглотки на 25 % выше у мужчин и на 77 % – у женщин.
Согласно действующим рекомендациям, лечение рака гортани III стадии T3N0М0 целесообразно начинать с конкурентной химиолучевой либо с индукционной химиотерапии [4]. В случае частичной регрессии после химиолучевой терапии или индукционной терапии выполняется оперативное вмешательство (резекция гортани, самостоятельная или расширенная ларингэктомия). При полной регрессии осуществляется динамическое наблюдение. При раке гортани III–IV стадий (T3N+M0) рекомендована индукционная химиотерапия с последующим оперативным лечением или конкурентная химиолучевая терапия. В случае частичного ответа на конкурентную химиолучевую терапию выполняется оперативное лечение, а при полной регрессии – динамическое наблюдение. При раке гортани IV стадии (T4aNлюбаяM0) рекомендовано оперативное лечение с последующей лучевой или химиолучевой терапией. При отказе пациента от оперативного вмешательства или неоперабель-ности процесса рекомендованы конкурентная хи-миолучевая терапия, индукционная химиотерапия или симптоматическая терапия в соответствии с оценкой состояния по шкале ECOG [4].
У пациентов с раком гортаноглотки в стадии Т1N+/T2–3NлюбаяM0 лечение рекомендовано начинать с индукционной химиотерапии с последующей операцией или с хирургического лечения [5]. В случае полной регрессии опухоли после индукционной химиотерапии назначается лучевая или химиолучевая терапия, что в дальнейшем требует динамического наблюдения. При раке горта-ноглотки в стадии T4aNлюбаяM0 рекомендуются оперативное лечение или индукционная химиотерапия с последующим оперативным лечением или конкурентная химиолучевая терапия [5].
Тем не менее на данный момент нет четких алгоритмов при лечении пациентов с раком гортани и гортаноглотки [1–3]. Несмотря на убедительные данные в пользу оперативного лечения, большинство специалистов и пациентов склоняется к химиолучевой терапии, пренебрегая более продолжительной безрецидивной жизнью без инвалидизации [2, 6].
Цель исследования – оценить эффективность индивидуального лечения, одногодичную без-рецидивную выживаемость у пациентов с раком гортани и гортаноглотки III–IV стадий, включая развитие осложнений в послеоперационном периоде в течение года.
Материал и методы
С июля 2022 г. по октябрь 2023 г. в отделении опухолей головы и шеи в КГБУЗ «Алтайский краевой онкологический диспансер», г. Барнаул было пролечено 100 пациентов с раком гортани и горта-ноглотки III–IV стадий, из них 95 (95 %) мужчин и 5 (5 %). женщин Средний возраст у мужчин составил 61,8 ± 3,8, у женщин – 57,8 ± 2,0 года. Установлены факторы риска, способствовавшие развитию заболевания: курение (индекс пачка/лет более 10) [7] и хронический ларингит, которые наблюдались у всех пациентов, хронический алкоголизм – у 22 (22 %) больных. Распределение больных по индексу массы тела (ИМТ): нормальная масса тела (ИМТ 18,5–25,0) отмечена у 49 (49 %) пациентов, нарушение массы тела – у 51 (51 %): дефицит массы тела (ИМТ 16–18,5) – у 14 (14 %), избыточная масса тела (ИМТ 25–30) – у 22 (22 %), ожирение I–II степени (ИМТ 30 и более) – у 15 (15 %) пациентов. Среди сопутствующей патологии преобладала патология сердечно-сосудистой системы. У 34 (34 %) пациентов выявлена гипертоническая болезнь, у 14 (14 %) – ПИКС и нарушения ритма, у 5 (5 %) – в анамнезе ОНМК. У 7 (7 %) пациентов имелось хроническое инфекционное заболевание (гепатиты, ВИЧ) и ХОБЛ. У 2 (2 %) пациентов в анамнезе был перенесенный тромбоз глубоких вен, ТЭЛА.
В отделении опухолей головы и шеи в КГБУЗ «Алтайский краевой онкологический диспансер», г. Барнаул разработан индивидуальный подход к лечению пациентов с раком гортани и гортаноглотки III–IV стадий. Наиболее важными критериями для такого подхода являются инвалидизация, приводящая к снижению качества жизни: потере голосовой функции, нарушению дыхательной и глотательной (после фарингэктомии) функций [2, 6, 8–10].
В зависимости от локализации опухолевого процесса пациенты были разделены на 2 группы. В первую группу включено 50 (50 %) пациентов с раком гортани, которым на первом этапе лечения выполнена радикальная операция. Среди них было 46 (92 %) мужчин и 4 (8 %) женщины (средний возраст – 63,2 ± 2,4 года). Одному (2 %) пациенту выполнена резекция гортани с лимфодиссекцией, 8 (16 %) – ларингэктомия с лимфодиссекцией, 41 (82 %) больному – ларингэктомия без лимфо-диссекции. Пациентам с раком гортани T2N1M0 выполнена резекция гортани с лимфодиссекцией, со стадией T3–4N1–2M0 – ларингэктомия с лим-фодиссекцией, со стадией T3–4N0M0 – ларингэктомия (в т. ч. расширенная) без лимфодиссекции.
Периоперационное ведение пациентов осуществлялось по общепринятым методикам с учетом имеющейся сопутствующей патологии, веса и ИМТ, а также клинико-лабораторных показателей крови и системы гемостаза. Профилактика ВТЭО проводилась антикоагулянтами (НМГ/энокса-парин), согласно рекомендациям АФР (2015) и рекомендациям RUSSCO (2022), с учетом массы тела [11–14]. Эластическая компрессия нижних конечностей выполнялась эластичными бинтами средней растяжимости или чулками I–II класса компрессии. Активизация пациента происходила в 1-е сут после операции. Исходно оценивался риск развития ВТЭО по шкале Caprini [11, 14–16], который варьировал от 5 до 12 баллов (высокая группа риска). Средний балл по Caprini составил 6,3 балла: 5 баллов – 14 (28 %) пациентов, 6 баллов – 20 (40 %) пациентов, 7 баллов – 9 (18 %) пациентов, 8 баллов и более – 6 (12 %) пациентов.
Для первичной профилактики ВТЭО НМГ (эноксапарин натрия) назначался в дозе 0,4 мл (4000 МЕ анти-Xа активности) 1 раз в сут за 12 ч перед операцией и далее с 1-х сут послеоперационного периода не менее 10 дней 1 раз в сут. Пациентам с массой тела менее 50 кг вводилось 0,2 мл (2000 МЕ антиХа активности) 1 раз в сут, а пациентам с массой тела выше 120 кг дозировка назначалась в 1,5 раза больше (0,6 мл 6000 МЕ антиХа активности), согласно рекомендациям не менее 14 дней. Также всем пациентам применялись эластическая компрессия нижних конечностей (чулки I–II класса компрессии или эластичные бинты средней растяжимости), ранняя активизация и адекватная гидратация [8, 11, 12, 14, 16]. Оценка риска кровотечений осуществлялась по шкале АССР 2016 г. [17]. Средний балл варьировал от 2 до 5 баллов (высокий риск).
В послеоперационном периоде пациентам выполнялась лучевая терапия в режиме IMRT – на область удаленной опухоли до СОД 56 Гр и на зону лимфооттока до СОД 50 Гр в течение 6 нед.
Во вторую группу включено 50 пациентов с раком гортаноглотки III–IV стадий, которым проводилась индукционная химиотерапия с последующей лучевой терапией. Оперативное лечение в этой группе пациентов не проводилось. Среди них было 49 (98 %) мужчин и 1 (2 %), женщина, средний возраст составил – 59,8 ± 2,6 года. В подборе схем лечения учитывались масса тела, ИМТ, сопутствующая патология, а также клиниколабораторные показатели крови и системы гемостаза, включая клиренс креатинина и СКФ. У всех пациентов данной группы риск развития ВТЭО составлял 1–2 балла по шкале Khorana [11, 14, 18]. Таким образом, у всех пациентов исходно был низкий и умеренный риск развития ВТЭО на фоне химиотерапии по шкале Khorana. Исходно фармакологическая профилактика ВТЭО не проводилась, за исключением пациента, имеющего нарушение ритма сердца. Оценка риска геморрагических осложнений осуществлялась по шкале АССР (2016) [17]. Средний балл варьировал от 4 до 5 баллов (высокий). Один (2 %) пациент получил индукционную химиотерапию по схеме СF, 24 (48 %) пациента – по схеме TPF, 3 (6 %) пациента – по схеме DCF и 22 (44 %) пациента – по схеме ТР. Далее проводилась самостоятельная лучевая терапия с облучением гортаноглотки до СОД 72 Гр и зон метастазирования – от 40 Гр до 54–56 Гр.
У всех больных исходно перед лечением и в динамике (у оперированных больных на 10–15-е сут перед выпиской, у получавших лекарственную терапию – после каждого курса химиотерапии) с целью выявления ВТЭО выполнялось дуплексное сканирование нижней полой вены, подвздошных, бедренных, подколенных, берцовых и подкожных вен на аппарате General Electric LOGIO P9.
Таким образом, средний возраст обеих групп пациентов составил около 60 лет. Нормальная и избыточная масса тела в обеих группах также была примерно одинаковой. В I группе было в 1,5 раза больше пациентов с ожирением, во II группе – в 1,5 раза больше пациентов с дефицитом массы тела. Такое распределение, вероятно, связано с локализацией опухоли, приводящей к затруднению глотания и наличию болевого синдрома. Основная масса пациентов I группы имела рак гортани III стадии, что связано с нарушением дыхания и речевой функции. Во II группе пациентов (рак гортаноглотки) преобладала IV стадия заболевания. В обеих группах преобладала сопутствующая сердечно-сосудистая патология (таблица).
Статистический анализ производился с помощью программного пакета Statistica 6.1, лицензионных программ Microsoft Office 2016 и включал оценку достоверности различия анализируемых данных с помощью Z-критерия (критерий Фишера). Статистически значимыми принимались различия при p<0,05.
Результаты
В раннем послеоперационном периоде у 3 (6,0 %) пациентов I группы на 3–4-е сут наблюдались клинически незначимые кровотечения из верхней трети трахеи в зоне контакта с трахеостомической трубкой. Из них у всех исходно был высокий риск развития кровотечения по шкале АССР (2016): 2 балла – у 2 пациентов, 5 баллов – у 1 пациента. Кровотечения купированы однократным внутривенным введением транексамовой кислоты 1000 мг, антикоагулянтная терапия была отменена. При этом профилактические дозы НМГ не пре-
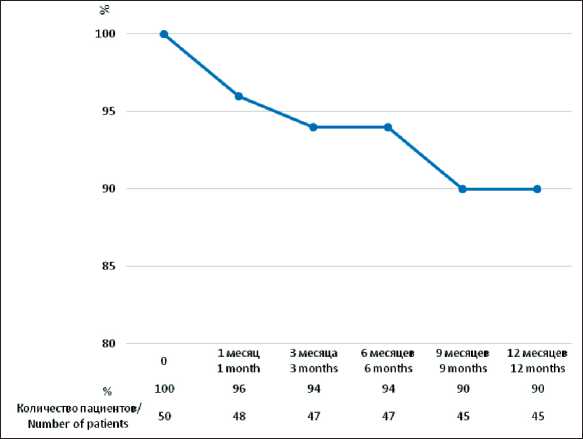
Рис. 1. Кумулятивная выживаемость больных раком гортани (метод Каплана–Майера) Примечание: рисунок выполнен авторами Fig. 1. Cumulative survival of patients with laryngeal cancer (Kaplan–Mayer method).
Note: created by the authors
Таблица /table
Характеристика групп пациентов с раком гортани и гортаноглотки, а также способы их лечения Characteristics of patients with laryngeal and laryngopharyngeal cancer. treatment options in the patients
|
Клинические признаки/Clinical signs |
I группа (рак гортани)/ Group I (laryngeal cancer) (n=50) |
I группа (рак гортаноглотки)/ Group II (laryngopharyngeal cancer) n=50) |
|
Пол/Gender |
||
|
Муж/Мale |
46 (92,0 %) |
49 (98,0 %) |
|
Жен/Women |
4 (8,0 %) |
1 (2,0 %) |
|
Средний возраст, лет/Average age, years |
63,2 ± 2,4 |
59,8 ± 2,6 |
|
Муж/Мale |
63,9 ± 2,2 |
59,8 ± 2,6 |
|
Жен/Women |
59,2 ± 7,2 |
52,0 ± 1,8 |
|
ИМТ, кг/м2/BMI, kg/m2 |
||
|
Нормальная масса тела/Normal body weight (18,5–25) |
24 (48,0 %) |
25 (50,0 %) |
|
Дефицит массы тела/Body weight deficiency (16–18,5) |
5 (10,0 %) |
9 (18,0 %) |
|
Избыточная масса тела/Overweight (25–30) |
12 (24,0 %) |
11 (22,0 %) |
|
Ожирение (30 и более)/Fatness (30 and more) |
9 (18,0 %) |
5 (10,0 %) |
|
Факторы риска/Risk factors |
||
|
Курение/Smoking |
50 (100 %) |
50 (100 %) |
|
Хронический ларингит/Chronic laryngitis |
50 (100 %) |
50 (100 %) |
|
Алкоголизм/Alcoholism |
4 (8,0 %) |
18 (36,0 %) |
|
Стадия по TNM/TNM stage |
||
|
Т2N1M0 |
1 (2,0 %) |
1 (2,0 %) |
|
Т2N2M0 |
1 (2,0 %) |
3 (6,0 %) |
|
T3N0M0 |
29 (68,0 %) |
12 (24,0 %) |
|
T3N1M0 |
2 (4,0 %) |
3 (6,0 %) |
|
T3N2M0 |
4 (8,0 %) |
17 (34,0 %) |
|
T3N3M0 |
1 (2,0 %) |
1 (2,0 %) |
|
T4N0M0 |
10 (20,0 %) |
2 (4,0 %) |
|
T4N1M0 |
– |
2 (4,0 %) |
|
T4N2M0 |
2 (4,0 %) |
8 (16,0 %) |
|
T4N3M0 |
– |
1 (2,0 %) |
|
Сопутствующая патология/Concomitant pathology |
||
|
Гипертоническая болезнь/Hypertension |
22 (44,0 %) |
14 (28,0 %) |
|
ПИКС/нарушение ритма/ Postinfarction cardiosclerosis/rhythm disturbance |
11 (22,0 %) |
4 (8,0 %) |
|
ОНМК/acute violation of cerebral circulation |
1 (2,0 %) |
4 (8,0 %) |
|
ХОБЛ/COPD |
5 (10,0 %) |
2 (4,0 %) |
|
Вирусные гепатиты/ВИЧ/Viral hepatitis/HIV |
3 (6,0 %) |
4 (8,0 %) |
|
ТГВ/ТЭЛА/DVT/PE |
1 (2,0 %) |
1 (2,0 %) |
|
Лечение/Treatment |
||
|
Резекция гортани с лимфаденэктомией/ Laryngeal resection with lymphadenectomy |
1 (2,0 %) |
– |
|
Ларингэктомия (в т.ч. расширенная (с резекцией глотки, резекцией щитовидной железы и т.д.))/ Laryngectomy (including extended (with pharyngeal resection, thyroid resection, etc.)) |
41 (82,0 %) |
|
|
Ларингэктомия с лимфодиссекцией/ Laryngectomy with lymphodissection |
8 (16,0 %) |
– |
|
CF (цисплатин + фторурацил/cisplatin + fluorouracil) |
– |
1 (2,0 %) |
|
DCF (доцетаксел + цисплатин + фторурацил/ docetaxel + cisplatin + fluorouracil) |
– |
3 (6,0 %) |
|
TPF (паклитаксел + цисплатин + фторурацил/ paclitaxel + cisplatin + fluorouracil) |
– |
24 (48,0 %) |
|
TP (карбоплатин + паклитаксел/carboplatin + paclitaxel) |
– |
21 (42,0 %) |
|
Примечание: таблица составлена авторами. |
||
|
Note: created by the authors. |
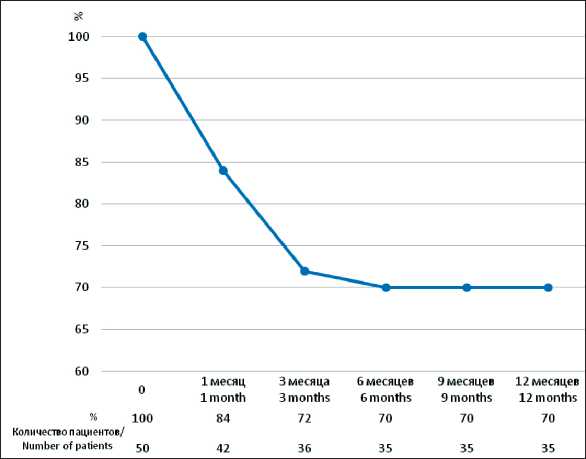
Рис. 2. Кумулятивная выживаемость больных раком гортаноглотки (метод Каплана–Майера). Примечание: рисунок выполнен авторами Fig. 2. Cumulative survival of patients with laryngopharyngeal cancer (Kaplan–Mayer method). Note: created by the authors
вышали рекомендуемые. У 7 (14,0 %) пациентов из-за несостоятельности швов сформировались фарингостомы. У всех больных этой группы исходно перед лечением, в динамике на 10–15-е сут и через 6–12 мес после оперативного лечения выполнялось УЗИ вен нижних конечностей. Случаев ВТЭО в стационаре, а также в течение 6–12 мес после завершения лечения не наблюдалось.
У больных I группы в течение года от начала лечения наблюдалась высокая кумулятивная выживаемость – 90,0 % (рис. 1). Через 1 год после лечения 41 (82,0 %) пациент с раком гортани III–IV стадий (Т3N0–2bM0,Т4N0M0) заболевания находится в ремиссии. У 4 (8,0 %) пациентов выявлены рецидив и прогрессирование опухолевого процесса через 4–6 мес после лечения, в настоящее время они получают химиотерапию I линии по схеме ТР. Вследствие прогрессирования опухоли через 9–11 мес после лечения умерли 5 (10,0 %) пациентов с раком гортани T4aN0M0 стадии.
У 4 (8,0 %) больных II группы, получавших химиотерапию с последующей лучевой терапией, наблюдались кровотечения из опухоли глотки. У 3 (6,0 %) пациентов кровотечение возникло на 2–3-и сут 1-го курса химиотерапии. Исходно, у всех пациентов II группы был установлен высокий риск развития кровотечения по шкале АССР (2016): у 2 (4,0 %) – 5 баллов, у 1 (2,0 %) пациента – 4 балла. У 1 (2,0 %) пациента профузное кровотечение возникло на 2-е сут 3-го курса химиотерапии. При этом исходно у него был также высокий риск развития кровотечений (5 баллов по АССР). У 2 пациентов диффузное кровотечение из опухоли, объемом до 100–150 мл купировано введением тра-нексамовой кислоты в течение 3 дней по 1 000 мг в сут. Двум пациентам с профузным кровотечением, объемом до 400–500 мл выполнена перевязка наружной сонной артерии на стороне поражения. Во всех случаях кровотечение успешно остановлено.
Гнойно-септические осложнения, ВТЭО, летальные исходы во время лечения не наблюдались.
Одногодичная кумулятивная выживаемость больных с раком гортаноглотки III–IV стадий составила 70 % (рис. 2). В настоящее время 19 (38,0 %) больных II группы после химиолучевой терапии находятся в ремиссии заболевания. У 9 (18,0 %) пациентов с раком гортаноглотки IV стадии (Т3N2– 3M0, Т4N0–3M0) наблюдалось прогрессирование опухолевого процесса. Продолженный рост опухоли в глотке и в лимфоузлах шеи выявлен у 7 (14,0 %) пациентов через 4–12 нед после лучевой терапии. До настоящего времени эти пациенты получали химиотерапию II или III линии. У 1 (2,0 %) пациента возникли метастазы в легкие через 6 мес после лечения, у 1 (2,0 %) пациента выявлен периферический рак легкого (аденокарцинома) с метастазом в головной мозг через 3 мес после лечения опухоли глотки. В процессе лучевой терапии находятся 7 (14,0 %) пациентов. В течение года во II группе умерло 15 (30,0 %) пациентов (рис. 2). Основной причиной смерти являлся распад опухоли у 5 (10,0 %) пациентов с раком гортаноглотки Т3–4N0–3b стадии. В 3 (6,0 %) случаях причиной смерти явились метастазы в легких, которые были выявлены через 3,5 мес после лечения. У 2 (4,0 %) пациентов развилась острая почечная недостаточность. У 2 (4,0 %) пациентов – внебольничная пневмония через 1 мес после лечения. Два (4,0 %) пациента с дисфагией II–III степени (рак гортано-глотки Т4аN2b-cМ0 стадии) отказались от установки назогастрального зонда или гастростомии и умерли от раковой кахексии. У 1 (2,0 %) пациента развилось апноэ, вследствие стеноза гортани III–IV степени.
Обсуждение
Несмотря на опубликованные клинические рекомендации по лечению больных с раком гортани и гортаноглотки, до сих пор не существует однозначного оптимального подхода к их ведению [1–3]. По статистическим данным за 2022 г., в РФ летальность от злокачественных новообразований гортани на 1-м году заболевания составляет 20,2 % [19]. На наш взгляд, оперативное лечение с последующим курсом лучевой терапии у больных раком гортани III–IV стадий является наиболее эффективным, поскольку через 12 мес от начала лечения кумулятивная выживаемость сохраняется на уровне 90,0 %, а 82,0 % больных находится в ремиссии. Благодаря разработанному индивидуальному подходу удалось достичь более эффективного лечения пациентов с раком гортани. При этом одногодичная летальность пациентов с раком гортани III–IV стадий в Алтайском крае была на 10,0 % ниже, чем в целом в Российской Федерации.
Исходно перед операцией у больных с раком гортани целесообразно оценивать риск развития ВТЭО по шкале Caprini. При этом у всех пациентов перед операцией наблюдался высокий риск ВТЭО по шкале Caprini (5 баллов и более). Подбор АК-профилактики с учетом веса больных и другие меры профилактики оправданы отсутствием развития ВТЭО и летальных исходов в стационаре от ТЭЛ. В послеоперационном периоде у 7 (14,0 %) больных с раком гортани сформировалась фарингостома и лишь у 3 (6,0 %) больных наблюдались клинически незначимые кровотечения из трахеостомы на фоне исходно высокого риска кровотечения, которые с успехом купировались однократным введением 1000 мг транексамовой кислоты.
Лечение пациентов с раком гортаноглотки требует индивидуального подхода. В этой группе оправдано отсутствие фармакологической профилактики ВТЭО, поскольку исходно у всех больных риск этих осложнений по шкале Khorana был низким и умеренным (1–2 балла). С другой стороны, на фоне исходно высокого риска развития геморрагических осложнений по шкале АССР (2016) при проведении химиотерапии отмечалось клинически незначимое кровотечение из опухолевой язвы глотки в 8,0 % случаев. Следует отметить, что у всех пациентов с кровотечением была IV стадия заболевания. При проведении химиотерапии отсутствовали ВТЭО, гнойно-септические осложнения и летальные исходы. Ввиду высокого риска неблагоприятного течения заболевания у 18,0 % пациентов наблюдалось прогрессирование опухоли, 30,0 % пациентов погибло в течение года после лечения. В стадии ремиссии находятся 38,0 % пациентов, 14,0 % больных продолжают лечение.
Индивидуальный подход лечения больных с раком гортаноглотки III–IV стадий в нашем регионе, в основе которого лежат 3 курса химиотерапии с последующей лучевой терапией, ассоциирован с
Список литературы Индивидуальный подход в лечении пациентов с раком гортани и гортаноглотки III-IV стадии в Алтайском крае
- Чижевская С.Ю., Чойнзонов Е.Л. Современные возможности и перспективы комбинированного лечения рака гортани и гортаноглотки. Сибирский онкологический журнал. 2007; (4): 127–31. [Chizhevskaya S.Yu., Choinzonov E.L. Modern possibilities and prospects of combined treatment of laryngeal and laryngopharyngeal cancer. Siberian Journal of Oncology. 2007; (4): 127–31. (in Russian)].
- Чойнзонов Е.Л., Белевич Ю.В., Чижевская С.Ю., Гольдберг В.Е., Фролова И.Г., Чернов В.И., Гольдберг А.В. Современные методы лечения больных с раком гортани и гортаноглотки. Сибирский онкологический журнал. 2016; 15(3): 91–96. [Choynzonov E.L., Belevich Ju.V., Chizhevskaja S.Ju., Goldberg V.Ev., Frolova I.G., Chernov V.I., Goldberg A.V. Modern methods of treatment of patients with cancer of the larynx and larynx. Siberian Journal of Oncology. 2016; 15(3): 91–96. (in Russian)]. doi: 10.21294/1814-4861-2016-15-3-91-96.
- Бойков В.П., Гладилина И.А., Павлюк Д.Ю., Струков И.Г. Лечебная тактика при раке гортаноглотки. Практическая онкология. 2003; 4(1): 51–55. [Boikov V.P., Gladilina I.A., Pavlyuk D.Yu., Strukov I.G. Therapeutic tactics for cancer of the larynx. Practical Oncology. 2003; 4(1): 51–55. (in Russian)].
- Мудунов А.М., Чойнзонов Е.Л., Решетов И.В. и др. Рак гортани: клинические рекомендации. МЗ РФ, 2020; 61 с. [Mudunov A.M., Choinzonov E.L., Reshetov I.V., et al. Laryngeal cancer: clinical recommendations. Ministry of Health of Russia. 2020; 61 p. (in Russian)].
- Аванесов А.А., Алиева С.Б., Алымов Ю.В. и др. Рак гортаноглотки: клинические рекомендации. МЗ РФ, 2020; 48 с. [Avanesov A.A., Aliyeva S.B., Alymov Yu.V., et al. Laryngopharyngeal cancer: clinical recommendations. Ministry of Health of Russia. 2020; 48 p. (in Russian)].
- Маджидов М.Г. Новый подход к химиолучевому лечению больных с местнораспространенным раком гортаноглотки. Вестник РОНЦ им. Н.Н. Блохина РАМН. 2006; 17(1): 18–19. [Majidov M.G. A new approach to chemoradiotherapy in patients with locally advanced laryngopharyngeal cancer. Bulletin of the N.N. Blokhin Russian Research Center of the Russian Academy of Sciences. 2006; 17(1): 18–19. (in Russian)].
- Гилифанов Е.А., Невзорова В.А. Показатели состояния гортани, уха у лиц с длительным стажем табачной зависимости. Российская оториноларингология. 2013; (3): 27–31. [Gilifanov E.A., Nevzorova V.A. Indicators of the state of the larynx, ear in people with long-term tobacco addiction. Russian Otorhinolaryngology. 2013; (3): 27–31. (in Russian)].
- Дайхес Н.А., Виноградов В.В., Решульский С.С., Исаева М.Л., Федорова Е Б., Хабазова А.М., Осипенко Е.В., Котельникова Н.М., Орлова О.С., Михалевская И.А., Кривых Ю.С. Комплексная реабилитация пациентов после ларингэктомии: основные вехи развития. Российская оториноларингология. 2022; 21(1): 93–104. [Daikhes N.A.,Vinogradov V.V., Reshulskii S.S., Isaeva M.L., Fedorova E.B., Khabazova A.M., Osipenko E.V., Kotelnikova N.M., Orlova О.S., Mikhalevskaya I.A., Krivykh Yu.S. Comprehensive rehabilitation of patients after total laryngectomy: major developmental milestones. Russian Otorhinolaryngology. 2022; 21(1): 93–104. (in Russian)]. doi: 10.18692/1810-4800-2022-1-93-104.
- Кожанов А.Л. Современные аспекты лечения и реабилитации больных при раке гортани. Опухоли головы и шеи. 2016; 6(2): 17–22. [Kozhanov A.L. Modern aspects of treatment and rehabilitation of patients with laryngeal cancer. Tumors of the Head and Neck. 2016; 6(2): 17–22. (in Russian)]. doi: 10.17650/2222-1468-2016-6-2-17-24.
- Ушаков В.С., Иванов С.В. Рак гортани: современные возможности и перспективы. Практическая онкология. 2003; 4(1): 56–60.[Ushakov V.S., Ivanov S.V. Laryngeal cancer: modern possibilities and prospects. Practical Oncology. 2003; 4(1): 56–60. (in Russian)].
- Андрияшкин А.В., Андрияшкин В.В., Арутюнов Г.П. и др. Российские клинические рекомендации по диагностике, лечению и профилактике ВТЭО. Флебология. 2015; (4–2): 1–51. [Andriyashkin A.V., Andriyashkin V.V., Arutyunov G.P., et al. Russian clinical guidelines for diagnosis, treatment and prevention of VTEO. Phlebology. 2015; (4–2): 1–51. (in Russian)].
- Сомонова О.В., Антух Э.А., Варданян А.В., Громова Е.Г., Долгушин Б.И., Елизарова А.Л., Сакаева Д.Д., Сельчук В.Ю., Трякин А.А., Черкасов В.А. Практические рекомендации по профилактике и лечению тромбоэмболических осложнений у онкологических больных. Злокачественные опухоли. 2022; 12(3s2–2): 159–70. [Somonova O.V., Antuh Je.A., Vardanjan A.V., Gromova E.G., Dolgushin B.I., Elizarova A.L., Sakaeva D.D., Selchuk V.Ju., Trjakin A.A., Cherkasov V.A. Practical recommendations for the prevention and treatment of thromboembolic complications in cancer patients. Malignant tumors. 2022; 12(3s2–2): 159–70. (in Russian)]. doi: 10.18027/2224-5057-2022-12-3s2-159-170.
- Haen P., Mege D., Crescence L., Dignat-George F., Dubois C., Panicot-Dubois L. Thrombosis Risk Associated with Head and Neck Cancer: A Review. Int J Mol Sci. 2019; 20(11). doi: 10.3390/ijms20112838.
- Селиверстов Е.И., Лобастов К.В., Илюхин Е.А. и др. Профилактика, диагностика и лечение тромбоза глубоких вен. Рекомендации российских экспертов. Флебология. 2023; 17(3): 152–296. [Seliverstov E.I., Lobastov K.V., Ilyukhin E.A., et al. Prevention, diagnosis and treatment of deep vein thrombosis. Recommendations of Russian experts. Phlebology. 2023; 17(3): 152–296. (in Russian)]. doi: 10.17116/flebo202317031152.
- Шкала Caprini (шкала оценки риска развития венозных тромбоэмболических осложнений у пациентов хирургического профиля). [Internet]. [cited 2024 Jan 10]. URL: https://actual-phlebology.ru/afdigit/shkala-caprini/ [Caprini scale (risk assessment scale for venous thromboembolic complications in surgical patients.) [Internet]. [cited 2024 Jan 10]. URL: https://actual-phlebology.ru/afdigit/shkala-caprini/ (in Russian)].
- Нарушения гемостаза у хирургических больных: руководство для врачей. Под ред. И.Н. Пасечника, С.А. Бернс. М., 2021. 296 с. [Hemostasis disorders in surgical patients: a guide for doctors. Ed. By I.N. Pasechnik, S.A. Burns. Moscow, 2021. 296 p. (in Russian)].
- Шкала АССР (шкала оценки прогнозирования риска геморрагического инсульта и клинически значимого кровотечения у больных, получающих непрямые антикоагулянты) [Internet]. [cited 2024 Jan 10]. URL: https://actual-phlebology.ru/afdigit/shkala-accp/ [ASSR scale (assessment scale for predicting the risk of hemorrhagic stroke and clinically significant bleeding in patients receiving indirect anticoagulants) [Internet]. [cited 2024 Jan 10]. URL: https://actual-phlebology.ru/afdigit/shkala-accp/ (in Russian)].
- Шкала Khorana (шкала оценки риска развития венозных тромбоэмболических осложнений у пациентов терапевтического профиля) [Internet]. [cited 2024 Jan 10]. URL: https://actual-phlebology.ru/afdigit/shkala-khorana/ [Khorana scale (risk assessment scale for venous thromboembolic complications in therapeutic patients) [Internet]. [cited 2024 Jan 10]. URL: https://actual-phlebology.ru/afdigit/shkala-khorana/ (in Russian)].
- Состояние онкологической помощи населению России в 2022 году. Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М., 2023. 252 с. [Cancer care for the population of Russia in 2022. Ed. By A.D. Kaprin, V.V. Starinsky, A.O. Shakhzadova. Moscow, 2023. 252 p. (in Russian)].


