Индуцированная алкоголем экспрессия сосудистого эндотелиального фактора роста и структурные изменения кардиомиоцитов крыс
Автор: Белогубов П.В., Рузов В.И., Слесарев С.М., Шарафутдинова Р.Р.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Физиология
Статья в выпуске: 2, 2022 года.
Бесплатный доступ
Цель - выявить влияние этанола на экспрессию связанных с гипоксией генов (HIF-1a, VEGF-А) и структурные изменения в кардиомиоцитах здоровых крыс. Материалы и методы. Структурные изменения кардиомиоцитов под воздействием этанола изучались на 60 беспородных половозрелых крысах. Животным контрольной группы вводился интра-гастрально стерильный 0,9 % водный раствор хлорида натрия, остальным животным - 40 % этанол. Длительность воздействия этанола на миокард составляла 4 и 8 сут. Морфологическое исследование сердца животных проводилось после декапитации под эфирным наркозом. Определялась экспрессия мРНК генов HIF-1a и VEGF-A из участка левого желудочка сердца и сывороточная концентрация сосудисто-эндотелиального фактора роста методом ПЦР. Морфологические исследования миокарда левого желудочка сердца проводились по гистологическим срезам методом световой микроскопии. Результаты. Короткое по продолжительности воздействие этанола сопровождалось признаками жировой и зернистой дистрофии цитоплазмы кардиомиоцитов с явлениями стаза эритроцитов в капиллярах, артериолах и венулах. Сывороточная концентрация VEGF-A у крыс контрольной группы была ниже по сравнению с группой крыс, подвергнутых воздействию этанола. Выявлены гендерные различия реакции на этанол, в частности более выраженная экспрессия мРНК HIF-1a и VEGF-A у самок по сравнению с самцами на фоне 4-дневного воздействия этанолом, что коррелировало с содержанием VEGF-А в сыворотке крови. Увеличение длительности алкогольного воздействия до 8 сут сопровождалось ростом экспрессии мРНК VEGF-A как у самок, так и самцов крыс. Выводы. Воздействие этанола вызывает активацию транскрипционных факторов HIF-1a и VEGF-А кардиомиоцитов крыс, что может быть расценено как механизм срочной адаптации без развития выраженных структурных дезадаптационных перестроек миокарда.
Vegf-a, hif-1a, гипоксия-ассоциированные факторы, воздействие этанола, экспрессия мрнк, алкоголь-индуцированные изменения миокарда
Короткий адрес: https://sciup.org/14124530
IDR: 14124530 | УДК: 616-092.9 | DOI: 10.34014/2227-1848-2022-2-102-116
Alcohol-induced expression of vascular endothelial growth factor and structural changes in rat cardiomyocytes
The aim of the study is to reveal the ethanol effects on the expression of hypoxia-associated factors (HIF-1a, VEGF-A) and structural changes in cardiomyocytes of healthy rats. Materials and methods. Ethanol-induced structural changes in cardiomyocytes were studied in 60 outbred mature rats. Control animals were intragastrically injected with sterile 0.9% saline, experimental animals -with 40 % ethanol. Ethanol exposure on myocardium lasted 4 and 8 days. Morphological study of the heart was carried out after decapitation preceded by ether anesthesia. PCR tests were used to determine mRNA expression of HIF-1a and VEGF-A genes from the left ventricle and serum concentration of vascular endothelial growth factor. Morphological studies of the left ventricle myocardium were carried out on histological sections using light microscopy. Results. A short ethanol exposure was accompanied by fatty and granular cytoplasm degeneration of car-diomyocytes with erythrocyte stasis in capillaries, arterioles and venules. VEGF-A serum concentration in control rats was lower if compared with ethanol-induced rats. Gender differences to ethanol response were revealed, in particular, a more pronounced HIF-1a and VEGF-A mRNA expression in females compared to males on the background of 4-day ethanol exposure, which correlated with VEGF-A level in blood serum. 8-day alcohol exposure was accompanied by an increase in VEGF-A mRNA expression in both female and male rats. Conclusion. Ethanol exposure causes activation of HIF-1a and VEGF-A transcription factors in cardiomyocytes of rats. It can be regarded as a mechanism of urgent adaptation without the development of pronounced structural maladaptive changes of the myocardium.
Текст научной статьи Индуцированная алкоголем экспрессия сосудистого эндотелиального фактора роста и структурные изменения кардиомиоцитов крыс
Введение. Негативное влияние этанола на организм, в т.ч. на деятельность сердечно-сосудистой системы, является общепризнанным и доказанным фактом. Однако выраженность его воздействия в зависимости от дозировки и концентрации в крови в полной мере не определена.
Изучение реакции клетки на недостаток или избыток кислорода имеет большое значение для понимания адаптивных и дезадаптив-ных (патологических) процессов в организме, а нарушение баланса между потребностью и доставкой кислорода является основной причиной миокардиальной недостаточности [1]. Одним из транскрипционных регуляторов генов, ответственных за реакцию клетки на снижение кислорода, является гипоксией индуцированный фактор-1-альфа (HIF-1α), обеспечи- вающий адекватный ответ на гипоксический стресс [2].
При изучении проблемы гипоксического воздействия на организм выявлены морфофункциональные точки приложения (объекты), принимающие участие в развитии адаптации клетки к гипоксии [1–3], важная роль в котором отводится HIF-1α [4].
Известно, что в нормальных условиях HIF-1α характеризуется коротким периодом полураспада, а его концентрация поддерживается на низком уровне [5].
Количество данных об участии HIF-1α в адаптационных и дезадаптационных процессах увеличивается с каждым годом. Исследования ведутся по нескольким направлениям: изучение специфических механизмов регулирования активности HIF-1α; определение роли генов-мишеней в биологических процессах, регулирующихся, в частности, HIF-1α, внутри клеток и при патофизиологических состояниях; развитие технологий для поиска клеточных специфических мишеней.
В последние десятилетия широко изучаются регуляторные механизмы синтеза, процессинга и стабилизации HIF-1α [6, 7]. По мнению N.L. Morris, S.M. Yeligar, влияние этанола на гипоксией индуцированный фактор-1-альфа состоит в повышении экспрессии HIF-1α как в ядерной, так и в цитоплазматической фракциях в обработанных этанолом клетках в нормоксических условиях [8]. Одним из возможных объяснений является способность этанола смещать окислительно-восстановительное равновесие, усугублять митохондриальный стресс и увеличивать использование кислорода, создавая гипоксическую среду, стимулирующую экспрессию HIF-1α [9].
Исследованиями ряда авторов установлено, что увеличение уровня HIF-1α приводит к повышению экспрессии генов, обеспечивающих стимулирование ангиогенеза через ген фактора роста эндотелия сосудов VEGF-A [10–12].
Показано, что VEGF-A активно экспрессируется в кардиомиоцитах и миофибробластах, что указывает на его аутокринную/пара-кринную роль в регуляции функции роста и выживания этих клеток [13–15].
Клиническое значение сосудисто-эндотелиального фактора роста неоднозначно и противоречиво. Ряд исследователей считает, что VEGF-A может оказывать влияние на формирование структурно-функциональных изменений сердечно-сосудистой системы, в частности нарастание индекса массы миокарда левого желудочка, появление или персистирование клинически значимых аритмий были связаны со снижением активности VEGF-A [16]. По мнению других авторов, немедленные эффекты VEGF-A, вероятно, носят адаптивный характер, тогда как отсроченные могут ассоциироваться с возникновением неблагоприятных клинических событий [17].
Научная гипотеза исследования состоит в том, что воздействие алкоголя вызывает внутриклеточную гипоксию, которая обусловливает увеличение уровня HIF-1α, что приводит к экспрессии гипоксия-зависимых генов, стимулирующих ангиогенез (ген VEGF-A) и адаптацию клетки к гипоксии.
VEGF-A относится к гепаринсвязываю-щим белкам и считается наиболее мощным проангиогенным фактором роста, участвующим в ангиогенезе [18–20].
В некоторых работах показано нарушение сигнализации VEGF-A и транслокации HIF-1α в эндотелиальных клетках крыс при воздействии этанола, что сопровождалось снижением сосудистости раны, обусловленным в т.ч. продуктами метаболизма этанола. Однако автор подчеркивает, что этанол не является фактором снижения секреции VEGF-A, а вызывает нарушение ответа эндотелиальных клеток на проангиогенные стимулы [21]. Выявленное увеличение HIF-1α как в ядерной, так и в цитоплазматической фракции обработанной этанолом клетки в нормоксических условиях свидетельствует о влиянии этанола на окислительно-восстановительные процессы, усилении митохондриального стресса, утилизации кислорода и создании тем самым гипоксической среды, способствующей повышению экспрессии HIF-1α [22].
Цель исследования. Выявить влияние этанола на экспрессию связанных с гипоксией генов (HIF-1α, VEGF-А) и структурные изменения в кардиомиоцитах здоровых крыс.
Материалы и методы. Эксперименты проводились c соблюдением рекомендаций Всемирной медицинской ассоциации Ethical Principles for Medical Research Involving Human Subjects (1964), в соответствии с Директивой 2010/63/EU Европейского парламента и Совета Европейского союза от 22 сентября 2010 г. о защите животных, использующихся для научных целей, а также принципами надлежащей лабораторной практики (приказ Министерства здравоохранения РФ от 01.04.2016 № 199н, ГОСТ Р 53434–2009). Протокол эксперимента был одобрен этическим комитетом ФГБОУ ВО «Ульяновский государственный университет».
С целью изучения механизма алкоголь-индуцированного повреждения миокарда проводилась оценка морфологических и биомар-керных показателей. Структурные изменения кардиомиоцитов под воздействием этанола изучались на 60 беспородных половозрелых крысах (30 самцов и 30 самок). Средний возраст самцов составлял 39 (37–40) нед., самок – 41 (39–44) нед., что соответствует молодому возрасту человека (1 нед. жизни крыс – 1 год жизни человека) [23]. Масса тела самок составляла 334 (324,75–344,25) г, самцов – 474,5 (468–480) г.
После фиксации животным контрольной группы вводился интрагастрально стерильный 0,9 % водный раствор хлорида натрия, остальным животным – 40 % этанол ежедневно из расчета 10 мл/кг, чтобы животные достигли легкой степени опьянения, при которой количество этанола в крови составляет от 0,5 до 1,5 ‰ [24, 25]. Спустя 1 ч производился забор 0,5 мл крови из хвостовой вены и определялась концентрация этанола методом газовой хроматографии на хроматографе Agilent 6850 (США). Морфологическое исследование сердца животных проводилось после декапитации под эфирным наркозом с соблюдением правил эвтаназии. Длительности воздействия этанола на миокард составляла 4 и 8 сут. Сроки (4-е и 8-е сут) проведения эксперимента выбраны на основе результатов ранее проведенного нами исследования, в котором аналогичным образом и при равных условиях проводилась оценка минимальных алкоголь-индуцированных изменений миокарда при ежедневном выведении животных из опыта и дальнейшем морфологическом исследовании. В ходе этого эксперимента было установлено, что минимальные морфологические изменения возникали с 4-х сут воздействия этанолом; 8-е сут эксперимента выбраны для сравнения с минимальными изменениями (4-е сут), так как предполагалось прогрессивное по силе негативное воздействие этанола на миокард. Исходя из этих данных в следующей серии экспериментов проводилось сопоставление ранних морфологических изменений миокарда с геномным ответом кардиомиоцитов (экспрессия иРНК HIF-1α, VEGF-A).
Для анализа экспрессии мРНК генов HIF-1α и VEGF-A брался участок левого желудочка в области верхушки сердца размером 0,5×0,5 см и фиксировался в растворе IntactRNA (ООО «Евроген», Россия) на 4-е и 8-е сут алкогольной интоксикации. Для выделения РНК из 100 мг фиксированной ткани использовался реактив ExtractRNA (OOO «Евроген», Россия). В последующем образцы подвергались обратной транскрипции (набор MMLV RT) и ПЦР. ПЦР в реальном времени проводилась в триплетах в двух сериях с использованием набора qPCRmix-HS SYBR на амплификаторе CFX-96 (BioRad, USA) на базе Научно-исследовательского медико-биологического центра Ульяновского государственного университета. Использовались праймеры (табл. 1), синтезированные на базе ООО «Евроген». Температура отжига для HIF-1a составляла 59 °С, для VEGF-A, β-actin – 60 °С. Подбор праймеров проводился с использованием программы Primer Express 3.0.1. Для приблизительного расчета температуры отжига праймера применялась формула Tm=2(A+T)+4(G+C). Температура корректировалась для совместного использования прай-меров в ПЦР. Анализ уровня мРНК HIF-1α и VEGF-A в ткани сердца проводился через нормализацию гена house-keeping – β-actin и расчет нормализованной экспрессии, выраженной в log10. Данные прологарифмированы по log10, чтобы выровнять разбросы. Нормализованная экспрессия для таргетных генов оценивалась автоматически при помощи программного обеспечения к прибору CFX96 Manager (BioRad, USA) по итогам полуколиче-ственной ПЦР-РВ через ссылку-мишень по формуле: Normalized Expression Sample GOI=RQ sample GOI/(RQ sample (Ref1)×RQ sample (Ref2)×…×RQ sample (Refn))/n (RQ – относительное количество пробы; GOI – интересующий ген (одна мишень); ссылка – ссылка-мишень в прогоне, содержащая одну или несколько ссылок-мишеней (генов или последовательностей) в каждой пробе).
Таблица 1
Table 1
Primers
|
Исследуемый ген Investigated gene |
Последовательность олигонуклеотидов Oligonucleotide sequence |
Температура отжига, °С Annealing temperature, °C |
|
HIF-1α |
Forward TCC CTT TTT CAA GCA GCA G Reverse GCT CCA TTC CAT CCT GTT CA |
59 |
|
VEGF-A |
Forward GCA CCC ATG GCA GAA GG Reverse CTC GAT TGG ATG GCA GTA GCT |
60 |
|
β-actin |
Forward GAA GTG TGA CGT TGA CAT CCG Reverse TGC TGA TCC ACA TCT GCT GGA |
60 |
Праймеры
Венозная кровь в объеме 1,5 мл для анализа уровня VEGF-A забиралась путем пунк-тирования правого предсердия.
Сывороточная концентрация VEGF-A оценивалась в сыворотке крови набором реактивов «Вектор-Бест» (Россия) (чувствительность 10 пг/мл, диапазон измерений 0–2000 пг/мл) на иммуноферментном анализаторе Hospitex diagnostics Plate Screen (Италия).
Морфологические исследования миокарда левого желудочка сердца проводились по гистологическим срезам методом световой микроскопии. Для этого образцы тканей левого желудочка сердца фиксировались в 10 % нейтральном растворе формалина с последующей проводкой и заливкой в парафин. Гистологические срезы толщиной 5–7 мкм окрашивались гематоксилин-эозином и по Ван-Ги-зону. Микропрепараты анализировались с помощью микроскопа Carl Zeiss Axiostar plus с последующей фотофиксацией на фотокамере Canon PC 1049. При морфологическом исследовании визуально оценивалось стромально-кардиомиоцитарное состояние гистологических образцов тканей.
Статистическая обработка данных осуществлялась при помощи статистического пакета SPSS версии 24.0. Результаты оценок по- казателей представлены в виде медианы (Me) и интерквартильного размаха (Q25 % – Q75 %). Для определения значимости различий между двумя наблюдениями использовался непараметрический U-критерий Манна – Уитни с дальнейшей оценкой соответствующего ему уровня значимости. Различие между сравниваемыми показателями считались достоверными при p<0,05.
Результаты и обсуждение. Концентрация этанола в крови у крыс составляла 0,92 (0,78–1,10) ‰ и не имела достоверных гендерных различий. По мнению ряда авторов, данная концентрация сопоставима с легкой степенью алкогольного опьянения у человека [24, 25].
Миокард контрольных (интактных) животных имел типичное строение (рис. 1). Пучки кардиомиоцитов ветвились слабо, были разделены тонкими соединительнотканными перегородками. Цитоплазма кардиомиоцитов преимущественно гомогенна, хорошо выражена поперечная исчерченность. Ядра кардиомиоцитов палочковидной формы, располагались по центру клетки. Между пучками волокон большое количество капилляров, часть из которых содержала эритроциты.
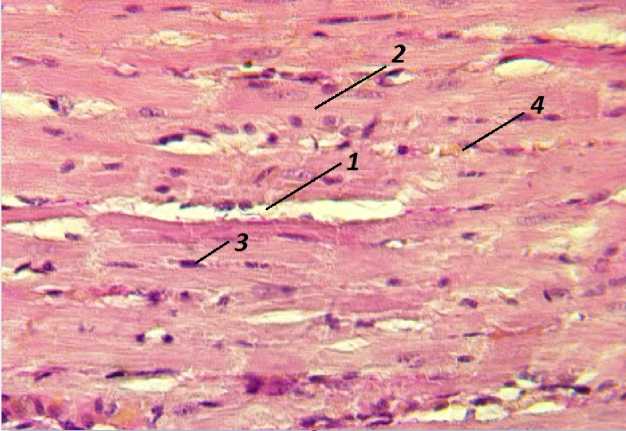
Рис. 1 . Миокард интактных беспородных белых крыс: 1 – прослойки рыхлой соединительной ткани;
2 – цитоплазма кардиомиоцитов с поперечной исчерченностью;
3 – ядро кардиомиоцита; 4 – капилляры.
Окраска гематоксилином и эозином, ×400
Fig. 1. Myocardium of intact outbred white rats (control). Hematoxylin and eosin staining (original magnification, ×400). Note: 1 – interlayers of loose connective tissue;
-
2 – cytoplasm of cardiomyocytes with transverse striations;
-
3 – cardiomyocyte nucleus; 4 – capillaries
Некоторые морфологические изменения миокарда крыс выявлялись после 4- и 8-дневного воздействия этанола (рис. 2) и не имели гендерных различий. Миокард данных животных имел типичное строение. Пучки кардиомиоцитов располагались преимущественно параллельно, незначительное их количество имело извитой ход. Поперечная исчерченность выражена, ядра палочковидные, располагались по центру клеток. Сосуды между пучками и в соединительных перегородках полнокровны. Обнаруживался стаз эритроцитов как в капиллярах (рис. 2, Г), так и в артериолах и венулах (рис. 2, А). В цитоплазме ряда кардиомиоцитов определялись признаки как пылевидной жировой дистрофии (рис. 2, А), так и зернистой дистрофии цитоплазмы (рис. 2, Б). Вокруг некоторых крупных кровеносных сосудов хорошо вы- ражены пучки коллагеновых волокон, имевшие извитой ход (рис. 2, В).
Таким образом, короткое по продолжительности воздействие этанола сопровождалось признаками жировой и зернистой дистрофии цитоплазмы кардиомиоцитов с явлениями стаза эритроцитов в капиллярах, артериолах и венулах.
Однако выявленные морфологические изменения в кардиомиоцитах полностью относить к проявлениям гипоксического морфогенеза не следует, учитывая отсутствие такого характерного признака, как гидропическая дистрофия [26], – одного из типичных проявлений ранней обратимой стадии гипоксического повреждения клетки, приводящего к утрате трансмембранного градиента электролитов [27].
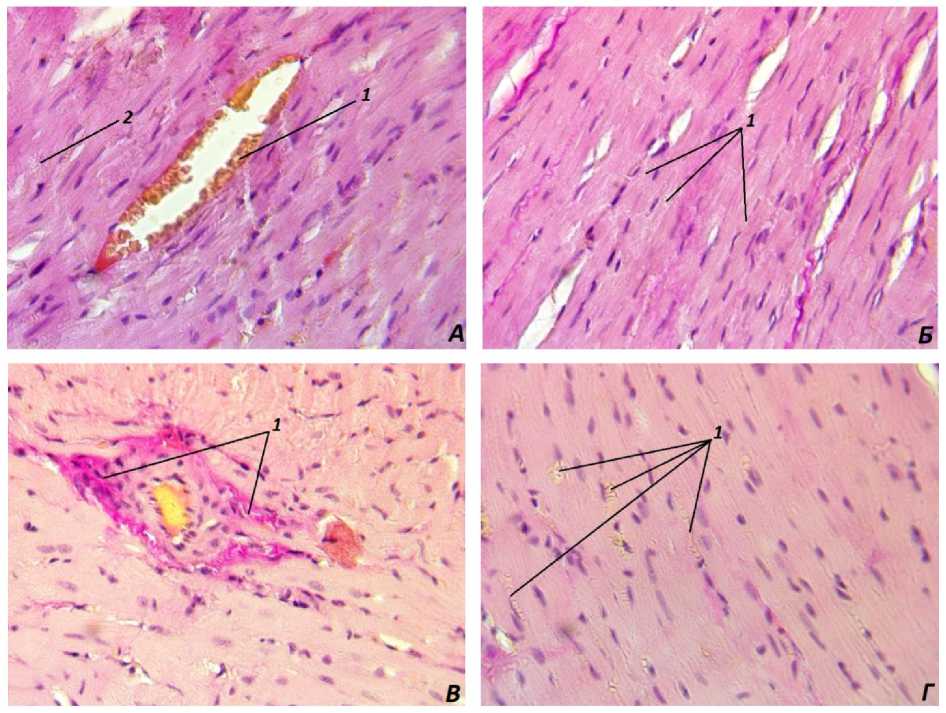
Рис. 2. Миокард беспородных белых крыс после воздействия этанола (8 дней):
A: 1 – стаз эритроцитов в микроциркуляторном русле миокарда;
2 – пылевидная жировая дистрофия кардиомиоцитов;
Б: 1 – зернистая дистрофия цитоплазмы кардиомиоцитов;
В: 1 – соединительнотканные образования вокруг кровеносного сосуда;
Г: 1 – стаз эритроцитов в капиллярах миокарда.
Окраска гематоксилином и эозином, ×400
Fig. 2. Myocardium of outbred white rats after ethanol exposure (8 days).
Hematoxylin and eosin staining (original magnification, ×400).
Note: A: 1 – erythrocyte stasis in the myocardial microcirculatory bed;
-
2 – dustlike fatty degeneration of cardiomyocytes;
Б: 1 – granular degeneration of cardiomyocyte cytoplasm;
-
В: 1 – bundles of collagen fibres around the blood vessel;
Г: 1 – erythrocyte stasis of in myocardial capillaries
Согласно современным концепциям адаптации, при воздействии экспресс-фактора клетка активирует транскрипционные факторы, в частности HIF-1α, который регулирует гены, детерминирующие в т.ч. неоваскуляризацию миокарда и энергетический метаболизм кардиомиоцитов [28, 29]. В группе интактных крыс исходный уровень экспрессии мРНК HIF-1α в миокарде составил 1,47 отн. ед. у самок и 1,56 отн. ед. у самцов, что почти в 1,5 раза ниже, чем в группе крыс, подвергнутых воздействию этанола. Сывороточная концентрация VEGF-А также была ниже по сравнению с группой крыс, подвергнутых воздействию этанола (табл. 2).
Проведенная оценка экспрессии гипо-ксия-ассоциированных факторов кардиомиоцитов крыс под воздействием этанола, представленная в табл. 2, свидетельствует об изменении показателей экспрессии и об однонаправленности этих изменений.
Следует отметить наличие гендерных различий реакции на этанол, в частности более выраженной экспрессии мРНК HIF-1α на фоне 4- и 8-дневного воздействия этанола, а также более высокой сывороточной концентрации
-
VEGF-A на фоне 4-дневного воздействия этанола у самок по сравнению с самцами. Увеличение длительности алкогольного воздействия до 8 сут сопровождалось ростом экспрессии мРНК VEGF-A как у самок, так и самцов крыс.
Таблица 2
Table 2
Гендерные особенности алкоголь-индуцированной реакции кардиомиоцитов Gender-specific characteristics of alcohol-induced cardiomyocyte reaction
|
Параметр Parameter |
Контроль (n=20) Control (n=20) |
Группа особей с алкогольной интоксикацией, 4-е сут (n=20) Rats intoxicated with alcohol, Day 4 (n=20) |
Группа особей с алкогольной интоксикацией, 8-е сут (n=20) Rats intoxicated with alcohol, Day 8 (n=20) |
|||
|
самки (n=10) females (n=10) |
самцы (n=10) males (n=10) |
самки (n=10) females (n=10) |
самцы (n=10) males (n=10) |
самки (n=10) females (n=10) |
самцы (n=10) Males (n=10) |
|
|
Экспрессия мРНК HIF-1α, отн. ед. HIF-1α mRNA expression, relative units |
1,47 (1,36–1,67) |
1,56 (1,47–1,67) |
2,56 (2,53–2,67) *, ** |
2,36 (2,28–2,44) * |
2,69 (2,55–2,80) *, ** |
2,32 (2,15–2,45) * |
|
Экспрессия мРНК VEGF-А, отн. ед. VEGF-A mRNA expression, relative units |
1,61 (1,42–1,86) |
1,39 (1,29–1,52) |
2,42 (2,30–2,48) *, *** |
2,29 (2,09–2,54) *, *** |
2,97 (2,66–3,01) * |
2,71 (2,48–2,92) * |
|
VEGF-А, пг/мл VEGF-A, pg/ml |
43,15 (38,75–44,55) |
43,45 (40–45,47) |
54,1 (51,6–59,15) *, ** |
50,05 (47,32–53,15) |
46,3 (41,65–49,15) |
47,55 (45,82–50,7) |
Примечание. * – достоверные различия с контрольной группой; ** – достоверные различия внутри группы; *** – достоверные различия между подгруппами особей одного пола.
Note. * – the differences are significant compared with the control group; ** – the differences are significant within a group; *** – the differences are significant compared with the subgroups of the same sex.
Общепризнано, что HIF-1α относится к универсальным сигнальным белкам, участвующим в реализации компенсаторно-приспособительных процессов в организме при гипоксии различного генеза [1, 30]. По мнению ряда авторов, HIF-1α является триггером, запускающим системные тканевые механизмы адаптации [31].
Повышение капилляризации миокарда крыс при действии этанола, сопровождающееся повышением сосудистой проницаемости, свидетельствует о развитии компенсаторно-приспособительных реакций на гипо- ксию, ассоциированную с экспрессией HIF-1α [32, 33].
Результаты нашего исследования показали, что кратковременное 4- и 8-дневное воздействие этанола, соответствующее легкой степени алкогольной интоксикации, вызывает активацию транскрипционных факторов HIF-1α и VEGF-А кардиомиоцитов крыс, что может быть расценено как механизм срочной адаптации без развития выраженных структурных дезадаптационных перестроек миокарда. Результаты исследования согласуются с данными других авторов [17, 34–36].
До настоящего времени остаются дискуссионными вопросы о кардиопротекторных и кардиодепрессивных эффектах алкоголя. Проводимые молекулярно-генетические исследования частично объясняют механизм действия этанола через модулирующий эффект на внутриклеточные сигнальные системы, что отражает адаптивную реакцию клетки вследствие экспрессии ряда белков [37]. При этом этанол запускает каскад реакций за счет кислородных сенсоров клетки, сигналы от которых активируют транскрипционный фактор HIF-1α [10]. Многочисленные исследования последних лет уделяют большое внимание изучению генетических аспектов компенсаторно-адаптационных реакций клетки на гипоксию, ведущая роль в них отводится специфическому регуляторному белку HIF-1α [38].
Известно, что HIF-1α регулирует экспрессию генов ангиогенеза, клеточной пролифе рации, апоптоза и т.д. [39–41]. Активация VEGF-A индуцирует экспрессию эндотелиальной NO-синтазы и образование оксида азота, что в свою очередь способствует вазодилятации [42]; снижение уровня VEGF-A обусловливает апоптоз эндотелия [43]. По мнению A. Bâ, алкоголь не столько нарушает структуру кардиомиоцитов, сколько повышает вероятность активации апоптического механизма [44], что нашло свое косвенное подтверждение в проведенном нами исследовании в виде отсутствия выраженного структурного ремоделирования кардиомиоцитов миокарда крыс. Экспериментально доказанным механизмом кардиопротек-торного эффекта умеренных доз алкоголя является повышение активности NO-синтазы [45], тирозинкиназы, АТФ-зависимых калиевых каналов [46, 47]. Перспективным является продолжение изучения молекулярно-генетических механизмов патогенеза алкогольного поражения миокардиоцитов и роли эндотелиальной синтазы оксида азота с учитом имеющихся в литературе данные о дозозависимом эффекте оксида азота: кардиопротекторном – при низких концентрациях и кардиодепрессивном – при высоких [37].
Выводы:
Список литературы Индуцированная алкоголем экспрессия сосудистого эндотелиального фактора роста и структурные изменения кардиомиоцитов крыс
- Лукьянова Л.Д. Современные проблемы адаптации к гипоксии. Сигнальные механизмы и их роль в системной регуляции. Патологическая физиология и экспериментальная терапия. 2011; 1: 3-19.
- Серебровская Т.В. Новая стратегия в лечении болезней: гипоксия-индуцируемый фактор. Вестник Международной академии наук. 2006; 1: 29-31.
- Солкин А.А., Белявский Н.Н., Кузнецов В.И., Николаева А.Г. Основные механизмы формирования защиты головного мозга при адаптации к гипоксии. Вестник ВГМУ. 2012; 1 (11): 6-14.
- Sadaghianloo N., Yamamoto K., Bai H., Tsuneki M., Protack C.D., Hall M.R., Declemy S., Hassen-Kho-dja R., Madri J., Dardik A. Increased Oxidative Stress and Hypoxia Inducible Factor-1 Expression during Arteriovenous Fistula Maturation. Ann. Vasc. Surg. 2017; 41: 225-234. DOI: 10.1016/j.avsg.2016.09.014.
- Серебровская Т.В. Гипоксия-индуцибельный фактор: роль в патофизиологии дыхания. Украинский пульмонологический журнал. 2005; 3: 77-81.
- Шустов Е.Б., Каркищенко Н.Н., ДуляМ.С., СеменовХ.Х., Оковитый С.В., Радько С.В. Экспрессия гипоксия-индуцибельного фактора HIF1a как критерий развития гипоксии тканей. Биомедицина. 2015; 4: 4-15.
- Sun J.Y., ChenX.Y., WangL., Ye W.X., Shen S.J., Yang J.L., YaoM, Yao D.F. Hypoxia-inducible factor-la mediates and regulates angiogenesis-related factors expression in hepatocellular carcinoma. Zhonghua Gan Zang Bing Za Zhi. 2020; 28 (11): 942-948. DOI: 10.3760/cma.j.cn501113-20200228-00074.
- Morris N.L., Yeligar S.M. Role of HIF-la in Alcohol-Mediated Multiple Organ Dysfunction. Biomole-cules. 2018; 8 (4): 170. DOI: 10.3390/biom8040170.
- Satishchandran A., Ambade A., Rao S., Hsueh Y.C., Iracheta-Vellve A., Tornai D., Lowe P., Gyongyo-si B., Li J., Catalano D., Zhong L., KodysK., Xie J., Bala S., Gao G., Szabo G. MicroRNA 122, Regulated by GRLH2, Protects Livers of Mice and Patients From Ethanol-Induced Liver Disease. Gastroenterology. 2018; 154 (1): 238-252. DOI: 10.1053/j.gastro.2017.09.022.
- Новиков В.Е., Левченкова О.С. Гипоксией индуцированный фактор (HIF-1a) как мишень фармакологического воздействия. Обзоры по клинической фармакологии и лекарственной терапии. 2013; 11 (2): 8-16. DOI: 10.17816/RCF1128-16.
- Kouvaras E., Christoni Z., Siasios I., Malizos K., Koukoulis G.K., Ioannou M. Hypoxia-inducible factor 1-alpha and vascular endothelial growth factor in cartilage tumors. Biotech. Histochem. 2019; 94 (4): 283-289. DOI: 10.1080/10520295.2018.1556806.
- Zhu Y., Wang Y., Jia Y., Xu J., Chai Y. Roxadustat promotes angiogenesis through HIF-1a/VEGF /VEGFR2 signaling and accelerates cutaneous wound healing in diabetic rats. Wound Repair Regen. 2019; 27 (4): 324-334. DOI: 10.1111/wrr.12708.
- Zhao T., Zhao W., Meng W., Liu C., Chen Y., Gerling I.C., Weber K.T., Bhattacharya S.K., Kumar R., Sun Y. VEGF-C/VEGFR-3 pathway promotes myocyte hypertrophy and survival in the infracted myocardium. Am. J. Transl. Res. 2015; 7 (4): 697-709.
- Braile M., Marcella S., Cristinziano L., Galdiero M.R., Modestino L., Ferrara A.L., Varricchi G., Marone G., Loffredo S. VEGF-A in Cardiomyocytes and Heart Diseases. Int. J. Mol. Sci. 2020; 21 (15): 5294. DOI: 10.3390/ijms21155294.
- Merentie M., Rissanen R., Lottonen-Raikaslehto L., Huusko J., Gurzeler E., Turunen M.P., Holappa L., Makinen P., Yla-Herttuala S. Doxycycline modulates VEGF-A expression: Failure of doxycycline-in-ducible lentivirus shRNA vector to knockdown VEGF-A expression in transgenic mice. PLoS One. 2018; 13 (1): e0190981. DOI: 10.1371/journal.pone.0190981.
- Шодикулова Г.З. Влияние L-аргинина на дисфункцию эндотелия у больных с врожденным пролапсом митрального клапана. Казанский медицинский журнал. 2014; 3 (95): 326-331.
- PotenteM., CarmelietP. The Link Between Angiogenesis and Endothelial Metabolism. Annu. Rev. Physiol. 2017; 79: 43-66 DOI: 10.1146/annurev-physiol-021115-105134.
- Melincovici C.S., Bo§ca A.B., §u§man S., Märginean M., Mihu C., Istrate M., Moldovan I.M., Roman A.L., Mihu C.M. Vascular endothelial growth factor (VEGF) - key factor in normal and pathological angiogenesis. Rom. J. Morphol. Embryol. 2018; 59 (2): 455-467.
- Pulkkinen H.H., Kiema M., Lappalainen J.P., Toropainen A., Beter M., Tirronen A., Holappa L., Niskanen H., Kaikkonen M.U., Ylä-Herttuala S., Laakkonen J.P. BMP6/TAZ-Hippo signaling modulates angiogenesis and endothelial cell response to VEGF. Angiogenesis. 2021; 24 (1): 129-144. DOI: 10.1007/s10456-020-09748-4.
- Gianni-Barrera R., Butschkau A., Uccelli A., Certelli A., Valente P., Bartolomeo M., Groppa E., Burger M.G., HlushchukR., Heberer M., Schaefer D.J., Gürke L., Djonov V., Vollmar B., Banfi A. PDGF-BB regulates splitting angiogenesis in skeletal muscle by limiting VEGF-induced endothelial proliferation. Angiogenesis. 2018; 21 (4): 883-900. DOI: 10.1007/s10456-018-9634-5.
- RadekK.A., MatthiesA.M., BurnsA.L., Heinrich S.A., Kovacs E.J., Dipietro L.A. Acute ethanol exposure impairs angiogenesis and the proliferative aspects of wound healing. Am. J. Physiol. Heart. Circ. Physiol. 2005; 289: 1084-1090. DOI: 10.1152/ajpheart.00080.2005.
- Chen Y., Zhao B., Zhu Y., Zhao H., Ma C. HIF-1-VEGF-Notch mediates angiogenesis in temporomandibular joint osteoarthritis. Am. J. Transl. Res. 2019; 11 (5): 2969-2982.
- Гелашвили О.А. Вариант периодизации биологически сходных стадий онтогенеза человека и крысы. Саратовский научно-медицинский журнал. 2008; 4 (22): 125-126.
- Ряховский А.Е., Еникеев Д.А., Байков Д.Э., Фаткуллин К.В. Экспериментальное моделирование различных степеней алкогольного опьянения у крыс. Медицинский вестник Башкортостана. 2017; 1 (67): 76-81.
- Вторушина Ю.С. Состояние опьянения в системе норм Общей и Особенной частей УК РФ. Сибирский юридический вестник. 2018; 2 (81): 71-75.
- Antonio C., Päpke C., RochaM., Diab H., Limami A.M., Obata T., Fernie A.R., van Dongen J.T. Regulation of primary metabolism in response to low oxygen availability as revealed by carbon and nitrogen isotope redistribution. Plant Physiol. 2016; 170 (1): 43-56. DOI: 10.1104/pp.15.00266.
- Цибульников С.Ю. Ишемические и реперфузионные повреждения сердца: роль Са-каналов 1-типа и №+/И+-обменника, анализ экспериментальных и клинических данных. Российский физиологический журнал им. И.М. Сеченова. 2019; 105 (7): 801-811.
- Zeriouh M., Sabashnikov A., Tenbrock A., Neef K., Merkle J., Eghbalzadeh K., Weber C., Liakopou-los O.J., Deppe A.C., Stamm C., Cowan D.B., Wahlers T., Choi Y.H. Dysregulation of proangiogeneic factors in pressure-overload left-ventricular hypertrophy results in inadequate capillary growth. Ther. Adv. Cardiovasc. Dis. 2019; 13: 1753944719841795. DOI: 10.1177/1753944719841795.
- Xiao Y., Wang T., Song X., Yang D., Chu Q., Kang Y.J. Copper promotion of myocardial regeneration. Exp. Biol. Med. (Maywood). 2020; 245 (10): 911-921. DOI: 10.1177/1535370220911604.
- Semenza G.L. Oxygensensing, hypoxia-induciblefactors, and disease pathophysiology. Annu. Rev. Pathol. 2014; 9: 47-71. DOI: 10.1146/annurev-pathol-012513-104720.
- Serocki M., Bartoszewska S., Janaszak-Jasiecka A., OchockaR.J., Collawn J.F., Bartoszewski R. miRNA sregulate the HIF switch during hypoxia: a novel therapeutic target. Angiogenesis. 2018; 21 (2): 183-202. DOI: 10.1007/s10456-018-9600-2.
- Chiu D.K., Tse A.P., Xu I.M., Di Cui J., Lai R.K., Li L.L., Koh H.Y., Tsang F.H., Wei L.L., Wong C.M., NgI.O., Wong C.C. Hypoxia inducible factor HIF-1 promotes myeloid-derived suppressor cells accumulation through ENTPD2/CD39L1 in hepatocellular carcinoma. Nat. Commun. 2017; 8 (1): 517. DOI: 10.1038/s41467-017-00530-7.
- Балыкин М.В., Сагидова С.А., Жарков А.С., Айзятулова Е.Д., Павлов Д.А., Антипов И.В. Влияние прерывистой гипобарической гипоксии на экспрессию hif-1a и морфофункциональные изменения в миокарде. Ульяновский медико-биологический журнал. 2017; 2: 125-134. DOI: 10.23648/UMBJ. 2017.26.6227.
- Zhang D., Lv F.L., Wang G.H. Effects of HIF-1a on diabetic retinopathy angiogenesis and VEGF expression. Eur. Rev. Med. Pharmacol. Sci. 2018; 22 (16): 5071-5076. DOI: 10.26355/eurrev_201808_15699.
- Fan J., Lv H., Li J., Che Y., Xu B., Tao Z., Jiang W. Roles of Nrf2/HO-1 and HIF-1 a/VEGF in lung tissue injury and repair following cerebral ischemia/reperfusion injury. J. Cell. Physiol. 2019; 234 (6): 76957707. DOI: 10.1002/jcp.27767.
- Xiang Y., Yao X., WangX., Zhao H., Zou H., Wang L., Zhang Q.X. Houshiheisan promotes angiogenesis via HIF-1 a/VEGF and SDF-1/CXCR4 pathways: in vivo and in vitro. Biosci. Rep. 2019; 39 (10): BSR 20191006. DOI: 10.1042/BSR20191006.
- Dopico A.M., Bukiya A.N., Martin G.E. Ethanol modulation of mammalian BK channels in excitable tissues: molecular targets and their possible contribution to alcohol-induced altered behavior. Front. Physiol. 2014; 5: 466. DOI: 10.3389/fphys.2014.00466.
- Lukyanova L.D., Sukoyan G. V., Kirova Y.I. Role of proinflammatory factors, nitric oxide, and some parameters of lipid metabolism in the development of immediate adaptation to hypoxia and HIF-1 a accumulation. Bull. Exp. Biol. Med. 2013; 154 (5): 597-601. DOI: 10.1007/s10517-013-2008-5.
- Rana N.K., Singh P., Koch B. CoCl2 simulated hypoxia induce cell proliferation and alter the expression pattern of hypoxia associated genes involved in angiogenesis and apoptosis. Biol. Res. 2019; 52 (1): 12. DOI: 10.1186/s40659-019-0221-z.
- RashidM., Zadeh L.R., Baradaran B., Molavi O., Ghesmati Z., Sabzichi M., Ramezani F. Up-down regulation of HIF-1 a in cancer progression. Gene. 2021; 798: 145796. DOI: 10.1016/j.gene.2021.145796.
- CasillasA.L., Chauhan S.S., Toth R.K., SainzA.G., Clements A.N., Jensen C.C., LanglaisP.R., Miranti C.K., Cress A.E., Warfel N.A. Direct phosphorylation and stabilization of HIF-1a by PIM1 kinase drives angiogenesis in solid tumors. Oncogene. 2021; 40 (32): 5142-5152. DOI: 10.1038/s41388-021-01915-1.
- Tran J., Magenau A., Rodriguez M., Rentero C., Royo T., Enrich C., Thomas S.R., Grewal T., Gaus K. Activation of Endothelial Nitric Oxide (eNOS) Occurs through Different Membrane Domains in Endothelial Cells. PLoS One. 2016; 11 (3): e0151556. DOI: 10.1371/journal.pone.0151556.
- Luengas-Martinez A., Hardman-Smart J., Rutkowski D., Purba T.S., Paus R., Young H.S. Vascular En-dothelial Growth Factor Blockade Induces Dermal Endothelial Cell Apoptosis in a Clinically Relevant Skin Organ Culture Model. Skin Pharmacol. Physiol. 2020; 33 (3): 110-118. DOI: 10.1159/000508344.
- Bä A. Alcohol and thiamine deficiency trigger differential mitochondrial transition pore opening mediating cellular death. Apoptosis. 2017; 22 (6): 741-752. DOI: 10.1007/s10495-017-1372-4.
- CinelliM.A., Do H.T., Miley G.P., Silverman R.B. Inducible nitric oxide synthase: Regulation, structure, and inhibition. Med. Res. Rev. 2020; 40 (1): 158-189. DOI: 10.1002/med.21599.
- Krenz M., Cohen M.V., Downey J.M. Protective and anti-protective effects of acute ethanol exposure in myocardial ischemia/reperfusion. Pathophysiology. 2004; 10 (2): 113-119. DOI: 10.1016/j.patho-phys.2003.10.006.
- Krylova I.B., Selina E.N., Bulion V.V., Rodionova O.M., Evdokimova N.R., Belosludtseva N.V., Shigae-vaM.I., Mironova G.D. Uridine treatment prevents myocardial injury in rat models of acute ischemia and ischemia/reperfusion by activating the mitochondrial ATP-dependent potassium channel. Sci. Rep. 2021; 11 (1): 16999. DOI: 10.1038/s41598-021-96562-7.


