Индукция физиологической активности чистой культуры гриба вешенка обыкновенная (Pleurotus ostreatus) на лабораторной стадии
Автор: Качмазов Г.С., Багаева У.В.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Биологические науки
Статья в выпуске: 2, 2016 года.
Бесплатный доступ
На основании сопоставления средней величины линейного прироста колонии чистой культуры гриба вешенка (Pleurotus ostreatus) в стандартных условиях со скоростью потребления кислорода, измеренного с помощью разработанного авторами манометрического метода, было установлено, что культуральные свойства и линейные размеры прироста колонии за определенный промежуток времени не могут быть использованы в качестве единственного критерия оценки качества культуры. Оценка физиологической активности биомассы является необходимым критерием в комплексе требований, предъявляемых к качеству чистой культуры, и определение величины дыхательной активности вполне может быть объективным критерием оценки физиологического потенциала биомассы. Включение в состав питательных сред источников целлюлозы и других растительных полимеров положительно влияет как на морфологические, так и на физиологические свойства чистой культуры. По результатам измерений линейных размеров колоний лучшими индукторами генеративной активности, использованными в эксперименте, являются лигнин гидролизный, лузга подсолнечника и отруби пшеничные. По результатам определения скорости потребления кислорода лучшими индукторами физиологической активности являются отруби пшеничные, измельченные листья каштана и лузга подсолнечника.
Вешенка обыкновенная, физиологическая активность, активность потребления кислорода, целлюлоза, лузга подсолнечника, отруби пшеничные, листья каштана, лигнин гидролизный, опилки бука, мезокарпий грейпфрута
Короткий адрес: https://sciup.org/14084607
IDR: 14084607 | УДК: 635.1
Induction of the physiological activity of pure strain of oyster mushroom (Pleurotus ostreatus) at laboratory stage
A comparison of the average value of the linear growth of the colony of pure culture of oyster mushrooms (Pleurotus ostreatus) under standard conditions with the average rate of oxygen consumption, estimated with the method developed by the authors, has demonstrated that cultural properties and the linear dimensions of the colony growth over time cannot be used as the sole criterion for culture quality evaluating. Evaluation of the physiological activity of the biomass is essential criterion in the complex requirements for the quality of a pure culture, and the determination of the respiratory activity may be an objective criterion for evaluating the physiological potential of biomass. Incorporation into the culture media of cellulose and other plant polymers positively affects both morphological and physiological properties of a pure culture. The results of linear dimensions measurements of the colonies indicated that the best inducers of generative activity are hydrolytic lignin, sunflower husk and wheat bran. Taking into account oxygen consumption rate the best inducers of physiological activity are wheat bran, crushed leaves of chestnut and sunflower husk.
Текст научной статьи Индукция физиологической активности чистой культуры гриба вешенка обыкновенная (Pleurotus ostreatus) на лабораторной стадии
Введение . В результате стабильного увеличения объемов производства и совершенствования технологических приемов промышленного культивирования не прекращаются теоретические и экспериментальные исследования высших базидиомицетов, к которым относятся практически все традиционно употребляемые человеком съедобные грибы [1]. Поскольку культура формируется еще на лабораторной стадии разводочного цикла, в разносторонних исследованиях высших базидиомицетов особое место занимает оптимизация физиологического и, как следствие, технологического потенциала чистой культуры [2].
Показатели характеризующие различные векторы метаболизма в разных фазах роста мицелиальных грибов, позволяют получить наиболее полную информацию о физиологически значимых процессах, происходящих в культивируемой биомассе. К таким показателям следует отнести потребленный кисло-род/потребленная глюкоза, потребленный кис-лород/общий азот, общий азот/сухая масса и др. [8–10].
В этой связи актуальными остаются дальнейшие исследования особенностей культивирования, определение условий, способствующих более быстрому росту и накоплению биомассы, подбор наиболее сбалансированных питательных сред для воспроизводства чистой культуры, разработка надежных методов контроля на лабораторной стадии разводочного цикла [3–7, 11].
Цель исследования. Оптимизация лабораторной стадии разводочного цикла чистой культуры и разработка достоверных методов контроля физиологической активности биомассы.
Конструирование сбалансированных питательных сред для воспроизводства чистой культуры, разработка надежных методов контроля на лабораторной стадии разводочного цикла остаются актуальными и при существующем уровне развития отрасли.
Материал и методы исследования. Физиологическая активность чистой культуры на питательных средах с различными видами клетчатки оценивалась нами по скорости захвата субстрата (мм/сут или дм2/сут) и показателю дыхательной активности – потребленный кислород (мл О 2 ) на единицу площади колонии (дм2) за единицу времени (час).
Чистую культуру выделяли из свежих плодовых тел грибов вешенка ( Pleurotus ostreatus ), приобретенных в торговой сети и у мелких производителей. Отбирались экземпляры хорошо сформированные, не поврежденные, без заметных признаков порчи и болезней. Кусочки первичного посевного материала, вырезанные стерильным скальпелем из плодового тела, отбирались с соблюдением всех требований микробиологической техники, исключающих вторичное инфицирование инокулята.
Первичный посев производили в чашки Петри с 2,5%-м сусло-агаром (СА), приготовленным из пивного сусла, содержащего 3 % СВ (сухих веществ), 0,5 % дрожжевого автолизата и антибиотик (гентамицин – 0,3 мл препарата на 100 мл среды).
Культуры инкубировали при температуре 24– 25оС до полного захвата поверхности агара (9– 10 дней). В течение этого времени регистрировали характер роста и выбраковывали чашки с признаками постороннего роста, с деформированными или содержащими различного рода включения колониями вешенки, что является свидетельством либо деградации культуры, либо ее скрытыми поражениями. Партии грибов, в которых выявлялась хотя бы одна колония с выраженными признаками деградации или болезни, выбраковывались полностью.
Для дальнейших исследований отбирались чашки с колониями, полностью соответствующими требованиям здоровой и активной культуры: белые без включений колонии, правильной формы с ровными краями, с хорошо сформированными волновыми кольцами. Чашки с выбранными колониями упаковывались в стерильные полиэтиленовые пакеты и хранились при 2– 4оС до использования.
Для постановки эксперимента СА с грибным мицелием из одной чашки нарезался круглым штампом ∅ 5,5 мм. Полученные блоки извлекались стерильной иглой и переносились в центр заранее приготовленных контрольных чашек с 2,5%-м СА, приготовленным из пивного сусла, содержащего 3 % СВ, 0,5 % дрожжевого автолизата и антибиотик в указанной выше дозе. Опытные среды, кроме перечисленных ингредиентов, вносили в дозе 2 % к объему среды тщательно измельченные источники целлюлозы: микрокристаллическая целлюлоза, лузга подсолнечника, очищенные от примесей пшеничные отруби, сухие опавшие листья каштана, сухие опавшие листья ясеня, лигнин гидролизный, мезокарпий грейпфрута, опилки бука. Чашки с инокулятом инкубировали при 24–25оС до полного захвата поверхности агара. В течение этого времени регистрировали скорость захвата поверхности среды и характер роста. Выбраковывались чашки с признаками постороннего роста и с деформированными или содержащими различного рода включения колониями вешенки.
Контрольные измерения скорости роста производили на 3-й, 5-й, 7-й и 10-й день инкубирования.
Определение показателя дыхательной активности производили на 15-й день инкубирования. Для этого использовали манометрический прибор собственной конструкции, состоящий из стеклянного эксикатора, манометрической трубки (бюретки), заполненной окрашенной метиленовым синим дистиллированной водой, и компенсаторной колбы. На дно реактора наливали 600–700 мл 10%-го раствора NaOH, что позволяло получить 6500 мл (6,5 дм3) свободного объема. Затем устанавливали фарфоровую подставку, на которую выстраивали из каждой серии по 13 чашек с посевами (без крышек) мицелием вниз для свободного воздухообмена. С помощью перепускного краника столбик жидкости устанавливался на «0». С этого момента регистрировалась высота поднятия столбика жидкости (мл) в течение 3 часов, что должно соответствовать потребленному количеству кислорода за регистрируемый промежуток времени. Полученную величину пересчитывали на 1 час и единицу площади колонии (дм2).
Результаты исследований и их обсуждение. Результаты эксперимента представлены в таблице. На 3-й день инкубации при оценке характера роста и измерении диаметра колоний установили, что как на контрольной, так и на экспериментальных средах единичные колонии росли со слабовыраженными неровностями по окружности, однако в процессе дальнейшего инкубирования такие неровности сглаживались и к 5–7-му дню не регистрировались. Средний диаметр колоний в контрольных чашках составил 22,4 мм (от 20,9 до 23,6), такого же диаметра колонии образовались на среде с целлюло- зой микрокристаллической – 22,4 мм (от 21,2 до 23,7), на среде с измельченной лузгой подсолнечника – 23,0 мм (от 22,0 до 23,8), с пшеничными отрубями – 21,8 мм (от 20,9 до 23,0), с измельченными листьями каштана – 22,5 мм (от 22,0 до 23,1), с лигнином гидролизным – 22,8 мм (от 22,0 до 23,2), с буковыми опилками – 20,6 мм (от 19,6 до 23,0), измельченным мезокарпием грейпфрута – 22,5 мм (от 21,5 до 23,5).
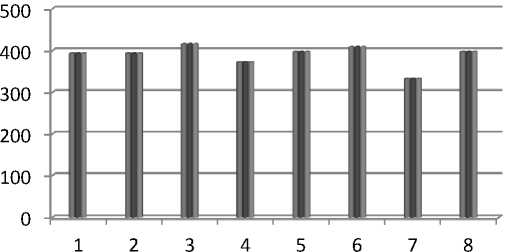
Соответственно этому площадь захвата колоний составила 393,88 мм2; 393,88; 415,26; 373,06; 397,40; 408,07; 333,12; 397,40 мм2 (рис. 1).
Показатели генеративной и дыхательной активности на различных субстратах
|
№ п/п |
Источник углерода |
3-й день |
5-й день |
7-й день |
10-й день |
О 2 |
|||||
|
∅ мм |
S мм2 |
∅ мм |
S мм2 |
∅ мм |
S мм2 |
∅ мм |
S мм2 |
Всего |
мл/дм2/ ч |
||
|
1 |
Контроль |
22,4 |
393,88 |
41,4 |
1345,45 |
69,6 |
3802,66 |
90,0 |
6358,50 |
4,5 |
0,1814 |
|
2 |
Целлюлоза |
22,4 |
393,88 |
39,3 |
1212,42 |
70,1 |
3857,49 |
90,0 |
6358,50 |
5,2 |
0,2097 |
|
3 |
Лузга подсолнечника |
23,0 |
415,26 |
51,0 |
2041,78 |
79,2 |
4924,02 |
90,0 |
6358,50 |
6,9 |
0,2782 |
|
4 |
Отруби пшеничные |
21,8 |
373,06 |
44,1 |
1526,67 |
73,8 |
4275,45 |
90,0 |
6358,50 |
7,7 |
0,3105 |
|
5 |
Листья каштана |
22,5 |
397,40 |
45,5 |
1625,14 |
71,6 |
4024,34 |
90,0 |
6358,50 |
7,1 |
0,2863 |
|
6 |
Гидролизный лигнин |
22,8 |
408,07 |
54,1 |
2297,54 |
83,3 |
5447,02 |
90,0 |
6358,50 |
6,1 |
0,2460 |
|
7 |
Опилки бука |
20,6 |
333,12 |
36,4 |
1040,09 |
66,3 |
3450,61 |
90,0 |
6358,50 |
6,5 |
0,2621 |
|
8 |
Мезокарпий грейпфрута |
22,5 |
397,40 |
46,1 |
1668,28 |
72,5 |
4126,15 |
90,0 |
6358,50 |
6,5 |
0,2621 |
-
■ 1 Контроль
-
■ 2 Целлюлоза
-
■ 3 Лузга
-
■ 4 Отруби
-
■ 5 Каштан
-
■ 6 Лигнин
-
■ 7 Бук
-
■ 8 Мезокарпий
Рис. 1. Площадь захвата на 3-й день инкубации, мм2
На 5-й день инкубации средний диаметр колоний в контрольных чашках составил 41,4 мм (от 36,5 до 47,0), на среде с целлюлозой микрокристаллической – 39,3 мм (от 37,3 до 42,3), на среде с измельченной лузгой подсолнечника – 51,0 мм (от 48,0 до 52,8), с пшеничными отрубями – 44,1 мм (от 39,3 до 48,5), с измельченными листьями каштана – 45,5 мм (от 43,3 до
-
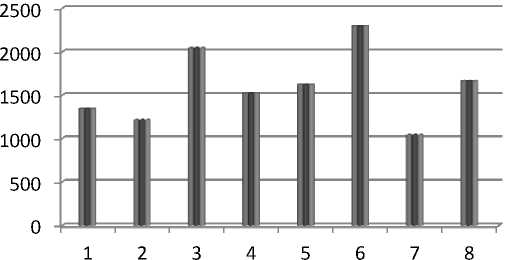
48,1) , с лигнином гидролизным – 54,1 мм (от 51,3 до 58,9), с буковыми опилками – 36,4 мм (от 34,0 до 39,1), измельченным мезокарпием грейпфрута – 46,1 мм (от 42,8 до 49,2). Соответственно этому площадь захвата колоний составила 1345,45 мм2; 1212,42; 2041,78; 1526,67; 1625,14; 2297,54; 1040,09; 1668,28 мм2(рис. 2).
-
■ 1 Контроль
-
■ 2 Целлюлоза
-
■ 3 Лузга
-
■ 4 Отруби
-
■ 5 Каштан
-
■ 6 Лигнин
-
■ 7 Бук
-
■ 8 Мезокарпий
Рис. 2. Площадь захвата на 5-й день инкубации
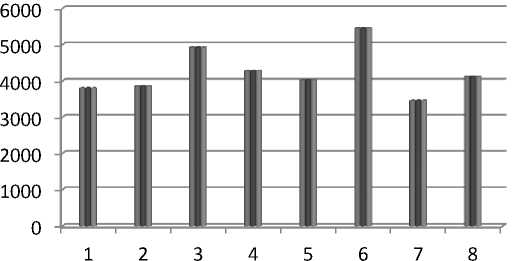
На 7-й день инкубации средний диаметр колоний в контрольных чашках составил 69,6 мм (от 65,3 до 73,9), на среде с целлюлозой микрокристаллической – 70,1 мм (от 68,3 до 73,3), на среде с измельченной лузгой подсолнечника – 79,2 мм (от 76,9 до 82,0), с пшеничными отрубями – 73,8 мм (от 70,4 до 78,6), с измельченными листьями каштана – 71,6 мм (от 64,5 до 75,8), с лигнином гидролизным – 83,3 мм (от 77,4 до 86,8), с буковыми опилками – 66,3 мм (от 64,4 до 70,0), измельченным мезокарпием грейпфрута – 72,5 мм (от 67,9 до 76,2). Соответственно этому площадь захвата колоний составила 3802,66 мм2; 3857,49; 4924,02; 4275,45; 4024,34; 5447,02; 3450,61; 4126,15 мм2 (рис. 3).
На 9-й день инкубации все среды были покрыты грибным мицелием, а на 10-й день в посевах с наиболее активным предшествующим ростом (целлюлоза, лузга, отруби, каштан, лигнин) регистрировался густой рост по стенкам чашек.
Выращенный мицелий, оцененный по культуральным свойствам, исследовали на дыхательную активность в манометрическом приборе.
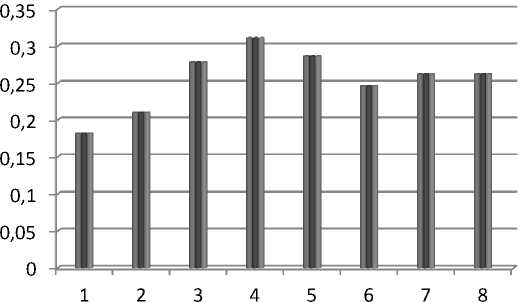
В результате было установлено (рис. 4), что 13 чашек Петри с мицелием, выращенным на контрольной среде общей площадью 8,2660 дм2, за 3 часа сместили водяной столбик на 4,5 мл по шкале бюретки, что соответствует объему потребленного кислорода. Из этого следует, что биомасса, выросшая на 1 дм2 сусло-агара указанного состава, за 1 час израсходовала 0,1814 мл О 2 . Мицелий, выращенный на среде с микрокристаллической целлюлозой общей площадью 8,2660 дм2, за 3 часа сместил водяной столбик на 5,2 мл по шкале бюретки, что соответствует объему потребленного кислорода. Из этого следует, что биомасса, выросшая на 1 дм2 сусло-агара указанного состава, за 1 час израсходовала 0,2097 мл О 2 .
-
■ 1 Контроль
-
■ 2 Целлюлоза
-
■ 3 Лузга
-
■ 4 Отруби
-
■ 5 Каштан
-
■ 6 Лигнин
-
■ 7 Бук
-
■ 8 Мезокарпий
Рис. 3. Площадь захвата на 7-й день инкубации, мм2
-
■ 1 Контроль
-
■ 2 Целлюлоза
-
■ 3 Лузга
-
■ 4 Отруби
-
■ 5 Каштан
-
■ 6 Лигнин
-
■ 7 Бук
-
■ 8 Мезокарпий
Рис. 4. Активность потребления кислорода, мл/дм2/ч
Мицелий, выращенный на среде с лузгой подсолнечника общей площадью 8,2660 дм2, за 3 часа сместил водяной столбик на 6,9 мл по шкале бюретки. Из этого следует, что биомасса, выросшая на 1 дм2 сусло-агара указанного состава, за 1 час израсходовала 0,2782 мл О 2 .
В тех же условиях мицелий, выращенный на среде с пшеничными отрубями, за 3 часа сместил водяной столбик на 7,7 мл по шкале бюретки. Из этого следует, что биомасса, выросшая на 1 дм2 сусло-агара указанного состава, за 1 час израсходовала 0,3105 мл О 2 .
Биомасса, выросшая на среде с измельченными листьями каштана, за 3 часа сместила водяной столбик на 7,1 мл. Из этого следует, что 1 дм2 сплошного роста на этой среде за 1 час израсходовал 0,2863 мл О 2 .
Биомасса, выросшая на среде с гидролизным лигнином, за 3 часа сместила водяной столбик на 6,1 мл. Из этого следует, что 1 дм2 сплошного роста на этой среде за 1 час израсходовал 0,2460 мл О 2 .
Мицелий, выращенный на среде с буковыми опилками общей площадью 8,2660 дм2, за 3 часа сместил водяной столбик на 6,5 мл по шкале бюретки. Из этого следует, что биомасса, выросшая на 1 дм2 сусло-агара указанного состава, за 1 час израсходовала 0,2621 мл О 2 .
Такой же результат показал мицелий на 13 чашках Петри, выращенный на среде с мезокарпием, за 3 часа сместивший водяной столбик на 6,5 мл по шкале бюретки, что соответствует объему потребленного кислорода. То есть биомасса, выросшая на 1 дм2 сусло-агара указанного состава, за 1 час израсходовала 0,2621 мл О2.
Выводы
-
1. Культуральные свойства и линейные размеры прироста колонии за определенный промежуток времени не могут быть использованы в качестве единственного критерия оценки качества культуры.
-
2. Оценка физиологической активности биомассы является необходимым критерием в комплексе требований, предъявляемых к качеству чистой культуры.
-
3. Определение величины дыхательной активности вполне может быть объективным критерием оценки физиологического потенциала биомассы.
-
4. Включение в состав питательных сред источников целлюлозы и других растительных полимеров положительно влияет как на морфологические, так и на физиологические свойства чистой культуры.
-
5. Лучшими индукторами генеративной активности, использованными в эксперименте, являются лигнин гидролизный ( ∅ 8,33 мм), лузга подсолнечника ( ∅ 7,92 мм) и отруби пшеничные ( ∅ 7,38 мм).
-
6. Лучшими индукторами физиологической активности, использованными в эксперименте, являются отруби пшеничные (0,3105 мл О 2 /дм2/ч), измельченные листья каштана (0,2863 мл О 2 /дм2/ч) и лузга подсолнечника (0,2782 мл О 2 /дм2/ч).
Список литературы Индукция физиологической активности чистой культуры гриба вешенка обыкновенная (Pleurotus ostreatus) на лабораторной стадии
- Бухало А. Высшие съедобные базидиомицеты в чистой культуре. -Киев: Наук. думка, 1988. -144 с.
- Викторов А.С. Разработка и освоение биотехнологии производства коммерческого мицелия на основе виноградной выжимки и лозы: автореф. дис. … канд. техн. наук. -Ялта, 1994. -18 с.
- Методы экспериментальной микологии: справ./И.А. Дудка, С.П. Вассер, И.А. Элланская . -Киев: Наук. думка, 1982. -552 с.
- Изучение интенсивности роста чистой культуры гриба вешенка/Г.С. Качмазов, И.К. Сатцаева, М.Т. Батырова //Пищевая промышленность. -2001. -№ 6. -С. 56.
- Оценка физиологической активности чистой культуры гриба вешенка (Pleurotus ostreatus)/Г.С. Качмазов, У.В. Багаева, В.А. Кочиева //Актуальные проблемы экологии и сохранения биоразнообразия России и сопредельных стран: мат-лы Всерос. науч. конф. Вып. XI. -Владикавказ: Изд-во СОГУ, 2015. -С. 20-25.
- Кураков А.В., Лаврентьев Р.Б., Соина В.С. Культурально-морфологические особенности роста мицелиальных грибов в анаэробных условиях//Микология и фитопатология. -2007. -Т. 41, № 6. -С. 526-535.
- Мюллер Е., Леффлер В. Микология: пер. с нем. -М.: Мир, 1995. -343 с.
- Рынок консервированных грибов в России 2010-2020 гг. Показатели и прогнозы. Исследования рынка//TEBIZGROUP. -2014. -82 с.
- Штаер О.В., Шнырева А.В. Структура мицелия в зоне антогонизма генетически различных индивидуумов Pleurotus ostreatus//Микология и фитопатология. -2008. -Т. 42, № 5. -С. 481-490.
- Ostreolysin enhances fruiting initiation in the oyster mushroom (Pleurotus ostreatus)/S. Berne, J. Pohleven, I. Vidic //Mycological Research. -2007. -Vol. 111, № 12. -P. 1431-1436.
- Мельникова Е.А., Литовка Ю.А., Миронов П.В. Морфологические особенности базидиального гриба Pleurotus pulmonarius в поверхностной и глубинной культуре//Вестник КрасГАУ. -2013. -№ 7. -С. 170-175.


