Индукция ионами ртути (II) микроядер в эритроцитах личинок зелёной жабы
Автор: Крюков В.И., Жучков С.А., Лазарева Т.Н., Киреева О.С., Поповичева Н.Н.
Журнал: Биология в сельском хозяйстве @biology-in-agriculture
Рубрика: Актуальные вопросы экологии
Статья в выпуске: 2 (35), 2022 года.
Бесплатный доступ
Изучены частоты микроядер (МЯ) и ядерных аномалий (ЯА) в эритроцитах личинок жабы Bufo viridis после 6-, 12-, 18- и 24-часового пребывания в воде содержащей ионы ртути (II) в концентрациях 5, 10, 20, 50, 100 и 150 мкг/л. При концентрациях ртути 5-50 мкг/л 6-часовая экспозиция вела к статистически недостоверному повышению частот МЯ и ЯА. Увеличение концентрации до 100 и 150 мкг/л вызывало статистически достоверное увеличение частоты МЯ и ЯА. Воздействие ионов ртути в течение 12, 18 и 24 часов вызывало статистически достоверное увеличение частот МЯ и ЯА при всех исследованных концентрациях. Рассмотрены возможные причины аномалий и дан краткий обзор исследований мутагенности ртути.
Ртуть, нитрат ртути, мутагенность, амфибии, bufo, микроядра, ядерные аномалии
Короткий адрес: https://sciup.org/147238695
IDR: 147238695 | УДК: 575.2.084
Induction by mercury ions (II) of micronuclei in erythrocytes of green toad larvae
The frequencies of micronuclei and nuclear anomalies in erythrocytes of larvae of the toad Bufo viridis were studied after 6-, 12-, 18-, and 24-hour exposure to water containing mercury (II) ions at concentrations of 5, 10, 20, 50, 100, and 150 µg/l. At mercury concentrations of 5-50 μg/l, a 6-hour exposure led to a statistically insignificant increase in the frequencies of micronuclei and nuclear anomalies. Increasing the concentration to 100 and 150 µg/l caused a statistically significant increase in the frequency of micronuclei and nuclear anomalies. Exposure to mercury ions for 12, 18 and 24 hours caused a statistically significant increase in the frequencies of micronuclei and nuclear anomalies at all concentrations studied. Possible causes of the anomalies are considered and a brief review of mercury mutagenicity studies is given.
Текст научной статьи Индукция ионами ртути (II) микроядер в эритроцитах личинок зелёной жабы
Целью эксперимента, результаты которого изложены ниже, был анализ цитогенетических эффектов ртути в эритроцитах личинок зелёной жабы.
Материалы и методы исследований
Объектом исследований служили эритроциты головастиков зелёной жабы Bufo viridis (L.), находившихся на 46-й и 47-й стадиях развития [1] и отловленных в природном водоёме. Водоём представлял собой заброшенный котлован, вырытый под фундамент здания и обвалованный извлечённым из него грунтом. Поверхностные стоки в водоём отсутствовали. Он пополнялся только атмосферными осадками. Поэтому можно предполагать, что в его воде не было каких-либо активных ксенобиотиков, способных влиять на исследуемые параметры. Отловленных головастиков трое суток выдерживали в лабораторном аквариуме, затем делили на группы по 7 особей. Одна группа интактных животных служила контролем. Другие группы подвергали воздействию исследуемых факторов.
Мутагенный эффект ртути исследовали, используя водные растворы нитрата ртути, Hg(NO3)2×H2O квалификации ч.д.а. Группы головастиков B. viridis помещали в аквариумы с водой, содержащей нитрат ртути в концентрациях 5, 10, 20, 50, 100 и 150 мкг Нg+2/л. на 6, 12, 18 и 24 ч. По истечении установленного времени воздействия вещества, головастиков пересаживали в аквариумы с чистой водой, где их выдерживали 24 ч. для реализации индуцированных солью металла цитогенетических нарушений в эритроцитах. По окончании указанного времени у 5 случайно выбранных в каждой группе личинок отсекали заднюю треть хвостового плавника и готовили мазки крови. Контрольные группы животных в течение все- го времени эксперимента содержали в чистой воде и мазки крови от них готовили одновременно с мазками крови опытных животных. Мазки крови высушивали, затем фиксировали в течение 30 мин в охлаждённой смеси этилового спирта с уксусной кислотой (3:1) промывали дистиллированной водой и окрашивали азур-эозином по Романовскому.
Препараты просматривали при увеличении (100×15×1,5)× (микроскоп «Laboval 4»). На окрашенных препаратах подсчитывали по 2 тыс. нормальных эритроцитов от каждого животного, фиксируя при этом (дополнительно к количеству нормальных эритроцитов) число клеток с микроядрами (далее – МЯ) и ядерными аномалиями (далее – ЯА). Экспериментальный материал получен до опубликования классификации ЯА [2], поэтому МЯ типизировали в соответствии со схемой [3] Краткая характеристика аномалий приведена в примечании к таблице 1.
Частоты МЯ и ЯА выражали в долях от общего числа проанализированных эритроцитов и процентах. Достоверность различий между сравниваемыми частотами определяли с помощью критерия u для сравнения малых (р<0,2) и больших (p>0,8) долей после их φ –преобразования [4, с. 154-169]. Интерполяция эмпирического распределения величин теоретическим известным распределением выполнена с использованием программы Stadia 4.5.
Результаты и обсуждение
Результаты микроскопического анализа показаны в табл. 1.
Таблица 1 – Количество микроядер и ядерных аномалий различных типов в периферической крови личинок
B. viridis , индуцированное различными экспозициями и концентрациями ртути
|
Время воздействия, ч |
Концентрация Нg+2, мкг/л |
Всего клеток |
Число клеток с микроядрами и ядерными аномалиями* |
||||||
|
1 а |
1 б |
1 в |
1 г-I |
г-II |
1 д |
1 е |
|||
|
Контроль |
10042 |
18 |
19 |
4 |
1 |
||||
|
6 |
5 |
10050 |
14 |
19 |
5 |
1 |
3 |
7 |
1 |
|
10 |
10049 |
9 |
26 |
4 |
– |
8 |
– |
2 |
|
|
20 |
10058 |
19 |
29 |
2 |
– |
– |
4 |
4 |
|
|
50 |
10063 |
18 |
40 |
2 |
– |
– |
3 |
– |
|
|
100 |
10092 |
35 |
42 |
2 |
– |
1 |
– |
12 |
|
|
150 |
10091 |
29 |
35 |
9 |
1 |
2 |
4 |
11 |
|
|
12 |
5 |
10068 |
22 |
25 |
2 |
1 |
11 |
4 |
3 |
|
10 |
10076 |
29 |
21 |
8 |
– |
5 |
9 |
4 |
|
|
20 |
10118 |
32 |
58 |
4 |
2 |
4 |
6 |
12 |
|
|
50 |
10103 |
35 |
28 |
14 |
2 |
7 |
11 |
6 |
|
|
100 |
10119 |
39 |
43 |
6 |
– |
8 |
9 |
17 |
|
|
150 |
10114 |
41 |
32 |
19 |
1 |
4 |
7 |
10 |
|
|
18 |
5 |
10078 |
31 |
25 |
4 |
2 |
8 |
5 |
3 |
|
10 |
10112 |
33 |
43 |
17 |
– |
7 |
9 |
2 |
|
|
20 |
10148 |
42 |
68 |
23 |
1 |
2 |
5 |
7 |
|
|
50 |
10155 |
39 |
55 |
27 |
2 |
9 |
14 |
9 |
|
|
100 |
10179 |
59 |
79 |
24 |
– |
4 |
13 |
– |
|
|
150 |
10198 |
70 |
96 |
11 |
– |
2 |
7 |
12 |
|
|
24 |
5 |
10099 |
29 |
41 |
19 |
– |
3 |
4 |
3 |
|
10 |
10106 |
34 |
36 |
14 |
1 |
9 |
8 |
4 |
|
|
20 |
10162 |
47 |
72 |
19 |
3 |
7 |
14 |
||
|
50 |
10160 |
43 |
54 |
24 |
4 |
16 |
11 |
8 |
|
|
100 |
10182 |
43 |
95 |
18 |
3 |
– |
6 |
17 |
|
|
150 |
10194 |
66 |
83 |
32 |
2 |
– |
4 |
7 |
|
*Примечание. Микроядра, изолированные от ядра (а), примыкающие к ядру (б), соединёнными с ядром нитью хроматина (в). Ядерные аномалии: неоформленного хроматиновый материал в виде палочек (г-I) или клубков (г-II), округлые образо- вания ядерного материала в виде лопастей (д), двуядерные» клетки (е).
Статистический анализ этих данных свидетель- статистически достоверному увеличению частоты ствует (табл. 2), что при 6-часовой экспозиции ртуть в аномалий. Экспозиции длительностью 12 часов и бо-концентрациях до 50 мкг/л не вызывала статистиче- лее вызывали статистически достоверное увеличение ски достоверного увеличения частот МЯ и ЯА. Одна- частот МЯ и ЯА при всех исследованных концентра-ко концентрации 100 и более мкг/л ртути приводили к циях.
Таблица 2 – Частоты эритроцитов с микроядрами в периферической крови личинок B. viridis после воздействия различных экспозиций и концентраций ртути
|
Время воздействия, ч |
Концентрация Hg+2, мкг/л |
Клеток с аномалиями |
Критерий Фишера |
Достоверность различий, Р |
|
|
количество |
частота (р ±τ·σ р ), % |
||||
|
Контроль |
42 |
0,42 ±0,13 |
|||
|
6 |
5 |
50 |
0,50+0,14 |
0,73 |
>0,05 |
|
10 |
49 |
0,49 ±0,14 |
0,63 |
>0,05 |
|
|
20 |
58 |
0,58 ±0,15 |
1,50 |
>0,05 |
|
|
50 |
63 |
0,63 ±0,15 |
1,95 |
>0,05 |
|
|
100 |
92 |
0,91 ±0,19 |
4,29 |
<0,001 |
|
|
150 |
91 |
0,90 ±0,18 |
4,22 |
<0,001 |
|
|
12 |
5 |
68 |
0,68 ±0,16 |
2,39 |
<0,05 |
|
10 |
76 |
0,75 ±0,17 |
3,06 |
<0,01 |
|
|
20 |
118 |
1,17 ±0,21 |
6,09 |
<0,001 |
|
|
50 |
103 |
1,02 ±0,20 |
5,08 |
<0,001 |
|
|
100 |
119 |
1,18 ±0,21 |
6,15 |
<0,001 |
|
|
150 |
114 |
1,13 ±0,21 |
5,83 |
<0,001 |
|
|
18 |
5 |
78 |
0,77 ±0,17 |
3,22 |
<0,01 |
|
10 |
109 |
1,11 ±0,20 |
5,69 |
<0,001 |
|
|
20 |
148 |
1,46 ±0,23 |
7,92 |
<0,001 |
|
|
50 |
155 |
1,52 ±0,24 |
8,43 |
<0,001 |
|
|
100 |
179 |
1,76 ±0,26 |
9,62 |
<0,001 |
|
|
150 |
198 |
1,94 ±0,27 |
10,60 |
<0,001 |
|
|
24 |
5 |
99 |
0,98±0,19 |
4,79 |
<0,001 |
|
10 |
106 |
1,05 ±0,20 |
5,23 |
<0,001 |
|
|
20 |
162 |
1,59 ±0,24 |
8,71 |
<0,001 |
|
|
50 |
160 |
1,57 ±0,24 |
8,60 |
<0,001 |
|
|
100 |
182 |
1,79 ±0,26 |
9,79 |
<0,001 |
|
|
150 |
194 |
1,90 ±0,27 |
10,40 |
<0,001 |
|
Для определения силы влияния концентраций ртути и продолжительности её экспозиции на частоту индуцируемых МЯ был проведён двухфакторный параметрический дисперсионный анализ (табл. 3). Его результаты доказывают существование статистически достоверного отклика исследуемого параметра (частоты МЯ и ЯА) на оба фактора.
Таблица 3 – Результаты двухфакторного дисперсионного анализа влияния длительности экспозиции и концентрации ртути на частоту эритроцитов с МЯ в периферической крови личинок B. viridis.
|
Источник |
Сумма квадратов |
Число степеней свободы |
Средняя сумма квадратов |
Сила влияния факторов |
|
Экспозиция |
2,667 |
3 |
0,889 |
0,9696 |
|
Концентрация Нg+2 |
1,729 |
5 |
0,346 |
0,9292 |
|
Регрес.остатки |
0,331 |
15 |
0,022 |
|
|
Общая вариация |
4,728 |
23 |
0,206 |
|
|
F (Экспоз.)=40,3 F (Концент.)=15,7 |
Р<0,001 Р<0,001 |
Степ. свободы =3, 15 Степ. свободы = 4, 15 |
Есть влияние Есть влияние |
|
Кроме интерфазных эритроцитов с МЯ и ЯА на препаратах были обнаружены аномальные эритроциты, находящиеся на стадии метафазы митоза. Анома- лии заключались в том, что эти клетки вместо полного набора хромосом содержала всего одну или несколько метафазных хромосом (рис. 1).
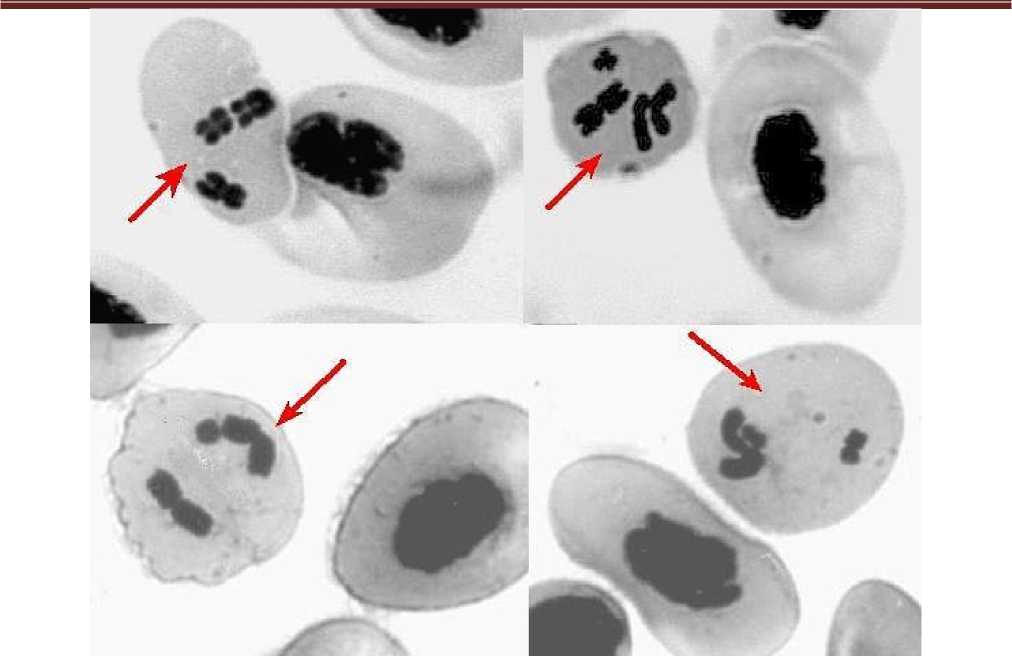
Рис. 1. Аномальные эритроциты с единичными метафазными хромосомами, возникшие после воздействия ртути
При сравнительном анализе частот различных МЯ и ЯА, индуцированных различными экспозициями ртути, видно некоторое уменьшение доли клеток с изолированными МЯ за счёт увеличения доли клеток с примыкающими МЯ, клеток с большими фрагментами хроматина и двуядерных клеток. Появление таких клеток свидетельствует о том, что неорганическая ртуть нарушает не только структуру хромосом, но и митотическое веретено деления и, возможно, механизмы цитокинеза. В настоящее время известно, что соединения ртути могут нарушать структуры клеточ- ного веретена благодаря аффинности к тиоловым группам. Аномальное распределение хромосом между делящимися клетками под влиянием НgCl2 ранее было обнаружено на клетках Vicia faba [5].
Зависимость частоты ядерных аномалий в эритроцитах личинок B. viridis от концентрации ртути при различной длительности экспозиции удовлетворительно интерполируется уравнениями вида · со следующими величинами коэффициентов (табл. 4).
Таблица 4 - Величины коэффициентов уравнения у=а+Ьx* , интерполирующих зависимость частоты микроядер и ядерных аномалий в эритроцитах личинок B. viridis от концентрации ртути при различной продолжительности ее воздействия
|
Длительность экспозиции, ч |
а |
b |
R |
F |
P |
|
6 |
0,389 |
4,36 ⋅ 10–2 |
0,968 |
59,3 |
1,00 ⋅ 10–4 |
|
12 |
0,596 |
5,56 ⋅ 10–2 |
0,829 |
8,8 |
1,90 ⋅ 10–3 |
|
18 |
0,625 |
0,119 |
0,947 |
34,9 |
2,00 ⋅ 10–4 |
|
24 |
0,707 |
0,111 |
0,918 |
21,3 |
4,00 ⋅ 10–4 |
Примечание: R – множественный коэффициент корреляции; F – значение критерия Фишера; Р – уровень значимости нулевой гипотезы.
Результаты исследований мутагенности ртути существенно зависят от химической природы образованного ею вещества и типа клеток, используемых для анализа.
Большинство бактериальных генетических тестов показали, что соединения ртути не мутагенны для прокариот. Объяснют это явление высокой рези- стентностью бактериальной клеточной мембраны к проникновению ионов ртути. У некоторых прокариот обнаружены ферментативные механизмы детоксикации неорганических и органических соединений ртути с использованием, соответственно, ртутной редуктазы (MerA) и ртутьорганической лиазы (MerB) [6].
У дрожжей хлорид ртути подавлял митотическую генную конверсию, что, возможно, связано с ингибированием ртутью ферментов репарации пред-мутационных повреждений [5].
Нитрат ртути в концентрации 1×10–5 М не проявлял мутагенных свойств при воздействии на клетки корневой меристемы С. capillaris, но иодид ртути был мутагенен при значительно меньшей концентрации (3×10–6 М) [7]. Хлорид ртути в концентрации 0,05 и 0,1%, хлорид этилртути (0,01-2,5%) и ацетат фе-нилртути (0,01-1,0%) вызывали аберрации хромосом, повышали частоту полиплоидных и двуядерных клеток в клетках меристемы корешков Allium сера, индуцировали у Vicia faba в мейозе образование МЯ и аберраций хромосом [8] Мутагенность ртути для растений Pisum sativum подтверждена исследованиями [9]
Доказана мутагенность различных соединений ртути для рыб [10-18]. Очень мало публикаций, освещающих вопросы мутагенности ртути для амфибий и пресмыкающихся. Установлено, что хлорид ртути (HgCl 2 ) и метилхлорид ртути (CH 3 HgCl) индуцировал нарушение митоза, разрывы хромосом и образование МЯ в клетках тритона Pleurodeles waltl [19]. В тканях кайманов, обитающих на территориях, прилегающих к горнодобывающим предприятиям Колумбии, установлено 6-15 кратное накопление ртути. У таких животных методом кометного анализа выявлено значительное увеличение частоты повреждений в ДНК [20]
Токсичность различных соединений ртути для птиц освещена во многих публикациях. Вместе тем публикаций результатов исследования мутагенности ртути и её соединений для птиц мы не обнаружили.
В культивируемых клетках млекопитающих ртуть даже при низких концентрациях индуцировала одноцепочечные разрывы ДНК. Соединения ртути увеличивали частоту мутирования в локусе тимидин-киназы в клетках лимфомы мыши [21], индуцировали сестринские хроматидные обмены и аберрации хромосом в культивируемых клетках СНО и лимфоцитах человека [22-24]. Эксперименты, выполненные с культурой эмбриональных фибробластов мыши, привели к заключению, что наблюдаемые мутации могут быть следствием окислительных процессов, а не прямым взаимодействием ртути с ядерной ДНК [25].
Соединения ртути, попадающие в организм млекопитающих, могут индуцировать точковые мутации, доминантные летальные мутации, хромосомные и геномные повреждения. Так, хлорид ртути в дозе 0,375 мг/кг внутрижелудочно вводимый крысам в течение 45 дней вызывал повреждения ДНК, обусловленные усилением окислительного стресса и митохондриальной дисфункцией [26]. Одноразовое внутрибрюшинное введение самцам крыс дихлорида ртути в количестве ЛД 50 и 2/3 ЛД 50 (7,5 мг/кг и 5 мг/кг, соответственно) приводило к статистически достоверному увеличению частоты МЯ в полихроматических эритроцитах костного мозга [27-28]. Хлорид ртути и хлорид метилртути индуцировали статистически достоверное увеличение частоты доминантных летальных мутаций у самок крыс и мышей [29-31].
У людей, употреблявших в пищу мясо и рыбу, загрязнённые соединениями ртути, а также лиц, подверженных в процессе профессиональной деятельности воздействию паров и аэрозолей ртутьсодержащих веществ, обнаруживали существенное увеличение частот сестринских хроматидных обменов, структурных и численных аберраций хромосом и МЯ в клетках различных тканей [32-35].
В последнее десятилетие получены сведения, указывающие на то, что ртуть может быть активна эпигенетически, поскольку способна влиять на метилирование ДНК у млекопитающих [36-37]. Широкое варьирование результатов исследования биологических свойств ртути может быть обусловлено не только различиями в протоколах и условиях экспериментов, но и различиями эпигенетических механизмов регуляции генов, участвующих в метаболизме ртути у организмов разных видов.
Заключение
Ртуть интенсивно используется в различных отраслях промышленности, и большое её количество поступает в окружающую среду с отходами, стоками и газовыми выбросами. Эксперты ВОЗ прогнозируют дальнейший рост концентрации ртути в окружающей среде в результате хозяйственной деятельности человека, а изменение климата, как ожидается, усугубит воздействие этого вездесущего загрязнителя. Токсичность ртути хорошо исследована, её канцерогенность остаётся предметом споров и дальнейших исследований онкологов. Факты мутагенность ртути установлены для растений и многих типов и видов животных. Вместе с тем степень изученности мутагенных эффектов у разных классов позвоночных животных очень различна. Мутагенность соединений ртути для амфибий, пресмыкающихся и птиц рассматривается в очень небольшом количестве публикаций. Полученные нами результаты доказывают потенциальную генетическую опасность неорганических соединений ртути для амфибий и указывают на необходимость генетического мониторинга животных, обитающих в водоёмах, расположенных в районах ртутного загрязнения экосистем.
Выводы
-
1. Пребывание личинок зелёной жабы в воде содержащей 5, 10, 20 и 50 мкг/л ионов ртути в течение 6 часов приводит к некоторому повышению частот микроядер и ядерных аномалий в эритроцитах подопытных животных, но этот рост остаётся статистически недостоверным.
-
2. Увеличение концентрации ионов ртути до 100 и 150 мкг/л при 6 часовой экспозиции вызывает статистически достоверное увеличение частот микроядер и ядерных аномалий в эритроцитах личинок.
-
3. Воздействие ионов ртути в течение 12, 18 и 24 часов вызывало статистически достоверное увеличение частот микроядер и ядерных аномалий при всех исследованных концентрациях.
Список литературы Индукция ионами ртути (II) микроядер в эритроцитах личинок зелёной жабы
- Дабагян Н.В., Слепцова Л.А. Травяная лягушка Rana temporaria L. //Объекты биологии развития. -М.: Наука, 1975. -С. 442-462.
- Крюков В.И. Вариант методики учёта ядерных аномалий в эритроцитах птиц. // Вестник аграрной науки, 2020, № 1. -С.81-100.
- Жулева Л.Ю., Дубинин Н.П. Использование микроядерного теста для оценки экологической обстановки в районах Астраханской области //Генетика. -1994. Т. 30, № 7. -С. 999-1004.
- Урбах В.Ю. Статистический анализ в биологических и медицинских исследованиях. -М.: Медицина, 1975. -295 с.
- Helmi S. et al. Genotoxity of inorganic mercury. / Helmi S., El-Seehi M., El-Ziat H. // Environ. and mol. mutagenes. 1989. V. 14. Suppl. -P. 87.
- Christakis C.F. et al. Expanded diversity and phylogeny of mer genes broadens mercury resistance paradigms and reveals an origin for MerA among thermophilic Archaea. / Christos A. Christakis, Tamar Barkay, Eric S. Boyd. // Front Microbiol. 2021. V.12 № 682605.
- Реутова Н.В. Мутагенный потенциал ряда тяжёлых металлов //Экологическая генетика. 2015. Т. 13. № 3. - С. 70-75
- Nandi S. Studies on the cytogenetic effect of some mercuric fungicides //Cytologia. 1985. V. 50. № 4. -P. 921-926.
- Azevedo R. et al. Inorganic Hg toxicity in plants: A comparison of different genotoxic parameters. / Raquel Azevedo, Eleazar Rodriguez, Rafael José Mendes et al. // Plant Physiol. Biochem. 2018. V. 125. -P. 247-254.
- Krishnaja A.P., Rege M.S. Induction of chromosomal aberrations in fish Boleophthalmus dussumieri after exposure in vivo to mitomycin C and heavy metals mercury, selenium and chromium. // Mutat. Res. 1982. V. 102. № 1. -P. 71-82.
- Al-Sabti K. An in vitro binucleated blocked hepatic cell technique for genotoxicity testing in fish //Mutat. Res. Environ. Mutatgenes and Related Subj. 1995. -V. 335, № 2. -P. 109-120.
- Cava§ T. In vivo genotoxicity of mercury chloride and lead acetate: Micronucleus test on acridine orange stained fish cells. // Food and Chemical Toxicology. 2008. V. 46. № 1. -P. 352-358.
- Rocha C.A.M. et al. The micronucleus assay in fish species as an important tool for xenobiotic exposure risk assessment - a brief review and an example using neotropical fish exposed to methylmercury / Carlos Alberto Machado da Rocha, Raquel Alves dos Santos, Marcelo de Oliveira Bahia et al. // Reviews in Fisheries Science. 2009. V. 17. № 4. -P 478-484. .
- Rocha C.A.M. et al. Studies of micronuclei and other nuclear abnormalities in red blood cells of Colossoma macropomum exposed to methylmer-cury. / Rocha, C.A.M. da, Cunha, L.A. da, Pinheiro, R.H. da S. et al. // Genetics and Molecular Biology. 2011 V. 34. № 4. -P. 694-697. .
- Rocha C et al. Comet Assay and Micronucleus Test in Circulating Erythrocytes ofAequidens tetramer-us Exposed to Methylmercury / Carlos Rocha, Bruno Cavalcanti, Claudia Ó. Pessoa et al. // In Vivo. November 2011, 25 (6) 929-933.
- Rodríguez A.P.C. et al. Chronic effects of methylmercury on Astronotus ocellatus, an Amazonian fish species. / Rodríguez, A.P.C., Maciel, P. Silva, L.C.P. et al. // Journal of Aquatic Pollution and Toxicology. 1917. V. 1. № 2 -P. 1-14.
- Nirchio M. et al. Genotoxic effects of mercury chloride on the Neotropical fish Andinoacara rivula-tus (Cichlidae: Cichlasomatini). / Nirchio M., Choco-Veintimilla O., Quizhpe-Cordero P.F. et al. // Revista de Biología Tropical, 2019. V. 67. № 4. -P. 745-754.
- Maktoof A.A. et al. Study the impact of the concentration of mercury chloride on micronuclei formation and some organs of juveniles of Ctenopharyngodon idella. / Afrah Abed Maktoof, Rasha Salih Nuhair, Awatif Mokar Al-Saaedi et al. // Indian Journal of Forensic Medicine & Toxicology. 2020. V. 14. № 3. -P. 2690-2695
- Zoll C. et al. Genotoxicity and bioaccumulation of methyl mercury and mercuric chloride in vivo in the newt Pleurodeles waltl. / C. Zoll, E. Saouter, A. Boudou et al. // Mutagenesis. 1988. V. 3. № 4. -P. 337-343.
- Marrugo-Negrete J. et al. Mercury levels and genotoxic effect in caimans from tropical ecosystems impacted by gold mining. / Marrugo-Negrete José, Durango Hernández José, Calao Ramos Clelia et al // Science of The Total Environment. 2019. V. 664.
- Oberly T.J., Piper C.E. Mutagenicity of metal salts in the L5178Y mouse lymhpoma assay //Environ. Mutagenes. 1980. V. 2, № 2. -P. 281.
- Howard W. et al. 1991. Induction of chromosome changes by metal compounds in cultured CHO cells / Howard W., Leonard B., Moody W. // Toxicol. Lett. 1991. V. 56, № 1-2. -P. 179-186.
- Betti C. et al. Genotoxic effects induced by mercuric compounds in human lymphocytes. / Betti C., Dav-ini T., Barale R. // Mutat. Res. Rev. Genet. Toxicol. 1992. V. 271. № 2. -P.165-166.
- Kochhar T.S. et al. Influence of organomercurials on the induction chromosome aberrations in CHO cells. / Kochhar T.S., Wilson A., Andersen A. // Environ. and Mol. Mutagenes. 1994. V. 23. -P. 33.
- Schurz F et al. Mutagenicity of mercury chloride and mechanisms of cellular defence: the role of metal-binding proteins. / F Schurz, M Sabater-Vilar, J Fink-Gremmels // Mutagenesis. 2000. V. 15, № 6. -P. 525-530.
- Aragao W.A.B.A. et al. DNA Damage and Proteomic Profile Changes in Rat Salivary Glands After Chronic Exposure to Inorganic Mercury. / Walessa Alana Braganga Aragao, Leonardo Oliveira Bittencourt, Leidiane Alencar de Oliveira Lima et al. // Biol. Trace. Elem. Res. 2022. DOI: 10.1007/s12011-021-02986-7.
- Бошнакова Е. Влияние на живачния двухлорид и на мангановия двухлорид въерху доминантните летални мутации у лабораторни животни //Генет. и селек. (Болгария). 1989а. Т. 22. № 1. -С. 7175.
- Бошнакова Е. Микронуклеус-тест при лабораторни животни, въздействувани с живачен двухло-рид и манганов двухлорид //Генет. и селек. (Болгария). 19896. Т. 22. № 3. -С. 253-258.
- Васильева И.М. и др. Определение мутагенного потенциала одного из загрязнителей окружающей среды - хлорида ртути. / Васильева И.М., Сдиркова Н.И., Засухина Г.Д. // Цитология и генетика. 1982. Т. 16, № 2. -С. 21-24.
- Zasukhina G.D. et al. Mutagenic effect of thallium and mercury salts on rodent cells with different repair activities. / Zasukhina G.D., Vasilyeva I.M., Sdirkova N.I. //Mutat. Res. 1983. V. 124, № 2. -P. 163-173.
- Verschaeve I., Leonard A. Dominant lethal test in female mice treated with methyl mercury chloride //Mutat. Res. 1984. V. 136, № 2. -P. 131-136.
- Monsalve M.V., Chiappe C. Genetic effects of methylmercury in human chromosomes. I. A cytogenetic study of people exposed through eating contaminated fish // Environ and Mol. Meta-genes. 1987. V.10, № 4. -P. 367-376.
- Loprieno G. et al. Cytogenetic monitoring of fishermen exposed to mercury through fish consumption. / Loprieno G., Franchi E., Petrozzi L. // Mutat. Res. Rev. Genet. Toxicol. 1992. V. 271, № 2. -P.192-193.
- Kocadal K. et al. Cellular pathologies and genotoxic effects arising secondary to heavy metal exposure: A review. / K. Kocadal, F.B. Alkas, D. Battal, S. Saygi. // Human and Experimental Toxicology. 2020. V. 39. № 1. -P. 3-13.
- Sanchez-Alarcon J. et al. Genotoxicity of mercury and its derivatives demonstrated in vitro and in vivo in human populations studies. Systematic review. / Juana Sanchez-Alarcon, Mirta Milic, Lilia Patricia Bustamante-Montes et al. // Toxics. 2021. V. 9. № 12. -P. 326.
- Basu N. et al. Effects of methylmercury on epigenetic markers in three model species: Mink, chicken and yellow perch. / Niladri Basu, Jessica Head, Dong-Ha Nam et al. // Comparative Biochemistry and Physiology. Part C: Toxicology & Pharmacology. 2013. V. 157. № 3. -P. 322-327.
- Basu N. et al. Ecogenetics of mercury: from genetic polymorphisms and epigenetics to risk assessment and decision-making. / Niladri Basu, Jaclyn M. Goodrich, Jessica Head // Environmental Toxicology and Chemistry. 2014. V. 33. -P. 1248-1258.


