Индукция микроядер в эритроцитах рыб водными вытяжками из ванадийсодержащих промотходов, захороненных на территории Орловской городской свалки ТБО
Автор: Крюков В.И., Лактюшина Н.В., Беляева А.О.
Журнал: Биология в сельском хозяйстве @biology-in-agriculture
Рубрика: Современные пробелы экологии
Статья в выпуске: 2 (27), 2020 года.
Бесплатный доступ
Изложены результаты исследования мутагенности компонентов, содержащихся в промышленном отходе производства пентаоксида ванадия - гипсовом шламе, в маркетинговых целях называемого «композицией известково-гипсовой» (КИГ). 25000 тонн КИГ были захоронены на необорудованной защитными сооружениями орловской городской свалке ТБО. Согласно расчётам, в захороненном шламе может содержаться около 920 тонн пентаоксида ванадия, обладающего канцерогенными и мутагенными свойствами. Образец захороненного шлама предоставлен для анализа общественной природоохранной организацией. Из шлама была получена водная вытяжка, в которую на 7 суток помещали рыб данио. По истечении этого срока готовили мазки крови рыб. В качестве контроля использовали мазки крови рыб, обитавших в чистой воде, а также в водной вытяжке из садовой почвы. В каждом варианте исследованы мазки крови от 6 рыб и по ≈7 тыс. эритроцитов от каждой рыбы. Частоты эритроцитов с микроядрами составили 1,03, 1,32 и 2,23 ‰ у рыб неделю выдержанных, соответственно, в чистой воде, вытяжке из садовой почвы и КИГ-вытяжке. Первые две величины не имеют статистически достоверных различий. Частота микроядер у рыб, неделю обитавших в КИГ-вытяжке отличается от контрольной частоты при Р≤0,001. Различия суммарных частот ядерных аномалий у рыб контрольной и КИГ выборки также статистически достоверны.
Рыбы, эритроциты, микроядра, ванадий, мутагенез
Короткий адрес: https://sciup.org/147231005
IDR: 147231005 | УДК: 504.75
Induction of micronuclei in the fish erythrocytes by a water extracts from vanadium-containing waste, which are buried in the territory of the Orel city solid waste dump
The article presents the results of the study of the mutagenicity of components, extracted from lime sludge. This lime sludge is a waste of vanadium pentoxide production. 25,000 tons of the lime sludge were buried in the Orel city landfill of municipal solid waste. According to the calculations, the buried sludge may contain about 920 tons of vanadium pentoxide, which has carcinogenic and mutagenic properties. A water extract was obtained from the sludge, in which zebrafish were placed for 7 days. After this period, blood smears of fish were prepared. The control was blood smears of fish, which were kept in clean water and in a water extract from garden soil. Blood smears from 6 fish were examined in each variant. Seven thousand red blood cells were analyzed in blood smears of each fish. The erythrocyte frequencies with micronuclei were 1.03, 1.32 and 2.23 ‰ in fish that lived, respectively, in clean water, in a soil extract and in a sludge extract. The first two values of micronuclei have no statistically significant differences. The frequency of micronuclei in fish from sludge extracts differs from the control frequency at P≤0.001. The total frequencies of nuclear anomalies in the erythrocytes of fish of the control group and fish living in the aqueous sludge extract are also statistically significant at P≤0.001.
Текст научной статьи Индукция микроядер в эритроцитах рыб водными вытяжками из ванадийсодержащих промотходов, захороненных на территории Орловской городской свалки ТБО
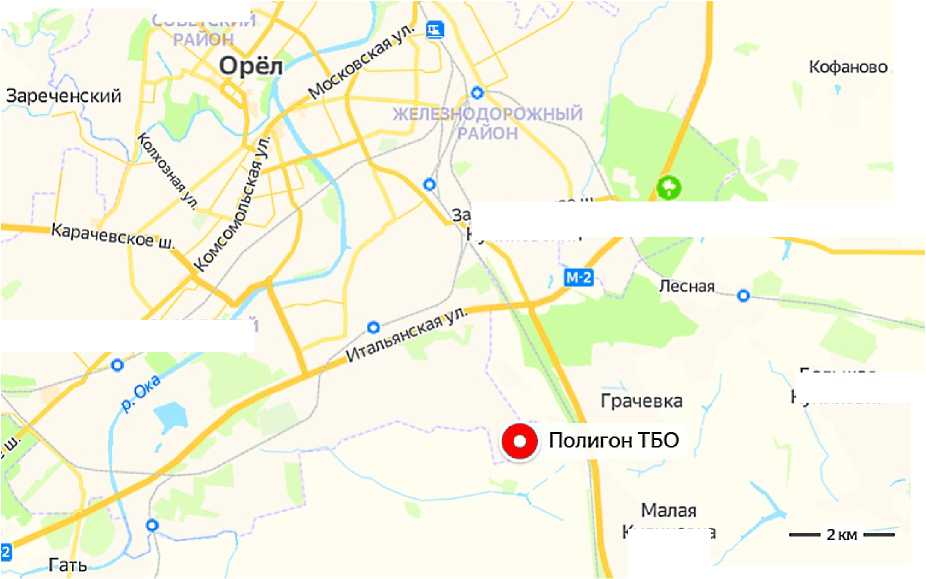
щая среда Орловской области [1-4]. Одной из серьёзных проблем охраны окружающей среды Орловской области является захоронение бытовых и промышленных отходов. В Орловской области существуют только два полигона со всеми официальными разрешительными документами: в Ливнах («Коммунсер-вис») и во Мценске (компания «Русресурс»). ТБО областного центра, в котором проживают 309 тыс. человек, складируются на необустроенной городской свал- ке, возникшей в 70-х годах прошлого столетия, в настоящее время занимающей площадь 33 гектара и испытывающей сложные организационные проблемы из-за столкновения экономических интересов ООО «Экополис» и АО «ЭкоСити». Именно эта необорудованная городская свалка стала источником серьёзной экологической проблемы. Она возникла в результате захоронения на территории городской свалки ТБО двадцати пяти тысяч тонн гипсового шлама, образующегося в ОАО «ЕВРАЗ Ванадий Тула» после переработки ванадийсодержащего сырья. Этот шлам вначале складировали в шломонакопителях самого ОАО «ЕВРАЗ Ванадий-Тула». После их заполнения перед предприятием встал вопрос захоронения вновь образующихся промотходов. Менеджеры ОАО «ЕВРАЗ Ванадий-Тула» нашли выход из положения: они переименовали гипсовый шлам в «композицию известково-гипсовую» (далее сокращённо - КИГ) и начали продавать её как материал для изоляции ТБО на свал- ках и полигонах. В 2013 году ОАО «ЕВРАЗ Ванадий -Тула» под видом КИГ складировал на необорудованных для хранения промотходов тульских полигонах ТБО более 40 тысяч тонн гипсового шлама. Это послужило Управлению Федеральной службы по надзору в сфере природопользования (Росприроднадзора) по Тульской области основанием для судебного иска к ОАО «ЕВРАЗ Ванадий-Тула». В сложившейся ситуации судебные инстанции встали на сторону акционерного общества, тем самым дав ему возможность сэкономить 177 млн. руб. штрафа за нанесение экологического вреда окружающей среде [5]. Однако для захоронения шлама нужно было искать другое место. Его нашли на орловской городской свалке ТБО. В 20152017 гг. 25 тыс. тонн гипсового шлама (КИГ) было закуплено орловским ЗАО «ОПЭК» и захоронено на территории Орловской городской свалки ТБО, расположенной, практически в черте города (рис. 1.)
СОВЕТСКИЙ
ЗАВОДСКОЙ 'РАЙОН
Крутая Гора
Куликовка
Рис. 1. Место захоронения на территории города Орла
25 тысяч тонн гипсового шлама (КИГ), содержащего пентаоксид ванадия.
«легощенское ш. дндриабужский Куликовский
Большая Куликовка
Используемые в ОАО «ЕВРАЗ Ванадий Тула» технологии не позволяют извлечь из гипсового шлама весь ванадий. Массовая доля пентаоксида ванадия в разных партиях гипсового шлама варьирует в пределах 1,4-4,0% [6] и в среднем составляет 3,69% [7]. Таким образом, на территории орловской городской свалки вместе с 25 тысячами тонн гипсового шлама ЗАО «ОПЭК» захоронил около 922 тонн пентаоксида ванадия. Под действием атмосферных осадков, содержащихся в гипсовом шламе, пентаоксид ванадия постепенно трансформируется в водорастворимые формы. По этой причине по краям свалки в канавах со стоками дождевых и талых вод концентрации ванадия регистрируются на уровне 58 ПДК [8]. По результатам анализа правовых оснований для размещения гипсового шлама на орловской городской свалке ТБО было возбуждено судебное разбирательство. По его решению все 25 тыс. тонн шлама должны были быть удалены с территории свалки. Однако решение суда не выполнено, и токсиканты, вымываемые атмосферными осадками из гипсового шлама, продолжают угрожать экологии реки Рыбница, в водосборе которой расположена свалка. Сложившаяся ситуация не привлекает внимания орловских природоохранных ведомств и беспокоит только общественные экологические организации. По просьбе одной из таких общественных организаций был выполнен анализ потенциальной мутагенности для рыб водных вытяжек гипсового шлама (КИГ), результаты которого представлены в данной публикации.
Материалы и методы. Материалом для исследования служил образец гипсового шлама (КИГ) мас- сой ≈5 кг, собранный на территории орловской городской свалки ТБО активистами одной из областных общественных природоохранных организаций. Для сравнения генотоксичности КИГ использовали образец садовой почвы, собранной на целинном участке садового товарищества «Дружба» с глубины от 10 до 20 см (после съёма верхнего 10-сантиметрового слоя почвы). Оба образца были доведены до воздушносухого состояния и измельчены. Пробы массой 1 кг каждая были залиты 10 литрами предварительно отстоянной в течение 3 суток питьевой водопроводной водой. Пробы были тщательно перемешаны и оставлены на 72 часа для экстракции водорастворимых компонентов и отстаивания. По истечении указанного времени по 6 литров прозрачной надосадочной жидкости с помощью сифона были слиты в 20-литровые аквариумы и разбавлены 12 литрами отстоянной водопроводной воды. Эти два 18-литровых образца водных вытяжек были использованы в анализе их генотоксичности для рыб. Третий аквариум с чистой, отстоянной в течение трёх суток водопроводной водой использовали как контрольный.
В каждый из трёх аквариумов на 7 суток поме- щали по 3 рыбы данио (Danio rerio). По истечении этого времени рыб анестезировали в суспензии эвгенола (гвоздичного масла) из расчёта 0,03 мл/л воды [9], отсекали хвостовой плавник, выступившую каплю крови помещали на предметное стекло и делали мазок стандартным методом. Мазки высушивали, фиксировали 30 мин в этанол-уксусной смеси, вновь высушивали и окрашивали уксуснокислым орсеином при комнатной температуре. Продолжительность окрашивания контролировали визуально. Препараты перед анализом кодировали. Все три варианта эксперимента выполнены в 2 повторностях. Мазки крови просматривали, используя микроскоп «Axio Imager.A1» (Zeiss) с видеокамерой «ProgRes CF». В каждом мазке анализировали по ≈7 тыс. эритроцитов, отмечая обнаруженные аномалии. Для дифференциации аномалий использовали ранее предложенный вариант методики [10], которая применима для анализа ядерных аномалий у всех животных, эритроциты которых содержат ядра (рис.2).
Статистический анализ и сравнение частот после их ϕ-преобразования проводили с использованием критерия U Фишера [11, с. 151-154, 166].

Рис. 2. Схематическое изображение ядерных аномалий эритроцитов [10]. Нормальный эритроцит птицы (1). Эритроциты с микроядром – изолированным (2), примыкающим (3), соединённым мостом (4). Двуядерные клетки с изолированными ядрами (5), примыкающими ядрами (6), соединённые мостами гантелеобразные (7) и в виде восьмёрки (8). Двулопастное ядро (9) и лопастные ядра – с примыкающей лопастью (10) и соединённой мостом лопастью (11). Эритроциты с почкующимся ядром (12) и пузырящимся ядром (13). Эритроциты с хвостатыми ядрами – нитевидным (14) и клювовидным (15). Эритроцит с зазубренным (16) ядром и с ядром со впадиной (17). Эритроцит с почковидным ядром (18). Эритроциты с вакуолизированным ядром (19) и перинуклеарной вакуолью (20). Эритроциты в состоянии кариопикноза (21), кариорексиса (22) и кариолизиса (23). Эритроцит со смещённым от центра к периферии ядром (24).
Результаты и обсуждение . В природе соединения ванадия встречаются в низких концентрациях, однако широкое применение ванадия в промышленности и поступление продуктов его переработки в окружающую среду селитебных территорий ведёт к повышению концентраций ванадия в питьевой воде, продуктах питания и атмосфере. Ванадий существует в природе с разными степенями окисления. Из них наиболее часто встречаются степени +3, +4 и +5. В живых организмах ванадий трёх-, четырёх-, и пятивалентных форм может превращаться из одной в другую путём переноса электрона. В клетках металл чаще обнаруживают в форме катиона металла V3+, в случае четырёхвалентного ванадия – в виде ионов [VO(OH) 3 ]–, [(VO) 2 (OH) 5 ]–, VO2+, и в виде H 2 VO 4 –, HVO 4 2–, VO 4 3–, VO 2 + – в случае ванадия пятивалентного. Пятивалентный ванадий представляет собой химически наиболее стабильную форму с наибольшей токсичностью [12]. Ванадий проявляет токсичность как в составе катионов, так и в составе анионов.
Ионы пятивалентного ванадия могут легко проникать в клетку через ионные каналы для фосфата и сульфата. Эта особенность и определяет их высокую токсичность. Скорость проникновения в клетки организма соединений ванадия зависит от их растворимости и химической природы. После всасывания ванадий быстро транспортируется кровью в различные ткани. Наиболее высокие его концентрации были обнаружены в почках, печени и лёгких. В мышцах и костях ванадий появляется позже, но сохраняется в них длительное время. Пятивалентный ванадий чаще обнаруживают во внеклеточных жидкостях. Внутри клеток чаще обнаруживают четырёхвалентный ванадий.
В течение нескольких десятилетий ванадий считался малотоксичным незаменимым микроэлементом, обладающим антидиабетическими и антиканцерогенными свойствами [13], но в 2006 году пентаоксид ванадия, по результатам экспериментов на животных, был охарактеризован как возможный канцероген для человека [14]. В 2009 г. канцерогенность пентаоксида ванадия была подтверждена американскими исследователями [15]. Поэтому в последнее десятилетие канцерогенные и мутагенные свойства ванадия активно исследовали с использованием различных тестерных видов организмов. Генетическая активность соединений ванадия зависит от химической структуры вещества, степени окисления металла в соединении, продолжительности воздействия, дозировки и пути проникновения в организм.
При использовании бактерий в качестве тест-систем результаты исследований мутагенности соединений ванадия оказались довольно противоречивыми. Соли четырёх- и пятивалентного ванадия в одних экспериментах показали довольно высокий уровень мутагенности, но в серии других опытов мутагенность у этих соединений отсутствовала [16-18].
Для насекомых соединения ванадия были мутагенными. После обработки гетерозиготных (+ flr3 / mwh +) личинок дрозофил солями трёх-, четырёх- и пятивалентного ванадия тест на индукцию соматических мутаций и рекомбинаций (SMART) показал увеличение частоты генетических нарушений [19]. Ин- дукция солями ванадия мутаций и соматических рекомбинаций в другом локусе (w) у дрозофил была подтверждена исследованием [20], в котором также были обнаружены различия между самками и самцами в генетической чувствительности к этому металлу.
Рыбы являются важным компонентом водных экосистем. Поскольку пятиокись ванадия растворима, то попадая в водоёмы, она может трансформироваться в различные другие ванадийсодержащие соединения и оказывать комплексное токсическое воздействие на водные организмы. [21].
Как модель для экотоксикологических исследований данио ( Danio rerio ) используют для биотестирования с середины 90-х годов прошлого столетия [22-24]. Было установлено, что между результатами токсикологических экспериментов, выполненных на данио и на лабораторных грызунах обычно наблюдается сильная корреляция. Это позволило заменить грызунов на рыб данио в лабораторных токсикологических и мутационных исследованиях. В настоящее время с использованием рыб данио исследуют изменение стабильности ДНК под влиянием различных факторов [25-29]. Одним из широко практикуемых методов мутационных исследований является анализ частоты возникновения микроядер и других ядерных аномалий в эритроцитах рыб. С использованием именно этого метода были получены следующие результаты.
Нормальные эритроциты данио имеют овальную форму с овальным же ядром. Клеточная мембрана и ядерная оболочка на препаратах имеют ровные края (рис. 2, 1 ). Суммарные количества всех проанализированных эритроцитов у рыб в контроле, почвенной вытяжке и КИГ-вытяжке составили 42562, 46095 и 44021, соответственно. В каждом из этих экспериментов у рыб доля нормальных эритроцитов составила (в %) 99,85 в контроле, 9982 в почвенной вытяжке и 99,46 в КИГ-вытяжке. Статистически достоверных отличий частот нормальных эритроцитов у рыб из почвенной вытяжки и контроля не обнаружили. Частота нормальных эритроцитов у рыб, выдержанных в КИГ-вытяжке была статистически достоверно ниже частоты нормальных эритроцитов у рыб контрольного варианта (P≤0,001).
Микроядра. К настоящему времени точные критерии морфологии микроядер, выявляемых в эритроцитах низших позвоночных животных и птиц, остаются довольно неопределёнными. Одни авторы учитывают в качестве микроядер только те хроматиновые структуры, которые чётко изолированы от основного ядра. Другие исследователи к микроядрам относят и те хроматиновые образования, которые контактируют с ядром. В ряде работ выделяют ещё и третью группу – хроматиновые структуры, отвечающие критериям «классических» микроядер, но соединённых с основным ядром хроматиновым тяжом различной ширины (различного диаметра). Эти структуры в разных работах именовали «микроядрами на ножке» или «микроядрами, соединёнными с ядром тонкой нитью». Принимая во внимание существующую неопределённость, было предложено [10] определять частоты всех трёх типов микроядер индивидуально, чтобы можно было выполнять сравнения частот всех трёх групп микро- ядер (рис. 2, 2-4), установленных разными авторами.
Частоты микроядер каждого из трёх типов у рыб изученных выборок показаны в табл. 1. Суммарная частота эритроцитов с микроядрами, обнаруженная у рыб контрольной выборки, составила 1,03‰. Спонтанная частота возникновения микроядер, установленная в исследовании [30, с. 112], составила 0,125‰. В другом исследовании спонтанная частота микро- ядер в эритроцитах данио контрольной группы была равна 1,2±0,4‰ [31, с. 10]. В работе [32, с. 42] была обнаружена существенно более высокая (1,15%) спонтанная частота микроядер. Столь существенные различия в спонтанных частот микроядер у рыб могут быть обусловлены многими причинами, но, вероятно, одной из основных причин является отсутствие чёткого стандарта для выявления самих микроядер.
Таблица 1 - Абсолютные количества и частоты микроядер (^) у рыб, пребывавших в течение 7 суток _____________ в чистой воде, почвенной вытяжке и КИГ-вытяжке ____________
|
Микроядра (количество / частота,) |
Контроль, чистая вода |
Почвенная вытяжка |
КИГ-вытяжка |
|
изолированные |
33 / 0,78 |
38 / 0,82 |
72 / 1,64*** |
|
примыкающие |
9 / 0,21 |
18 / 0,39 |
30 / 0,50* |
|
соединённые мостом |
2 / 0,04 |
5 / 0,11 |
4 / 0,09 |
|
Суммарная частота |
44 / 1,03 |
61 / 1,32 |
106 / 2,23*** |
Различия статистически достоверны: * – при Р≤0,05; ** – Р≤0,01 и *** – при Р≤0,001.
У рыб, обитавших в течение недели в почвенной вытяжке, частоты микроядер всех трёх типов, а также суммарная их частота были несколько выше соответствующих контрольных величин, но статистически достоверно от них не отличались. Следовательно, водорастворимые компоненты, содержащиеся в садовой почве, не являются генотоксичными для рыб.
Напротив, частота изолированных микроядер у рыб, неделю просуществовавших в воде КИГ-вытяжки, была вдвое выше контрольной величины и статистически достоверно отличалась от неё при Р≤0,001. Столь же достоверные различия были обнаружены между частотами изолированных микроядер у рыб, подвергнутых воздействию факторов вытяжек из КИГ и почвы.
Доля примыкающих микроядер у этой группы рыб также более чем в 2 раза была выше контрольной величины и эти различия были статистически достоверны при Р≤0,05. Частоты микроядер, соединённых мостом с основным ядром, во всех трёх выборках были очень низкими, поэтому даже двух- и трёхкратные различия их значений были статистически недостоверными. Суммарная частота микроядер всех трёх типов у рыб, подвергнутых воздействию КИГ-вытяжки, статистически достоверно отличалась от контрольной величины при Р≤0,001. Статистически достоверные различия при Р ≤0,01 также были установлены между суммарными частотами микроядер у рыб, неделю обитавших в КИГ-вытяжке и в немутагенной вытяжке из почвы.
Двуядерные клетки. В соответствии с предложенной классификацией [10] обнаруженные двуядерные клетки были дифференцированы на 4 группы: а) с изолированными ядрами, б) с примыкающими ядрами, в) с гантелеобразными, соединёнными мостом, ядрами и г) с ядрами-«восьмёрками» (рис. 2, 5-8) . Частоты этих ядерных аномалий в эритроцитах рыб, пребывавших в почвенной вытяжке, не отличались от контрольных частот. В то же время у рыб, подвергнутых воздействию КИГ-вытяжки, статистически достоверные различия были обнаружены в частотах изолированных ядер (при Р ≤0,01), ядер-«восьмёрок» (при Р ≤0,001) и суммарных частотах всех двуядерных кле- ток (при Р ≤0,001). Поскольку возникновение двуядерных клеток связано с нарушениями процессов карио- и цитокинезов, то следует заключить, что водорастворимые вещества, содержащиеся в КИГ, могут представлять угрозу для рыб тех водоёмов, в которые попадают стоки атмосферных осадков с территории орловской городской свалки, а это, прежде всего, река Рыбница, являющаяся притоком Оки.
Двулопастные ядра (рис. 2, 9 ) не были обнаружены в эритроцитах рыб контрольной выборки и рыб, подвергнутых воздействию факторов почвенной вытяжки. В то же время у рыб, неделю проживших в воде КИГ-вытяжки, частота двулопастных ядер была равной 0,11‰, и это увеличение частоты данной аномалии было статистически достоверным при Р ≤0,01.
Лопастные ядра (рис. 2, 10-11 ) отсутствовали в эритроцитах рыб контрольной выборки и рыб, выдержанных в воде почвенной вытяжки. У рыб, подвергнутых воздействию факторов КИГ-вытяжки, частота лопастных ядер (0,27‰) была статистически достоверно выше контрольной (Р ≤0,001).
Почкующиеся и пузырящиеся ядра (рис. 2, 12, 13 ) в эритроцитах рыб контрольной выборки и рыб из почвенной вытяжки не были обнаружены. В эритроцитах рыб из КИГ-вытяжки эти нарушения встречались с частотами, значения которых (0,11 и 0,09‰, соответственно) статистически достоверно (P≤0,01) отличались от контрольной величины.
Хвостатые ядра . Сравнение частот хвостатых ядер (рис. 2, 14, 15 ) представляет особый интерес, т.к., по мнению ряда исследователей, хвостатые ядра представляют собой свидетельства образования мостов между делящимися ядрами, что в свою очередь является результатом образования дицентрических хромосом.
У рыб контрольной выборки и рыб, проживших неделю в воде почвенной вытяжки, хвостатых ядер не обнаружено. Частоты хвостатых ядер в эритроцитах рыб из КИГ-вытяжки (0,57‰) статистически достоверно отличались от контрольных частот при Р≤0,001. Это означает, что химические компоненты, содержащиеся в КИГ-вытяжке, способны индуцировать образование дицентрических хромосом.
Частота зазубренных ядер (рис. 2, 16 ) в эритроцитах рыб во всех трёх выборках варьировала незначительно и статистически достоверных различий между ними не обнаружено.
Ядра со впадиной (рис. 2, 17 ) в эритроцитах контрольной выборки рыб и рыб, выдерживаемых в почвенной вытяжке, были равными (0,07 ‰). Воздействие факторов КИГ-вытяжки увеличивало частоту этих нарушений до 0,23‰. Различия этих частот статистически достоверны (Р ≤0,05).
Почкообразных ядер (рис.2, 18 ) в эритроцитах рыб всех трёх групп не отмечено.
Ядерные и перинуклеарные вакуоли (рис. 2, 19, 20 ) не были обнаружены в эритроцитах рыб контрольной выборки и рыб, выдержанных в почвенной вытяжке. У рыб, которых содержали в воде КИГ-вытяжки, частоты этих нарушений, составив 0,20 и 0,07 ‰, соответственно, статистически достоверно отличались от контрольных величин при Р ≤0,001 и Р ≤0,05.
Деструктивные ядра (кариопикноз, кариорек-сис, кариолизис). Эритроциты разрушаются в селезёнке и печени и поэтому частота эритроцитов с деструктивными ядрами (рис. 2, 21-23) существенно ниже аналогичных частот в клетках буккального эпителия млекопитающих. Тем не менее, различия частот деструктивных ядер в эритроцитах рыб косвенно могут свидетельствовать о различиях интенсивности вредоносного воздействия на них факторов внешней среды. В эритроцитах данио контрольной выборки ядра в состоянии кариопикноза, кариорексиса и ка-риолизиса не были обнаружены. У рыб, проживших неделю в почвенной вытяжке, была выявлена небольшая (0,02 ‰) частота эритроцитов с ядрами в состоянии кариорексиса. У рыб из КИГ-вытяжки частота эритроцитов с пикнотичными ядрами составила 0,07‰, а частота эритроцитов в состоянии кариорек- сиса – 0,14‰. Эти различия были статистически достоверны при Р ≤0,05 и Р ≤0,001, соответственно.
Поскольку ядра, смещённые к периферии эритроцитов (рис. 2, 24 ), рассматриваются некоторыми исследователями как клеточная аномалия, мы также учитывали частоту этих морфологических отклонений, хотя неравномерность встречаемости таких эритроцитов по площади мазка рождает предположение об образовании таких эритроцитов в результате механического воздействия на клетки в процессе выполнения мазка. Тем не менее эритроциты со смещённым к периферии ядром встречались у рыб подвергнутых воздействию факторов КИГ-вытяжки втрое чаще (0,45‰), чем у рыб контрольной выборки (0,14‰), и эти различия были статистически достоверны при Р ≤0,05.
Безъядерные клетки . При воздействии на рыб веществ, обладающих митотоксическими свойствами, возможно образование клеток с аномальной плоидно-стью, а также клеток, лишённых ядер. У рыб контрольной выборки, а также рыб, выдержанных в почвенной вытяжке, безъядерные эритроциты не обнаружены. У рыб, проживших неделю в КИГ-вытяжке, были обнаружены безъядерные эритроциты, частота которых составила 0,18‰. Возрастание частоты статистически достоверно при Р ≤0,001.
Суммарная частота всех ядерных аномалий эритроцитов у рыб, выдержанных в почвенной вытяжке (0,18%) не имела статистически достоверных отличий от частот аномалий в контрольной группе рыб (табл. 2). В то же время частота аномалий в эритроцитах рыб, проведших 7 суток в КИГ-вытяжке (0,54%), статистически достоверно ( P ≤0,001) отличалась от частот аномалий в эритроцитах рыб контрольной группы ( U =10,33) и рыб из почвенной вытяжки ( U =9,11).
Таблица 2 – Абсолютные количества и частоты (%) эритроцитов с нормальными и аномальными ядрами у рыб из 3 исследованных групп
|
Исследовано эритроцитов |
Контроль, чистая вода |
Почвенная вытяжка |
КИГ-вытяжка |
|||
|
Нормальных |
Аномальных |
Нормальных |
Аномальных |
Нормальных |
Аномальных |
|
|
1 рыба |
7084 |
12 |
8622 |
14 |
7302 |
40 |
|
2 рыба |
7134 |
8 |
8723 |
9 |
7481 |
39 |
|
3 рыба |
7011 |
8 |
7357 |
18 |
7294 |
41 |
|
4 рыба |
7187 |
13 |
7155 |
14 |
7537 |
39 |
|
5 рыба |
7025 |
13 |
7104 |
17 |
7084 |
35 |
|
6 рыба |
7058 |
8 |
7056 |
13 |
7030 |
42 |
|
Всего, |
42499 |
62 |
46017 |
85 |
43728 |
236 |
|
в % |
99,85 |
0,15 |
99,82 |
0,18 |
99,46*** |
0,54*** |
|
В сумме |
42561 |
46102 |
43964 |
|||
Различия статистически достоверны: *** – при Р≤0,001.
На основании полученных результатов следует сделать вывод о том, что водорастворимые компоненты, соодержащиеся в гипсовом шламе (КИГе), способны индуцировать ядерные аномалии в эритроцитах периферической крови рыб. Поскольку химический состав вытяжки провести не представлялось возможным, мы не можем утверждать, что причиной анализа был именно пентаоксид ванадия. Однако, в любом случае, следует считать, что водная вытяжка из КИГ представляет опасность для рыб.
Публикаций о генотоксичности соединений ванадия для амфибий, пресмыкающихся и птиц нам обнаружить не удалось. Следовательно, эти аспекты мутагенности ванадия остаются не изученными.
В организм млекопитающих ванадий поступает в основном через желудочно-кишечный тракт и дыха- тельную систему. Проникновение через кожу минимально. Лишь 10% ванадия, попавшего в пищеварительный тракт или 25% вдыхаемого, всасывается и транспортируется кровью в различные ткани организма [13]. Внимание специалистов было приковано к соединениям ванадия из-за обнаруженных у них канцерогенных свойств. Рост частоты возникновения опухолей лёгких было обнаружено у мышей и крыс после ингаляционного воздействия пентаоксида ва-нандия. Механизм индуцирования опухолей пока не установлен, но онкологи не исключают, что пятиокись ванадия индуцирует опухоли посредством прямого воздействия на генетический материал клеток. Токсические, канцерогенные и мутагенные эффекты соединений ванадия у животных различных классов представляют большой интерес с экологических позиций. Большое значение эти факты имеют для понимания потенциальной опасности для человека загрязнения среды соединениями ванадия.
Мусор на орловской свалке ТБО, где захоронены отходы ванадиевого производства, периодически возгорается и тогда в воздух вместе с продуктами горения могут подниматься мелкие частицы гипсового шлама (КИГ), содержащего пентаоксид ванадия. В такой ситуации особый интерес представляют респираторные эффекты этого вещества.
В лабораторных экспериментах давно было установлено, что поступление в лёгкие грызунов аэрозоля пятиокиси ванадия на протяжении 70-90 суток, приводило к периваскулярным отёкам, кровоизлияниям, и в некоторых случаях – к бронхиту или пневмонии [33, 34]. При ингаляционном поступлении в организм пентаоксид ванадия вызывал рак лёгких у крыс и мышей [35]. У людей хроническое вдыхание пыли пентаоксида ванадия в промышленности приводит к риниту, фарингиту, бронхиту, пневмониту, хроническому кашлю, одышке. Установлено, что работники ванадиевых производств более других подвержены простудным заболеваниям и другим респираторным заболеваниям. Ванадий оказывается более токсичным при вдыхании, чем при пероральном введении в организм. Кроме того, крупные животные переносят интоксикацию ванадием хуже, чем мелкие лабораторные грызуны [14].
Результаты исследований хронического перорального поступления соединений ванадия в организм грызунов рассмотрены в большом количестве публикаций. Их анализ представлен в ряде обзоров [14, 18, 38-41]. Установлено, что хроническое поступление метаванадата натрия (NaVO 3 ) в организмы мышей приводило к нарушению миелиновых оболочек во многих отделах головного мозга, что сопровождалось снижением прироста массы тела, и нарушением координации движений [42]. Поступление крысам в течение 3 месяцев с питьевой водой метаванадата натрия вызывало гистологические изменения в селезёнке, почках и легких [43], атрофию семенных канальцев и сильные нарушения сперматогенеза [44]. При хроническом воздействии метаванадата натрия на самок крыс у них было обнаружено увеличение частоты гибели яйцеклеток до имплантации, а также рост числа резорбированных плодов и детёнышей, рождённых мёртвыми [45].
Сведения у мутагенности соединений ванадия для млекопитающих несколько противоречивы. В одном из первых исследований, выполненных in vitro на культуре клеток китайского хомячка V79 пентаоксид ванадия не вызывал увеличения частот сестринских хроматидных обменов и генных мутаций [46].
Вдыхание мышами порошка пентаоксида ванадия в концентрации 1, 2, 3, 8 и 16 мг / м3 в течение 3 месяцев не увеличило частоту микроядер в нормохроматических эритроцитах животных обоих полов, но вызвало признаки клеточной токсичности, измеренной соотношением количеств полихроматических эритроцитов к эритроцитам нормохроматическим [38]. В другой серии экспериментов на мышах были обнаружены половые различия генотоксических и цитотоксических эффектов пентаоксида ванадия. [47]. Мышей обоих полов на протяжении одного месяца принуждали вдыхать V 2 O 5 (0,02 М) по 2 часа два раза в неделю. Образцы крови у животных отбирали еженедельно. Анализ частоты микроядер позволил обнаружить более высокую, по сравнению с самками, восприимчивость самцов к генотоксичности пентаоксида ванадия. Авторы исследования полагают, что отсутствие генотоксических эффектов у самок может быть следствием лучшей защитой от окислительного стресса за счёт более высокого уровня эстрогена [47].
В исследовании на мышах [48] не было обнаружено увеличения частоты микроядер в полихроматических эритроцитах костного мозга у животных после 24 часов воздействия внутрибрюшинно введённых однократных доз ортованадата натрия (15 и 25 мг/кг). В другом исследовании генотоксичности ортованадата натрия самцам мышей в течение 5 недель перорально вводили питьевую воду, содержащую исследуемое вещество в концентрациях 0,75, 7,5, 75, 750 и 1500 мг/л. К концу эксперимента мыши в каждом варианте опыта получили в сумме по 0,06, 0,57, 5,49, 20,8 и 33,0 мг элементарного ванадия на кг живой массы. Микро-ядерный тест в ретикулоцитах периферической крови и комет-тест первичных повреждений ДНК показали статистически достоверное увеличение анализируемых нарушений у мышей, которые получали орто- ванадат ванадия в максимальных концентрациях 750 и 1500 мг/л. Авторы исследования [49] сделали вывод, что генотоксическая активность пятивалентного ванадия проявляется in vivo только после воздействия на животных очень высоких доз ортованадата натрия, что может быть обусловлено слабой биодоступностью элемента. Приняв во внимание тот факт, что столь высокие концентрации ванадия, как исследованные в эксперименте, не встречаются в питьевой воде, авторы пришли к выводу, что ванадий в питьевой воде не представляет генотоксической опасности [49]. В эксперименте, выполненном Villani P. et al. (2007) [50], самцам мышей в течение 5 недель перорально вводили VOSO4 в дозах 10, 100, 500 и 1000 мг / л. После истечения срока воздействия был проведён комет-анализ повреждений ДНК и микроядерный тест клеток этих животных, показавшие отсутствие мутагенного эффекта исследованного соединения ванадия.
Наряду с публикациями, результаты которых свидетельствовали об отсутствии мутагенных свойств у соединений ванадия, опубликовано много работ, характеризующих соединения ванадия как мутагенные и канцерогенные для млекопитающих (см. обзор [18, 51]). Неоднозначность результатов экспериментов указывает на необходимость дальнейшего экспериментального исследования мутагенных свойств соединений ванадия.
Анализы внутриклеточного распределения ванадия показали максимальное его накопление в ядре, что может способствовать воздействию этого металла на ДНК [52]. Ряд исследований показал, что введение лабораторным грызунам различных, содержащих ванадий веществ вызывает образование микроядер, аберраций хромосом и анеуплоидии в клетках костного мозга и гонад [48, 53, 54]. У самцов мышей, которым в течение 20-60 дней вводили по 2,8 мг пентаоксида ванадия на кг живой массы в сутки, установлен рост числа разрывов ДНК в клетках, уменьшение количества образуемых сперматозоидов, снижение их подвижности, а после скрещивания с интактными самками – снижение у последних коэффициента фертильности, числа имплантаций, живых плодов и их массы, а также к росту числа резорбций плодов [55] На этом основании авторы пришли к выводу, что пя-тиокись ванадия проявляет у мышей репротоксиче-ские и генотоксические свойства. Повышение частоты гиперплоидии сперматозоидов было установлено после однократного введения самцам мышей ортованадата натрия в дозах 15 и 25 мг / кг [48]. В клетках костного мозга крыс установлено снижение митотического индекса после 3-недельного ежедневного перорального введения крысам пентаоксида ванадия в дозе 4 мг/кг, но не обнаружено повышения частоты аберраций хромосом. Однако в другом эксперименте внутрибрюшинное введения мышам пентаоксида ванадия в дозах 0,17, 2,13 и 6,4 мг / кг в течение 5 дней приводило к увеличению частоты микроядер [56]. Внутрижелудочное введение мышам однократной дозы ванадилсульфата (SVO5), ортованадата натрия (Na3VO4) и метаванадата аммония (NH4VO3) в дозах 100, 75 и 50 мг/кг, соответственно, увеличивало частоту микроядер в полихроматических эритроцитах, а также долю гипоплоидных и гиперплоидных клеток в костном мозге [53]. Мутагенность ортованадата натрия для клеток костного мозга и ооцитов подтверждена в недавних исследованиях [54].
Заключение
Захоронение 25 тысяч тонн гипсового шлама, содержащего пентаоксид ванадия, на территории городской свалки, не оборудованной необходимыми защитными сооружениями и расположенной фактически в черте города, было если не преступлением, то, в любом случае, ошибкой.
Пыль пентаоксида ванадия канцерогенна. Принимая во внимание тот факт, что на свалке постоянно происходит возгорание бытовых отходов, перемешанных с гипсового шламом, существует постоянный риск выноса в атмосферу города аэрозольных частиц пентаоксида ванадия, что может негативно отражаться на здоровье людей.
Результаты нашего исследования свидетельствуют о потенциальной мутагенности водорастворимых компонентов гипсового шлама. Свалка находится в водосборе реки Рыбницы. Водорастворимые компоненты гипсового шлама, захороненного на свалке, могут с атмосферными осадками попадать в реку и негативно влиять на рыбу.
Мутагенность соединений ванадия для рыб, амфибий, рептилий и птиц остаётся неизученной. Полученные нами результаты о мутагенности ванадийсодержащего гипсового шлама, указывают на необходимость дальнейших исследований генотоксичности ванадия для животных и людей.
Выводы
-
1. Недельное пребывание рыб данио в водной вытяжке из ванадийсодержащего гипсового шлама (композиции известково-гипсовой), 250 тыс. тонн которого были захоронены на орловской городской свалке ТБО, приводит к статистически достоверному (P≤0,001) повышению частоты микроядер в эритроцитах периферической крови.
-
2. Суммарные частоты ядерных аномалий всех типов, обнаруженных у рыб, подвергнутых недельному воздействию факторов вводной вытяжки из гипсового шлама (композиции известково-гипсовой) статистически достоверно отличались от суммарных частот таких аномалий при P≤0,001.
-
3. Установленный факт требует более детального изучения возможных негативных экологических последствий захоронения промотходов на территории свалки ТБО, расположенной фактически в черте города с 300-тысячным населением.
Биология в сельском хозяйстве №2 (27), 2020
Список литературы Индукция микроядер в эритроцитах рыб водными вытяжками из ванадийсодержащих промотходов, захороненных на территории Орловской городской свалки ТБО
- Савкин В.И. Орловская область: проблемы и механизм устойчивого управления эколого-экономическим развитием // Региональная экономика: теория и практика. - 2010. - № 27 (169). -С. 63-67.
- Лялин Ю.С. Орловская область. Серия «Региональная экологическая политика» - М.: Изд-во РОДП «Яблоко», 2011. - 24 с. ISBN 978-5-43990009-1
- Доклад «Об экологическом развитии Российской Федерации в интересах будущих поколений». Гос. совет РФ. - М.: Кремль. 2016. - 387 с.
- Яковлева Е.В., Тимоничев В.В. Экологические проблемы Орловской области. / «Наука молодых - будущее России». Сб. статей 2-й Междунар. научной конференции. В 5 тт. - Курск: "Университетская книга". - 2017. - С. 286-289.
- Федеральный арбитражный суд Центрального округа. Постановление от 23 июля 2014 г. по делу N А68-9650 / 2013 / Консультант Плюс [Электронный ресурс]. - Режим доступа: URL: http :/www. consultant.ru/cons/cgi/online.cgi?req=doc &base=ACN&n=87362#027941291289794634 (15.01.2020)
- Линников О.Д., Родина И.В. Переработка ванадий-содержащих гипсовых шламов, образующихся при нейтрализации сточных вод / Всероссийской научной конференции с международным участием «Дни наук о Земле на Урале». - Екатеринбург: Институт геологии и геохимии УрО РАН, 2012. 160 с.
- Старостина И.В., Пендюрин Е.А. Изучение возможности использования сопутствующих продуктов при организации полигонов ТБО // Экология и промышленность России. - 2015. - Т. 19. № 4. - С. 50-53.
- Миляхин С. Ситуация на орловской городской свалке // Орловская Среда. [Электронный ресурс]. - Режим доступа: URL: http ://orelsreda. ru/a-vaska-slushaet-da-est/ Дата обращения 15.01.2020.
- Руководство по применению анестетика «гвоздичное масло» в аквакультуре. Научно-технические и методические документы. «Аквакультура», Вып. 6. - М.: Изд-во ВНИРО, 2011. - 64 с.
- Крюков В.И. Вариант методики учёта ядерных аномалий в эритроцитах птиц // Вестник аграрной науки. - 2020. - № 1. - С.81-100.
- Урбах В.Ю. Статистический анализ в биологических и медицинских исследованиях. - М.: Медицина, 1975. - 295 с.
- World Health Organization. Vanadium. Environmental health criteria, № 81. - Geneva: WHO; 1988. -170 p.
- MukherjeeB. et. al, 2004. Vanadium - an element of atypical biological significance / B.Mukherjee, B.Patra, S.Mahapatra, P.Banerjee, A.Tiwari, M. Chatterjee, / Toxicology Letters. - 2004. - V 150. -№ 2. - P. 135-143.
- IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. Volume 86. Cobalt in Hard Metals and Cobalt Sulfate, Gallium Arsenide, Indium Phosphide and Vanadium Pentoxide. Lyon, France. 2006. - 353 p.
- American Conference of Governmental Industrial Hygienists (ACGIH), «Vanadium pentoxide: chemical substances 7th edition documentation, 9» in Appendix B: Threshold Limit Values (TLVs) and Biological Exposure Indices (BEIs ), 2012.
- Kada T. et al. Screening of environmental chemical mutagens by the rec-assay system with Bacillus sub-tilis. / Kada T., Hirano K. y Shirasu Y. // In: Chemical mutagens: Principles and methods for their detection (F.J. de Serres y A. Hollaender, Eds.). New-York: Plenum Press. 1980. V 5, -P. 149-173.
- Kanematsu N. et al. Rec assay and mutagenicity studies on metal compounds. / Kanematsu N., Hare M., Kada I / Mutat. Res. 77. № 2. -P. 109-116.
- Costigan M. et al. Concise international chemical assessment document 29: Vanadium pentoxide and other inorganic vanadium compounds / Costigan M., Cary R. and Dobson S. - Geneva: World Health Organization; 2001. -59 p. ISBN 92 4 153029 4.
- Abundis M.H.M. Determinación de la mutación y recombinación somáticas en la inducción de efectos genotóxicos por tres sales de vanadio en Drosophila melanogaster. Tesis de Maestría. UNAM, México.
- Barrera F.S.M., Villalobos C.H.D. (1998). Genotoxic effects of vanadyl sulfate in Drosophila melano-gaster. Invest. Clin. 39, Suppl. 1, 123-137.
- Screening assessment for the challenge vanadium oxide (vanadium pentoxide). Chemical Abstracts Service. Registry Number 1314-62-1. - Environment Canada, Health Canada. September 2010. -103 p.
- Методические рекомендации по применению методов биотестирования для оценки качества воды в системах хозяйственно-питьевого водоснабжения. МР № ЦОС ПВ Р 005-95 -М.: Изд-во ГОССТАНДАРТ России. 1995. - 51 с.
- Временное методическое руководство по нормированию уровней содержания химических веществ в донных отложениях поверхностных водных объектов (на примере нефти). - М.: РЭФИА, НИА - Природа, 2002. [Электронный ресурс]. -Режим доступа: URL: https://www.rags.ru/stroyka/text/48871/ Дата обращения 11.03.2020.
- Методические указания по разработке нормативов качества воды водных объектов рыбохозяй-ственного значения, в том числе нормативов предельно допустимых концентраций вредных веществ в водах водных объектов рыбохозяйствен-ного значения. Утверждены Приказом Росрыбо-ловства от 04.08.2009 № 695 (ред. от 22.12.2016).
- Ali S. et al. Large-scale assessment of the zebrafish embryo as a possible predictive model in toxicity testing. / Ali, S., van Mil, H. G. and Richardson, M. K. // PLoS One/ 2011/ 6(6):e21076. DOI: 10.1371/journal.pone.0021076.
- Ducharme, N. A.et al., 2015 Comparison of toxicity values across zebrafish early life stages and mammalian studies: implications for chemical testing. / Ducharme N.A., Reif D.M., Gustafsson J.A., Bondes-son M. // Reprod. Toxicol. - 2015. - V. 55. - P. 3-10.
- Dar S.A. et al. An introduction about genotoxicology methods as tools for monitoring aquatic ecosystem: present status and future perspectives / Sabzar Ahmad Dar, Abdul Rehman Yousuf and Masood-ul-Hassan Balkhi // Fisheries and Aquaculture Journal. 2016, V.7. № 1. DOI: 10.4172 / 2150-3508.1000158
- Козикова Л. В. и др. Зебрафиш (Danio rerio) - модельный объект для изучения биологии развития и тест-система экологических рисков / Л. В. Козикова, Е. А. Полтева, С. А. Лохматова // Генетика и разведение животных. - 2016. - № 2. -С.13-19.
- Cayuela M.L. et al. The Zebrafish as an Emerging Model to Study DNA Damage in Aging, Cancer and Other Diseases / Maria Luisa Cayuela, Kathleen B. M. Claes, Miguel Godinho Ferreira, Catarina Martins Henriques, Fredericus van Eeden, Maté Varga, Jeroen Vierstraete, and Maria Caterina Mione / Frontiers in Cell Developmental Biology. 2018. V 6. - P. 178. doi: 10.3389/fcell.2018.00178
- De Oliveira R., 2009 Zebrafish early life-stages and adults as a tool for ecotoxicity assessment. - Dis-sertaçâo apresentada à Universidade de Aveiro para cumprimento dos requisitos necessarios à obtençâo do grau de Mestre em Toxicologia e Ecotoxicologia. Universidade de Aveiro. Departamento de Biologia. - Ano. 2009. - 157 p.
- Lerebours A. et al. Genotoxic effects of exposure to waterborne uranium, dietary methylmercury and hy-peroxia in zebrafish assessed by the quantitative RAPD-PCR method. / Adelaide Lerebours, Sébastien Cambier, Lindsay Hislop, Christelle Adam-Guillermin, Jean-Paul Bourdineaud. // Mutation Research - Genetic Toxicology and Environmental Mu-tagenesis, Elsevier, 2013, V 755. № 1. - P. 55-60.
- Гасанова С.Х., Симаков Ю.Г. Биотестирование генотоксичности загрязнителей воды по образованию микроядер в эритроцитах данио (с.42) // Тезисы докладов Международной конференции «Биодиагностика в экологической оценке почв и сопредельных сред», Москва, 4-6 февраля 2013 г. - М.: БИНОМ, 2013 - 296 с ISBN 978-5-99631618-2.
- Roscin I.V. Vanadium. In: «Toxicology of the rare metals» Ed. by Izraelson Z.I. - Jerusalem, Israel Program for Scientific Translations, 1967, pp. 52-59.
- Stacey N.H., Klaassen C.D. Inhibition of lipid peroxidation without prevention of cellular injury in isolated rat hepatocytes. // Toxicology and applied pharmacology. - 1981. - V. 58. №1. - P. 8-18.
- Ress N.B. et al. Carcinogenicity of inhaled vanadium pentoxide in F344 / N rats and B6C3F1 mice // N.B. Ress, B.J. Chou, R.A. Renne, J.A. Dill, R.A. Miller, J.H. Roycroft, J.R. Hailey, J.K. Hase-man, and J.R. Bucher // Toxicological Sciences. -2003. - V 74, № 2. - P. 287-296.
- Бандман А.Л. Ванадий и его соединения. В кн. «Вредные химические вещества. Неорганические соединения V=VIII групп»: Справ. изд.; Под ред. В.А Филова и др. - Л.: Химия, 1989. - 592 с.
- Opinion of the scientific panel on dietetic products, nutrition and allergies on a request from the Commission related to the tolerable upper intake level of vanadium. // The EFSA Journal. 2004. V 33. -P. 1-22.
- National Toxicology Program. NTP toxicology and carcinogenesis studies of vanadium pentoxide (CAS No. 1314-62-1) in F344 / N rats and B6C3F1 mice (inhalation). // Natl. Toxicol. Program. Tech. Rep. Ser. 2002 / NTP TR 507. NIH Publication No. 034441. - 343 p.
- Chemical information review document for oral exposure to tetravalent and pentavalent vanadium compounds. Supporting nomination for toxicological evaluation by the National Toxicology Program. -U.S. Department of Health and Human Services. 2008. -56 p. [Электронный ресурс]. - Режим доступа: URL:http://ntp.niehs.nih.gov/ Дата обращения 12.04.2020.
- Vanadium. Biochemical and molecular biological approaches. Editor: Michibata Hitoshi. - Springer Science & Business Media, 2011. - 228 p. ISBN-13: 978-9400709126. ISBN-10: 9400709129
- Toxicological profile for vanadium. U.S. Department of Health and Human Services. - Public Health Service Agency for Toxic Substances and Disease Registry. - 2012. - 255 p.
- Azeez I.A. et al. Regional myelin and axon damage and neuroinflammation in the adult mouse brain after long-term postnatal vanadium exposure / Idris A. Azeez, Funmilayo Olopade, Claudia Laperchia, Anna Andrioli, Ilaria Scambi, Silas K. Onwuka, Marina Bentivoglio, and James O. Olopade. // J. Neuropa-thol. Exp. Neurol. 2016. V. 75, № 9. - P. 843-854. doi: 10.1093 / jnen / nlw058
- Domingo J. et al. Short-term toxicity studies of vanadium in rats. / Domingo J., Llobet J., Tomas J., Cor-bella J. // J. Appl. Toxicol. V.5. № 6. - P.418-421.
- Soussia A. et al. Antioxidant protective effect of Malva sylvestris on vanadium induced testicular oxida-tive stress in male Wistar rats / Ahlem Soussia, Manel Gargouria, Wafa Marouanea and Abdelfattah El Fekia // Biochem. Ind. J. - 2019. - V.13. № 1. -P. 136-151.
- Morgan A.M., Eltawil O.S. Effects of ammonium metavanadate on fertility and reproductive performance of adult male and female rats February 2003Pharmacological Research 47(1):75-85 DOI: 10.1016 / S1043 -6618(02)00241 -4
- Zhong B, et al. Genotoxicity of vanadium pentoxide in Chinese hamster V79 cells. / Zhong B., Gu Z., Wallace W., Whong W., Ong T. // Mutat. Res. - 1994. - V. 321. № 1-2. - P. 35-42.
- Rojas-Lemus M. et al. Sex differences in blood genotoxic and cytotoxic effects as a consequence of vanadium inhalation: micronucleus assay evaluation. / Marcela Rojas-Lemus, Mario Altamirano-Lozano and Teresa I. Fortoul. // J. Appl. Toxicol. 2014. V. 34. № 3. - P. 258-264. doi: 10.1002 / jat.2873. Epub 2013 Apr 26.
- Attia, S.M. et al. Orthovanadate increased the frequency of aneuploid mouse sperm without micronu-cleus induction in mouse bone marrow erythrocytes at the same dose level / Attia, S.M., Badary, O.A., Hamada, F.M., et al. 2005. // Mutat. Res. 2005. V. 583. № 2. - P. 158-167.
- Leopardi Pi et al. Assessment of the in vivo genotoxic-city of vanadate: analysis of micronuclei and DNA damage induced in mice by oral exposure / Leopardi P, Villani P., Cordelli E., Siniscalchi E., Veschetti E., Crebelli R. // Toxicol. Lett. 2005 V. 158. № 1. - P.39-49.
- Villani P. et al. Evaluation of genotoxicity of oral exposure to tetravalent vanadium in vivo / Villani P., Cordelli E., Leopardi P., Siniscalchi E., et al. // Toxicol. Lett. 2007. V. 170. № 1. -P. 11-18.
- Rodríguez-Mercado J.J., Altamirano-Lozano M.A. Vanadio: contaminación, metabolismo y genotoxi-cidad // Rev. Int. Contam. Ambient. 2006. V. 22. № 4. - P. 173-189.
- Sabbioni, E. et al. Cellular retention, cytotoxicity and morphological transformation by vanadium (IV) and vanadium (V) in BALB / 3T3 cell lines / Sabbioni, E., Pozzi, G., Pintar, A. et al. // Carcinogenesis. 1991. V 12. № 1. - P. 47-52.
- Ciranni, R. et al. Vanadium salts induce cytogenetic effects in vivo treated mice / Ciranni R., Antonetti M., Migliore L. // Mutat. Res. 1995. V 343, № 1 -P. 53-60.
- Mailhes, J.B. et al. Vanadate, an inhibitor of tyrosine phosphatases, induced premature anaphase in oocytes and aneuploidy and polyploidy in mouse bone marrow cells / Mailhes, J.B., Hilliard, C., Fuseler, J.W., London, S.N. 2003. // Mutat. Res. 2003. V 538. № 1-2. -P. 101-107.
- Altamirano-Lozano M. et al. Reprotoxic and genotoxic studies of vanadium pentoxide in male mice. / Altamirano-Lozano M., Alvarez-Barrera L., Basurto-Alcantara F., Valverde M., Rojas E. // Tera-tog. Carcinog. Mutagen. 1996 V16. -P. 7-17.
- Giri A.K. et al. Cytological and cytochemical changes induced through certain heavy metals in mammalian systems / Giri A.K., Sanyal R., Sharna A., Talukder G. // Natl. Acad. Sci. Lett. 1979. V2. - P. 391-394.


