Инфекция под биопленкой - «новая» проблема у больных в критическом состоянии
Автор: Тюрин В.П., Замятин М.Н., Гусаров В.Г., Даминов В.Д., Лузин М.В., Шилкин Д.Н.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 1 т.12, 2017 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140188622
IDR: 140188622 | УДК: 616.9:616-052
Infection under biofilm - a “new” problem in patients in critical condition
Текст статьи Инфекция под биопленкой - «новая» проблема у больных в критическом состоянии
Национальный медико-хирургический Центр им. Н.И. Пирогова, Москва
УДК: 616.9:616-052
INFECTION UNDER BIOFILM – A “NEW” PROBLEM IN PATIENTS IN CRITICAL CONDITION
За последние два десятилетия достигнуты существенные успехи современной реаниматологии в лечении многих критических состояний. Однако, несмотря на повышение эффективности проводимой интенсивной терапии врачи стали сталкиваться с новыми трудностями ведения пациентов в периоде после выхода из критического состояния. Для реанимационных больных появились новые нозологические единицы: полинейропатия, саркопения, инфекция, ассоциированная с экстремально резистентными микроорганизмами и многие другие проблемы, трудно поддающиеся стандартным методам терапии. Одной из таких проблем стало формирование биопленок. Биопленка – это микробное сообщество, состоящее из микроорганизмов, которые прикреплены к поверхности или друг к другу, заключены в матрикс синтезированных ими внеклеточных полимерных веществ, имеют измененный фенотип, параметры роста и экспрессии специфичных генов (в том числе генов антибиотикорезистентности – прим. автора) по сравнению с одиночными, планктонными бактериальными клетками. Биопленка является стандартной и наиболее распространенной формой существования бактерий в природе. Типичными примерами биопленки в организме человека являются биопленки на поверхности кариозной полости, слизистой толстой кишки, эндотрахеальной трубки при проведении длительной ИВЛ и многие другие примеры. В большинстве случаев микроорганизмы биопленки не вызывают клинически манифестируемых инфекций, но бывают и исключения из правил.
Пациент 56 лет, с марта 2014 года по апрель 2015 года проходил лечение в клиниках г. Москвы по поводу целого ряда критических состояний. С марта по май 2014 года лечение в ГКБ №83 г. Москвы в связи с двусторонней пневмонией на фоне сахарного диабета, осложнившейся флегмоной мягких тканей крестцовой области и септическим шоком. Проводилась интенсивная терапия в условиях реанимационного отделения, искусственная вентиляция легких (ИВЛ), трахеостомия, достигнут положительный эффект от проводимого лечения. В дальнейшем с мая по сентябрь 2014 года в ЦКБ №2 им. Н.А. Семашко ОАО РЖД в отделении гнойной хирургии проводилось лечение глубокого пролежня крестца, однако состояние осложнилось нарастанием острой дыхательной недостаточности (ОДН), что потребовало перевода в отделение реанимации и интенсивной терапии (ОРИТ) и вновь проведения ИВЛ. После стабилизации состояния пациент с сентября по октябрь 2014 года проходил дальнейшее лечение в НИИ им. А.В. Вишневского в отделении раневой инфекции по поводу пролежня крестцовой области, и снова состояние пациента осложнилось развитием септического шока, потребовавшего проведения интенсивной терапии в условиях реанимационного отделения. Далее пациент был переведен в кардиореанимацию ЦКБ №2 им. Н.А. Семашко ОАО РЖД, где с октября по ноябрь 2014 года проводилась терапия инфекционного эндокардита аортального клапана. Течение заболевания осложнилось кардиогенным шоком, проводилась антибактериальная терапия даптомицином с положительным эффектом, состояние стабилизировалось и с ноября 2014 по апрель 2015 года было продолжено лечение пролежня крестца в условиях отделения гнойной хирургии ЦКБ №2 им. Н.А. Семашко ОАО РЖД. Таким образом, в течение одного года непрерывной госпитализации больной перенес 4 критических состояния, сопровождавшихся шоком и потребовавших длительного лечения в ОРИТ.
27.04.15 пациент был переведен в НМХЦ им. Н.И. Пирогова (далее –
Центр) с целью выполнения пластики пролежня крестца.
На момент поступления имел место глубокий, обширный вялогранули-рующий пролежень крестца 4 стадии размерами 11 х 6,5 см. Обращал на себя внимание тяжелый преморбидный фон: сахарный диабет 2 типа, тяжелого течения; хроническая дыхательная недостаточность 3 степени на фоне хронической обструктивной болезни легких, перенесенной резекции нижних долей обоих легких по поводу эхинококкоза, перенесенной двусторонней пневмонии и респираторного дистресс-синдрома взрослых; хроническая сердечная недостаточность (ХСН); диабетическая нефропатия с исходом в хроническую болезнь почек 3 стадии; ожирение 3 степени. В течение 1,5 месяцев в Центре пациенту проводилось лечение глубокого пролежня крестца, которое включало в себя этапные хирургические обработки, осте-онекрэктомию копчиковых и крестцовых позвонков, сеансы плазматерапии – внутритканевое перифокальное введение аутоплазмы и аппликация на ткани в дне пролежня тромбоцитарной пленки для стимуляции репаративных процессов. Результатом проводимого лечения 21.05.2015 года явилось закрытие пролежня области крестца тканевым лоскутом с правой ягодицы на питающих сосудистых ножках. Лоскут зажил первичным натяжением (рис. 1) и в июне 2015 года пациент был переведен в профильное отделение для проведения медицинской реабилитации.
В августе 2015 у пациента отмечено нарастание дыхательной недостаточности. По данным компьютерной томографии (КТ) органов грудной клетки отмечалось снижение прозрачности легочной паренхимы (рис. 2), при этом признаки системного воспаления отсутствовали: нормотермия, лейкоциты крови 9,12 х 109/л, прокальцитонин (ПКТ) 0,478 нг/мл. По данным микробиологического исследования бронхо-альвеолярной лаважной жидкости отмечался рост Pseudomonas aeruginosa в диагностически значимом титре, однако учитывая рост вышеуказанного микроорганизма из других локусов и отсутствие клинико-лабораторной картины инфекции, ситуация расценена как множественная колонизация в результате длительной госпитализации.

Проводилась дифференциальная диагностика между фиброзирующим альвеолитом на фоне массивной лекарственной терапии и отеком легких на фоне декомпенсации ХСН. Посиндром-ная терапия не дала ожидаемого клинического и рентгенологического эффекта. Через месяц отмечено ухудшение КТ картины в легких (рис. 3) и вновь полное отсутствие признаков системного воспаления: нормотермия, лейкоциты крови 7,87 х 10 9 /л, ПКТ 0,487 нг/мл.
В дальнейшем больной многократно обсужден на консилиумах, был консультирован ведущими специалистами Центра и других лечебных учреждений, занимающихся легочной патологией. За последующие две недели пациент получал терапию ex juvantibus атипичной (пневмоцистной?) пневмонии (бисептол 1820 мг х 2 р/сутки), бактериальной нозокомиальной пневмонии, вызванной Pseudomonas aeruginosa (меропенем 2 г х 3 р/сутки внутривенно в виде продленных инфузий, колистин 6 000 000 МЕ х 2 р/сутки), фиброзирующего альвеолита (пульс-терапия метилпреднизолоном 500 мг х 1 р/сут. внутривенно №3, далее 24 мг/сут. per os). Однако, несмотря на лечение состояние пациента продолжало прогрессивно ухудшаться, снижение воздушности легочной ткани по данным КТ приобрело угрожающий характер (рис. 4), параллельно нарастали явления ОДН, что вновь потребовало перевода в ОРИТ, ретрахеостомии и проведения ИВЛ. Признаки системного воспаления по-прежнему отсутствовали: нормотермия, лейкоциты крови 8,13 х 10 9 /л, ПКТ 0,252 нг/мл. Отсутствие воспалительной реакции при наличие тяжелой паренхиматозной ОДН, картина КТ в легких, а также отсутствие эффекта от этиотропной антибиотикотерапии все больше склоняли к мысли о фиброзирующем альвеолите, встал вопрос о возможной трансплантации легких.
Приблизиться к установке правильного диагноза и изменить терапевтический подход помогло приглашение на консультацию к пациенту руководителя НИИ пульмонологии, академика РАН, А.Г. Чучалина. С учетом анамнеза пациента, клинической картины, данных КТ, неэффективности традиционной терапии, им было высказано мнение, что у пациента ни что иное, как инфекция легких под биопленкой, ассоциированная с Pseudomonas aeruginosa. Было предложено вести этого больного как пациента с муковисцидозом. Главными компонентами лечения инфекции легких
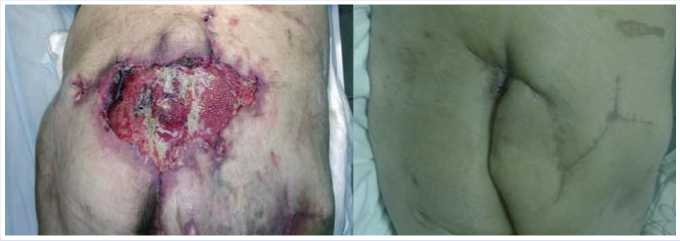
Рис. 1. Результаты хирургического лечения пролежня
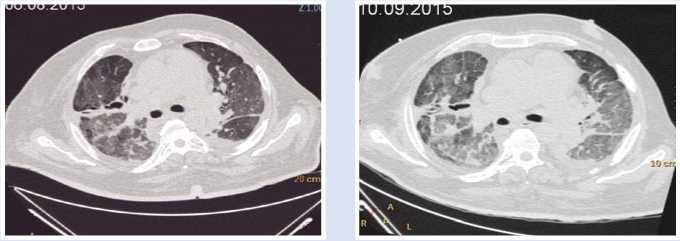
Рис. 2. Компьютерная томография легких при первых признаках ОДН
под биопленкой были сеансы интрапуль-мональной пневмоперкуссии, ингаляции дорназы альфа – генно-инженерного варианта природного фермента человека, который расщепляет внеклеточную ДНК, системная и ингаляционная антибио-тикотерапия - меропенем 2 г х 3 р/сут. внутривенно в виде продленных инфузий, колистин 2 000 000 МЕ х 2 р/сут. в течение 3 недель, внутривенное введение иммуноглобулинов в дозе 0,3 г/кг.
Метод интрапульмональной пневмоперкуссии представляет собой гибридную форму ИВЛ. Под «перкуссиями» принято понимать пневматические диффузионные конвективные «воздушные толчки», подаваемые в дыхательные пути пациента с определенной частотой. Для осуществления интрапульмональной пневмоперкуссии используется объемно диффузионный респиратор, состоящий из двух блоков: для объемной ИВЛ и вну-трилегочной перкуссии. Метод был предложен медицинским инженером Форестом М. Бердом и реализован в устройстве «Фазитрон» (рис. 5). Перкуссии вызывают обратные пневматические толчки, активируя слизь и систему мукоцилиарного бронхоальвеолярного клиренса, что является крайне важным у большинства вентилируемых пациентов [2].
В результате многокомпонентной интенсивной терапии в течение 20 суток удалось достичь полного регресса изме-
Рис. 3. Отрицательная динамика изменений в легких после месяца консервативной терапии ОДН
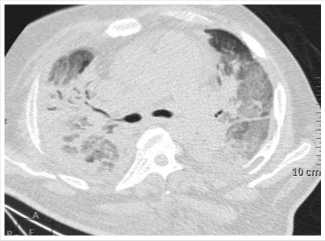
Рис. 4. Дальнейшее прогрессирование изменений – тотальное поражение легких при компьютерной томографии нений в легких по данным КТ органов грудной клетки (рис. 6), компенсации ОДН, что позволило перевести пациента на самостоятельное дыхание, стабилизировать состояние и продолжить медицинскую реабилитацию в условиях профильного отделения. Таким образом, суммарная длительность лечения пациента в условиях ОРИТ Центра составила 166 суток, длительность ИВЛ 21 сутки. В настоящее время пациент вертикали-зирован, ходит с ходунками, нуждается в ингаляции кислорода с потребностью 2 л/минуту.
Представленный клинический случай является яркой демонстрацией новых особенностей течения патологии критических состояний, связанных с современными достижениями реанима-
Ястребов И.П., Кошевой А.А., Хомчук И.А., Завацкий В.В., Сенчик К.Ю., и др. ВОЗМОЖНОСТИ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ МЕСТНОРАСПРОСТРАНЁННОЙ ОСЛОЖНЁННОЙ
ОПУХОЛИ МАЛОГО ТАЗА В МНОГОПРОФИЛЬНОМ СТАЦИОНАРЕ СКОРОЙ ПОМОЩИ

Рис. 5. Аппарат «Фазитрон» для пневмоперкуссии
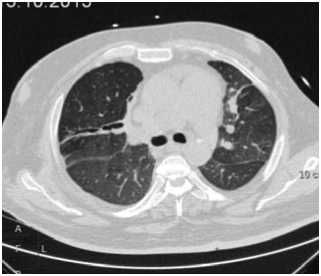
Рис. 6. Полный регресс изменений в легких после курса комплексной терапии
тологии. Агрессивные методы интенсивной терапии тяжелых инфекций могут закономерно индуцировать проявление природных свойств микроорганизмов защищаться от неблагоприятных условий внешней среды, что в свою очередь меняет клиническую картину инфекционного процесса и требует применения новых
ВОЗМОЖНОСТИ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ МЕСТНОРАСПРОСТРАНЁННОЙ ОСЛОЖНЁННОЙ
ОПУХОЛИ МАЛОГО ТАЗА В МНОГОПРОФИЛЬНОМ СТАЦИОНАРЕ СКОРОЙ ПОМОЩИ
Ястребов И.П.1, Кошевой А.А.1,
Хомчук И.А.2, Завацкий В.В.1,
Сенчик К.Ю.4, Фолевко С.Ю.1,
Киреева Г.С.3, Антонова А.М.1, Шумакова Т.А.1, Бабков О.В.1, Святненко А.В.1, Демко А.Е.1, Соловьев И.А.2, Суров Д.А.2
-
1 Санкт-Петербургский НИИ скорой помощи им. И.И. Джанелидзе, г. Санкт-Петербург
-
2 Военно-медицинская Академия
им. С.М. Кирова, г. Санкт-Петербург
-
3 НИИ онкологии им. Н.Н. Петрова,
г. Санкт-Петербург
-
4 ЦНИИ робототехники и технической кибернетики, г. Санкт-Петербург
УДК: 616.718.192-006-089
терапевтических подходов, основанных на понимании патогенеза этих изменений. Достичь успеха в лечении такой патологии помогает, в первую очередь, мультидисциплинарное взаимодействие врачей разных специальностей. Приобретенный опыт терапии инфекции легких под биопленкой в настоящее время
POSSIBILITIES OF SURGICAL
TREATMENT OF LOCALLY-ADVANCED COMPLICATED PELVIC TUMORS AT THE EMERGENCY HOSPITAL
Jastrebov I.P., Koshevoj A.A., Homchuk I.A., Zavackij V.V., Senchik K.Yu., Folevko S.Yu., Kireeva G.S., Antonova A.M., Shumakova T.A., Babkov O.V., Svjatnenko A.V., Demko A.E., Solovev I.A., Surov D.A.
Больная М., 52 лет, рост – 168 см, масса тела – 44 кг (ИМТ – 16,4) поступила в НИИ СП им. Джанелидзе 23.12.2015 г. с диагнозом: «Рак шейки матки III В ст. Надвлагалищная ампутация матки с придатками (от 02.11.2011 г.). Внутриполостная и дистанционная лучевая терапия (от 2011 г.) Полихимиотерапия (4 линии). Прогрессирование: местный рецидив. Двусторонний гидронефроз. Двусторонняя нефростомия (от 14.10.2014 г.). Распад опухоли с образованием тонкокишечно-шеечного свища. Отключение петли тонкой кишки, несущей свищ (от 27.08.2015 г.) Прогрессирование: распад опухоли, кровотечение». На момент поступления в НИИ СП возможности специализированного лечения были исчерпаны.
В связи с рецидивирующими клинически значимыми кровотечениями рутинно используется у больных реаниматологического профиля, находящихся на лечении в Центре.
25.12.2015 г. выполнены аортография, селективная эмболизация ветви левой внутренней подвздошной артерии и верхней прямокишечной артерии. Учитывая анамнестические и клинические данные за распад опухоли в малом тазу с формированием влагалищно-прямокишечного и пузырно-влагалищного свищей, 28.12.2015 г. сформирован двуствольный противоестественный задний проход, вскрыт и дренирован абсцесс малого таза. В послеоперационном периоде проводилась многокомпонентная консервативная терапия, в том числе антибактериальная, гемоплазмотранс-фузии, нутритивная поддержка. Отмечалось длительное поступление гнойного отделяемого по дренажу из полости распада опухоли (ведущий возбудитель – E.сoli, St. pneumoniae).
В рамках дообследования больной были выполнены фиброколоноскопия, фиброгастродуоденоскопия, цистоскопия, СКТ головы, груди, живота, таза с контрастированием, МРТ органов малого таза, а также объективно оценен функциональный статус больной (РИИ почек, ФВД, ЭХО-кардиография, УЗИ сосудов нижних конечностей, тромбоэластография).
При МРТ малого таза от 14.01.2016 г. определялся массивный рецидив опухоли с инвазией мочевого пузыря, прямой кишки и стенок малого таза. Об-


