Инфраренальная транспозиция верхней брыжеечной артерии при синдроме Wilkie (клиническое наблюдение)
Автор: Парфенов И.П., Хамитов Ф.Ф., Маточкин Е.А., Фомин В.С.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические случаи
Статья в выпуске: 3 (77), 2021 года.
Бесплатный доступ
Введение. Артериомезентериальная компрессия ДПК приводит к развитию хронического нарушения пассажа пищи по пищеварительному тракту с развитием дуоденальной непроходимости в 3-17% наблюдений. Это симптомокомплекс, обусловленный сдавлением нижней горизонтальной части двенадцатиперстной кишки верхней брыжеечной артерией, отходящей от аорты под острым углом. Сдавление ДПК возникает, когда угол отхождения ВБА (верхней брыжеечной артерии) от аорты менее 20°, хотя в норме он составляет 30-50°. Предложены различные методы хирургических вмешательств. Вместе с тем, операции на верхней брыжеечной артерии и аорте, которые, несомненно, носят этиопатогенетический характер представлены редкими клиническими наблюдениями.Клиническое наблюдение. Вниманию предлагается клиническое описание успешного использования сосудистых технологий в курации синдрома Wilkie у пациента М. 30 лет с инфраренальной транспозицей верхней брыжеечной артерии. Наш первый опыт операции по транспозиции верхней брыжеечной артерии в инфраренальный отдел аорты при синдроме Wilkie показал ее высокую эффективность и низкую травматичность.Заключение. Данный вид хирургических вмешательств следует проводить в клиниках, обладающих значительным опытом как в абдоминальной, так и сосудистой хирургии.
Синдром wilkie, артерио-мезентериальная компрессия, хроническая дуоденальная непроходимость, синдром верхней брыжеечной артерии
Короткий адрес: https://sciup.org/142230987
IDR: 142230987 | УДК: 616.342, | DOI: 10.17238/2072-3180-2021-3-46-50
Infrarenal transposition of the superior mesenteric artery in Wilkie syndrome (case report)
Introduction. Arteriomesenteric compression of the DPC leads to the development of a chronic violation of the passage of food through the digestive tract with the development of duodenal obstruction in 3-17% of cases. This is a symptom complex caused by compression of the lower horizontal part of the duodenum by the upper mesenteric artery extending from the aorta at an acute angle. Compression of the DPC occurs when the angle of departure of the VBA (upper mesenteric artery) from the aorta is less than 20°, although it is normally 30-50°. Various methods of surgical interventions are proposed. At the same time, operations on the superior mesenteric artery and aorta, which are undoubtedly of an etiopathogenetic nature, are represented by rare clinical observations.Clinical observation.The article presents a clinical description of the successful use of vascular technologies in the curation of Wilkie syndrome in a patient M. 30 years old with an infrarenal transposition of the superior mesenteric artery. Our first experience of surgery for the transposition of the superior mesenteric artery into the infrarenal aorta in Wilkie syndrome has shown its high efficiency and low injury rate.Conclusion. This type of surgical intervention should be performed in clinics with significant experience in both abdominal and vascular surgery.
Текст научной статьи Инфраренальная транспозиция верхней брыжеечной артерии при синдроме Wilkie (клиническое наблюдение)
Впервые патологическое состояние сдавления двенадцатиперстной кишки (ДПК) верхней брыжеечной артерией было описано в 1842 году австрийским патологоанатомом профессором C. Rokitansky, а более детально синдром был изучен D.Wilkie, который в 1927 году обобщил собственный опыт лечения 75 пациентов. В структуре всей патологии желудочно-кишечного тракта данный синдром встречается в 1–2,5 % наблюдений [1, 2]. Артериомезентериальная компрессия ДПК приводит к развитию хронического нарушения пассажа пищи по пищеварительному тракту с развитием дуоденальной непроходимости в 3–17 % наблюдений при цифрах летальности, достигающие 33 % по данным ряда статистик [3].
Это симптомокомплекс, обусловленный сдавлением нижней горизонтальной части двенадцатиперстной кишки верхней брыжеечной артерией, отходящей от аорты под острым углом. Сдавление ДПК возникает, когда угол отхождения ВБА (верхней брыжеечной артерии) от аорты менее 20°, хотя в норме он составляет 30–50°.
Провоцирующие факторы синдрома Wilkie:
-
• резкое снижение веса, которое сопровождается сокращением объема висцерального жира – при этом расстояние между аортой и брыжеечной артерией уменьшается;
-
• поясничный лордоз, сколиоз:
-
• слабость мышц живота;
-
• строгий постельный режим после травм и операций
Наиболее подвержены развитию синдрома верхней брыжеечной артерии подростки, у которых происходит быстрый скачкообразный рост без компенсаторного увеличения веса.
В компенсированной и субкомпенсированной стадиях сосудистой компрессии проводится диетотерапия и медикаментозное лечение. Основные задачи консервативных мероприятий – усиление питания и уменьшение степени дуоденальной непроходимости. Лечебная диета предполагает прием жидкой, полужидкой и протертой пищи малыми порциями [4].
Для коррекции состояния применяется ряд препаратов: прокинетики, спазмолитики, ферментные препараты, антибактериальные средства.
Преимущественно пациенты с синдромом артериомезен-териальной компрессии госпитализируются в отделения абдоминальной хирургии, и это неудивительно, учитывая симптомы со стороны желудочно-кишечного тракта. Критериями отбора больных для проведения оперативного вмешательства являются прогрессирующая потеря массы тела, выраженный дуоденостаз, развитие осложнений синдрома верхней брыжеечной артерии (СВБА).
Предложены различные методы хирургических вмешательств при СВБА:
-
• Лапароскопическое пересечение связки Трейтца
-
• Дуоденоеюностомия, наиболее распространенная операция при синдроме ВБА, была впервые предложена в 1907 году Бладгу-дом. Дуоденоеюностомия, выполняемая как открытая операция, так и лапароскопически, включает создание анастомоза между ДПК и тощей кишкой, минуя сжатие, вызванное ВБА [3, 5].
-
• Менее распространенные хирургические методы лечения синдрома ВБА включают дуоденоеюностомию по Ру, га-строеюностомию, переднюю транспозицию третьего сегмента двенадцатиперстной кишки [6, 7].
Несмотря на многообразие хирургических вмешательств, авторы отмечают высокую частоту развития различных послеоперационных осложнений (6–15 %), а также цифры летальности до 5 % [5, 7]. Вместе с тем, операции на верхней брыжеечной артерии и аорте, которые несомненно носят этиопатогенети-ческий характер, представлены редкими клиническими наблюдениями [7, 8].
Вашему вниманию предлагается клиническое описание успешного использования сосудистых технологий в курации синдрома Wilkie у пациента М. 30 лет.
Клиническое наблюдение
Больной М., 30 лет, госпитализирован в клинику 5.05.2021 г. с жалобами на интенсивные боли в эпигастрии, возникающие спустя 20 минут после приема пищи, стихающие при занятии коленно-локтевого положения. Данная симптоматика сопровождалась диспептическими явлениями (тошнотой и рвотой), постоянным привкусом желчи во рту, неустойчивостью стула. Кроме того, пациент отмечал, что на протяжении последних 3 лет было выявлено и прогрессировало расширение вен семенного канатика слева.
Анамнез заболевания: Указанные жалобы появились и прогрессивно нарастали в течение 5 лет. Тогда же и был установлен диагноз артериомезентериальной компрессии ДПК. Больной постоянно принимал лекарственные препараты, назначенные гастроэнтерологом; при этом отмечалось улучшение только в снижении рвотного рефлекса. Неоднократно консультировался абдоминальными хирургами. От предложенной общехирургической операции воздерживался. Ухудшение состояния около полугода, за этот период времени отмечает значительную потерю массы тела.
Анамнез жизни. Рос и развивался соответственно возрасту, из перенесенных заболеваний отмечал лишь простудные и детские инфекции, вредных привычек не имел, детей нет.
Объективный осмотр на момент госпитализации: состояние удовлетворительное, астеническое телосложение, рост 180 см, вес 60 кг (ИМТ-18,5 кг/м2), кожные покровы бледные, подкожная жировая клетчатка скудная, тургор кожи снижен. В легких дыхание везикулярное, хрипов нет. Тоны сердца ясные, АД 100\60 мм рт. ст., пульс ритмичный с частотой 75 в минуту. Язык суховат, обложен коричневым налетом. Живот не вздут, болезненный в эпи-мезогастрии. Печень не увеличена. Мочеиспускание не нарушено. По ходу левого семенного канатика и на левом яичке отмечаются умеренно расширенные вены.
Инструментальное обследование, проведенное к в клинике:
УЗИ брюшной полости – гастростаз, дуоденостаз (расширение ДПК кишки до 45 мм, тощий и толстый кишечник спавшиеся).
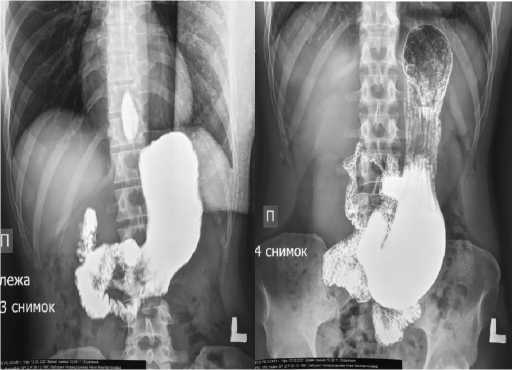
X-ray желудка и ДПК: выраженный гастродуоденостаз (желудок расширен до малого таза) (рис.1 А, В).
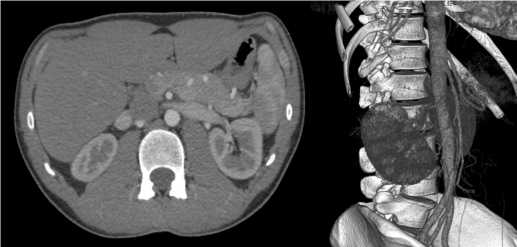
МСКТ брюшной полости c сосудистым контрастированием (рис. 2 А, В) — артериомезентериальная компрессия ДПК и левой почечной вены. Картина хронической дуоденальной непроходимости.
На основании жалоб больного, клинической картины, данных инструментального обследования установлен диагноз: артериомезентериальная компрессия ДПК и левой почечной вены. Хроническая дуоденальная непроходимость. Расширение вен левого семенного канатика.
Принимая во внимание клинико-инструментальные данные обследования, а также в связи с безуспешностью многолетней консервативной терапии и клиникой прогрес- сирования заболевания больному предложено оперативное лечение: инфраренальная транспозиция верхней брыжеечной артерии. Получено согласие, больной подготовлен к операции.
В
Рис. 1. А, В. Р-скопия желудка в положениях лежа (1А) и стоя (1В)
Fig. 1. A, B. X-ray of the stomach in the supine (1A) and standing (1B) positions
А В
Рис. 2 А. Компрессия левой почечной вены между аортой и ВБА (стрелка указывает почечную вену); 2 В. 3D-реконструкция брюшной аорты и ее ветвей: острый угол отхождения ВБА от брюшного отдела аорты (стрелка указывает ВБА)
Fig. 2 A. Compression of the left renal vein between the aorta and SMA (arrow indicates renal vein); 2 B. 3D-reconstruction of the abdominal aorta and its branches: an acute angle of departure of the
SMA from the abdominal aorta (the arrow indicates the SMA)
На операции:
Под общим обезболиванием произведена верхняя срединная лапаротомия. В брюшной полости около 100 мл светло-серозной жидкости, желудок растянут по длине до 32 см, начальные отделы ДПК расширены до 40 мм. Петли тонкой и толстой кишки не расширены. Инфраренальный отдел брюшной аорты диаметром 15 мм, не изменен, левая почечная вена расширена до 25 мм (рис. 3).
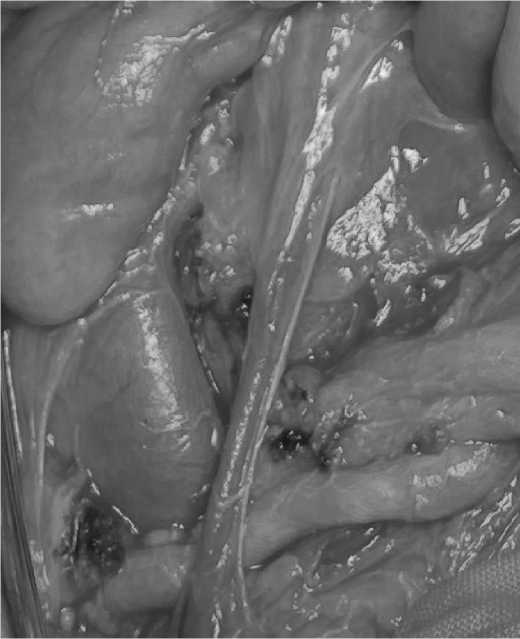
Рис. 3. Расширенная левая почечная вена (интраоперационная фотография)
Fig. 3. Dilated Left Renal Vein (intraoperative Photography)
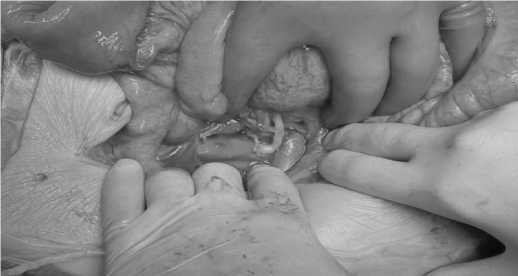
Рис. 4. Реимплантация ВБА в инфраренальный отдел аорты (интраоперационная фотография)
Fig. 4. Reimplantation of SMA into the infrarenal aorta (intraoperative photography)
В корне брыжейки тонкой кишки выделен ствол ВБА ниже отхождения a. colica media, диаметром 5 мм. Отмечался выраженный рубцово-спаечный процесс вокруг артерии, который вместе с ней и вызывал компрессию нижней горизонтальной части ДПК. Острым путем проведена мобилизация ВБА до ее отхождения от брюшной аорты с отведением тела поджелудочной железы кверху и рассечением спаек вдоль верхней брыжеечной артерии. После системной гепаринизации (внутривенно 5000 ед. гепарина) ВБА перевязана и прошита у устья, низведена в инфраренальную позицию. Произведено боковой пережатие брюшной аорты сразу ниже левой почечной вены зажимом Сатинского. В брюшной аорте сформировано окно длиной 10 мм, шириной 5 мм, выполнено анастомозирование ВБА с аортой «конец в бок» проленовой нитью 6\0 (рис. 4). Время ишемии кишечника составило 12 минут.
После завершения сосудистого этапа отмечена отчетливая перистальтика кишечника, цвет кишечника бледно-розовый, проксимальный отдел ДПК спавшийся. Операция завершена дренированием брюшной полости, послойным ушиванием раны.
Послеоперационный период протекал гладко. На следующий день после операции у больного пропал привкус желчи в ротовой полости. Прием пищи возобновлен согласно концепции Fasttrack. Проходимость жидкой и твердой пищи – беспрепятственны. На 5-е сутки после операции выполнено контрольное МСКТ-ангиографическое исследование брюшной полости (рис. 5 А, В). На контрольных исследованиях ВБА отходит от брюшной аорты под тупым углом.
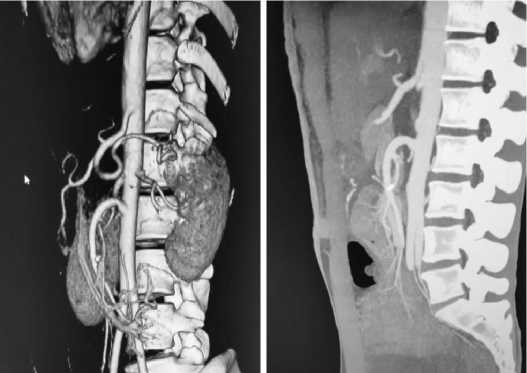
А В
Рис. 5 А, В. Послеоперационные 3D реконструкция (А) и ангиография (Б). (стрелками указана ВБА)
Fig. 5 A, В. Postoperative 3D-reconstruction (A) and angiography (B). (arrows indicate VBA)
Больной выписан из клиники на 6-е сутки после операции в удовлетворительном состоянии. Осмотрен через 3 месяца. Жалоб не предъявляет. Проходимость пищи удовлетворительная. Прежних симптомов нет. Моторика кишечника удовлетворительная, что объективно оценено по данным электроэнтеро-графии с последующей резонансной стимуляцией (патенты РФ №2648819, №2714075): нарушений моторики и перистальтики не выявлено. Прибавил в весе 4,5 кг.
Обсуждение
Синдром артериомезентериальной компрессии очень редкое заболевание, которое чаще всего находится в сфере деятельности общих хирургов, на что четко указывает литературная статистика [1, 2, 3]. В то же время, в основе развивающегося симптомокомплекса лежит сдавление ДПК верхней брыжеечной артерией. В нашем клиническом наблюдении была выполнена сосудистая операция при участии абдоминальных хирургов. Надо подчеркнуть, что для нас стал определенной неожиданностью обнаруженный на операции выраженный спаечный перипро-е цесс по ходу ВБА и, в особенности, в области сдавлении ДПК. Таким образом, формировался плотный рубцовый тяж вокруг артерии, усугубляя необратимость патологического сдавления.
В техническом исполнении операции требовалось не только полная мобилизация верхней брыжеечной артерии непосредственно от устья, но и тщательное рассечение рубцовых тяжей вокруг артерии на протяжении. Следует отметить, что при тщательном соблюдении принципов сосудистой хирургии, а именно предварительной полной мобилизации верхней брыжеечной артерии и подготовки площадки в инфраренальном отделе аорты можно отказаться от профилактических мероприятий по защите кишечника от ишемии.
Заключение
Наш первый опыт операции по транспозиции верхней брыжеечной артерии в инфраренальный отдел аорты при син-й дроме Wilkie показал ее высокую эффективность и низкую травматичность. Данный вид хирургических вмешательств следует проводить в клиниках, обладающих значительным опытом как в абдоминальной, так и сосудистой хирургии.
Список литературы Инфраренальная транспозиция верхней брыжеечной артерии при синдроме Wilkie (клиническое наблюдение)
- Zaraket V., Deeb L. Wilkie's Syndrome or Superior Mesenteric Artery Syndrome: Fact or Fantasy? Case Rep Gastroenterol, 2015, Jun, № 5;9(2), рр.194-199. DOI: 10.1159/000431307
- Lee T.H., Lee J.S., Jo Y., Park K.S., Cheon J.H., Kim Y.S., Jang J.Y., Kang Y.W. Superior mesenteric artery syndrome: where do we stand today? J Gastrointest Surg., 2012, Dec; № 16(12), рр. 2203-2211. http://doi. org/ DOI: 10.1007/s11605-012-2049-5
- Capitano S., Donatelli G., Boccoli G. Superior Mesenteric Artery Syndrome-Believe in it! Report of a Case. Case Rep Surg., 2012, № 11, 282646. DOI: 10.1155/2012/282646
- Bronswijk M., Fransen L., Vanella G., Hiele M., van der Merwe S. Successful treatment of superior mesenteric artery syndrome by endoscopic ultrasound-guided gastrojejunostomy. Endoscopy, 2021, Feb; № 53(2), рр. 204-205. DOI: 10.1055/a-1190-3228
- Wan S, Zhang L, Yang J, Gao X, Wang X. Superior Mesenteric Artery Syndrome Improved by Enteral Nutritional Therapy: A Retrospective Case-Series Study in a Single Institution. Ann Nutr Metab., 2020, № 76(1), рр. 37-43. DOI: 10.1159/000506620
- Kubo T, Adachi Y, Kikuchi T, Mita H, Endo T. Percutaneous endoscopic gastrojejunostomy for treating superior mesenteric artery syndrome. Gastrointest Endosc., 2019, Dec; 90(6), рр. 983-984. http://doi. org/ DOI: 10.1016/j.gie.2019.07.001
- Pourhassan S, Grotemeyer D, Fürst G, Rudolph J, Sandmann W. Infrarenal transposition of the superior mesenteric artery: a new approach in the surgical therapy for Wilkie syndrome. J Vasc Surg., 2008, Jan; № 47(1), 201-204. DOI: 10.1016/j.jvs.2007.07.037
- Grotemeyer D, Pourhassan S, Sandmann W. Paradigmenwechsel in der Behandlung des Wilkie-Syndroms: Von der Darmumleitung zur Transposition der A. mesenterica superior. Internist (Berl)., 2009, Apr; № 50(4), рр. 484-448. German. DOI: 10.1007/s00108-008-2263-0


