Интраоперационная нейровизуализация в хирургическом лечении пациентов с повреждениями периферических нервов конечностей
Автор: Айтемиров Ш.М., Нинель В.Г., Коршунова Г.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Травматология и ортопедия
Статья в выпуске: 2 т.11, 2015 года.
Бесплатный доступ
Цель: оценить возможности интраоперационной нейровизуализации в определении тактики хирургического лечения пациентов с повреждением периферических нервов конечностей. Материал и методы. Основу работы составило исследование 43 пациентов с повреждениями периферических нервов конечностей, которым выполнено комплексное обследование, включающее электронейромиографию, ультрасонографию и контрастную нейрографию. Результаты. В итоге комплексного интраоперационного обследования получены диагностические критерии, позволившие во многом определить тактику дифференцированного лечения у пациентов с повреждением нервных стволов конечностей. Заключение. Результаты комплексного интраоперационного тестирования стали основой разработки алгоритма диагностики и тактики хирургического лечения повреждений периферических нервов.
Интраоперационная ультрасонография, периферические нервы, повреждения, хирургическое лечение
Короткий адрес: https://sciup.org/14918112
IDR: 14918112
Intraoperative neurovisualization in the surgical treatment of peripheral nerve injuries
Objective. The present study examines the value of intraoperative neurovisualization as an imaging tool for decision making in the management of traumatic nerve injuries. Materials and methods. 43 patients with traumatic nerve lesions were examined by electrodiagnostic study, ultrasonography and contrast neurography. Results. A complex intraoperative examination have been used to guide surgical decision making in patients with peripheral nerve injuries of limbs. Conclusion. The results of complex intraoperative examination became the basis of diagnosis and treatment algorithm for surgical treatment of peripheral nerves injuries.
Текст научной статьи Интраоперационная нейровизуализация в хирургическом лечении пациентов с повреждениями периферических нервов конечностей
онаре необходима исчерпывающая и объективная диагностика характера, степени и уровня поражения периферических нервов, которая нередко представляет собой сложную задачу [1].
В настоящее время широко используются возможности современной инструментальной доопера-ционной диагностики травматических повреждений периферических нервов (ЭНМГ, УЗИ, тепловизионное исследование, МРТ) [2–4].
Вместе с тем методы дооперационной диагностики не всегда совпадают с интраоперационными на- ходками и не в состоянии разрешить ряд практически важных вопросов, возникающих непосредственно во время оперативных вмешательств [5].
Литературные данные свидетельствуют об актуальности внедрения во время операций современных технических средств и технологий, позволяющих получать разностороннюю информацию о структуре поврежденного нервного ствола [6]. Этим требованием соответствуют такие методики, как интраоперци-онное ультразвуковое исследование нервных стволов и контрастная нейрография.
Цель : о ценить возможности интраоперационной нейровизуализации в определении тактики хирургического лечения пациентов с повреждением стволов периферических нервов конечностей.
Материал и методы. Под нашим наблюдением находилось 43 пациента с повреждениями периферических нервов конечностей в возрасте от 11 до 72 лет (лиц мужского пола 32, женского 11). Большинство пациентов (35 человек, или 83,7%) поступило в нейрохирургический стационар до года после травмы, а 7 (16,3%) госпитализированы через год и более с момента травмы после безуспешного консервативного лечения. При поступлении, по клинико-неврологическим данным, у 13 (30,2%) пострадавших были повреждены стволы срединного, у 15 (34,9%) выявлено повреждение локтевого, у 8 (18,6%) поражение лучевого, у 5 (11,6%) седалищного и еще у 2 (4,7%) малоберцовой порции седалищного нерва. После комплексного до- и интраоперационного обследования, включающего электронейромиографию, ультрасонографию и контрастную нейрографию, выполнены следующие оперативные вмешательства:
-
— иссечение невромы с последующей нейрорафией и прямой электростимуляцией ствола нерва;
-
— иссечение внутриствольной невромы либо рубцово-измененного участка ствола нерва с последующей нейрорафией и прямой его электростимуляцией;
-
— невролиз анатомически сохранного ствола нерва с последующей его прямой электростимуляцией.
Для предварительного определения уровня, зоны и характера расстройств чувствительности, степени и глубины двигательных и трофических нарушений проводилось клинико-неврологическое обследование у всех (n=43) пациентов с помощью 5-балльной системы оценки чувствительных и двигательных нарушений в зоне иннервации поврежденного нерва, при которой 1 балл соответствовал отсутствию чувствительности и мышечных сокращений, 5 баллов — наличию чувствительности и сокращению мышц.
Электронейромиографические и электромиогра-фические исследования выполнены у всех (n=43) больных, при этом изучались показатели амплитуды М-ответа, скорости проведения импульса по эфферентным (СПИэфф.) и афферентным (СПИафф.) волокнам ствола нерва, параметров потенциала действия двигательных единиц (ПДДЕ), а также наличие либо отсутствие потенциала фибрилляций (ПФ), позитивно острых волн (ПОВ). Данные нейрофизиологические методики во многом способствовали уточнению локализации и степени тяжести повреждения стволов периферических нервов до и в ходе оперативного вмешательства. Использование в работе интраоперационного нейрофизиологического тестирования позволяет уточнить степень нарушения проводимости на открытом стволе поврежденного нерва, что значительно повышает степень информативности о тяжести аксонального поражении нерва.
Рентгенологическое обследование применялось в тех случаях (n=4), когда повреждения периферических нервов конечностей сочетались с переломами костных структур, и при контрастировании нервного ствола (n=43) во время операции. Визуализация на операционном столе контрастированного ствола нерва осуществлялась с помощью мобильной цифровой рентгенохирургической установки ОЕС 9800 (США). Контрастирование поврежденных нервных стволов производилось путем введения под эпинев-рий нерва неионного водорастворимого контраста «Омнипак-300», который предварительно разводили физиологическим раствором до 50% концентрации. Контраст вводился под эпиневрий порциями (по 0,3– 0,5 мл в зависимости от толщины нерва) до стойкого увеличения диаметра ствола нервного проводника в 1,5–2 раза по сравнению с исходным его размером. Порционное введение контраста позволяло избежать разрыва эпиневрия, а увеличение диаметра нерва в 1,5–2 раза обеспечивало тугое заполнение эпиневральной трубки, что, как показали наши исследования, создает условия для лучшей визуализации нерва на рентгенограмме. Рентгенографию производили через 4–6 мин после введения последней дозы контраста. Такая экспозиция была необходима для более равномерного распределения контраста под эпиневрием нерва. Контрастная нейрография позволяет уточнить характер и протяженность повреждения ствола и дифференцировать методы хирургического пособия у пострадавших с травмой периферических нервов конечностей.
Ультрасонографическое исследование поврежденных стволов периферических нервов конечностей было выполнено у 43 пострадавших перед оперативным вмешательством и на операционном столе, которое проводилось на аппарате «Sonoace R3» фирмы Medison. Современная ультразвуковая аппаратура позволяет сканировать стволы периферических нервов широкополосными линейными и конвексными датчиками с частотой от 2 до 20 МГц, использование которых зависит от формы, калибра, глубины залегания ствола нерва и пространственного расположения относительно соседних структур (сосудов, сухожилий), а также цели и задач исследования и нозологии поражения нервного ствола. В любом случае при интерпретации результатов исследования необходимо ориентироваться на существующие в литературе данные о чувствительности, специфичности и точности теста [7, 8]. Высокоразрешающее ультразвуковое исследование периферических нервов позволяет оценить контуры, размеры, формы и эхо-структуру нервного ствола и выявить характер его повреждения (диастаз, неврома, вну-триствольная неврома, рубцововый процесс и др.), что значительно оптимизирует лечебную тактику. Интраоперационное ультразвуковое исследование не только позволяет уточнять данные, полученные перед оперативным пособием, но и дает возможность с помощью ультразвукового конвексного датчика на поперечных срезах нерва оптимизировать степень иссечения невромы и патологически измененного участка ствола нерва.
Статистическую обработку полученных результатов проводили с использованием пакета программ Statistica 10.0 for Windows (StatSoft Inc.). Проверку нормальности распределения вариационных рядов осуществляли по критерию Шапиро — Уилка, после чего применяли параметрический метод вариационной статистики с определением средней арифмети- ческой (М) и ошибки средней арифметической (m). Различия считали статистически значимыми при p≤0,05.
Результаты. Результаты клинико-неврологического исследования показали, что из 43 пациентов у 31 (72,1%) наблюдалась клиника посттравматического полного аксонального повреждения нерва, а у 12 (27,9%) клиника нейропатии с частичным нарушением функции поврежденного нерва. Однако при первичном электронейромиографическом обследовании 43 пациентов с различной степенью тяжести повреждения периферических нервов верхней и нижней конечности у 26 (60,5%) больных отсутствие вызванных мышечных ответов при стимуляции нервов на уровне дистальных и проксимальных точек, наличие в мышцах только потенциалов спонтанной активности позволяли предположить полное нарушение проводимости пораженного нерва.
У 17 (39,5%) пациентов проводимость по стволам нервов была частично сохранена, о чем свидетельствовало наличие низкоамплитудных М-ответов. При проведении игольчатой электромиографии в мышцах, иннервируемых пораженным нервом, регистрировались активные ПФ и ПОВ, но при максимальном произвольном напряжении мышцы удалось выделить ПДДЕ, как правило, с увеличенными параметрами длительности (до 13,5–18 мс) и амплитуды (свыше 800 мкв). В таблице представлены средние показатели ЭНМГ-исследования нервов пораженной и здоровой конечностей.
Показатели вызванной мышечной активности, времени проведения импульса на уровне терминалей и скорости проведения импульса на уровне предплечья были значительно снижены и достоверно отличались от данных здоровой конечности.
Проведение ЭНМГ и ЭМГ-исследований позволило в 11,6% случаев уточнить степень нарушения проводимости поврежденного нерва и перевести данных пациентов в группу наблюдений с частичным его поражением.
Для уточнения тяжести и характера поражения периферических нервов верхних и нижних конечностей всем пострадавшим (n=43) выполнялась высокоразрешающая ультрасонография. Среди 43 пациентов у 21 (48,8%) получены эхо-признаки анатомического перерыва и невромы, что являлось объективным подтверждением тяжести травматического поражения нервного ствола, у 22 (51,2%) обнаружено снижение эхогенности нервной ткани (n=19) и локальное изменение формы нерва (n=3), которые свидетельствовали о частичном повреждении периферического нерва.
Интраоперационное обследование пострадавших включало: ЭНМГ-тестирование УЗ-сканирование и контрастную нейрографию открытого ствола поврежденного периферического нерва.
При интраоперационном исследовании проводимости нерва игольчатым стимулирующим электродом наносили раздражение на нерв и регистрировали вызванный невральный потенциал (ВП нерва) при помощи игольчатых сенсорных электродов. В результате ЭНМГ-мониторинга 43 пострадавших только у 25 (58,1 %) не удалось получить Вп нерва, что подтверждало полное нарушение проводимости. У 18 (41,9%) наличие низкоамплитудного ВП нерва (не более 3,4 мкв) указывало на частичное нарушение проводимости стволов нервов верхней и нижней конечности. Интраоперационное тестирование позволило уточнить исходные ЭНМГ-данные о тяжести нарушения проводимости нервного ствола. Несмотря на то, что данные нейрофизиологического исследования позволяют судить о тяжести и степени нарушения проводниковой функции нерва и глубине денервационных процессов в мышечной ткани, но не позволяют увидеть структурные нарушения в нервном стволе. Это особенно важно для больных с ЭНМГ и ЭМГ-признаками частичного нарушения проводимости, но с тяжелым аксональным поражением повреждения нерва, когда прогноз восстановления проводимости вызывает сомнения. Здесь должен быть решен вопрос о объеме оперативного вмешательства, о невролизе или нейрорафии.
При интраоперационном контрастировании стволов поврежденных нервов среди 43 пострадавших у 23 (53,5%) визуализировался дефект столба контраста от 0,5 до 1 см, что указывало на тяжесть травматического поражения нерва, у 20 (46,5%) обнаружено истончение либо сужение столба контраста (n=16) и локальный дефект, либо неравномерное заполнение контрастом ствола нерва (n=4), что было патогномо-нично частичному повреждению периферического нерва. Несмотря на то, что контрастная нейрография является инвазивной методикой и дает важную дополнительную информацию о протяженности, но по ее результатам нельзя судить о глубине перерождения и структуре травматических изменений в поврежденном стволе нерва.
В этой связи нами проведено УЗ-сканирование ствола поврежденного нерва на операционном столе. Из 43 пациентов у 22 (51,2%) выявлена эхо-картина полного анатомического перерыва ствола нерва, что указывало на грубое аксональное повреждения неврального ствола. У 21 (48,8%) пострадавших обнаружено снижение эхогенной структуры ствола нерва (n=16) и уменьшение его диаметра, а также локальное изменение эхогенности нерва (n=5), характерное для рубцового процесса либо наличия внутристволь-ных невром. Полученные результаты наиболее наглядно представлены на диаграмме (рис. 1).
Обсуждение. Сопоставление результатов ЭНМГ-исследования, УЗ-сканирования, проведенных до операции, с данными интраоперационного обследования позволило во многом уточнить степень,
ЭНМГ-данные пораженных нервов верхних и нижних конечностей (n=43)
|
Поврежденный нерв |
М-ответ (мВ) |
ЛП (мс) |
СПИэфф (м/с) |
|||
|
пораженный нерв |
здоровый нерв |
пораженный нерв |
здоровый нерв |
пораженный нерв |
здоровый нерв |
|
|
Лучевой |
0,25±0,1* |
8,3±1,3 |
8,33±0,7* |
3,87±0,15 |
24,6±3,1* |
58,6±6,2 |
|
Срединный |
1,05±0,59* |
10,32±1,29 |
6,52±0,9* |
2,43±0,32 |
37,4±6,8* |
72,4±4,9 |
|
Малоберцовый |
1,37±0,5* |
9,1±1,6 |
9,7±1,3* |
5,2±0,7 |
32,8±4,9* |
61,9±8,2 |
П р и м еч а н и е : * — P<0,05 по отношению к здоровому нерву противоположной конечности.
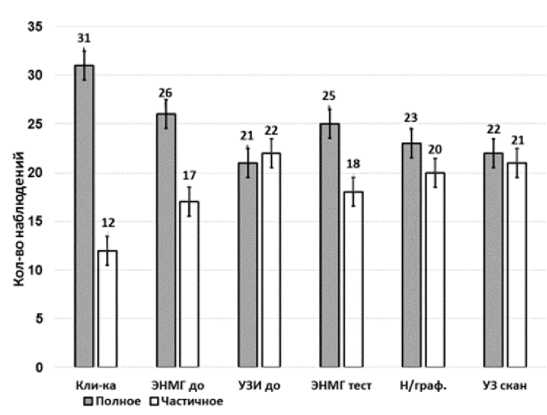
Рис. 1. Результаты комплексного до- и интраоперационного обследования пациентов протяженность, глубину структурных изменений периферических нервов конечности. При неврологическом обследовании в 72,1% наблюдений имелась клиника полного нарушения проводимости по нервным стволам, что характерно для полного аксонального повреждения нерва. Однако, по данным ЭНМГ-тестирования, на операционном столе полное нарушение проводимости по стволу периферического нерва имело место только у 58,1% пациентов, т.е. на 14,0% была уточнена тяжесть поражения нерва. Примечательно, что, по данным эхограммы, анатомический перерыв был зарегистрирован в 51,2% случаев, что позволило уточнить диагноз по сравнению с дооперационным УЗ-сканированием на 2,4% процента, интраоперационным ЭНМГ-тестированием на 6,9% и контрастной нейрографией на 2,3%.
Частичное повреждение нервных стволов, судя по результатам клинико-неврологического обследования, было обнаружено в 27,9% наблюдений. При ЭНМГ-тестировании на операционном столе эта цифра увеличилась на 14,0%, а во время УЗ-сканировании нерва на операции количество пациентов с частичным повреждением, наоборот, уменьшилось на 4,7% по сравнению с доопераци-онными результатами. Если сравнить данные ЭНМГ-тестирования и сканирования нерва на операционном столе с дооперационными результатами (11,6 и 13,7% соответственно), то диагноз частичного повреждения эти две методики уточняют в 2,4% случаев, что позволяет утверждать о высокой их информативности. Однако во время контрастирования нерва количество пациентов с частичной степенью повреждения нервов уточнена в 2,3% наблюдениях по отношению к УЗ-сканированию и ЭНМГ-тестированию. Информативность интраоперационного ультразвукового исследования подтверждается и тем фактом, что у пациентов (n=21) с анатомически сохранным стволом нерва обнаружены локальные изменения его эхогенности (n=5), характерные для рубцового процесса либо наличия внутриствольных невром, которые коренным образом изменили тактику лечения.
Приводя результаты этих сопоставлений, мы отдаем себе отчет в том, что сравнение нейрофизиологических и морфоструктурных исследований в какой-то степени является не совсем корректным, но комплекс этих методик позволяет улучшить качество интраоперационной диагностики. Того же мнения придерживается и ряд других авторов [9–11].
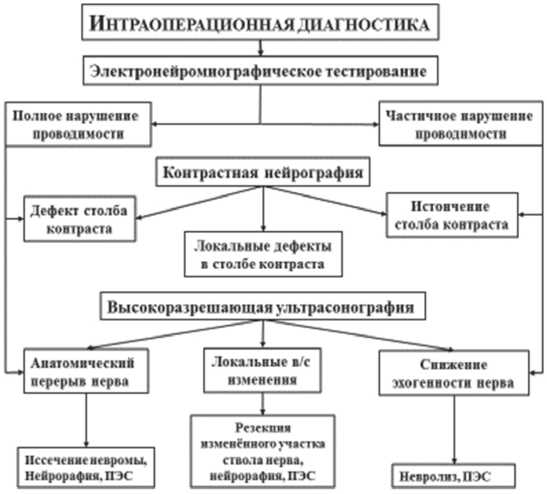
Рис. 2. Алгоритм интраоперационной диагностики и тактики хирургического лечения: ПЭС — прямая электростимуляция ствола нерва; В/С — внутристволовые (изменения)
Результаты комплексного интраоперационного тестирования стали основой для разработки диагностико-тактического алгоритма (рис. 2).
Так, при частичном нарушении проводимости, наличии эхо-признаков анатомической целостности ствола нерва и истончении столба контраста на нейрограммах возникают показания к выделению нерва из спаек (невролиз) с имплантацией на его ствол электродов для последующей прямой электростимуляции.
Если во время интраоперационного тестирования обнаружено полное нарушение проводимости нерва, при ультразвуковом сканировании найдены эхо-признаки анатомического перерыва его ствола с центральной невромой, а на нейрограмме выявляется дефект столба контраста, то возникают показания к иссечению невромы, нейрорафии с установкой на ствол нерва электродов для последующей прямой электростимуляции. В случаях обнаружения эхо-признаков грубых внутриствольных изменений и дефекта столба контраста при контрастировании ствола нерва на фоне полного нарушения его проводимости тактика хирургического лечения склонялась в пользу резекции измененного участка, нейрорафии с имплантацией электродов для последующей долгосрочной прямой электростимуляции его ствола.
Выводы:
-
1. Для определения тактики хирургического лечения пациентов с травмой периферических нервов конечностей помимо методов дооперационно-го клинико-неврологического и инструментального обследования особое значение следует придавать комплексной интраоперационной диагностике с использованием ЭНМГ-тестирования, УЗ-сканирования и контрастирования ствола нерва.
-
2. Ультрасонография является высокоразрешающим методом диагностики, что позволяет ее использовать для объективной оценки тяжести и характера повреждения ствола нерва как перед операцией, так и интраоперационно.
-
3. Диагностические критерии, полученные во время комплексного интрао-перационного тестирования, где центральное место занимает ультрасонография, позволяют усовершенствовать хирургические
методики и разработать алгоритм дифференцированного их применения у пациентов с повреждениями периферических нервов конечностей.
Список литературы Интраоперационная нейровизуализация в хирургическом лечении пациентов с повреждениями периферических нервов конечностей
- Рассел С.M. Диагностика повреждения периферических нервов. Москва: Бином, 2009; 256 с.
- Еськин H.A., Матвеева Н.Ю., Приписнова С.Г. Возможности ультразвукового исследования в диагностике повреждений и заболеваний периферических нервов верхней конечности. Вестник травматологии и ортопедии им. Н.Н. Приорова 2008; (2): 82-87
- Коршунова Г.А. Значение электромиографии в отборе пострадавших с повреждением периферических нервов верхней конечности для проведения восстановительной электронейромодуляции. Российский нейрохирургический журнал им. А.Л. Поленова 2013; 5 (1): 16-19
- Filler AG, Maravilla KR, Tsuruda JS. MR neurography and-muscle MR imaging for image diagnosis of disorders affectingthe peripheral nerves and musculature. Neurol Clin 2004; 22 (6-7): 643-682
- Салтыкова В.Г., Голубев И.О., Меркулов М.В., Шток А.В. Роль ультразвукового исследования при планировании объема пластики периферических нервов. Ультразвуковая и функциональная диагностика 2012; (4): 62-68
- Джумагишиев Д.К. Контрастная нейрография в комплексной диагностике повреждений периферических нервов (клинико-экспериментальное исследование): автореф. дис... канд. мед. наук. Саратов, 2007; 24 с.
- Салтыкова, В.Г. Ультразвуковая диагностика состояния периферических нервов (норма, повреждения, заболевания): автореф. дис. д-ра мед. наук. Москва, 2011; 49 с.
- Берснев В.П., Кокин Г.С. Итоги выполнения плана НИР «Разработка новых методов диагностики и комплексного лечения повреждений и заболеваний периферической нервной системы» за 2001-2004 гг. В кн.: Поленовские чтения. СПб., 2005. С. 121
- Голубев В.Г., Крупаткин А.И., Панов Д.Е. Использование новых методов функциональной диагностики при повреждениях срединного и локтевого нервов//Травматология и ортопедия 2005; (2): 105-106
- Кхир Бек Мохамад. Комплексная диагностика и оптимальный подход к лечению травматических повреждений лучевого нерва: автореф. дис.... канд. мед. наук. М., 2009; 23 с.


