Интраоперационная ультразвуковая оценка радикальности удаления объемных образований головного мозга
Автор: Ветшева Н.Н., Васильев С.А., Фисенко Е.П., Ховрин В.В., Федоров Д.Н., Галян Т.Н., Зуев А.А., Песня-прасолов С.Б., Сандриков В.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.6, 2011 года.
Бесплатный доступ
Впервые в нашей стране проведен интраоперационный ультразвуковой мониторинг 116 больным с образованиями головного мозга, находившимся на стационарном лечении в нейрохирургическом отделении Российского научного центра хирургии им. акад. Б.В. Петровского РАМН в период с апреля 2007 по март 2010. В ходе исследования разработали комплекс ультразвуковых дифференциально-диагностических критериев оценки резекционной полости на предмет наличия остаточной опухолевой ткани. Все интраоперационные данные сравнивали с результатами до- и послеоперационной МРТ, гистологическим исследованием материала. Доказано что, комплексное интраоперационное ультразвуковое исследование с применением современных режимов обработки изображений является высокоинформативным методом оценки радикальности выполненного вмешательства.
Интраоперационное ультразвуковое исследование, образования головного мозга
Короткий адрес: https://sciup.org/140187882
IDR: 140187882 | УДК: 616.831-006-089.197.6:534.003.12
Intraoperative ultrasound diagnosis radical removal of brain tumor
For the first time in our country carried out intraoperative ultrasound monitoring of 116 patients with formations of the brain, who was hospitalized in the neurosurgical department of the Russian Scientific Center of Surgery named. acad. B.V. Petrovsky RAMS during the period April 2007 to March 2010. In the study developed a set of ultrasonic differential diagnostic criteria for resection cavity for the presence of residual tumor tissue. All intraoperative data were compared with results of pre-and postoperative MRI, and histological examination of the material. Proved that a complex intraoperative ultrasound with application of modern modes of image processing is a highly informative method for assessing the efficacy of the treatment procedures.
Текст научной статьи Интраоперационная ультразвуковая оценка радикальности удаления объемных образований головного мозга
На современном этапе развития нейрохирургии для решения важнейших задач, таких как увеличение продолжительности и качества жизни онкологических пациентов, необходимо совершенствовать методы до-, интра- и последоперационной диагностики.
На дооперационном этапе компьютерная (КТ) и магнитно-резонансная томографии (МРТ) дают обзорную картину головного мозга, позволяют оценить объем образования и распространенность процесса, определить границы предполагаемой краниотомии [14]. Смещение внутримозговых структур во время операций не позволяет ориентироваться хирургам на ранее полученные инструментальные данные, и риск неполного удаления внутримозгового образования остается высоким [12]. А как известно выживаемость нейроонкологических больных прямо связана с радикальностью [6].
Для достижения лучших результатов во время операций на головном мозге стали использовать интраоперационное ультразвуковое исследование (ИОУЗИ), которое открыло новые возможности оценки области интереса и позволило вплотную приблизиться к решению проблемы дифференциальной диагностики опухолевой и мозговой ткани, [9]. Также при ИОУЗИ стали выявлять остаточную опухолевую ткань в зоне резекции [7]. Однако данные авторов в ультразвуковой оценке послеоперационного ложа на предмет определения остаточной ткани разрознены, основаны на малом числе наблюдений и разноречивы.
В России опубликованы единичные работы, посвященные изучению ультразвуковой интраоперационной диагностики в нейроонкологии. По данным исследования А.В. Савелло (2008), в 79,7% оперативных вмешательств по поводу внутримозговых новообразований после выполнения контрольного ИОУЗИ объем резекции был увеличен, за счет выявления неудаленных фрагментов. В своей работе Р.А. Лапшин (2006) отмечает рост доли тотально удаленных образований при применении УЗ-контроля. Однако работы носят в основном описательный характер, на сегодняшний день нет четких ультразвуковых критериев оценки резекционной полости.
Для определения радикальности удаления внутричерепного новообразования в качестве «стандарта» используют результаты послеоперационных КТ, МРТ с контрастным усилением, гистологического исследования биопсийного материала из ложа опухоли [3].
Дальнейшее изучение проблем интраоперационного мониторинга удалений внутримозговых образований должно способствовать повышению качества хирургической помощи и как следствие улучшению выживаемости и качества жизни онкологических больных.
Цель исследования . Определить эффективность ультразвукового интраоперационного исследования в оценке радикальности удаления объемных образований головного мозга.
Материалы и методы
В наблюдение вошли 116 пациентов прооперированных в РНЦХ им. акад. Б.В. Петровского РАМН за период с апреля 2007 г. по март 2010 г. Из них мужчин – 66 (56,9%), женщин – 50 (43,1%), средний возраст составил 49,2±17,2 см. Среди нозологий преобладали внутримозговые опухоли глиального ряда различной степени злокачественности – 55 пациентов (47,7%), так же в исследование вошли 49

(42,2%) пациентов с менингиомами головного мозга и 12 (10,1%) пациентов с метастастатическими опухолями головного мозга.
Всем пациентам на до- и послеоперационном этапе проводили МРТ с контрастным усилением. МРТ выполняли на аппарате 1,5 Т Magneton, Avanto, Siemens (Германия) до и на фоне введения гадолиний-содержащего контрастного препарата (0,1–0,2 ммоль/ кг массы тела). Определяли локализацию и размер краниотомного доступа, оценивали объем поражения и распространенность процесса. В послеоперационном периоде МРТ выполнялось для оценки и выявления возможных ранних п/о осложнений и контроля радикальности оперативного вмешательства.
ИОУЗИ внутримозговых образований проводили при помощи специализированных УЗ-сканеров B&K (Дания), конвексными датчиками с меняющейся частотой 5,0–8,0 МГц и 5,0–10,0 МГц и рабочей поверхностью 0,5 х 0,7 см, 0,7 х 1,5 см и 1,0 х 5,0 см. Выбор датчика зависел от цели исследования и площади трепанационного окна. Поверхностно расположенные структуры и образования (до 3 см глубиной) оценивали с частотой сканирования 11,0–7,5 МГц, для осмотра области глубже 3 см от твердой мозговой оболочки (ТМО), уменьшали частоту до 7,0–5,0 МГц.
Во время операции в качестве метода навигации после трепанации использовали ИОУЗИ, для определения локализации патологического очага, оценке границ предполагаемой резекции, выявления перифокального отека.
Комплексное ИОУЗИ включало в себя: сканирование в режиме серой шкалы, цветовое допплеровское картирование (ЦДК) скоростей кровотока и энергии пока, импульсно-волновое допплеровское сканирование, трехмерную реконструкцию изображения.
По завершению основного этапа операции проводили контрольное сканирование, на предмет обнаружения остаточной опухолевой ткани. Заполняли резекционную полость физиологическим раствором и сканировали через жидкость. Оценивали толщину стенок резекционной полости и проводили сравнение ее отдельных участков между собой. Измерение гиперэхогенного кольца резекционной полости выполняли перпендикулярно к внутренней стенке ложа опухоли. В режиме ЦДК исследовали сосудистый рисунок окружающих тканей. Проведение 3D ультразвукового контроля выполнено у 29 (25%) пациентов, когда данных В-режима было недостаточно или не удавалось четко вывести интересующий участок.
При выявлении остаточной ткани опухоли выполняли ее удаление с последующей гистологической верификацией.
Кратность применения контрольного ИОУЗИ у одного пациента составила в среднем 3,2 раза (от 1 до 5 раз). Полученные в ходе ИОУЗИ результаты также сравнивали с до- и послеоперационными МРТ.
Результаты анализировали с применением статисти- ческих методов. Достоверными считались различия при p<0,05. Для оценки эффективности диагностических исследований вычисляли чувствительность, специфичность и точность метода.
Результаты исследования и их обсуждение
При УЗ-сканировании область, где выполнялась резекция опухоли, была представлена в виде анэхогенной конусовидной структуры с гиперэхогенным контуром, описываемым в литературе как «эффект кольца», возникающим вследствие коагуляции и механического воздействия на ткань [10].
По нашим данным толщина гиперэхогенного кольца остаточной полости при тотальном удалении опухоли составляла 2,0–5,0 мм (в среднем 3,0±0,9 мм).
На вид резекционной полости влиял способ удаления образования. Так, применение менее травматичного ультразвукового дезинтегратора оставляло тонкую полоску до 3,0 мм, а использование биполярной коагуляции приводило к формированию грубых стенок полости с поврежденными тканями, толщина которых достигала 5,0 мм (рис. 1).
При гистологическом исследовании гиперэхогенного участка стенки резекционной полости при тотальном удалении образования получали периваскулярный и перицеллюлярный отек ткани головного мозга.
При наличии остаточной ткани опухоли толщина гиперэхогенного кольца превышала 5,0 мм (8,0±2,3 мм), что достоверно отличалось (р<0,05) от толщины стенок ложа опухоли при ее тотальном удалении (рис. 2).
При мониторировании резекционной полости в ходе операции мы подтвердили данные N. Erdogan с со-авт. (2005) о том, что за остаточную опухолевую ткань следует принимать участок повышенной эхоплотности уходящий от хирургической зоны резекции в ткань мозга от 5,0 мм и более.
Однако исследователи не учитывали толщину интактных стенок послеоперационного ложа у каждого конкретного пациента. При этом точность ИОУЗИ в определении остаточной ткани была низкой – 72% [4]. Дальнейший анализ нашего исследования показал, что необходимо сравнивать различные участки ложа опухоли у каждого конкретного пациента.
Ориентируясь на неравномерное утолщение стенки резекционной полости >3,0 мм M. Woydt (1996) при помощи ИОУЗИ оценивал остаточную ткань опухоли со специфичностью до 81%. При этом не исключал возможность ложноотрицательных результатов. По данным нашей работы различные участки стенки резекционной полости у одного пациента не должны отличаться по толщине более чем на 2,5 мм.
Сводные данные по оценке резекционной полости представлены в таблице 1.
В результате нашего исследования мы пришли к выводу, что за остаточную опухолевую ткань следует принимать участок неравномерного утолщения стенки
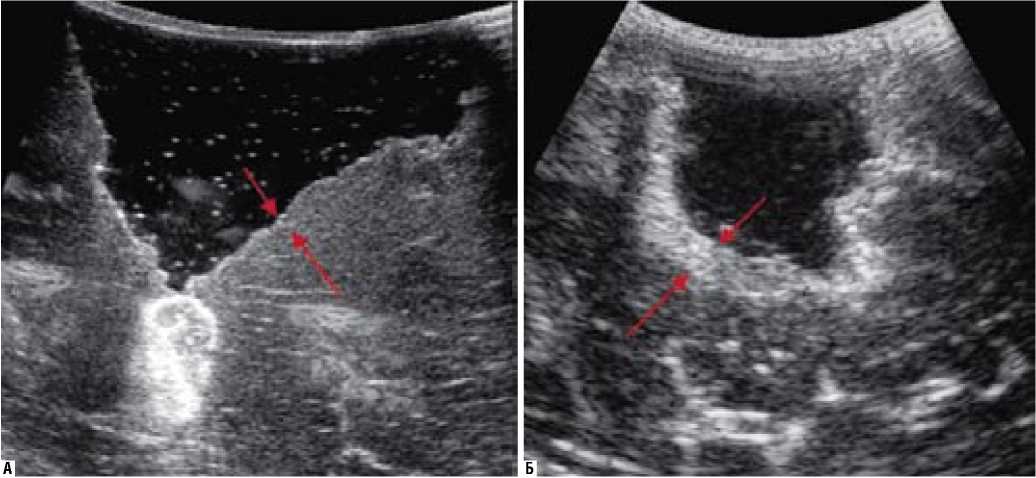
Рис. 1. ИОУЗИ головного мозга. Остаточная полость при тотальном удалении образования. А – толщина стенок резекционной полости менее 3 мм. Б – толщина стенок резекционной полости 3–5 мм
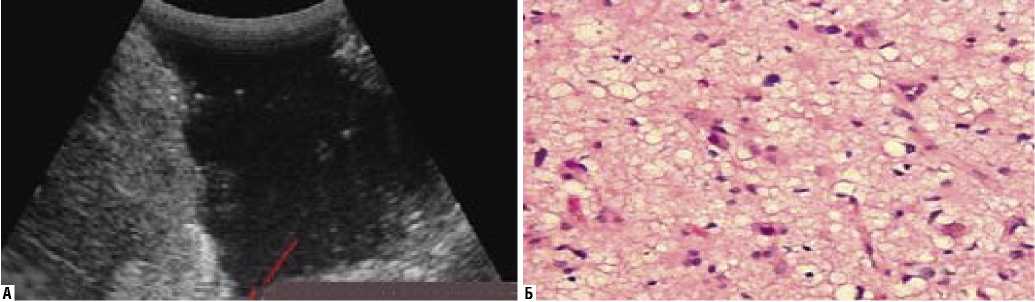
Рис. 2. Остаточная опухолевая ткань. А – ИОУЗИ резекционной полости. Остаточная опухолевая ткань (показана стрелками). Б – гистологические исследование материала. Фибриллярная астроцитома. ГЭх400
Табл. 1. Толщина стенки резекционной полости по данным ИОУЗИ
В процессе выполнения работы мы столкнулись с некоторыми трудностями, описанными также ранее другими исследователями. Артефакты от сгустков крови, воздуха и кровоостанавливающих материалов при ультразвуковом сканировании резекционной полости могут приводить как к ложноположительным, так и к ложноотрицательным результатам [8]. Чтобы избежать этого во время исследования, предварительно санировали остаточную полость, проводили адекватный гемостаз, после чего выполняли повторные сканирования.
Кроме того, проходящие рядом с зоной резекцией сосудистые структуры в ряде случаев имитировали остаточную опухолевую ткань, что могло также привести к ложноположительным результатам. Применение режимов цветового и энергетического картирования при контрольном ИОУЗИ позволило исключить ошибку и избежать нежелательной хирургической травмы (рис. 3).
Трехмерная реконструкция изображения позволила полипозиционно оценить интересующие участки, наглядно представить топографию резекционной полости и уточнить локализацию остаточной опухолевой ткани. Оценка зоны резекции в различных сечениях и
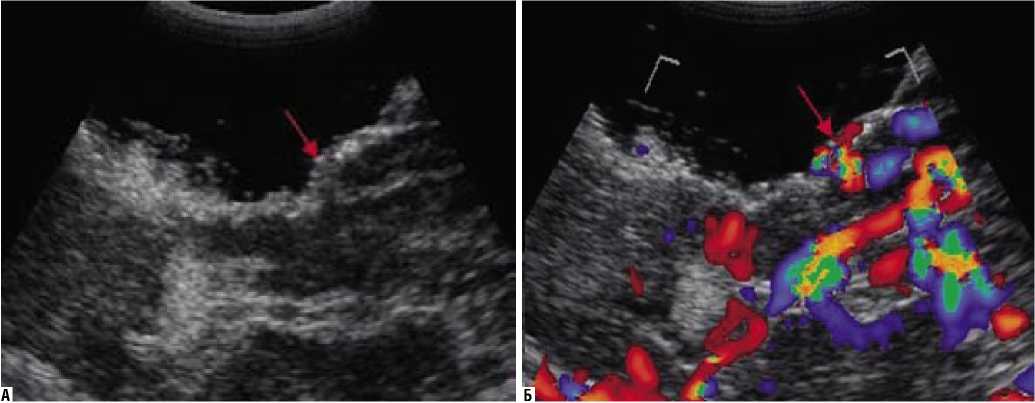
Рис. 3. ИОУЗИ стенки резекционной полости при тотальном удалении внутримозгового образования. А – В-режим. Б – Режим ЦДК. Стрелкой указан сосуд, принятый в В-режиме за остаточную ткань
плоскостях при построении 3D реконструкции позволило отдифференцировать гиперэхогенные борозды, расположенные в непосредственной близости от ложа, и остаточную опухолевую ткань (рис. 4).
В доступной литературе работ о применении допплеровских режимов и 3D реконструкции ультразвуковых изображений при ИОУЗ-контроле мы не встретили.
Применяя для оценки резекционной полости комплексное ИОУЗИ и разработанные нами критерии, удалось снизить % ложноотрицательных результатов по сравнению с литературой с 12,5–14% [4, 5] до 7,4% при серошкальном сканировании и 4,4% при применении режима трехмерной реконструкции.
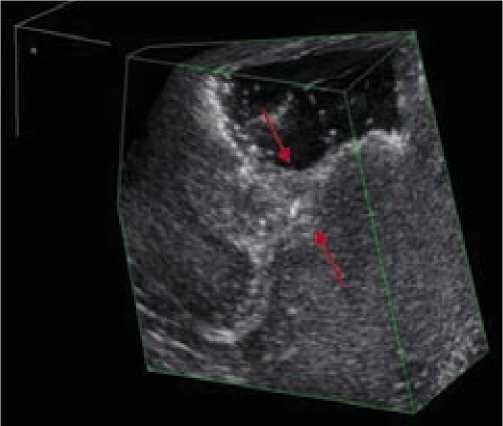
Рис. 4. ИОУЗИ головного мозга. Режим трехмерной реконструкции. Резекционная полость после тотального удаления опухоли. Стрелками указана борозда, имитирующая в В-режиме остаточную опухолевую ткань
Таким образом, комплексное интраоперационное ультразвуковое исследование с применением современных режимов обработки изображений является высокоинформативным методом оценки радикальности выполненного вмешательства. Основными ультразвуковыми критериями наличия остаточной опухолевой ткани следует считать выявление гиперэхогенных структур в ложе опухоли, вдающихся в белое вещество головного мозга более чем на 5,0 мм и/или превышающих по толщине остальные стенки остаточной полости более чем на 2,5 мм.
Список литературы Интраоперационная ультразвуковая оценка радикальности удаления объемных образований головного мозга
- Лапшин Р.А. Нейронавигация в хирургии объемных образований головного мозга: автореф. дисс. на соиск. уч. ст. канд. мед. Наук/Р.А. Лапшин. -С.-П., 2006, -24 с.
- Савелло А.В. Комплексное дифференцированное применение методов пред-и интраоперационной визуализации, нейронавигации и рентгенохирургии на этапе хирургического лечения пациентов с внутричерепными опухолями: автореф. дисс. на соиск. уч. ст. докт. мед. наук/А.В. Савелло, С.-П., 2008, -34 с.
- Терновой С.К. Компьютерная и магнитно-резонансная томография в оценке радикальности хирургического лечения опухолей головного мозга/Терновой С.К., Арабинский А.В., Евзиков Г.Ю., Осиповская А.С.//Медицинская визулиза-ция. -2006 -№ 6. -С. 84 -93.
- Erdogan N. Ultrasound Guidance in Intracranial Tumor Resection: Correlation with Postoperative Magnetic Resonance Findings./Erdogan N.; Tucer B.; Mavili E.; Menku A.; Kurtsoy A.//Acta Radiologica. -2005 -Vol. 46. -№ 7 -Р. 743-749.
- Hofer N. Intraoperative navigated ultrasound for the control of tumor resection in cerebral gliomas/Hofer N., C. Wurth, Nadji-Ohl M.//German Medical Science GMS Publishing House; 2009 -P. 06-09.
- Jeremic B. Clinical prognostic factors in patients with malignant glioma treated with combined modalfty approach/Jeremic B., Milicic B., Grujicic D., Dagovic A., Aleksandrovic J., Nikolic N.//Am J Clin Oncol-Cancer Clin Trials. -2004. -№ 27. Р. 195-204.
- Lindseth F. Image fusion of ultrasound and MRI as an aid for assessing anatomical shifts and for improving overview and interpretation in ultrasound guided neurosurgery/, Ommedal S., Bang J., Unsgard G., Hernes T.//CARS 2001: Proceedings of the 15th International Congress and Exhibition in Computer Assisted Radiology and Surgery, Berlin, June 27-30, 2001. -Р. 523-525.
- Matz P. Cavernous malformation. Results of image-guided resection/Matz P., McDermott M., Gutin P., Dillon W., Wilson C.//J Image Guid Surg. -1995. -№ 1. Р. 273-279.
- Nobusada Sh. Delineation of Brain Tumor Margins Using Intraoperative Sononavigation: Implications for Tumor Resection/Nobusada Shinoura, Masamichi Takahashi, Ryozi Yamada.//J Clin Ultrasound. -2006. -№ 34. -Р. 177-183.
- Unsgaard G. Brain operations guided by real-time two-dimensional ultrasound: new possibilities as a result of improved image quality/Unsgaard G., Gronningsaeter A., Ommedal S., Nagelhus Hernes T.A.//Neurosurgery. -2002. -№ 51. -Р. 402-412.
- Unsgaard G. Intra-operative 3D ultrasound in neurosurgery/Unsgaard G., O. M. Rygh, T. Selbekk, T. B. Muller, F. Kolstad, F. Lindseth and T. A. Nagelhus Hernes.//Acta Neurochir (Wien). -2006. -№ 148. -Р. 235-253.
- Wirtz C. Clinical evaluation and follow-up results for intraoperative magnetic resonance imaging in neurosurgery/Wirtz C.R., Knauth M., Staubert A., Bonsanto M.M., Sartor K., Kunze S., Tronnier V.M://Neurosurgery. -2000. -№ 46. -Р. 1112-1122
- Woydt M. Correlation of intraoperative ultrasound with histopathologic findings after tumor resection in supratentorial gliomas/Woydt M., Krone A., Becker G., Schmidt K., Roggendorf W, Roosen K.//Acta Neurochir (Wien). -1996. -№ 138. -Р. 1391-1398.
- Woydt M. Ultrasound-guided neuronavigation of deep-seated cavernous haemangi-omas: clinical results and navigation techniques/Woydt M., A. Krone, N. Soeren& K. Roosen.//Br J Neurosurgery. -2001. -№ 15(6). -Р. 485-495.


