Интраперитонеальное химиоперфузионное лечение диссеминированного рака яичника диоксадэтом в сравнении с цисплатином в эксперименте
Автор: Беспалов В.Г., Беляева О.А., Киреева Г.С., Сенчик К.Ю., Стуков А.Н., Беляев А.М.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 2 (62), 2014 года.
Бесплатный доступ
Проведено сравнительное изучение противоопухолевой активности цисплатина и диоксадэта в химиоперфузионном лечении на модели асцитной опухоли яичника (ОЯ) у 172 самок крыс линии Вистар. Асцитная ОЯ перевивалась внутрибрюшинно по 0,5 мл асцитической жидкости каждой крысе в концентрации 2×10 7 опухолевых клеток/мл. Препараты вводили однократно через 48 ч после перевивки ОЯ в максимально переносимых дозах (МПД). Нормотермическую интраперитонеальную химиоперфузию (НИПХ) и гипертермическую интраперитонеальную химиоперфузию (ГИПХ) с цисплатином и диоксадэтом осуществляли в дозах, в 5−20 раз превышающих дозы этих препаратов при их обычном интраперитонеальном введении. Противоопухолевые эффекты препаратов оценивали по увеличению продолжительности жизни животных. При нормо- и гипертермической химиоперфузии цисплатин увеличивал МПЖ на 317 % и 183 % (р
Нормо-и гипертермическая интраперитонеальная химиоперфузия, опухоль яичников, диоксадэт, цисплатин
Короткий адрес: https://sciup.org/14056413
IDR: 14056413 | УДК: 618.11-006:615.28]-092.9
Intraperitoneal chemoperfusion treatment of advanced ovarian cancer with dioxadet compared to cisplatin in experimental study
Comparative study of antitumor activity of cisplatin and dioxadet in chemoperfusion treatment was carried out on ascitic ovarian cancer model in 172 Vistar female rats. Ovarian cancer was inoculated intraperitoneally at a volume of 0.5 ml per rat with concentration of tumor cells 2×10 7/ ml. The drugs were administered once in 48 hours after inoculation of ovarian cancer in maximum tolerated doses (MTD). Normothermic intraperitoneal chemoperfusion (IPEC) and hyperthermic intraperitoneal chemoperfusion (HIPEC) were performed with cisplatin or dioxadet at doses that were 5−20 times higher than those for their standard intraperitoneal administration. Antitumor effects of the drugs were estimated in increase of median survival time (MST). In case of IPEC and HIPEC cisplatin increased the MST by 317 % and 183 % (р
Текст научной статьи Интраперитонеальное химиоперфузионное лечение диссеминированного рака яичника диоксадэтом в сравнении с цисплатином в эксперименте
Заболеваемость раком яичника (РЯ) в России составляет 2,5 % в общей структуре заболеваемости злокачественными новообразованиями и 4,6 % среди гинекологических опухолей (3-е место после рака тела и шейки матки). Согласно данным попу- ляционных регистров, 5-летняя выживаемость при РЯ варьирует в пределах от 12 до 42 % [4]. Прогрессирование РЯ происходит преимущественно в виде диссеминации по брюшине с развитием карциноматоза [1]. Для лечения перитонеального карцино- матоза и асцита используется внутрибрюшинная (в/б) химиотерапия цитостатиками, позволяющая увеличить концентрацию лекарственного вещества в брюшной полости, усилить его проникновение в опухолевую ткань и уменьшить системное токсическое действие [8].
Одним из вариантов в/б химиотерапии является высокотехнологичный метод интраперитонеальной химиоперфузии. Сочетание данного метода лечения с локальной гипертермией рассматривается как перспективный вариант лечения карциноматоза брюшной полости, позволяющий значительно увеличить выживаемость больных диссеминированным РЯ. Согласно данным одного из последних метаанализов гипертермическая интраперитонеальная химиоперфузия (ГИПХ) с цисплатином или другими цитостатиками после циторедуктивной операции обеспечивает среднюю продолжительность жизни пациентов с РЯ до 64 мес, тогда как при стандартной внутривенной химиотерапии цисплатином этот показатель составляет около 30 мес. Однако результаты этого же исследоваия свидетельствуют о том, что токсичность химиотерапии III степени регистрировалась у 40 % больных, IV степени – у 15 % больных [6]. Для улучшения результатов лечения больных с диссеминированным РЯ и снижения токсичности в/б химиотерапии необходим поиск новых противоопухолевых препаратов [2].
В «НИИ онкологии им. Н.Н. Петрова» был разработан отечественный противоопухолевый препарат из группы алкилирующих соединений этиленими-нов – диоксадэт, обладающий высоким контактным противоопухолевым действием [5]. Ранее нами было показано, что при обычном в/б введении в максимально переносимых дозах (МПД) диоксадэт проявил противоопухолевую активность, сравнимую с цисплатином [3]. В то же время диоксадэт отличается меньшей системной токсичностью и не вызывает спаек в брюшной полости, что характерно для цисплатина [5].
Цель исследования – изучить противоопухолевое действие диоксадэта в сравнении с цисплатином в химиоперфузионном лечении РЯ в эксперименте.
Материал и методы
Исследование проведено на 172 самках крыс линии Вистар с массой тела 200–260 г из питомника «Рапполово» РАМН. Животные получали стандартный полнорационный брикетированный комбикорм (рецепт ПК-120) производства компании «Лабора- торкорм» (Москва) и водопроводную питьевую воду без ограничений.
Использован штамм ОЯ, созданный в 1958 г. перевивкой ОЯ от крысы, подвергшейся трансплацентарному воздействию 7,12-диметилбенз(а)антрацена. Штамм ОЯ был получен из РОНЦ им. Н.Н. Блохина РАМН. При проведении эксперимента штамм ОЯ постоянно перевивали в/б нескольким крысам: всего для поддержания штамма были использованы 44 крысы. От одной крысы на 5–7-й день после перевивки ОЯ брали асцит, разбавляли его стерильным физиологическим раствором и вводили в/б точное количество опухолевых клеток (1×107) всем крысам, включенным в эксперимент.
После перевивки ОЯ крысы рандомизировались на 9 групп: I группа (n=19) – контроль (0,5 мл физиологического раствора в/б); II группа (n=11) – нормотермическая интраперитонеальная перфузия физиологическим раствором (НИПП); III группа (n=14) – гипертермическая интраперитонеальная перфузия физиологическим раствором (ГИПП); IV группа (n=12) – цисплатин, растворенный в физиологическом растворе в дозе 4 мг/кг массы тела в/б; V группа (n=12) – цисплатин при НИПХ (нормотермическая интраперитонеальная химиоперфузия) в дозе 40 мг/кг; VI группа (n=14) – цисплатин при ГИПХ в дозе 20 мг/кг; VI группа (n=19) – диоксадэт, растворенный в физиологическом растворе в дозе 1,5 мг/кг массы тела в/б; VII группа (n=14) – диокса-дэт при НИПХ в дозе 30 мг/кг; VIII группа (n=13) – диоксадэт при ГИПХ в дозе 15 мг/кг. Все описанные манипуляции проводились однократно через 48 ч после перевивки ОЯ.
США). Использованы лекарственные препараты: ди-оксадэт, цисплатин (Фармахеми Б.В., Нидерланды) в виде раствора для инъекций (0,5 мг/мл), гемобаланс (Nature Vet, Австралия), кетопрофен (Фламакс, ЗАО «ФармФирма «Сотекс», Россия), тиопентал натрия (ОАО «Акционерное Курганское общество медицинских препаратов и изделий «Синтез», Россия), цефтриаксон (Медокеми Лтд., Кипр). Диоксадэт в виде порошка для приготовления раствора для инфузий был синтезирован компанией «Кемконсалт» (Россия) в соответствии с лабораторным технологическим регламентом синтеза данного препарата.
Перед проведением перфузии в брюшную полость помещали цифровой термометр и катетеры на приток (в левой подвздошной области) и на отток (в правой подвздошной области) жидкости и затем зашивали в 2 слоя абдоминальную стенку с использованием стерильного рассасывающегося шовного материала для мышечной ткани и плетеного нерассасывающегося стерильного шовного материала для кожи. Температура перфузата, поступавшего в брюшную полость, составляла 36–37°С при НИПХ и 40,5–41,5°С при ГИПХ. Время перфузии составляло 45 мин, объем перфузата - 200 мл. После химиоперфузии проводилась промывка брюшной полости 0,9 % раствором натрия хлорида (20 мин), катетеры и термометры вынимались, и стенка брюшной полости зашивалась таким же образом. На протяжении операции крыса лежала на теплой грелке для предотвращения гипотермии организма. В день после операции и через
24 ч животному внутримышечно вводили цефтриаксон (Медаксон, «Медокеми Лтд.», Кипр) в дозе 93 мг/кг, гемобаланс подкожно 0,1 мл и 10 мл 0,9 % раствора натрия хлорида подкожно.
Результаты оценивали по продолжительности жизни крыс. День перевивки ОЯ был принят за нулевой. Противоопухолевые эффекты препаратов оценивали по увеличению продолжительности жизни (УПЖ) по сравнению с контрольными животными, не получавшими лечения.
УПЖ в % рассчитывали по формуле:
МПЖО – МПЖК
УПЖ = ———————— × 100, МПЖК где МПЖО и МПЖК –, медиана продолжительности жизни крыс опытной и контрольной группы соответственно.
Результаты эксперимента подвергали статистической обработке на персональном компьютере с помощью программ GraphPad Prism 6, SPSS Statistics 17.0. Статистический анализ показателей выживаемости проводили с использованием критерия Лиллиефорса, показателей МПЖ в группах – с помощью непараметрического критерия U (Манна – Уитни), кривых выживаемости – по тесту Мантел – Кокса (Long-rank test). Различия считали статистически значимыми при p<0,05.
Результаты исследования
Статистически значимые различия от контроля по кривым выживаемости в результате лечения ци-
Влияние диоксадэта и цисплатина при обычном и химиоперфузионном введении на продолжительность жизни у крыс самок с асцитной опухолью яичника
Таблица
|
Группа |
Показатель |
||
|
СПЖ, сут |
МПЖ, сут |
УПЖ по сравнению с I группой |
|
|
I. Контроль (n=19) |
14,4 ± 2,28 |
9 |
- |
|
II. НИПП (n=11) |
14,8 ± 1,52 |
16 |
78 % |
|
III. ГИПП (n=14) |
29,6 ± 6,13 |
22,5 I |
150 % |
|
IV. Цисплатин в/б (n=12) |
22,8 ± 2,41 |
19,5 I, II |
117 % |
|
V. Цисплатин НИПХ (n=12) |
39,3 ± 5,67 |
37,5 I, II, IV |
317 % |
|
VI. Цисплатин ГИПХ (n=14) |
34,6 ± 6,48 |
25,5 I |
183 % |
|
VII. Диоксадэт в/б (n=19) |
28,5 ± 3,24 |
28 I, II |
211 % |
|
VIII. Диоксадэт НИПХ (n=14) |
30,14 ± 3,95 |
31 I, II |
244 % |
|
IX. Диоксадэт ГИПХ (n=13) |
46,2 ± 6,44 |
49 I, III, VII |
444 % |
Примечание: разница статистически значима: I – по сравнению с I группой, II – по сравнению со II группой, III – по сравнению с III группой,IV - по сравнению с IV группой, VII – по сравнению с VII группой. СПЖ – средняя продолжительность жизни.
СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2014. № 2 (62)
сплатином и диоксадэтом наблюдались с 9-х сут и до конца эксперимента. По тесту Мантела – Кокса статистически значимые различия наблюдались между кривыми выживаемости нормотермической химиоперфузии цисплатином (р=0,0002), диокса-дэтом (р=0,0005) и физиологическим раствором и отсутствовали между кривыми выживаемости гипертермической химиоперфузии цисплатином (р=0,6117), диоксадэтом (р=0,0958) и физиологическим раствором (таблица, рис. 1).
Как видно из таблицы, при НИПХ с цисплатином (V группа) и диоксадэтом (VIII группа) по сравнению с I группой наблюдали увеличение МПЖ соответственно на 317 % (p<0,001) и 244 % (p=0,001), причем при НИПХ цисплатин (V группа) по сравнению с его обычным в/б введением (IV группа) увеличивал МПЖ на 92 % (p=0,039), а диоксадэт (VIII группа) – лишь на 11 % (p>0,05). При ГИПХ с цисплатином (VI группа) и диоксадэ-том (IX группа) по сравнению с I группой наблюдали увеличение МПЖ соответственно на 183 % (p=0,002) и 444 % (p<0,001). Причем для цисплатина статистически значимой разницы по сравнению с его обычным в/б введением (IV группа) и ГИПП с физиологическим раствором (III группа), не было, тогда как диоксадэт при ГИПХ (IX группа) по сравнению с его обычным в/б введением (VII группа) и ГИПП с физиологическим раствором (III группа) увеличивал МПЖ соответственно на 75 % (p=0,002) и 118 % (p=0,038) (таблица).
Обсуждение
Применение цисплатина и диоксадэта в виде НИПХ и ГИПХ увеличивает их противоопухолевую активность, причем усиление противоопухолевых эффектов цисплатина проявляется больше при НИПХ, а диоксадэта при ГИПХ. Следовательно, технология химиоперфузионного лечения позволяет вводить цитостатики в значительно более высоких дозах по сравнению с обычным в/б введением, без сопутствующего увеличения токсичности за счет фиксированного уровня всасывания химиопрепаратов в системный кровоток из брюшной полости [7]. Так, в данном исследовании НИПХ с цисплатином и диоксадэтом осуществлялась в дозах 40 и 30 мг/кг массы тела соответственно, что в 10 и 20 раз превышает МПД препаратов при их обычном внутрибрюшинном введении, тогда как ГИПХ – в дозах 20 и 15 мг/кг массы тела соответственно, что в 5 и 10 раз превышает
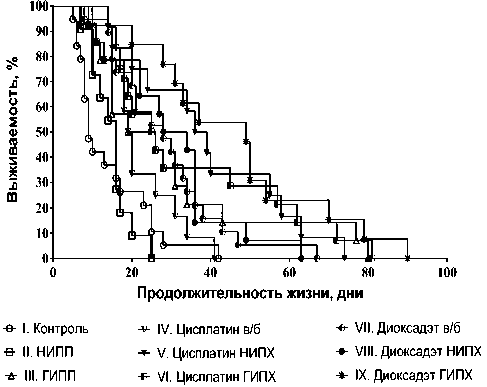
Рис. 1. Влияние диоксадэта и цисплатина при нормо- и гипертермической химиоперфузии на выживаемость животных с опухолью яичников.
Примечание: НИПП – нормотермическая интраперитонеальная перфузия; ГИПП – гипертермическая интраперитонеальная перфузия; НИПХ – нормотермическая интраперитонеальная химиоперфузия; ГИПХ – гипертермическая интраперитонеальная химиоперфузия
МПД препаратов при их обычном интраперитонеальном введении.
Полученные в ходе эксперимента результаты позволяют говорить о том, что химиоперфузионное лечение диссеминированного РЯ является более эффективным, чем стандартная интраперитонеальная химиотерапия. Наибольшее увеличение выживаемости экспериментальных животных было выявлено в группе, получавшей ГИПХ с диокса-дэтом. На основании этого данный режим может быть рекомендован для внедрения в клиническую практику для лечения карциноматоза брюшины у больных с далеко зашедшими стадиями РЯ.
Заключение
В эксперименте на самках крыс линии Вистар с перевиваемой асцитной ОЯ показано, что интраперитонеальная нормо- и гипертермическая химиоперфузии позволяют вводить цитостатические препараты в значительно более высоких дозах, чем при обычном внутрибрюшинном введении, что увеличивает выживаемость животных. НИПХ или ГИПХ с диоксадэтом или цисплатином увеличивают МПЖ на 75–92 % по сравнению с их обычным в/б введением. В условиях НИПХ противоопухолевое действие цисплатина проявляется сильнее действия диоксадэта. С другой стороны, диоксадэт при ГИПХ более эффективен в лечении диссеминированного РЯ, чем цисплатин. У крыс с перевитой ОЯ по сравнению с нелеченными животными УПЖ при ГИПХ с цисплатином составило 183 %, при ГИПХ с диоксадэтом – 444 %.
Работа выполнена при поддержке гранта Минобрнауки России «Разработка инновационной технологии лечения диссеминированного рака яичника», Соглашение 8305, и стипендии Президента Российской Федерации молодым ученым и аспирантам, осуществляющим перспективные научные исследования и разработки по приоритетным направлениям модернизации российской экономики, на 2012–2014 годы «Разработка инновационного противоопухолевого лекарственного препарата для химиоперфузионного лечения канцероматоза брюшины».


