Интратекальная химиотерапия в комплексном лечении детей с рабдомиосаркомой параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием
Автор: Родина А.Д., Поляков В.Г., Крылов А.С., Кашанина А.Л., Горбунова Т.В., Варфоломеева С.Р.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 1 т.25, 2026 года.
Бесплатный доступ
Введение. Рабдомиосаркома параменингеальной локализации с интракраниальным распространением характеризуется агрессивным течением и высоким риском лептоменингеального метастазирования (ЛМ). Исторически поражение центральной нервной системы (ЦНС) считалось инкурабельным состоянием с выживаемостью, не превышающей 10–20 %. Основным препятствием для проникновения большинства лекарственных препаратов и создания эффективной концентрации является гематоэнцефалический барьер (ГЭБ). В связи с этим поиск эффективных и нетоксичных методов контроля над лептоменингеальными метастазами является одной из наиболее актуальных задач детской онкологии. Интратекальная химиотерапия (ИТХТ), заключающаяся в прямом введении цитостатиков в спинномозговую жидкость, позволяет обойти ГЭБ и создать высокие терапевтические концентрации препаратов непосредственно в очаге поражения при минимальной системной токсичности. Цель исследования – оценить эффективность и безопасность интратекальной химиотерапии в комплексном лечении детей с рабдомиосаркомой параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием и улучшить показатели выживаемости данной когорты детей. Материал и методы. В исследование был включен 21 пациент с гистологически верифицированным диагнозом рабдомиосаркомы параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием, получавший лечение в НИИ детской онкологии и гематологии им. акад. Л.А. Дурнова в период с 2021 по 2024 г. Результаты. При медиане наблюдения 34,3 мес общая 2-летняя выживаемость составила 65 %. Данный показатель определялся высокой эффективностью раннего контроля над опухолевыми клетками за гематоэнцефалическим барьером: общая 2-летняя выживаемость достигла более 80 % как в группе профилактической, так и в группе терапевтической интратекальной химиотерапии первой линии. Это достоверно выше по сравнению с группой рецидива, где общая 2-летняя выживаемость составила 20 % (p<0,05), и существенно превосходит данные, представленные в зарубежной литературе о медиане выживаемости – 4–6 мес при лептоменингеальном метастазировании [1]. Профиль токсичности ИТХТ был благоприятным, без случаев тяжелой нейротоксичности. Заключение. Интенсивная интратекальная химиотерапия в комплексном лечении детей с рабдомиосаркомой параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием является эффективным и безопасным методом контроля над опухолевыми клетками за гематоэнцефалическим барьером, позволяющим значительно улучшить выживаемость в этой прогностически крайне неблагоприятной группе пациентов.
Рабдомиосаркома, параменингеальная локализация, дети, интратекальная химиотерапия, лептоменингеальное метастазирование, центральная нервная система, гематоэнцефалический барьер
Короткий адрес: https://sciup.org/140314345
IDR: 140314345 | УДК: 616-006.364.03-053-08:615.28 | DOI: 10.21294/1814-4861-2026-25-1-28-45
Intrathecal chemotherapy in the complex treatment of children with parameningeal rhabdomyosarcoma with intracranial spread and/or leptomeningeal metastasis
Introduction. Parameningeal rhabdomyosarcoma with intracranial spread is a highly aggressive pediatric malignancy with a high risk of leptomeningeal metastasis. Historically, central nervous system (CNS) involvement was considered an incurable condition with a survival rate of no more than 10–20 %. The bloodbrain barrier is the primary barrier to the penetration of most drugs and the creation of effective concentrations. Therefore, the search for effective and non-toxic methods for controlling leptomeningeal metastases is one of the most pressing challenges in pediatric oncology. Intrathecal chemotherapy (ITCT) delivers cancer drugs directly into the cerebrospinal fuid, bypassing the BBB. It enables high concentrations of medication to directly target cells, reducing systemic toxicity. The purpose of the study was to evaluate the effcacy and safety of intrathecal chemotherapy in a multidisciplinary approach to the treatment of children with parameningeal rhabdomyosarcoma with intracranial spread and/or leptomeningeal metastasis, and to improve survival rates in this cohort of children. Material and Methods. The study included 21 patients with a histologically verifed diagnosis of parameningeal rhabdomyosarcoma with intracranial spread and/or leptomeningeal metastasis, who received treatment at the L.A. Durnov Research Institute of Pediatric Oncology and Hematology of the Russian Academy of Medical Sciences from 2021 to 2024. The study was approved by the local ethics committee. Results. With a 34.3-month median follow-up, the overall 2-year survival rate was 65 %. This indicates the effectiveness of early tumor control by overcoming the blood-brain barrier. The overall 2-year survival rate was signifcantly higher in both the prophylactic and therapeutic frst-line intrathecal chemotherapy groups than in the relapse group (80 % vs 20 %, p<0.05) and signifcantly exceeded the median survival time of 4–6 months reported by other authors [1]. The toxicity profle of ITCT was favorable, with no cases of severe neurotoxicity. Conclusion. Intensive intrathecal chemotherapy in the combination treatment of children with parameningeal rhabdomyosarcoma with intracranial extension and/or leptomeningeal metastasis is an effective and safe method for treating and preventing CNS tumor cell infltration. This therapy can signifcantly improve survival of patients with extremely unfavorable prognosis.
Текст научной статьи Интратекальная химиотерапия в комплексном лечении детей с рабдомиосаркомой параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием
Лептоменингеальные метастазы (ЛМ) при солидных опухолях характеризуются проникновением опухолевых клеток через гематоэнцефалический барьер оболочки головного и спинного мозга в субарахноидальное пространство, что приводит к их распространению по центральной нервной системе (ЦНС). Данное течение заболевания встречается при многих солидных опухолях. У взрослых пациентов ЛМ наиболее часто ассоциировано с раком легкого, молочной железы и меланомой, в то время как в педиатрической практике оно характерно для мелкокруглоклеточных сарком, таких как рабдомиосаркома, саркома Юинга, нейробластома, а также для ретинобластомы [1, 2].
Патогенез лептоменингеального метастазирования является многофакторным, однако выделяют несколько основных путей инвазии. Наиболее частыми считаются прямое интракраниальное распространение опухоли из смежных анатомических зон и периневральная инвазия по ходу черепных и периферических нервов [3]. Помимо этого, описываются и гематогенные пути метастазирования как через артериальное кровообращение с формированием очагов в паренхиме мозга, так и ретроградно через венозное сплетение Бейтсона [4].
Клинические проявления лептоменингеального метастазирования крайне разнообразны, что обусловлено мультифокальным характером поражения и требует высокой онкологической настороженности. Синдром поражения черепных нервов – наиболее часто вовлекаются VI, VII и VIII пары черепных нервов, что клинически проявляется диплопией, парезом мимической мускулатуры и нарушениями слуха соответственно. Синдром поражения спинного мозга и его корешков характеризуется корешковыми болями, сенсорными нарушениями, слабостью в конечностях и дисфункцией тазовых органов. Синдром внутричерепной гипертензии и менингизма возникает вследствие нарушения ликвородинамики или прямого раздражения мозговых оболочек и проявляется головной болью, тошнотой, рвотой и изменениями психического статуса [5].
Учитывая неспецифичность клинической картины и сложный анамнез онкологического пациента, дифференциальная диагностика лептоменингеального метастазирования является критически важной задачей. Дифференциальный диагноз включает широкий спектр как неинфекционных, так и инфекционных состояний. К неинфекционным причинам, имитирующим ЛМ, относятся побочные эффекты предшествующей терапии (химио- и лучевой), паранеопластические синдромы, аутоиммунные заболевания (например, нейросаркоидоз), а также токсико-метаболическая энцефалопатия. Особое внимание следует уделять инфекционным процессам, поскольку онкологические пациенты часто находятся в состоянии иммуносупрессии. В дифференциальный диагноз должны входить менингиты и энцефалиты бактериальной (туберкулез, листериоз), грибковой (Cryptococcus, Candida) и вирусной этиологии (цитомегаловирус, вирус простого герпеса, вирус Эпштейна–Барр и др.) [6].
Для выявления лептоменингеального метастазирования применяется комплексный подход, который опирается на оценку трех основных элементов: клиническую картину (стандартизированное неврологическое обследование для выявления характерных симптомов), цитологическое исследование спинномозговой жидкости и нейровизуализацию (магнитно-резонансная томография (МРТ) головного и спинного мозга с контрастным усилением для выявления характерных признаков поражения оболочек, радиоизотопное исследование головного мозга с 99mTc-пертехнетатом).
Следует отметить, что концепция профилактической ЦНС-направленной терапии при параме-нингеальной рабдомиосаркоме не является новой. В 1980-х гг. в рамках исследований IRS предпринимались попытки использования интратекальной химиотерапии и/или краниоспинального облучения. Однако данные работы показали неоднозначные результаты и не привели к статистически значимому улучшению выживаемости [7, 8]. Как следствие, рутинная профилактическая интрате-кальная или лучевая терапия не была включена в стандартные протоколы лечения детей с рабдомиосаркомой параменингеальной локализации ведущих международных групп, и вопрос о ее целесообразности оставался открытым.
Современная стратегия лечения лептоменингеального метастазирования носит мультимодальный и строго персонализированный характер. Арсенал терапевтических опций включает в себя системную терапию (химио-, таргетную, иммунотерапию), лучевую терапию, интратекальное введение препаратов, а в отдельных случаях – хирургическое вмешательство и поддерживающую терапию [9]. Конкретная тактика и комплекс методов формируются с учетом множества факторов, среди которых наиболее значимыми являются гистологический тип и молекулярный профиль опухоли, распространенность опухолевого заболевания, а также неврологический статус и общий прогноз пациента [2].
В недавнем обзоре X. Wang et al. [10] подробно описана эволюция интратекальной химиотерапии для лечения ЛМ при солидных опухолях, демонстрирующая переход от интратекального введения традиционных цитостатиков к персонализированным подходам с применением таргетной и иммунотерапии. Исторически основу интратекальной химиотерапии составляли классические цитостатики, такие как метотрексат, тиотепа и цитарабин. Несмотря на способность достигать высоких концентраций в центральной нервной системе, их применение было сопряжено с двумя важными проблемами. Во-первых, значительная нейротоксичность, особенно у метотрексата (арахноидит, миелопатия, лейкоэнцефалопатия) [11]. Во-вторых, крайне короткий период полувыведения из ликвора (3–4 ч для цитарабина и тиотепы), что требовало частых, болезненных и рискованных люмбальных пункций (2–3 раза в нед) для поддержания терапевтической концентрации [12, 13]. Попыткой решить проблему короткого периода полувыведения стало создание липосомального цитарабина, чей период полураспада (141 ч) позволил сократить частоту введений до одного раза в 2 нед [14].
Следующий этап эволюции был связан с поиском агентов, более эффективных и специфичных для солидных опухолей. Топотекан, ингибитор топоизомеразы I, зарекомендовал себя как один из наиболее эффективных и хорошо переносимых препаратов для интратекального введения, особенно в педиатрической практике [15]. Его аналог, ингибитор топоизомеразы II этопозид, также показал возможность достижения терапевтических концентраций, однако его применение ограничено более выраженной нейротоксичностью [16]. Перспективным направлением стало и применение Пеметрекседа, который после интратекального введения обеспечивает высокие и длительные (до 24 ч) концентрации в ЦСЖ при минимальной системной токсичности [17]. Во взрослой онкологической практике настоящим прорывом стало интратекальное применение таргетных и иммуноонкологических препаратов, что открыло эру персонализированной терапии ЛМ. Учитывая, что при системном введении Трастузумаба его концентрация в спинномозговой жидкости ничтожно мала, его прямое интратекальное введение стало высокоэффективной и безопасной опцией для пациентов с HER2-положительными опухолями [18]. Аналогично, интратекальное введение ингибитора PD-1 Ниволумаба показало свою безопасность и перспективность при ЛМ меланомы. Первое же клиническое исследование продемонстрировало, что комбинированное введение позволяет достичь длительного контроля над заболеванием у ранее инкурабельных пациентов [19].
На ранней экспериментальной стадии находится изучение других таргетных агентов. Доказательная база по интратекальному применению Нимотузумаба и Бевацизумаба на данный момент крайне ограничена и основана лишь на единичных клинических случаях и небольших исследованиях, что не позволяет сделать выводы об их реальной эффективности [20, 21].
Несмотря на относительно невысокую частоту встречаемости, составляющую 5–8 % у пациентов с солидными опухолями [22], ЛМ является прогностически крайне неблагоприятным событием. Развитие данного осложнения кардинально меняет терапевтическую тактику и определяет необхо- димость применения специфических лечебных подходов. Однако анализ мировой и отечественной литературы свидетельствует об отсутствии единых стандартизированных протоколов интратекальной химиотерапии (ИТХТ) при данной патологии, что особенно актуально для онкопедиатрической практики.
Целью исследования явилась оценка исходов лечения детей с параменингеальной рабдомиосаркомой с интракраниальным распространением и/ или лептоменингеальным метастазированием, получавших терапию с включением интратекальной химиотерапии.
Материал и методы
Исследование проведено на базе отделения опухолей головы и шеи НИИ детской онкологии и гематологии им. акад. Л.А. Дурнова. В исследование включен 21 пациент с морфологически верифицированным диагнозом рабдомиосаркома параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием в возрасте от 2 до 18 лет, которые наблюдались и лечились в НИИ детской онкологии и гематологии им. акад. Л.А. Дурнова ФГБУ «НМИЦ им. Н.Н. Блохина» Минздрава России, Москва, Российская Федерация (далее НИИ ДОиГ) в период с 2021 по 2024 г. Обязательным условием включения в исследование было наличие подписанного информированного согласия на участие в исследовании от законных представителей и/или самого пациента. Сбор данных проводился путем анализа первичной медицинской документации (амбулаторные карты и истории болезни).
Статистическая обработка данных выполнена в программной среде R версии 4.3.1 с использованием пакетов survival (3.8.3) и survminer (0.5.1). Оценка выживаемости проводилась методом Каплана–Мейера. Сравнение кривых выживаемости между подгруппами осуществлялось с помощью логрангового теста (log-rank test). Статистически значимыми считались различия при p<0,05.
Пациенты, выбывшие из наблюдения или завершившие исследование без наступления исследуемого исхода, обрабатывались как правосторонне цензурированные наблюдения. Анализ проводился по двум конечным точкам: общая выживаемость (Overall Survival, OS): время до смерти от любой причины; выживаемость, специфичная для рака (Cancer-Specific Survival, CSS): время до смерти, непосредственно связанной с прогрессированием рабдомиосаркомы. Медиана времени наблюдения, рассчитанная методом Reverse Kaplan–Meier, составила 29,6 мес.
Демографический анализ группы показал следующие характеристики. Возрастное распределение было смещено в сторону младшего школьного возраста: почти половина пациентов (48 %) были в возрасте от 4 до 9 лет. Отмечалось незначитель- ное преобладание детей женского пола: 12 (57 %) девочек и 9 (43 %) мальчиков.
Анализировались жалобы пациентов при первичном обращении. Следует отметить, что у одного пациента могло быть несколько жалоб одновременно. Наиболее частые жалобы: наличие пальпируемого видимого новообразования (n=20; 95 %), асимметрии лица (n=15; 71 %) и экзофтальма (n=13; 62 %). Функциональные нарушения включали затруднение носового дыхания (n=14; 66 %), а также орбитальные симптомы в виде снижения зрения (n=13; 62 %). Общие симптомы, такие как слабость, отмечались реже (n=7; 33 %). Средняя продолжительность анамнеза заболевания от появления первых симптомов до постановки диагноза составила 5 мес.
Первичная диагностика у всех пациентов включала биопсию опухоли с последующим гистологическим и иммуногистохимическим исследованиями, которые во всех случаях подтвердили диагноз рабдомиосаркомы. Наиболее распространенным гистологическим подтипом в общей когорте являлся эмбриональный, выявленный у 76 % пациентов.
Первичное обследование пациентов перед началом лечения было комплексным и включало несколько этапов. Общеклиническая оценка включала сбор анамнеза, физикальный осмотр, стандартные лабораторные исследования (общий и биохимический анализы крови, коагулограмма) и оценку функции жизненно важных органов с помощью электрокардиографии (ЭКГ) и эхокардиографии (Эхо-КГ). Оценка распространенности опухолевого процесса проводилась с использованием расширенного комплекса методов визуализации. Для оценки локального статуса всем пациентам выполнялась магнитно-резонансная томография (МРТ) основания черепа, головного и спинного мозга с контрастным усилением. Стадирование опухолевого процесса включало компьютерную томографию (КТ) органов грудной клетки, УЗИ брюшной полости и регионарных лимфоузлов, позитронно-эмиссионную томографию, совмещенную с КТ (ПЭТ/КТ) всего тела с 18F-ФДГ, и сцинтиграфию костей скелета.
Специализированная оценка лептоменингеального поражения проводилась на основании комплексной оценки данных цитологического исследования ликвора и МРТ головного и спинного мозга с контрастным усилением. Статическая сцинтиграфия головного мозга с 99mTc-пертехнетатом использовалась как дополнительный метод для выявления зон повышенной проницаемости ГЭБ и косвенных признаков ЛМ (рис. 1).
На момент первичной диагностики у большинства пациентов отмечалась высокая распространенность опухолевого процесса (рис. 2). Наиболее часто опухоль локализовалась в крылонебной ямке (n=16; 76 %) и околоносовых пазухах (n=12; 57 %). Реже вовлекались основная пазуха (n=10; 48 %),
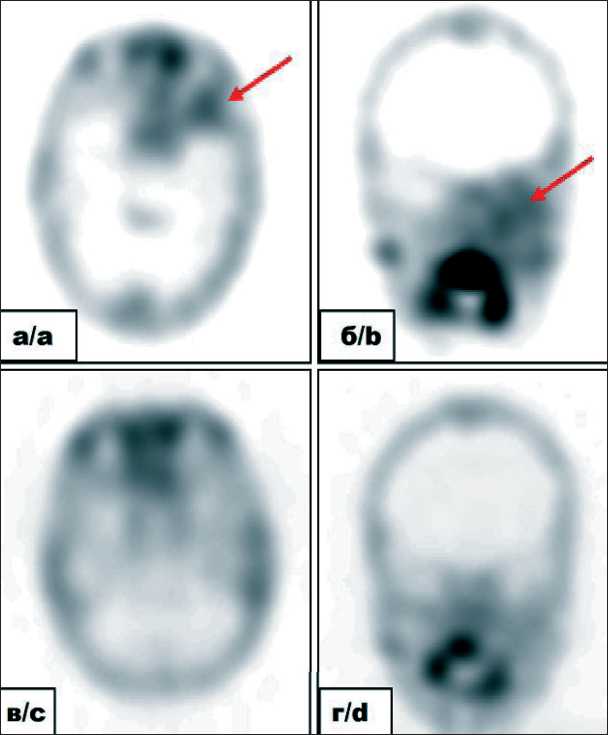
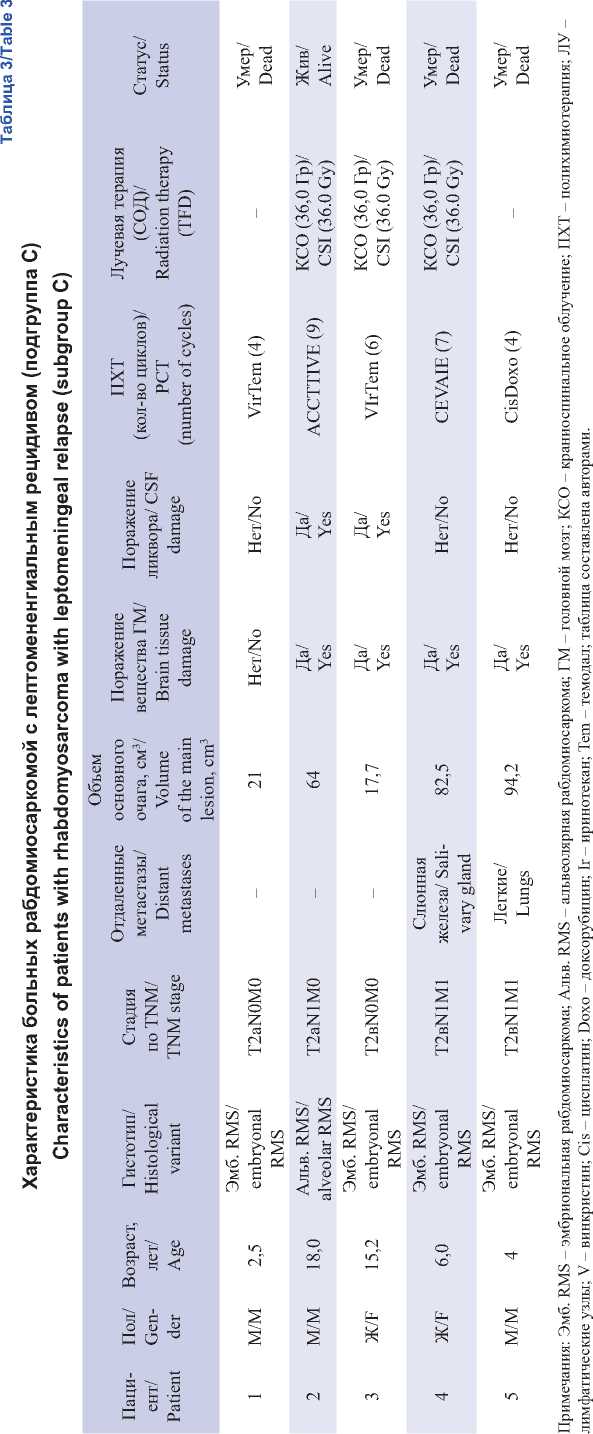
Рис. 1. Собственные результаты томосцинтиграмм головного мозга с 99mTc-пертехнетатом пациентки П. с диагнозом: Альвеолярная рабдомиосаркома параменингеальной локализации с интракраниальным распространением, лептоменингеальные метастазы в головном мозге, стадия IV (T2вN0M1.
IRS IVa). На томограммах в аксиальной (а) и фронтальной (б) проекциях до начала лечения определяется очаговоповышенное распределение РФЛП в проекции первичной опухоли параменингеально слева (общий носовой ход, верхнечелюстная пазуха, левая орбита и средняя черепная ямка) – красные стрелки. Признаки поражения «по контакту» оболочек головного мозга в области средней черепной ямки слева. При контрольном исследовании после 9 курсов химиотерапии, 6 курсов интратекальной химиотерапии, лучевой терапии в объеме краниоспинального облучения (СОД 36 Гр), на область первичного распространения опухоли
(СОД 50,4 Гр) по протоколу CWS 2014 (группа метастатических сарком): на томограммах в аксиальной (в) и фронтальной (г) проекциях определяется незначительно повышенное распределение РФЛП в проекции первичной опухоли параме-нингеально слева. По сравнению с инициальным исследованием отмечается выраженная положительная динамика.
Примечание: рисунок выполнен авторами
Fig. 1. Results of brain tomoscintigrams with 99mTc-pertechnetate of patient P. diagnosed with alveolar parameningeal rhabdomyosarcoma with intracranial extension, leptomeningeal metastases in the brain. Stage IV. T2вN0M1. IRS IVa. Tomograms in axial (a) and frontal (b) projections before starting treatment show focally increased distribution of radiopharmaceuticals in the projection of the primary tumor parameningeally on the left (common nasal meatus, maxillary sinus, left orbit and middle cranial fossa) – red arrows. There are signs of damage to the meninges by contact in the left middle cranial fossa. CT scans after 9 cycles of chemotherapy, 6 cycles of intrathecal chemotherapy, and craniospinal irradiation (total dose: 36 Gy) to the area of the primary tumor (total dose:
50.4 Gy) according to the CWS 2014 protocol (group of metastatic sarcomas) show a slightly increased distribution of the radiopharmaceuticals in the projection of the primary tumor parameningeally on the left in the axial (c) and frontal (d) projections. Compared with the initial study, a marked positive trend is observed.
Note: created by the authors
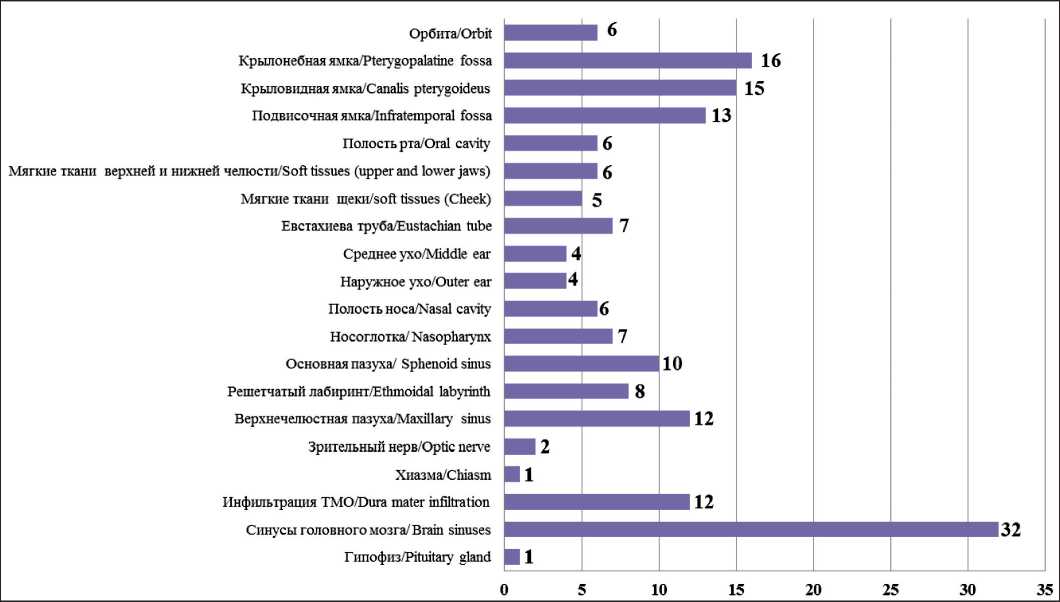
Рис. 2. Частота вовлечения различных анатомических областей в опухолевый процесс на момент постановки диагноза. Примечание: рисунок выполнен авторами
Fig. 2. Frequency of tumor metastases to different anatomical sites at the time of diagnosis. Note: created by the authors
а также полость носа и носоглотка (n=7; 33 %). Прорастание в среднюю черепную ямку было выявлено у 9 (43 %) пациентов, в переднюю и заднюю черепные ямки – у 5 пациентов в каждом случае (по 24 % соответственно). Инфильтрация твердой мозговой оболочки (ТМО) наблюдалась у 12 (57 %) пациентов, инвазия в вещество головного мозга – у 18 (86 %).
Системное метастазирование выявлено у значительной части когорты: поражение регионарных лимфатических узлов диагностировано у 13 (62 %) пациентов, отдаленные метастазы в кости и костный мозг – у 6 (29 %), лептоменингеальное метастазирование – у 13 (62 %), сочетание регионарных и отдаленных метастазов – у 10 (48 %) пациентов.
Для обеспечения безопасности и своевременной коррекции терапии проводился комплексный мониторинг состояния пациентов. Оценка общего статуса осуществлялась по шкалам ECOG-ВОЗ и Карновского. Мониторинг специфической токсичности включал регулярные консультации офтальмолога и оториноларинголога. Динамика неврологического дефицита отслеживалась с помощью стандартизированных анкет. Переносимость лечения оценивалась по данным клинического осмотра и лабораторных тестов.
В исследование включались пациенты с гистологически верифицированной рабдомиосаркомой параменингеальной локализации. В зависимости от статуса ЦНС пациенты были стратифицированы на две группы для назначения интратекальной химиотерапии.
В группу профилактической ИТХТ включались пациенты, у которых по данным МРТ головного и/или спинного мозга с внутривенным контрастированием выявлялось интракраниальное распространение опухоли, но не было признаков лептоменингеального метастазирования, согласно результатам цитологического исследования ликвора, МРТ головного и/или спинного мозга, а также статической сцинтиграфии головного мозга.
В группу терапевтической ИТХТ вошли пациенты с подтвержденным лептоменингеальным метастазированием, что устанавливалось на основании обнаружения опухолевых клеток при цитологическом исследовании ликвора и/или наличия характерного контрастного усиления мозговых оболочек по данным МРТ головного и/ или спинного мозга, а также признаков поражения оболочек, выявленных при статической сцинтиграфии головного мозга.
Критериями невключения в исследование являлись: возраст старше 18 лет, наличие тяжелой сопутствующей патологии (выраженная неврологическая, сердечно-сосудистая, печеночная, почечная или дыхательная недостаточность), а также отказ пациента (в возрасте старше 15 лет) или его законных представителей от участия.
Следует отметить, что когорта пациентов в данном исследовании была гетерогенной по времени включения и предшествующей терапии. Группа первичных больных (n=16) проспективно получала лечение согласно описанному протоколу с применением профилактической или ранней
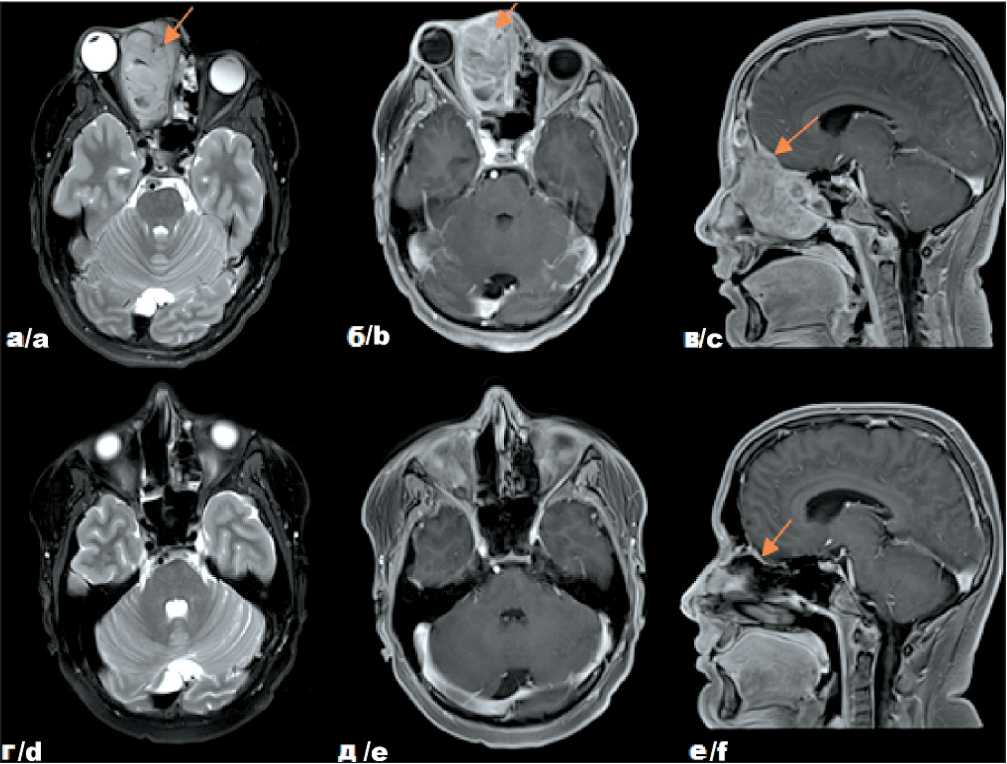
Рис. 3. Собственные результаты исследований пациента Р. с диагнозом: Альвеолярная рабдомиосаркома параменингеальной локализации с интракраниальным распространением, метастатическое поражение лимфатических узлов шеи справа, стадия III (T2bN1M0. IRS IIIа), до начала лечения – на томограммах в аксиальной (а) (б) и сагиттальной (в) проекциях и после комбинированного лечения – на томограммах в аксиальной (г) (д) и сагиттальной (е) проекциях. Примечание: рисунок выполнен авторами Fig. 3. Patient R. diagnosed with alveolar parameningeal rhabdomyosarcoma with intracranial spread, lymph node metastases on the right of the neck. Stage -III. T2bN1M0. IRS IIIa. Before starting treatment – tomograms in axial (a) (b) and sagittal (c) projections; after completing treatment – tomograms in axial (d) (e) and sagittal (f) projections. Note: created by the authors
терапевтической ИТХТ. Группа пациентов с рецидивом ЛМ (n=5) состояла из пациентов, которые получали первичное лечение без ИТХТ (в рамках стандартной терапии до 2021 г.) и были включены в анализ уже на этапе развития рецидива.
Подгруппа А (n=8) включала пациентов без исходного лептоменингеального метастазирования (табл. 1). Данная подгруппа была гетерогенной по своим клиническим характеристикам, но состояла исключительно из пациентов с высоким и очень высоким риском прогрессирования. В нее вошли: 4 пациента с IIIа стадией по классификации IRS (с наличием или отсутствием метастазов в регионарных лимфоузлах), один пациент с альвеолярной рабдомиосаркомой и метастазами в лимфоузлах (N1), а также 3 пациента с отдаленными метастазами в легких и костях/костном мозге (IV стадия).
Все пациенты в данной подгруппе получали риск-адаптированную терапию в соответствии с их прогностической группой, согласно протоколу CWS 2014. Пациентам группы высокого риска (n=4) проведено 9 курсов химиотерапии по схеме I2VA (ифосфамид 3 000 мг/м2/сут в 1–2-й дни каждого курса лечения, винкристин 1,5 мг/м2 в 1-й день каждого курса, дактиномицин 1,5 мг/м2 в 1-й день каждого курса), лучевая терапия на область первичной опухоли (СОД 50,4 Гр) и на регионарные лимфоузлы шеи (СОД 45,0 Гр). Поддерживающая терапия не проводилась. Пациент из группы очень высокого риска (рис. 3) получил 9 курсов химиотерапии в альтернирующем режиме, включающем схемы I2VA и I2VAd (ифосфамид 3 000 мг/м2/сут в 1-й и 2-й дни каждого курса лечения, винкристин 1,5 мг/м2 в 1-й день каждого курса, адриамицин 40 мг/м2/сут в 1–2-й дни курса), лучевая терапия аналогична группе высокого риска (СОД 50,4 Гр на первичный очаг, 45,0 Гр на лимфоузлы). После завершения интенсивной фазы лечения пациенты получали 6-месячную поддерживающую терапию. Пациентам группы первично-метастатических сарком (n=3) проведено 9 курсов химиотерапии в альтернирующем режиме, включающем три схемы: I3VA (ифосфамид 3 000 мг/м2/сут в 1–3-й дни каждого курса лечения, винкристин 1,5 мг/м2 в 1-й день каждого курса, дактиномицин 1,5 мг/м2 в 1-й день каждого курса), I3VЕ (ифосфамид 3 000 мг/м2/сут в 1–3-й дни каждого курса лечения, винкристин 1,5 мг/м2 в 1-й день каждого курса, этопозид 150 мг/м2 в 1–3-й дни каждого курса лечения) и CEV (карбоплатин 500 мг/м2 в 1-й день курса, эпирубицин 150 мг/м2 в 1-й день курса, винкристин 1,5 мг/м2 в 1-й день курса), лучевая терапия проводилась на первичный опухолевый очаг (СОД 50,4 Гр) и регионарные лимфоузлы (СОД 45,0 Гр). Трем пациентам с метастазами в костях дополнительно проводилось облучение метастатических очагов в СОД 41,4 Гр. Поддерживающая терапия проводилась согласно протоколу.
Таблица 1/table 1
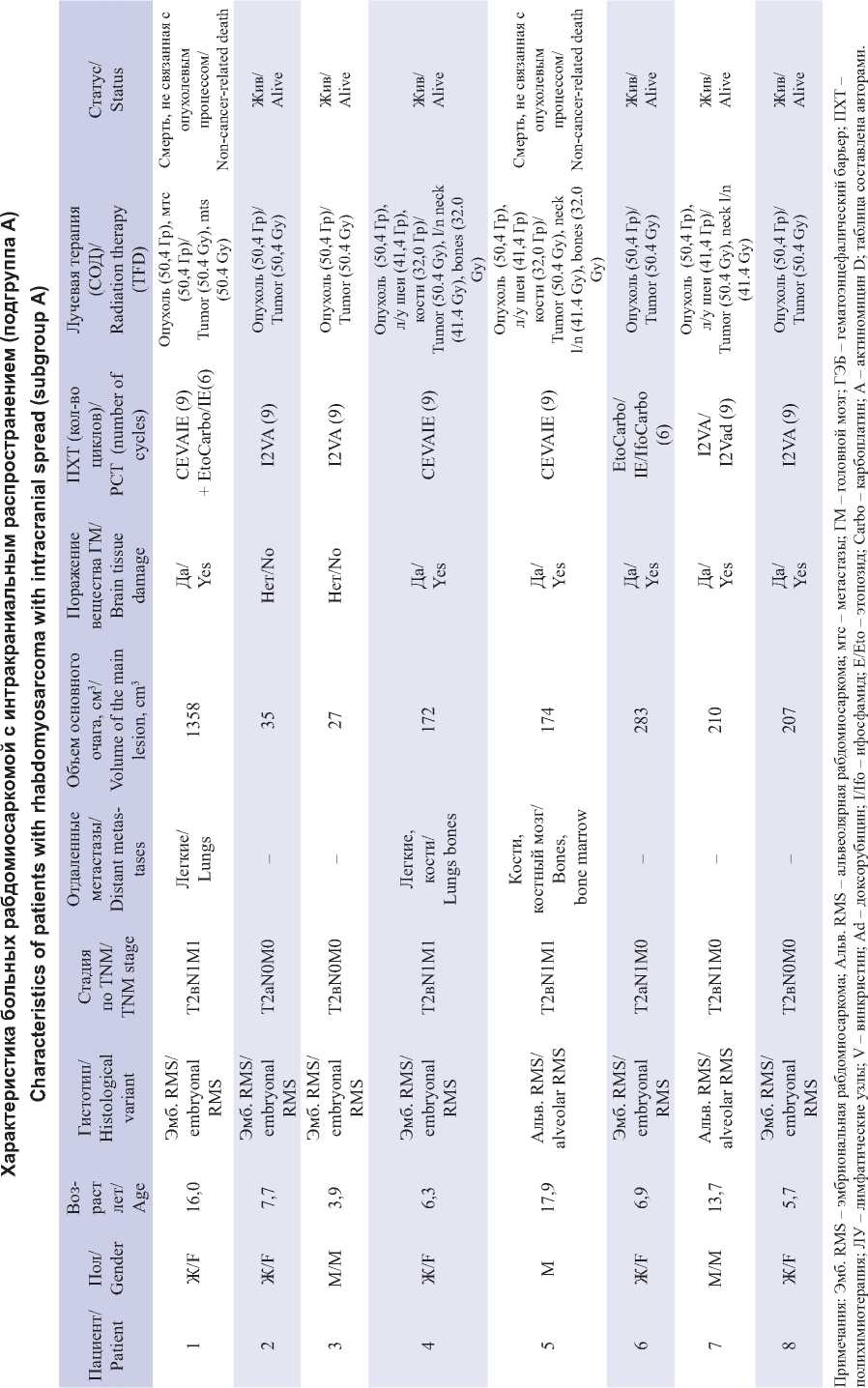
Notes: Emb. RMS – embryonal rhabdomyosarcoma; Alv. RMS – alveolar rhabdomyosarcoma; mts – metastases; B – brain, BBB – blood-brain barrier; PCT – polychemotherapy; LN – lymph nodes; V – vincristine; Ad – doxorubicin; I/Ifo – ifosfamide; E/Eto – etoposide; Carbo – carboplatin; A – actinomycin D; created by the authors.
Пациентам данной подгруппы с целью профилактики лептоменингеального метастазирования проводилось 8 курсов интратекальной химиотерапии: индукционный этап (до лучевой терапии) – 4 курса ИТХТ в 1-й день каждого курса (метотрексат и преднизолон в возрастных дозировках) и консолидирующий этап (после лучевой терапии) – 4 курса в 1-й день каждого курса (топотекан в дозе 0,2 мг/м2). Каждое интратекальное введение сопровождалось обязательным предварительным цитологическим исследованием ликвора для мониторинга статуса ЦНС. После завершения интенсивной фазы лечения пациенты получали поддерживающую терапию в течение 6 мес, состоящую из перорального приема винорельбина (25 мг/м2 в 1, 8, 15-й дни) и ежедневного приема циклофосфамида (25 мг/м2).
Единственным зарегистрированным нежелательным явлением, связанным с процедурой ин-тратекального введения препаратов, был легкий постпункционный синдром у 1 (12 %) пациента, который был успешно купирован ненаркотическими анальгетиками.
У одного пациента после завершения терапии был диагностирован метастатический рецидив с поражением костей и костного мозга. Проведение двух курсов противорецидивной химиотерапии оказалось неэффективным, и пациент скончался. По данным контрольной МРТ головного и спинного мозга признаков лептоменингеального поражения не выявлено. Также отмечен один летальный исход вследствие интеркуррентного заболевания, наступивший через 9 мес после завершения терапии; при этом на момент смерти у пациента сохранялась стойкая полная ремиссия основного заболевания.
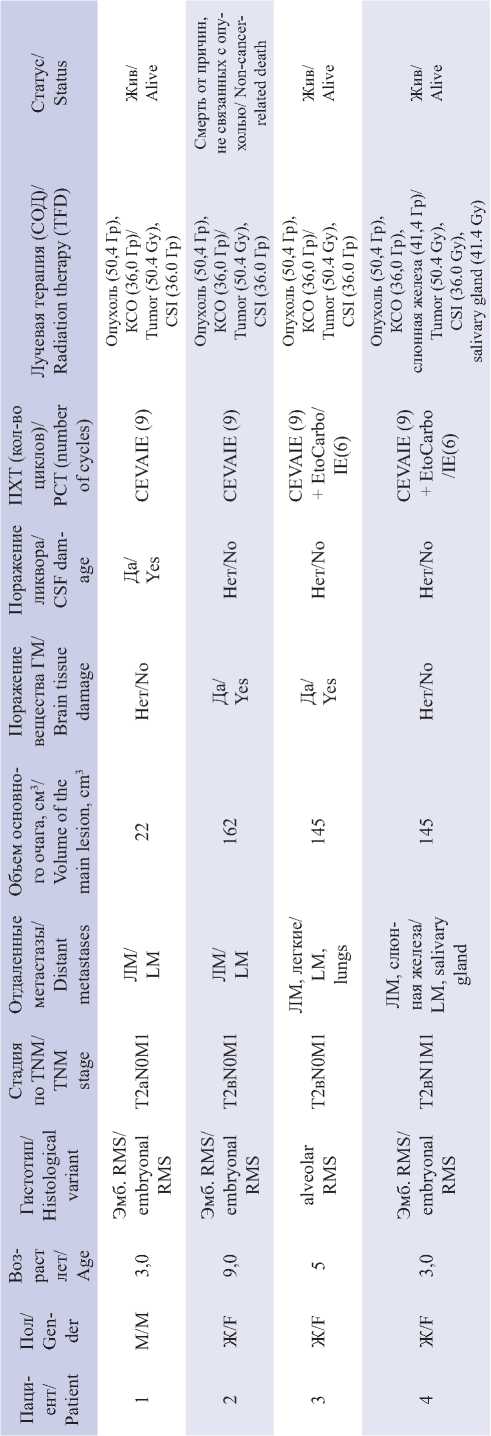
Подгруппу B (n=8) составили пациенты с инициальным лептоменингеальным метастазированием (табл. 2), выявленным при первичной диагностике.
Диагностика лептоменингеального метастазирования (ЛМ) основывалась на комплексном подходе. Прямое подтверждение диссеминации было получено у 2 (25 %) из 8 пациентов на основании цитологического исследования ликвора. В качестве дополнительного метода, кроме МРТ основания черепа, головного и спинного мозга с контрастным усилением, использовалась статическая сцинтиграфия оболочек головного мозга с 99mTc-пертехнетатом, которая выявила нарушение проницаемости гематоэнцефалического барьера как косвенный признак поражения ЦНС у 6 (75 %) из 8 пациентов.
Пациенты данной подгруппы получали интенсивную комбинированную терапию, включающую системную, интратекальную, лучевую и поддерживающую терапию (рис. 4). Проведено 9 курсов химиотерапии в альтернирующем режиме, включающем три схемы: I3VA, CEV и I3VЕ. Ин- тратекальная химиотерапия проводилась по терапевтической схеме и включала введение препаратов метотрексат, преднизолон в возрастных дозировках в 1-й и 8-й дни каждого курса. После лучевой терапии пациенты переводились на консолидирующую интратекальную химиотерапию – 4 курса с интратекальным введением топотекана (0,2 мг/м2 в 1-й день каждого курса). Каждое интратекаль-ное введение сопровождалось цитологическим исследованием ликвора для мониторинга ответа. Лучевая терапия включала облучение нескольких зон: первичный опухолевый очаг (СОД 50,4 Гр), краниоспинальная область (СОД 36,0 Гр) – для контроля лептоменингеального метастазирования, регионарные лимфоузлы шеи (СОД 45,0 Гр) – у 5 (63 %) пациентов, на метастатически пораженные кости (СОД 41,4Гр) – у 1 (12 %) пациента. После завершения интенсивной фазы проводилась 12месячная поддерживающая терапия.
Один (5 %) пациент был исключен из исследования в связи с отказом от дальнейшего лечения и наблюдения. Два (25 %) летальных исхода были обусловлены не прогрессированием опухоли, а инфекционными осложнениями интенсивной химиотерапии (молниеносный сепсис, вызванный Pseudomonas aeruginosa на фоне длительной аплазии кроветворения) у пациентов с рабдомиосаркомой параменингеальной локализации с интракраниальным распространением и лептоменингеальным метастазированием, отдаленными метастазами в костях. При этом непосредственно интратекальная терапия переносилась хорошо.
Профиль токсичности был благоприятным. Единственным зарегистрированным нежелательным явлением стал постпункционный синдром I степени по шкале CTCAE у 1 (12 %) пациента. Клинически он проявлялся головной болью и был полностью купирован приемом ненаркотических анальгетиков.
Подгруппу C (n=5) составили пациенты, у которых лептоменингеальное метастазирование развилось во время рецидива заболевания (табл. 3). Лечение в данной подгруппе носило персонализированный характер и основывалось на применении различных противорецидивных протоколов, которые, однако, имели общие принципы: интенсивную системную и интратекальную химиотерапию. Один пациент получил 4 цикла многокомпонентной химиотерапии на основе карбоплатина в дозе 150 мг/м2 – c 1-го по 4-й день цикла и этопозида – 150 мг/м2 – c 1-го по 4-й день цикла; ифосфамида в дозе 2000 мг/м2– c 1-го по 4-й день цикла и этопозида – 150 мг/м2 –c 1-го по 4-й день цикла; карбоплатина в дозе 150 мг/м2 – c 1-го по 4-й день цикла и ифосфамида в дозе 2000 мг/м2 – с 1-го по 4-й день цикла. Двое пациентов получили 4 курса по схеме, включающей винкристин в дозе 1 мг/м2 в 1, 8 и 15-й день курса, иринотекан в дозе 50 мг/м2 в 1–5-й дни курса, темозоломид 150 мг/м2 – c 1-го по 5-й день
Таблица 2/table 2
Характеристика больных рабдомиосаркомой с интракраниальным распространением с инициальным ЛМ (подгруппа В) Characteristics of patients with rhabdomyosarcoma with intracranial spread and initial lM (subgroup B)
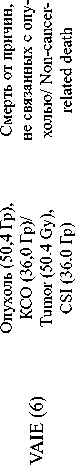

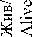
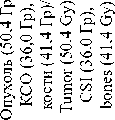
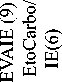
и +
Окончание таблицы 2/end of table 2

о м
ч
X c
о
S
о
s к
I s
га
о
и s
ад ra
S га р. о С
^ U га
S'
.3 га ffl
ад га 8 га
о
м к о о
Q
^ ю о
и
О
w s ч ra
ra ra T О
Q
о о а о
Й о
га
(Й
Q
га и га
S
ад ra
О c

м
О
ад
га о
Рч Ч

Notes: Emb. RMS – embryonal rhabdomyosarcoma; Alv. RMS – alveolar rhabdomyosarcoma; BM – brain; CSI – craniospinal irradiation; PCT – polychemotherapy; LN – lymph nodes; V – vincristine; Cis – cisplatin; Doxo – doxorubicin; Ir – irinotecan; Tem – temodal; created by the authors.
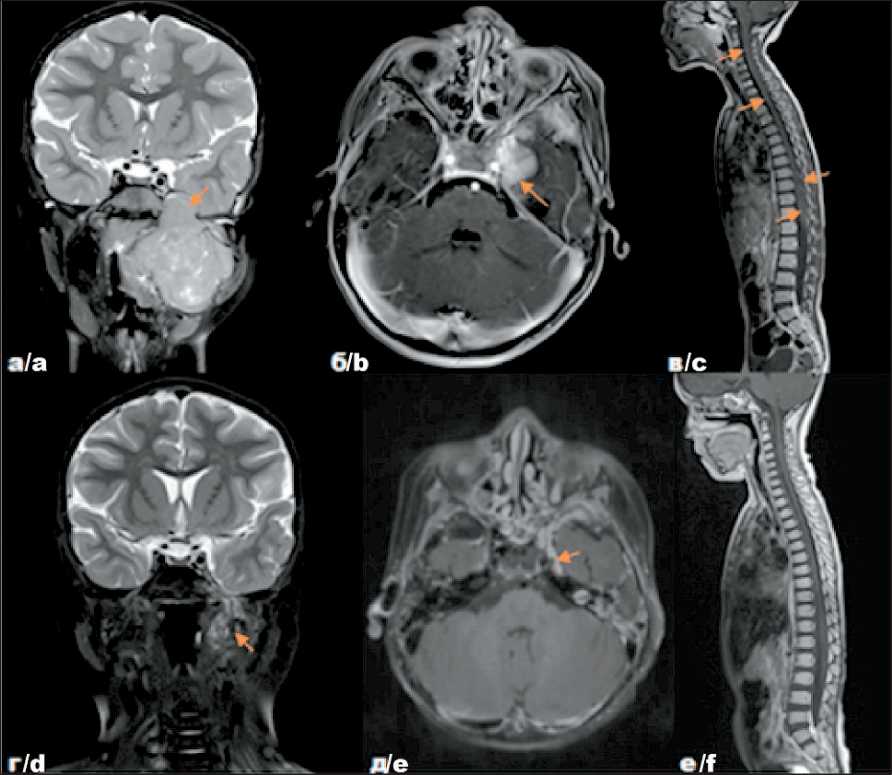
Рис. 4. Собственные результаты исследований пациентки П. с диагнозом: Эмбриональная рабдомиосаркома параменингеаль-ной локализации с интракраниальным распространением, метастатическое поражение лимфатических узлов, лептоменингеальные метастазы в спинном мозге, стадия IV (T2вN1M1. IRS IVa) до лечения – на томограммах во фронтальной (а), аксиальной (б) и сагиттальной (в) проекциях и после комбинированного лечения – на томограммах во фронтальной (г), аксиальной (д) и сагиттальной (е) проекциях. Примечание: рисунок выполнен авторами
Fig. 4. Patient P. diagnosed with embryonal parameningeal rhabdomyosarcoma with intracranial spread, lymph node metastases, leptomeningeal metastases of the spine. Stage IV. T2вN1M1. IRS IVa. Before starting treatment – tomograms in frontal (a), axial (b) and sagittal (c) projections; after completing treatment – tomograms in frontal (d), axial (e) and sagittal (f) projections. Note: created by the authors
цикла. Один пациент получил 4 курса комбинации на основе цисплатина в дозе 100 мг/м2 в 1-й день цикла, доксорубицина в дозе 20 мг/м2 во 2-й и 3-й дни цикла. Один пациент получил наиболее интенсивное лечение, состоявшее из 9 курсов по альтернирующей схеме ACCTTIVE (винкристин 1,5 мг/м2 в 1-й день курса, циклофосфамид 1 200 мг/м2 в 1-й день курса, доксорубицин 20 мг/м2 – с 1-го по 3-й день курса/топотекан 1 мг/м2 – с 1-го по 4-й день курса; карбоплатин 150 мг/м2 – с 1-го по 4 день цикла/карбоплатин 150 мг/м2 – с 1-го по 4-й день цикла; этопозид 150 мг/м2 – с 1-го по 4-й день цикла), далее после интенсивной фазы получал 8 курсов пероральной поддерживающей терапии (трофос-фамид, идарубицин, этопозид). Интратекальную химиотерапию в терапевтическом режиме получали все пациенты, интенсивность варьировалась от 4 до 8 курсов, включая индукционный (метотрексат/ преднизолон в возрастных дозировках в 1-й и 8-й дни каждого курса) и консолидирующий (топоте-кан из расчета 0,2 мг/м2 в 1-й день каждого курса химиотерапии) этапы. Лучевая терапия проведена 3 (60 %) пациентам на краниоспинальную область в СОД 36,0 Гр.
У 4 (80 %) пациентов отмечалась первичная рефрактерность к лечению, терапия закончилась летальным исходом от прогрессирования основного заболевания. У одного из них на фоне терапии зафиксировано дальнейшее прогрессирование в виде появления метастаза в гипофизе, у другого – усиление пиарахноидального контрастирования по данным МРТ головного мозга с внутривенным контрастированием (рис. 5). У одного пациента, достигшего временного ответа, развился повторный лептоменингеальный рецидив всего через 4 мес после окончания терапии. У еще одного пациента зафиксирован диссоциированный ответ на терапию – на фоне четвертого курса противорецидивного лечения, несмотря на достижение полного ответа со стороны лептоменингеальных метастазов, было отмечено прогрессирование в виде продолженного роста интракраниального солидного компонента опухоли. Данный случай повторного прогрессирования привел к летальному исходу через 2 мес.
Обсуждение
Полученная нами частота ЛМ в дебюте заболевания (38 %) значительно превышает данные, пред-
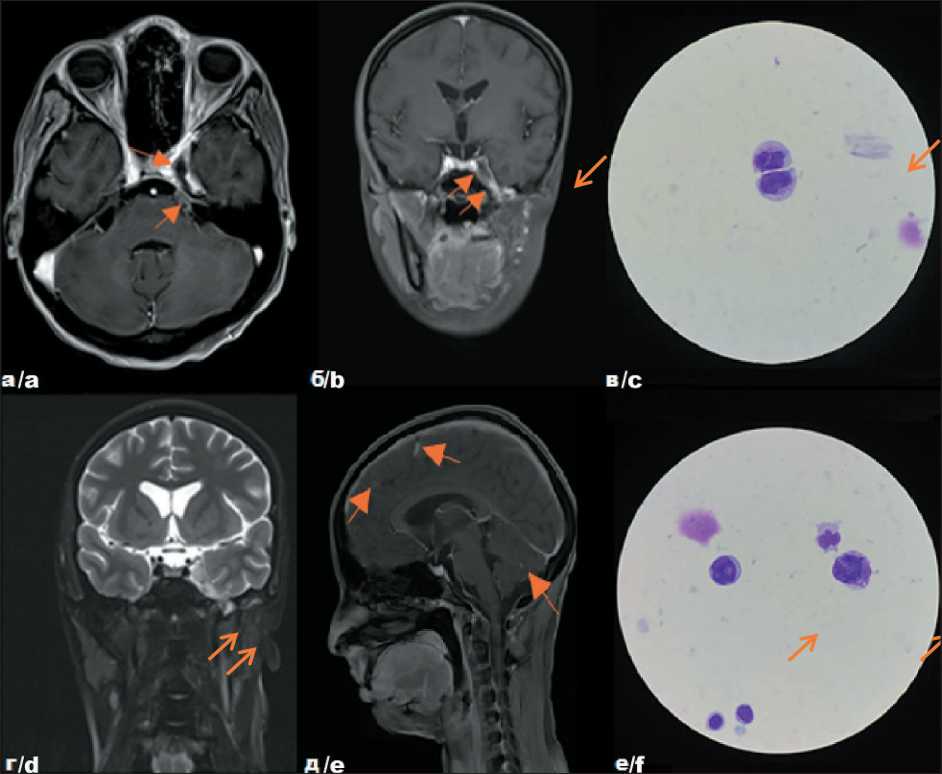
Рис. 5. Собственные результаты исследований пациентки Т. с диагнозом: Эмбриональная рабдомиосаркома параменингеаль-ной локализации с интракраниальным распространением, стадия Т2bN0M0 IRSIII. Рецидив I, до начала противорецидивного лечения – на томограммах в аксиальной (а), фронтальной (б) проекциях и после комбинированного лечения – на томограммах во фронтальной (г) и сагиттальной (д) проекциях, цитологическая картина (в) (е) спинномозговой жидкости.
Примечание: рисунок выполнен авторами
Fig. 5. Patient T. diagnosed with embryonal parameningeal rhabdomyosarcoma with intracranial spread. Stage – T2bN0M0 IRSIII. Relapse I. Before starting anti-relapse treatment – tomograms in axial (a), frontal (b) projections; after treatment –tomograms in frontal (d) and sagittal (e) projections, cytological picture (c) (f) of cerebrospinal fluid. Note: created by the authors
ставленные в большинстве исследований, где этот показатель, как правило, не превышает 10–15 % [23]. Мы связываем это, в первую очередь, с учетом критериев отбора пациентов для нашего исследования. В отличие от работ, анализирующих общую популяцию с параменингеальной рабдомиосаркомой, наша когорта состояла исключительно из пациентов группы наиболее высокого риска, с уже доказанным интракраниальным распространением опухоли и/или лептоменингеальным метастазированием. Именно интракраниальное распространение является ключевым предиктором диссеминации по оболочкам головного мозга. Таким образом, наши данные отражают истинную частоту ЛМ в этой, наиболее прогностически неблагоприятной, подгруппе пациентов.
Наше исследование убедительно доказывает, что ключевым фактором, определяющим исход у детей с параменингеальной рабдомиосаркомой с интракраниальным распространением и лептоменингеальным метастазированием, является своевременность и адекватность интратекальной химиотерапии в составе комплексной терапии. Основываясь на этом, мы предлагаем четкую стратификацию пациентов для назначения двух типов интратекального лечения: профилактическая интратекальная химиотерапия (пИТХТ) показана пациентам с высоким риском диссеминации, а именно, при наличии интракраниального распространения опухоли, доказанного МРТ головного и спинного мозга с внутривенным контрастированием, но при отсутствии опухолевых клеток в ликворе; терапевтическая интратекальная химиотерапия (тИТХТ) показана при уже состоявшемся поражении ЦНС, верифицированном цитологически (опухолевые клетки в ликворе) и/или радиологически (признаки ЛМ на МРТ головного и спинного мозга с внутривенным контрастированием или сцинтиграфии головного мозга с 99mTc-пертехнетатом).
Эффективность такого подхода подтверждается результатами выживаемости (рис. 6). Проведение профилактической интратекальной химиотерапии ассоциировано с высокими показателями 2-летней общей выживаемости, достигающими 87 % при медиане наблюдения 31,6 мес. Аналогично, применение интратекальной химиотерапии в качестве терапии I линии также демонстрирует благоприятные результаты: 2-летняя общая выживаемость – 85 % при медиане наблюдения 23,5 мес. Полученные данные свидетельствуют о высокой эффективности обоих подходов в лечении данной категории пациентов. Подгруппа с развитием
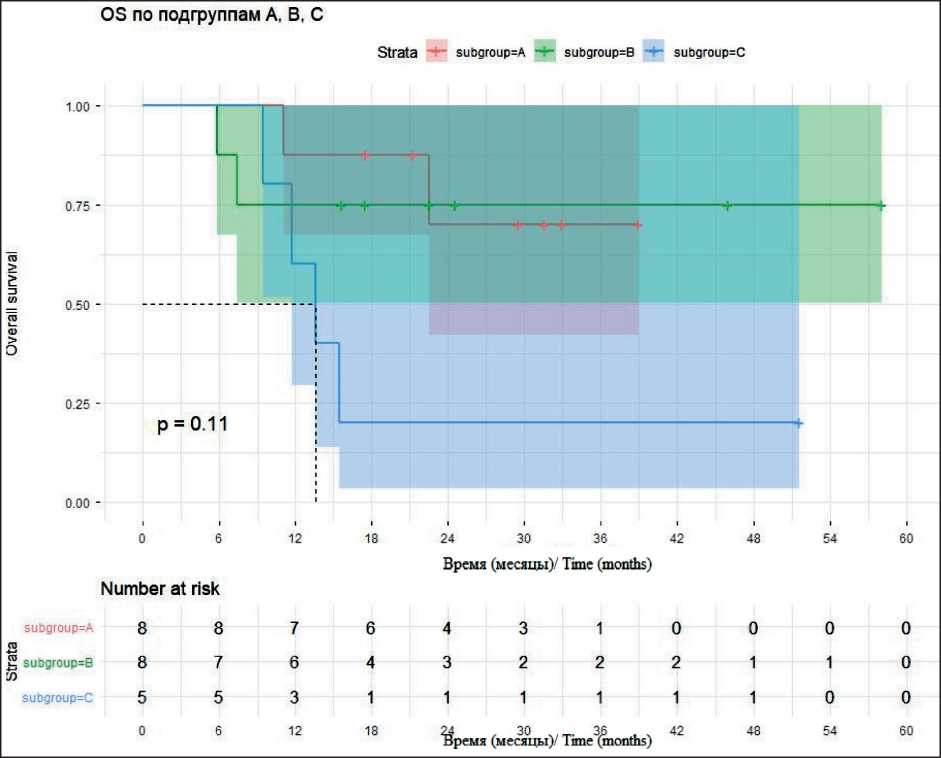
Рис. 6. Показатели общей 2-летней выживаемости пациентов с рабдомиосаркомой параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием в зависимости от статуса ЦНС.
Примечание: рисунок выполнен авторами
Fig. 6. Overall 2-year survival rates in patients with parameningeal rhabdomyosarcoma with intracranial spread and/or leptomeningeal metastasis depending on the status of the central nervous system. Note: created by the authors
лептоменигиального рецидива характеризовалась значимо худшими показателями выживаемости (из 5 пациентов в этой группе зарегистрировано 4 летальных исхода), 2-летняя ОВ – 20 % (p<0,05). Медиана наблюдения составила 51,5 мес. Только один пациент остался жив к моменту завершения наблюдения.
Логранговый тест выявил значимые различия в специфичной выживаемости между подгруппами (χ2=7,3; df=2; p=0,03). Основной вклад в различия вносит подгруппа C, демонстрирующая худшие исходы. При анализе общей выживаемости значимых различий между подгруппами не выявлено (p=0,1).
Увеличенная медиана наблюдения (29,6 мес) повышает достоверность оценок выживаемости на сроках до 24 мес. Выявлено значимое различие в специфичной для рака выживаемости между подгруппами. Подгруппа C характеризуется агрессивным течением заболевания: 4 из 5 пациентов умерли от прогрессирования в течение 18 мес, а 18-месячная CSS составила лишь 20 %. Подгруппы A и B демонстрируют высокие и сопоставимые показатели долгосрочной выживаемости (CSS на уровне 85–88 % к 24 мес), что свидетельствует об эффективности примененной терапевтической стратегии для данных категорий пациентов. На- личие случаев смерти от других причин (9,5 % когорты) объясняет расхождение между показателями OS и CSS, подчеркивая важность анализа обеих конечных точек.
Резкий контраст в исходах между группой раннего/профилактического лечения и группой рецидива ЛМ является ключевым результатом нашей работы. Плохой прогноз у пациентов с рецидивом, к сожалению, соответствует мировым данным и подтверждает фатальный характер уже развившегося, массивного лептоменингеального канцероматоза. Однако именно этот факт доказывает правильность нашей стратегии предотвращения. Полученные данные могут указывать на различия в эффективности терапевтических подходов, однако для подтверждения этих выводов требуется большее количество наблюдений.
Ключевой вопрос, который возникает при анализе наших положительных результатов, – почему они столь разительно отличаются от данных исторических исследований 1980–1990-х гг. [7], в которых интратекальная терапия не показала своей эффективности. Мы полагаем, что ответ кроется в кардинальной эволюции всего комплекса лечебно-диагностических подходов за последние десятилетия. Во-первых, изменились возможности диагностики и, как следствие, точность стратифика-
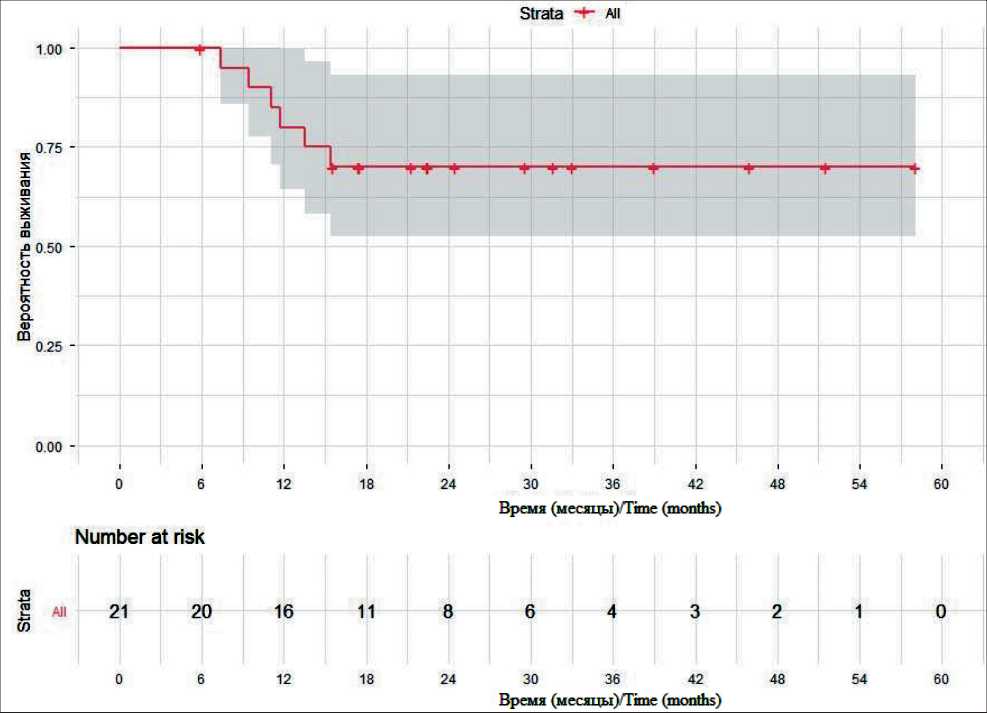
Рис. 7. Показатели общей 2-летней выживаемости пациентов с рабдомиосаркомой параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием. Примечание: рисунок выполнен авторами Fig. 7. Overall 2-year survival rates in patients with parameningeal rhabdomyosarcoma with intracranial extension and/or leptomeningeal metastasis. Note: created by the authors
ции. В эпоху КТ было сложно достоверно оценить минимальное интракраниальное распространение. Современная МРТ-диагностика позволяет нам с высокой точностью выделять именно ту когорту пациентов, которая имеет максимальный риск развития ЛМ, и применять превентивные меры с учетом факторов риска. Во-вторых, интенсивность и эффективность системной химиотерапии несравнимо возросли. Современные многокомпонентные протоколы обеспечивают лучший системный контроль над заболеванием, что может быть критически важным для успеха локальной интратекальной терапии. Наконец, в-третьих, современные технологии лучевой терапии обеспечивают превосходный локальный контроль над опухолью у основания черепа, тем самым устраняя источник дальнейшей диссеминации. Кроме того, при включении в протокол краниоспинального облучения достигается надежный контроль над всеми отделами центральной нервной системы.
Одной из главных клинических проблем при лечении параменингеальной рабдомиосаркомы у детей является тяжелый лучевой мукозит, неизбежно развивающийся на фоне химиолучевой терапии [24]. На этом фоне было критически важно оценить, не вносит ли интенсивная интратекальная химиотерапия дополнительный, неприемлемый вклад в общую токсичность. В нашей когорте первичных больных частота летальных исходов, не связанных с прогрессированием, составила 18,8 % (3 из 16), важно подчеркнуть, что ни один из этих случаев не был напрямую связан с нейротоксичностью или осложнениями интратекальной терапии. Мы связываем этот факт с высокой интенсивностью всего комплекса лечения, требуемого для пациентов с IV стадией заболевания, которые получали агрессивную многокомпонентную системную химиотерапию и лучевую терапию на большие объемы, что неизбежно приводит к глубокой и длительной миелосупрессии и высокому риску жизнеугрожающих инфекций. Таким образом, высокая токсическая смертность является отражением общей тяжести этой уникальной когорты пациентов, а не специфическим осложнением ИТХТ.
Наше исследование показало, что предложенный протокол интратекальной терапии обладает благоприятным профилем безопасности. Единственным зарегистрированным нежелательным явлением, непосредственно связанным с процедурой, был постпункционный синдром (головная боль I степени тяжести) у 2 (9 %) пациентов, который полностью купирован приемом ненаркотических анальгетиков. Тяжелой или необратимой нейротоксичности не зафиксировано.
Таким образом, мы считаем, что успех нашего подхода заключается не просто в факте применения интратекальной терапии, а в ее интеграции в современную, высокоинтенсивную мультимодальную терапевтическую парадигму, нацеленную на точно отобранную группу пациентов. Общая 2-летняя выживаемость данной группы пациентов составила 65 % (рис. 7).
Заключение
Полученные данные убедительно демонстрируют, что включение интенсивной интратекальной химиотерапии в протоколы лечения кардинально меняет прогноз для детей с параменингеальной рабдомиосаркомой и поражением ЦНС. Достижение общей 2-летней выживаемости на уровне 65 % в этой, исторически считавшейся инкурабель-ной, группе пациентов является значительным клиническим прорывом. Ключевым фактором успеха является способность ИТХТ обеспечивать эффективную санацию ЦНС, что было достигнуто у подавляющего большинства наших пациентов.


