Интравитреальное введение ингибиторов ангиогенеза как этап щадящей витреоретинальной хирургии пролиферативной диабетической ретинопатии
Автор: Шишкин М.М., Юлдашева Н.М.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.6, 2011 года.
Бесплатный доступ
Цель исследования: оценить эффективность интравитреального введения ингибитора ангиогенеза Луцентиса как подготовительного этапа щадящей витреоретинальной хирургии при далекозашедшей ПДР. Материал и методы: Под нашим наблюдением находился 41 пациент (63 глаза) с далекозашедшей ПДР. I группа (п=27) - витрэктомия по методике щадящей витреоретинальной хирургии, группа II (п=36) - щадящая ВРХ с предварительным интравитреальным введением Луцентиса (2,3 мг). Группы наблюдения были идентичны по возрасту, полу, уровню зрительных функций и длительности основного заболевания. Результаты. Наблюдение за состоянием глаз пациентов II группы ни в одном случае не выявило осложнений, характерных для интравитреальных инъекций. Необходимость применения интраокулярной диатермии в ходе ВРХ в I группе - в 22,2%, во II группе - в 8,3% наблюдений. Газовоздушная тампонада во II группе - в 58,3%, в Iгруппе силиконовая тампонада - в 66,7%. Время оперативного пособия у пациентов II группы до 97,4±11,6 минут, у пациентов I группы - 118,3±15,3 минут. Острота зрения через 2 месяца у 58,3% больных II группы - 0,17±0,12, в I группе в 33,3% случаев - 0,09±0,021 (р=0,0087). Заключение. Предварительное введение ингибиторов ангиогенеза позволяет добиться лучших анатомических и функциональных результатов при ВРХ далекозашедшей ПДР и может рассматриваться как подготовительный этап щадящей витреоретинальной хирургии.
Ингибитор ангиогенеза, диабетическая ретинопатия
Короткий адрес: https://sciup.org/140187911
IDR: 140187911 | УДК: 617.735-002:616.379-008.64-089
Intravitreal injection of angiogenesis inhibitors as a stage of sparing vitreoretinal surgery of proliferative diabetic retinopathy
Purpose: To evaluate the effect of intravitreal injection of Lucentis (IVL) on diabetic vitrectomy and on the postoperative course. Methods: 41 patients (63 eyes) undergoing diabetic vitrectomy were distributed to sparing vitrectomy (group I) or vitrectomy with preoperative IVL (group II). Lucentis was injected 2 to 4 days before surgery. Patients of both groups were matched as much as possible according to surgical indication and preoperative visual acuity. Main outcome measures were the feasibility of surgery and the postoperative complications. Feasibility of surgery was evaluated through recording surgical time, intraoperative bleeding, use of endodiathermy, use of silicone oil tamponade. Results: Follow up ranged between 5 and 6 months. There was significant reduction of mean surgical time, bleeding frequency, and diathermy use in group II compared to group I. Gas or air was used in 83,3% of patients in group II while silicone oil represented 66,7% of group I. Postoperative visual acuity improvement was highly significant in both groups. Postoperative bleeding was reported in 22,2% of cases in group I and in 5,6% in group II. In group II, no complications related to Lucentis injection or progression of traction were reported during the preoperative period. Conclusion: Preoperative IVL was helpful in achieving the surgical and anatomical goals by reducing the time of surgery, the intraoperative and postoperative bleeding, and the use of silicone oil with subsequent reduction of second surgery.
Текст научной статьи Интравитреальное введение ингибиторов ангиогенеза как этап щадящей витреоретинальной хирургии пролиферативной диабетической ретинопатии
В настоящее время диабетическая ретинопатия является ведущей причиной необратимой слепоты среди трудоспособного населения развитых стран мира. Потеря зрения при ее далекозашедшей пролиферативной стадии обусловлена нарушением целостности гематоретиналь-ного барьера с формированием фиброваскулярной ткани и нарастанием тракционных воздействий на сетчатку и зрительный нерв [10, 15, 17, 23, 25]. Витреоретинальная хирургия - патогенетически обоснованный метод лечения далекозашедшей пролиферативной диабетической ретинопатии (ПДР). Главной целью витреоретинальной хирургии (ВРХ) пролиферативной диабетической ретинопатии до недавнего времени принято было считать полное удаление измененного стекловидного тела (СТ) и пролиферативной ткани, интимно сращенной с поверхностью сетчатки, для предотвращения рецидива пролиферации. Однако, при таком радикальном подходе практически были неизбежны ятрогенные разрывы сетчатки и интраоперационные кровотечения [1, 24]. Необходимость устранения названных осложнений обуславливает увеличение объема оперативного пособия [3], применения таких высокоэнергетических методов как диатермия, эндолазеркоагуляция, что в итоге усугубляет существующие нарушения метаболизма интраокулярных структур. Разработка и внедрение методов щадящей витреоретинальной хирургии при лечении пациентов с тяжелыми формами ПДР значительно снижают частоту таких осложнений, но не позволяют полностью предотвратить опасность интраоперационных кровотечений [3].
Современные представления о патогенезе диабетической ретинопатии (ДР) обогатились новым пониманием роли сосудистого эндотелиального фактора роста (VEGF) [12, 13], ответственного и за патологическую проницаемость сосудов, и за патологический ангиогенез в сетчатке [13, 23, 27]. Синтез и внедрение в клиническую практику антител к VEGF, способных временно блокировать его действие, стало революционным открытием в лечении ПДР. Это дало толчок к развитию новых взглядов на возможность применения ингибиторов ангиогенеза в лечении данной патологии [23]. Наиболее широко данный препарат применяют при диабетическом макулярном отеке, где его действие направлено на уменьшение повышенной проницаемости сосудов [6, 14, 16]. В доступной специализированной литературе часто ссылаются на применение ингибиторов ангиогенеза как дополнительного фармакологического метода при лазеркоагуляции сетчатки при диабетической ретинопатии [5, 11, 28]. Парал-

Шишкин М.М., Юлдашева Н.М.
ИНТРАВИТРЕАЛЬНОЕ ВВЕДЕНИЕ ИНГИБИТОРОВ АНГИОГЕНЕЗА КАК ЭТАП ЩАДЯЩЕЙ ВИТРЕОРЕТИНАЛЬНОЙ ХИРУРГИИ ПРОЛИФЕРАТИВНОЙ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ лельно появились отдельные публикации о применении ингибиторов ангиогенеза в качестве фармакологической подготовки пациентов с ПДР к витреоретинальной хирургии. Положительное действие этих препаратов авторы связывают с быстрой облитерацией новообразованных сосудов и уменьшением риска интраоперационных кровотечений [13]. Но, в то же время, по наблюдениям некоторых авторов, после интравитреального введения ингибиторов ангиогенеза отмечалось усиление витрео-макулярных тракций [9, 21].
Цель : оценить эффективность и безопасность интравитреального введения ингибитора ангиогенеза Луцентиса как подготовительного этапа щадящей витре-оретинальной хирургии при далекозашедшей ПДР
Материал и методы
Под нашим наблюдением находилось 41 пациент (63 глаза) с далекозашедшей ПДР в возрасте от 21 до 67 лет. Диагноз далекозашедшей стадии пролиферативной диабетической ретинопатии выставляли согласно классификации профессора Л.И. Балашевича (2004). Длительность сахарного диабета составила в среднем 19,7±5,7 лет. Пациентов разделили на две группы наблюдения. I группу (контрольную) составили 18 пациентов (27 глаз), которым в период с 2006 по 2007 гг. была проведена витре-оретинальная хирургия без предварительного введения ингибитора ангиогенеза. Группу II составили 23 пациента (36 глаз) с далекозашедшей стадией ПДР, которым за 3–7 суток до ВРХ предварительно интравитреально был введен Луцентис (2,3 мг) (Рис. 1 А, Б). Данное исследование выполнено в период c 2006 по 2010 гг. в рамках ограниченных клинических исследований, разрешенных этическим комитетом НМХЦ им. Н.И. Пирогова, при информированном согласии пациентов. Группы наблюдения были идентичны по возрасту, полу, уровню зрительных функций и длительности основного заболевания.
Методы исследования включали визометрию, регистрацию критической частоты слияния мельканий (КЧСМ), исследование свето- и цветоощущения, тонометрию, периметрию, биомикроскопию передних отделов глаза и задних отделов с помощью бесконтакт-
Рис. 1. А – Ингибитор ангиогенеза Луцентис (Genetech, USA). Б – интрави-треальная инъекция Луцентиса (2,3 мг)
ных высокодиоптрийных линз и фоторегистрацией, В-сканирование витреальной полости и оптическую когерентную томографию (ОКТ) витреоретинального интерфейса. Длительность оперативного вмешательства регистрировали по данным видеозаписи хода операции, где началом вмешательства принимали постановку портов и концом – герметизацию склеральной раны на месте постановки портов.
Острота зрения в обеих группах не превышала в среднем 0,05±0,01. Результаты исследования критической частоты слияния мельканий (КЧСМ) у пациентов были в пределах от 13 до 22 Гц. У пациентов обеих групп по результатам офтальмобиомикроскопии, В сканирования приблизительно в одинаковом проценте наблюдений отмечали наличие таких осложнений ПДР, как полные и частичные гемофтальмы, витреомакулярные и витре-опапиллярные тракции, регматогенные и тракционные отслойки сетчатки (Табл. 1).
Луцентис вводили интравитреально в условиях стерильной операционной по стандартной методике (Рис. 1). Витреоретинальные вмешательства были проведены одним и тем же хирургом, на одном и том же оборудовании. Все операции на глазах пациентов обеих групп наблюдения были выполнены по методике щадящей витреоретинальной хирургии, основной особенностью которой было щадящее отношение к сетчатке и ко II анатомической зоне: двухпортовый доступ, применение комбинированных инструментов (осветитель – ирригатор), а также инструментов малого калибра [3] (Рис. 2 А, Б).
Статистическая обработка полученных результатов была выполнена с помощью пакета прикладных программ статистического анализа AnalystSoft, BioStat 2007.
Результаты
Наблюдение за состоянием глаз пациентов II группы в сроки 2–4 суток после инъекции ни в одном случае не выявило осложнений, характерных для интравитреаль-ных инъекций, описанных другими авторами (эндофтальмит, усиление тракции). Результаты динамического наблюдения за общим состоянием пациентов II группы в течение 2 месяцев после ВРХ не выявили каких либо характерных осложнений в состоянии здоровья исследуемых, которые можно было бы связать с системным действием Луцентиса, описанном другими авторами [19, 25].
Табл. 1. Показания для витреоретинальной хирургии далекозашедшей ПДР в группах наблюдения
|
I группа (n=27) |
II группа (n=36) |
|
|
Гемофтальм |
33,3% |
36,1% |
|
Витреомакулярный синдром |
18,5% |
22,2% |
|
Витреопапиллярный синдром |
29,6% |
28,6% |
|
Регматогенная отслойка сетчатки |
7,4% |
5,6% |
|
Тракционная отслойка сетчатки |
40,7% |
44,4% |
Шишкин М.М., Юлдашева Н.М.
ИНТРАВИТРЕАЛЬНОЕ ВВЕДЕНИЕ ИНГИБИТОРОВ АНГИОГЕНЕЗА КАК ЭТАП ЩАДЯЩЕЙ ВИТРЕОРЕТИНАЛЬНОЙ ХИРУРГИИ ПРОЛИФЕРАТИВНОЙ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ
На 2–3 сутки после введения Луцентиса 13 (36,1%) пациентов отметили улучшение зрения соответствующего глаза. При офтальмобиомикроскопии отмечали уменьшение выраженности васкуляризации фиброваскулярных мембран – в 52,8% наблюдений. В остальных наблюдениях (47,2%) достоверно оценить изменения на глазном дне не удалось из-за гемофтальма, но отмечена тенденция к просветлению измененного стекловидного тела (Рис. 3 А, Б).
Особенности ВРХ после интравитреального введения Луцентиса. В ходе ВРХ при удалении ФВМ у пациентов I группы частота геморрагий составила в среднем 1,7±0,26 (варьировала от 1 до 3 случаев) в ходе вмешательства. В этой группе достоверно чаще регистрировали интраоперационные кровотечения при иссечении фиброваскулярных мембран, что потребовало в 22,2% применения интраокулярной диатермии, и в 74,1% – повышения ВГД за счет подъема флакона с ирригационным раствором. Во II группе частота интраоперационных геморрагий составила в среднем 0,4±0,1 (с вариацией от 0 до 2 случаев) в ходе вмешательства. Необходимость применения интраокулярной диатермии у пациентов II группы возникла в 8,3% наблюдений.
У пациентов II группы достоверно чаще завершали операцию газовоздушной тампонадой витреальной полости (58,3%), и только в 41,7% наблюдений потребовалось тампонада силиконовым маслом. В I группе наблюдения ВРХ значительно чаще вынуждены были завершать силиконовой тампонадой (66,7%), в то время как тампонаду газовоздушной смесью удалось применить только в 33,3% случаев.
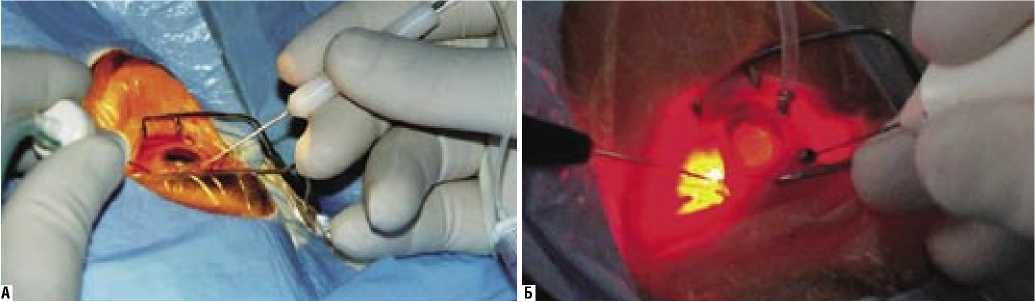
Рис. 2. Методы щадящей витреоретинальной хирургии: А – двухпортовый доступ, применение комбинированного инструмента, Б – трансклеральная иллюминация
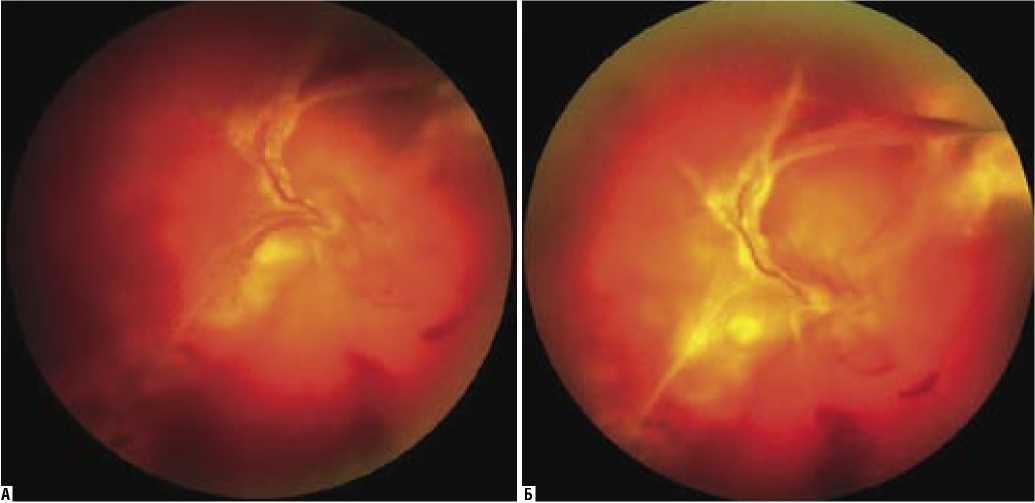
Рис. 3. Фотография глазного дна пациента с далекозашедшей ПДР: А – состояние сетчатки до интравитреального введения Луцентиса; Б – состояние сетчатки на 4 сутки после интравитреального введения Луцентиса
Шишкин М.М., Юлдашева Н.М.
ИНТРАВИТРЕАЛЬНОЕ ВВЕДЕНИЕ ИНГИБИТОРОВ АНГИОГЕНЕЗА КАК ЭТАП ЩАДЯЩЕЙ ВИТРЕОРЕТИНАЛЬНОЙ ХИРУРГИИ ПРОЛИФЕРАТИВНОЙ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ
Меньшее число интраоперационных осложнений у пациентов II группы позволило сократить время оперативного пособия до 97,4±11,6 минут, в то время как у пациентов I группы длительность вмешательства в среднем составила 118,3±15,3 минут.
Послеоперационное течение. В раннем послеоперационном периоде у пациентов I группы отмечали наличие крови в стекловидной камере различной степени выраженности, вследствие кровотечения из остатков фиброваскулярных мембран в 22,2% наблюдений, во II группе это осложнение наблюдали только лишь в 5,6% случаев. Ятрогенные разрывы у пациентов I группы произошли в 2 случаях, у пациентов II группы таких осложнений не было.
Острота зрения через 2 месяца у 58,3% больных II группы составила в среднем 0,17±0,12, в I группе средняя острота зрения 0,09±0,021 достигнута только в 33,3% случаев. Разница в остроте зрения до вмешательства и после вмешательства, а также в сравнении между группами была статистически достоверной (р=0,0087).
Ни в одном случае, при наблюдении в сроки 3–6 месяцев признаков репролиферации в центральных отделах глазного дна в обеих группах не отмечено. Однако, в 22,2% наблюдений в I группе и в 8,3% наблюдений во II группе отмечены рецидивы пролиферации в области склеростом, с рецидивирующими кровоизлияниями.
Развитие катаракты в послеоперационном периоде отмечено у пациентов I группы в 25,9% наблюдений, во II группе – в 19,4% случаев (во всех случаях при силиконовой тампонаде).
Обсуждение. Фармакологическое подавление сосудистого эндотелиального фактора роста – самое широко изучаемое направление в современной офтальмологической практике [18, 22, 23, 27]. В течение последних нескольких лет во многих странах мира получено официальное разрешение на интравитреальное введение Луцентиса при возрастной макулярной дегенерации [18]. Имеются предварительные сообщения о положительных результатах его применения при диабетическом отеке макулы [6, 16]. Но практически отсутствуют систематизированные исследования о применении данного препарата в качестве предоперационной подготовки перед ВРХ у пациентов с далекозашедшей ПДР. Проведенное нами исследование было направлено не только на изучение ожидаемых положительных эффектов, но и регистрацию описанных другими авторами как местных, так и системных побочных эффектов при применении Луцентиса [19, 25].
Полученные результаты подтвердили ожидаемый положительный эффект у большинства обследуемых пациентов II группы. Так, уже на 2–3 сутки после введения Луцентиса у 36,1% пациентов регистрировали улучшение остроты зрения, которое коррелировало с офтальмоскопической картиной пораженного глаза. Отмеченный положительный эффект мы связываем с уменьшением повышенной проницаемости сосудов сетчатки и в результате – уменьшение диабетического отека макулы. Это подтверждали данные офтальмобиомикроскопии и ОКТ. В 52,8% наблюдений при офтальмобиомикроскопии нами отмечено запустевание большинства новообразованных сосудов фиброваскулярных мембран, также мы отмечали повышение прозрачности измененного стекловидного тела в 47,2% наблюдений на 2–4 сутки после инъекции.
Применение Луцентиса способствовало снижению частоты интраоперационных осложнений, что оптимизировало выполнение ВРХ у пациентов II группы и обуславливало сокращение времени оперативного пособия. Даже неполная облитерация новообразованных сосудов фиброваскулярных мембран позволила упростить процедуру рассечения мембран во II группе наблюдения. Отсутствие выраженных интраоперационных кровотечений в указанной группе почти свело к нулю необходимость удаления организовавшихся фибринных сгустков с поверхности сетчатки, что значительно снизило частоту ятрогенных разрывов в ходе вмешательства, и позволило добиться более высоких функциональных результатов в послеоперационном периоде. Результаты наших наблюдений совпадают с данными, полученными Lee M.S., Abrams G.W. (2001), которые свидетельствуют о высокой частоте развития ятрогенных разрывов у пациентов, которым проводили удаление сгустков крови в ходе вмешательства. Отсутствие трудно купируемых интраоперационных кровотечений только в 8,3% наблюдений потребовало применения интраокулярной диатермии. Соответственно, у пациентов II группы операцию чаще завершали газовой тампонадой (58,3%) по сравнению с I группой, где более чем в половине случаев (66,7%) применяли силиконовую тампонаду. Это способствовало уменьшению периода восстановления после ВРХ, сокращало частоту послеоперационной катаракты, обусловленной силиконовой тампонадой и в большинстве наблюдений отказу от последующих плановых операций.
Согласно исследованиям ряда авторов, примерно в 60% наблюдений при традиционных методах витре-оретинальной хирургии в течение первых 6 месяцев после вмешательства, наблюдаются интравитреальные геморрагии [1, 24]. Источниками геморрагий в раннем послеоперационном периоде, по мнению тех же авторов, являются остатки фиброваскулярных мембран [1, 24]. Согласно нашим наблюдениям применение методики щадящей ВРХ позволило снизить частоту подобных осложнений до 22,2% наблюдений, а предварительное применение Луцентиса во II группе сократило их до единичных случаев (n=2).
Значительным достижением методики щадящей ВРХ явилось сокращение времени вмешательства, что было обусловлено меньшим количеством интраоперационных осложнений и способствовало более бережному отношению к организму пациента в целом, в связи с сокращением времени общей анестезии или в ряде случаев полной ее заменой на локальную анестезию. Применение Луцентиса в качестве предоперационной подготовки у пациентов с ПДР позволило еще больше сократить

Шишкин М.М., Юлдашева Н.М.
ИНТРАВИТРЕАЛЬНОЕ ВВЕДЕНИЕ ИНГИБИТОРОВ АНГИОГЕНЕЗА КАК ЭТАП ЩАДЯЩЕЙ ВИТРЕОРЕТИНАЛЬНОЙ ХИРУРГИИ ПРОЛИФЕРАТИВНОЙ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ время вмешательства с 118,3±15,3 минут до 97,4±11,6 минут, в сравнении с методикой только щадящей ВРХ. Это обусловлено отсутствием необходимости выполнения диатермии и удаления сгустков крови с поверхности сетчатки в большинстве наблюдений. Кроме того, низкая частота интраоперационных геморрагий обеспечивала хорошую визуализацию интраокулярных структур и способствовала снижению частоты ятрогенных осложнений. Аналогичные результаты были получены Chen E. и Park C.H. (2006).
Среди причин прочих осложнений, отмеченных другими авторами, остается неясным усиление тракционного компонента после интравитреального введения ингибиторов ангиогенеза [21]. Но в нашем исследовании ни в одном случае подобного осложнения не отмечено, возможно из-за малого количества наблюдений и непродолжительного периода между инъекцией и ВРХ.
Применение Луцентиса в качестве дополнительной предоперационной подготовки обусловили более высокие функциональные показатели в отдаленном послеоперационном периоде. В частности, во II группе к концу 2 месяца после ВРХ острота зрения 0,1 и выше была достигнута в 58,3% наблюдений, в то время как в I группе острота зрения в пределах 0,1-0,2 была зарегистрирована в 33,3%. Высокие функциональные результаты после ВРХ обусловлены на наш взгляд и проведением щадящей методики вмешательства, и предварительным введением Луцентиса. К сравнению, проведение традиционной методики ВРХ, по данным Ashraf M El-Batarny (2008), позволило у аналогичной категории больных получить остроту зрения от 0,05 до 0,1 в 33% наблюдений, а предварительное введение ингибитора ангиогенеза позволило добиться такого же уровня остроты зрения в 40% наблюдений [7].
Заключение
Предварительное введение ингибиторов ангиогенеза позволяет добиться лучших анатомических и функциональных результатов при ВРХ у пациентов с далекозашедшей ПДР, а также сокращения времени оперативного пособия. Положительный эффект их применения обусловлен уменьшением интраоперационных и послеоперационных кровоизлияний в стекловидную камеру, снижением показаний для силиконовой тампонады, а следовательно необходимости проведения повторного вмешательства.
Список литературы Интравитреальное введение ингибиторов ангиогенеза как этап щадящей витреоретинальной хирургии пролиферативной диабетической ретинопатии
- Сдобникова С.В., Столяренко Г.Е. Роль задней гиалоидной мембpаны в патогенезе и тpансцилиаpной хиpуpгии пpолифеpативной диабетической pетинопатии//Вест., офтальмологии. -1999. -№ 1. -С. 11-15.
- Шишкин М.М. Передняя пролиферативная витреоретинопатия//Автореф. дис....док. мед. наук., 2000. -328 с.
- Шишкин М.М., Касатикова Е.В., Ирхина А.В. Щадящая витреоретинальная хирургия при далекозашедшей пролиферативной диабетической ретинопатии//офтальмология. -2006. -Том 3 № 2. -С. 23-25.
- Шишкин М.М., Ирхина А.В. Эффективность авастина при подготовке пациентов с пролиферативной диабетической ретинопатией к витреоретинальной хирургии//Ерошевские чтения: Труды Всероссийской конференции. Самара. 2007. -С. 417-419.
- Экгардт В.Ф., Троицкова Е.В., Павлова Ю.Е. Эффективность интравитреального введения авастина при неоваскуляризации различной локализации у больных диабетической ретинопатией//Материалы V Евро-Азиатской конференции по офтальмохирургии, Екатеринбург -2009. -С. 208-209.
- A Phase 2 Randomized Clinical Trial of Intravitreal Bevacizumab for Diabetic Macular Edema//Ophthalmology. -2007. -Vol. 114(10). -P. 1860-1867.
- Ashraf M. El-Batarny Intravitreal bevacizumab as an adjunctive therapy before diabetic vitrectomy//Clinical Ophthalmology. -2008. -Vol. 2(4). -P. 709-716.
- Chen E., Park C.H. Use of intravitreal bevacizumab as a preoperative adjunct for tractional retinal detachment repair in severe proliferative diabetic retinopathy. Retina. 2006 Jul-Aug; 26(6): 699-700.
- Clemens C.R. et al. Macular hole formation in the presence of a pigment epithelial detachment after three consecutive intravitreal antivascular endothelial growth factor injections. J Ocul Pharmacol Ther. 2010 Jun; 26(3): 297-9.
- Congdon N.G., Friedman D.S., Lietman T. Important causes of visual impairment in the world today//JAMA -2003. -Vol. 290. -P. 2057-2060.
- Erdol H., et al. The results of intravitreal bevacizumab injections for persistent neovascularizations in proliferative diabetic retinopathy after photocoagulation therapy//Retina. -2010. -Vol. 30(4). -P. 570-577.
- Ferrara N. Role of vascular endothelial growth factor in physiologic and pathologic angiogenesis: therapeutic implications//Semin. Oncol. -2002. -Vol. 29 (6, Suppl. 16). -P. 10-14.
- Ferrara N. Vascular endothelial growth factor: basic science and clinical progress//Endocr. Rev. -2004. -Vol. 25(4). -P. 581-611.
- Jeong Won Seo, In Won Park, Intravitreal Bevacizumab for Treatment of Diabetic Macular Edema//Korean Journal of Ophthalmology. -2009. -Vol. 23. -P. 17-22.
- Joussen A, Smyth N, Niessen C. Pathophysiologyof diabetic macular edema//Dev. Ophthalmol. -2007. -Vol. 39. -P. 1-12.
- Karim R., Tang B. Use of antivascular endothelial growth factor for diabetic macular edema//Clinical Ophthalmology. -2010. -Vol. 4. -P. 493-517.
- Lightman S., Towler H.M. Diabetic retinopathy//Clin. Cornerstone. -2003. -Vol. 5. -P. 12-21.
- Lloyd R., et al. Food and Drug Administration approval process for ophthalmic drugs in the US//Curr. Opin. Ophthalmol. -2008. -Vol. 19(3). -190-194.
- Mason J.O. et al. Intravitreal injection of bevacizumab (Avastin) as adjunctive treatment of proliferative diabetic retinopathy. Am J Ophthalmol. 2006 Oct; 142(4): 685-8.
- Moorthy S., Cheung N. Cerebrovascular accidents and ranibizumab//Ophthalmol-ogy. -2009. -Vol. 116(9). -P. 1834-1835.
- Moradian S. et al. Intravitreal Bavacizumab in active progressive proliferative diabetic retinopathy//Graef.Arch.Clin.Exp.Ophthalm. -2008. -Vol. 246(12). -P. 1699-1705.
- Rotsos T. et al. Intravitreal anti-VEGF treatment in eyes with combined choroidal neovascularisation and vitreomacular traction syndrome//Br. J. Ophthalmol. -2010. Vol. 94(9). -P. 1205-1210.
- Simo R. et al. Angiogenic and antiangiogenic factors in proliferative diabetic retino-pathy//Curr. Diabet. Rev. -2006. -Vol. 2. -P. 71-98.
- Tolentino F. et al. Vitreous hemorrhage after closed vitrectomy for proliferative diabetic retinopathy//Ophthalmology. -1989. -Vol. 96(10). -P. 1495-500.
- Tong L. et al. Association of macular involvement with proliferative retinopathy in type 2 diabetes.//Diabet. Med. -2001. -Vol.18: 388-394.
- Ueta T. et al. Ranibizumab and stroke//Ophthalmology. -2010. -Vol. 117(9). -P. 1860-1.
- Wirostko B.,Wong T.Y., Simo R. Vascular endothelial growth factor and diabetic complications//Prog. Retin. Eye Res. -2008. -Vol. 27. -P. 608-621.
- Yong Woon Shin, et al. Effects of an Intravitreal Bevacizumab Injection Combined With Panretinal Photocoagulation on High-Risk Proliferative Diabetic Retinopathy//Korean J. Ophthalmol. -2009. -Vol. 23. -P. 266-272.


